EGFR表达与结肠癌侵袭转移的相关性及其调控作用
蔡宇翔, 谢仲鹏, 张怀念
武汉大学中南医院病理科,武汉 430071
作为临床最常见的恶性消化道肿瘤之一,结肠癌(colon cancer)具有发生发展迅速、侵袭范围广、转移速度快、病死率高的特点[1]。依据现今的外科医疗条件,早期结肠癌可通过根治性手术切除得到理想的治疗效果[2],而晚期结肠癌一般采用手术与化疗相辅助的治疗方案,但是结肠癌患者的术后再次复发以及癌细胞的不可控性转移是导致结肠癌患者死亡的最重要的原因之一[3]。随着分子病理学在临床应用技术上的突破,肿瘤细胞侵袭、转移相关的分子研究逐渐应用于结肠癌的诊断、治疗中[4]。表皮生长因子受体(epidermal growth factor receptor,EGFR)是原癌基因CerbB-1的表达产物,具有酪氨酸激酶跨膜活性,其介导的信号通路能够调节细胞核内基因的表达,影响细胞的生长分化[5]。有报道称,EGFR直接参与器质性肿瘤如大肠癌、大肠腺癌的形成过程[6],近年来越来越多的研究证实EGFR在结肠癌中存在过表达的现象[7],并且伴随有整合素β6(anti-integrin beta 6,ITGB6,属于跨膜糖蛋白受体,是一种粘附分子)表达异常的情况出现,但未见关于EGFR以及ITGB6与结肠癌侵袭转移关系的报道。本研究以临床结肠癌组织标本以及结肠癌细胞株为研究对象,探讨EGFR对结肠癌细胞增殖、侵袭及迁移的影响及其作用机制,希望为结肠癌的诊断和治疗提供新的线索和靶向位点。
1 材料与方法
1.1 结肠癌患者临床资料及组织样本收集
收集2017年3月~2019年3月于我院接受手术治疗的120例结肠癌患者的临床资料以及手术切除的癌组织及其对应的正常癌旁组织(距离癌组织超过2.5 cm处)。患者包括男60例,女60例,年龄38~72岁,中位年龄51岁。所有患者均以手术切除病灶,术前均未接受化疗或者放疗。所有入选患者均对本研究的目的知情,并已经签署同意书。用以上组织构建结肠癌组织芯片,在免疫组织化学染色后组织标本均未出现缺失,且组织病理学检测证实为原发性结肠癌。将患者的性别、年龄、肿瘤大小、组织分化程度、T分期、淋巴结转移、浸润深度、临床分期情况分别与EGFR的表达做Spearman相关性分析。本研究经医院伦理委员会审核批准。
1.2 实验材料
1.2.1 细胞 人结肠癌细胞株HCT116来自上海中科院细胞库,EGFR过表达病毒载体rAAV9-EGFR及空载体rAAV9-EGFR-NC(阴性对照)由中国医学科学院北京协和医学院生物医学工程研究所提供。
1.2.2 主要试剂 DMEM培养液(TOYOBO,日本);Trizol试剂盒(TaKaRa,日本);Ⅰ、Ⅲ型胶原兔多克隆抗体(Abcam,美国);麻醉剂、ITGB6抗体、EGFR抗体、鼠抗GAPDH单克隆抗体(Jackson,美国),Transwell小室(BD,美国);CCK-8试剂盒、反转录试剂盒、Western blot试剂盒(Sigma,美国);全蛋白抽提试剂盒、免疫组化试剂盒(QIAGEN,德国);Lipofectamine 3000转染试剂(Vector,美国)。
1.2.3 主要仪器 苏净Airtech超净工作台(北京六一仪器厂);SANYO MCO-15AC细胞培养箱(美国强生公司);Nikon Ti-U/Ti-s倒置荧光显微镜(日本三菱公司);5810R型高速离心机(日本岛津公司);Roche R480实时荧光定量PCR仪(美国Promega公司);Multiskan MK3酶标仪(美国Corning公司)。
1.3 实时荧光定量聚合酶链式反应(qRT-PCR)检测结肠组织中EGFR mRNA的表达
Trizol法提取结肠癌组织总RNA,按照PrimeScrip反转录试剂盒反转录成cDNA,所有操作严格按照试剂盒要求执行。采用SYBR Premix Ex Taq说明书配置PCR反应体系,反应条件为①预变性:75℃,120 s;②变性:90℃,5 min;③退火:60℃,60 s;④延伸72℃,30 s;⑤PCR仪采集荧光信号40个循环,以U6作为内参。U6上游引物为5′-CT-CGCTTCGGCAGCACA-3′,下游引物为5′-AAC-GCTTCACGAATTTGCGT-3′;EGFR上游引物为5′-ACTGTCTCCCAACCCTTGTA-3′,下游引物为5′-GTGCAGGGTCCGAGGT-3′。mRNA相对表达量用2-ΔΔCt表示,每个样本独立重复实验3次。
1.4 免疫组化法检测EGFR的蛋白表达
将结肠癌组织样本固定包埋并切片,用二甲苯和梯度乙醇脱蜡后置于柠檬酸盐缓冲液中进行修复,以充分暴露抗原决定簇。然后用3%双氧水室温下浸泡10 min,封闭,分别加稀释好的一抗4℃过夜孵育,次日冲洗干净,分别加入适量生物素标记的二抗室温孵育30 min,清洗。加适量二氨基联苯胺(DAB)作用2~5 min后用去离子水终止反应,苏木精复染1.5~2 min,清洗后以梯度乙醇脱水,二甲苯浸泡并干燥后用中性树胶封片,镜检观察并记录实验结果。染色评判标准以肿瘤细胞细胞膜和细胞质内出现黄色或棕黄色颗粒为阳性,每个切片随机取10个400倍视野,以100个细胞为计数单位,按染色面积及细胞被染色强度计分,计分原则如下:染色面积范围~10%为0分,~25%为1分,~50%为2分,~75%为3分,>75%为4分;细胞无染色0分,弱黄色1分,黄色染色2分,棕黄色3分。两计分之和大于或等于3分则为表达阳性,低于3分则为表达阴性。由肿瘤病理科2位医师双盲阅片,单独评分,最后统一汇总,对有争议的评分需要经病理科2位以上主任医师复核修订,得到最终结果。
1.5 细胞培养以及转染
将高侵袭性HCT116细胞接种于含有10%灭活胎牛血清的DMEM培养液中,置于37℃、5%CO2细胞培养箱中培养,细胞融合度达85%时,胰蛋白酶消化传代。取对数生长期细胞进行转染,采用Lipofectamine 3000通过脂质体介导法,将浓度均为100 nmol/L的rAAV9-EGFR和rAAV9-EGFR-NC转染至细胞,转染操作完成后,常规培养细胞48 h进行后续实验。细胞分为rAAV9-EGFR组、rAAV9-EGFR-NC组以及空白对照组(HCT116细胞,仅加入Lipofectamine 3000试剂)。
1.6 CCK-8及平板克隆实验检测细胞增殖
调整细胞密度,以1×105个/孔接种于96孔培养板中,分组处理同上,轻轻混匀后,置入37℃培养箱继续培养,每孔加CCK-8溶液20 μL,37℃避光4 h后,弃掉孔内液体,再加DMSO各100 μL,置于37℃摇床上快速振荡15 min,以便充分溶解结晶物,最后将96孔板置于酶标仪上检测492 nm处的吸光度(A)值。将上述各组细胞按每孔5×103个细胞的密度铺6孔板继续培养,隔周更换新鲜培养液,2周后用考马斯亮蓝染色,以大于30个细胞的克隆记为一个集落,在显微镜下通过100倍视野进行观察并拍照,并随机选取5个视野记录集落形成数量,计算平均值,每组设3个样品,重复实验3次。
1.7 Transwell小室检测细胞侵袭
实验前12 h更换细胞培养液为无血清培养液,将40 μL基质胶铺于Transwell小室中,消化细胞并用1 μL PBS清洗2遍,将500 μL无血清培养液加入24孔板,取5×105细胞重悬,向Transwell小室中加入200~250 μL细胞悬液,保证下层完全培养液与Transwell小室间无气泡。置于培养箱内正常培养24 h,加用甲醇配制、PBS稀释的0.1%结晶紫染液500 μL进行染色,室温避光15 min,PBS漂洗后用棉棒擦拭Transwell小室内部,倒置晾干,置于倒置荧光显微镜下通过200倍视野观察穿过膜的细胞并拍照计数,随机选取5个视野进行细胞计数,计算平均值。
1.8 划痕实验检测细胞迁移
调整细胞密度,以5×104个/孔接种于24孔培养板中,分组处理同上,继续培养48 h,弃掉培养液,用灭菌的10 μL加样枪枪头沿直线做划痕,加入100 μL PBS将细胞碎片冲洗掉,然后以无血清培养液,37℃、5%CO2温箱培养,分别于0 h和24 h在倒置显微镜下观察细胞迁移情况以及划痕宽度。采用图像分析软件Image J测量细胞划痕间距,并根据公式:细胞迁移率=(24 h边缘距离-0 h边缘距离)/0 h边缘距离×100%,计算出各组细胞的迁移率。
1.9 Western blot检测各组HCT116细胞中EGFR、ITGB6的表达
按照细胞浓度1×106个/mL加入300 μL的RIPA蛋白裂解液,裂解30 min,12000 r/min 4℃离心10 min,收集上清,采用BCA试剂盒检测蛋白浓度,将蛋白样品和上样缓冲液混合,100℃水浴变性5 min,然后加入至制备好的SDS-PAGE凝胶(5%浓缩胶,10%分离胶)上样孔中,每孔25 μL,浓缩胶时调整电压为60 V,分离胶电压为120 V,结束后取出凝胶,4℃转膜1.5 h,采用5%脱脂奶粉封闭PVDF膜2 h,加入一抗,4℃过夜,TBST洗膜后加入辣根过氧化物标记的羊抗兔IgG,37℃孵育2 h后加入ECL显影,采用自动凝胶成像系统采集图像,以GAPDH作为内参,分析蛋白表达水平。
1.10 统计学分析
数据统计采用SPSS 19.0软件,做图工具采用Graphpad 5.01,两组间比较采用t检验,多组间比较采用单因素方差分析,以P<0.05为差异具有统计学意义。
2 结果
2.1 结肠癌组织和癌旁组织中EGFR mRNA的表达
qRT-PCR结果如图1示,与癌旁组织比较,结肠癌组织中EGFR的mRNA表达量明显上升(P<0.05)。
2.2 免疫组化检测结肠癌组织中EGFR蛋白的表达
免疫组化结果如图2所示:EGFR阳性染色主要存在于细胞膜及细胞质中,EGFR在结肠癌组织中以阳性表达为主,而在正常癌旁组织中以阴性表达为主。在收集的120例结肠癌组织中EGFR的表达阳性率为66.7%(80/120),而在癌旁组织中仅为8.3%(10/120),差异有统计学意义(P<0.05)。
2.3 EGFR表达与结肠癌患者临床病理特征的相关性分析
相关性分析显示(表1),结肠癌组织EGFR的表达与患者性别、年龄、肿瘤大小、肿瘤分化程度以及T分期无显著相关(均P>0.05);而与淋巴结转移、浸润深度、临床医学分期相关(均P<0.01)。
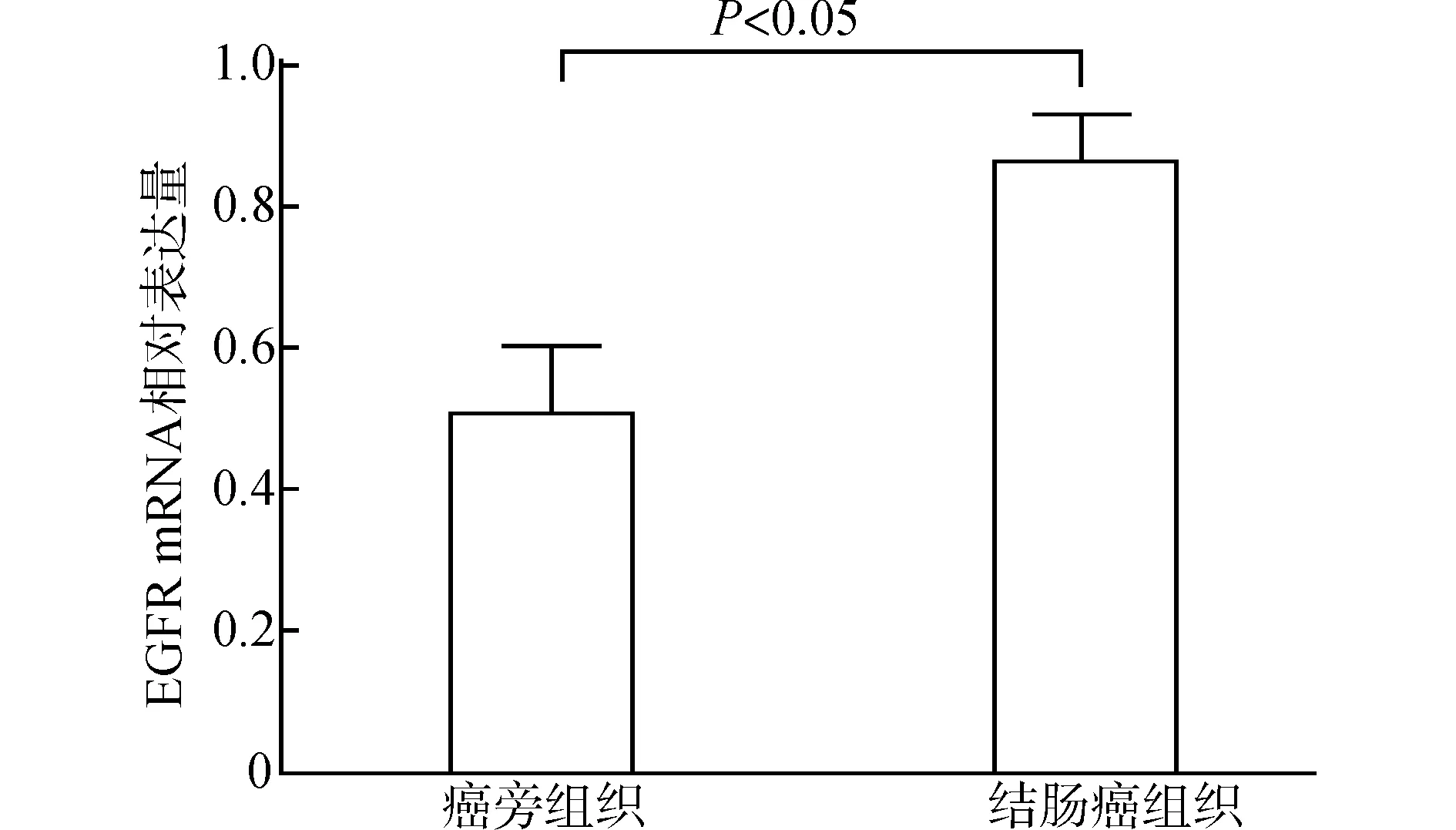
图1 qRT-PCR检测结肠癌与癌旁组织EGFR mRNA的表达Fig.1 qRT-PCR detection of the mRNA expression of EGFR
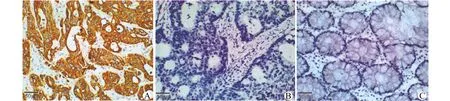
A:EGFR在结肠癌组织中阳性表达;B:EGFR在结肠癌组织中阴性表达;C:EGFR在癌旁组织中阳性表达图2 免疫组化检测EGFR在结肠癌及癌旁组织中的表达Fig.2 Immunohistochemical detection of the expression of EGFR in colon cancer and adjacent tissues
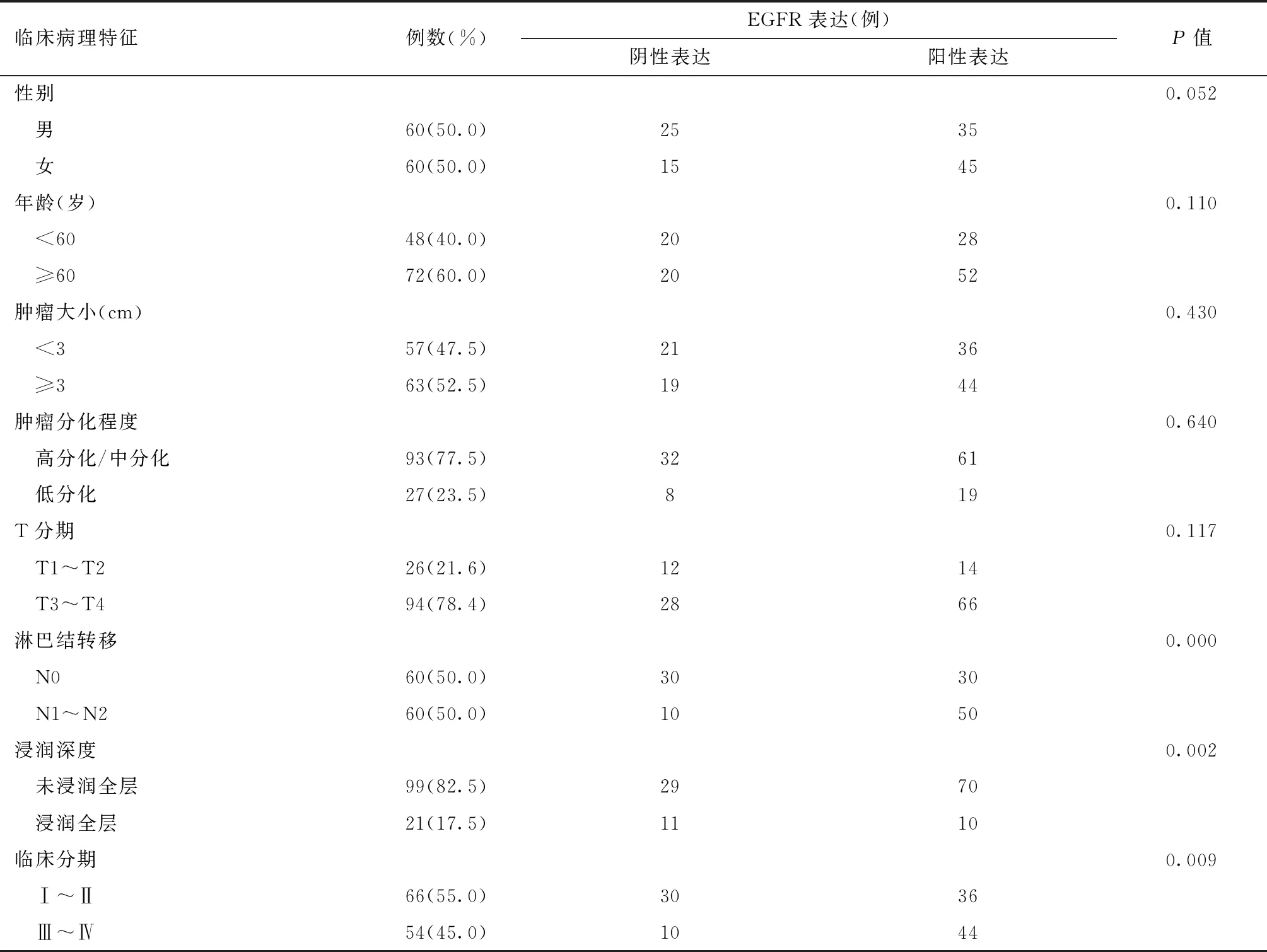
表1 EGFR的表达与结肠癌临床病理特征的相关性分析(n=120)Table 1 The correlation analysis between the expression of EGFR and clinicopathological charateristics of colon cancer(n=120)
2.4 过表达EGFR对HCT116细胞增殖能力的影响
CCK-8实验结果显示,与空白对照组相比,过表达EGFR的rAAV9-EGFR组A492 nm明显升高,差异有统计学意义(P<0.05,图3A);平板克隆实验结果显示,过表达EGFR后,rAAV9-EGFR组细胞克隆数明显增多(P<0.05,图3B、3C)。说明过表达EGFR后,HCT116细胞增殖能力明显增强。
2.5 过表达EGFR对HCT116细胞侵袭能力的影响
Transwell小室细胞侵袭实验结果显示,与空白对照组比较,过表达EGFR的rAAV9-EGFR组细胞穿过基质胶的数量明显增多,差异具有统计学意义(P<0.05)。该结果表明过表达EGFR后,HCT116细胞侵袭能力明显增强。见图4。
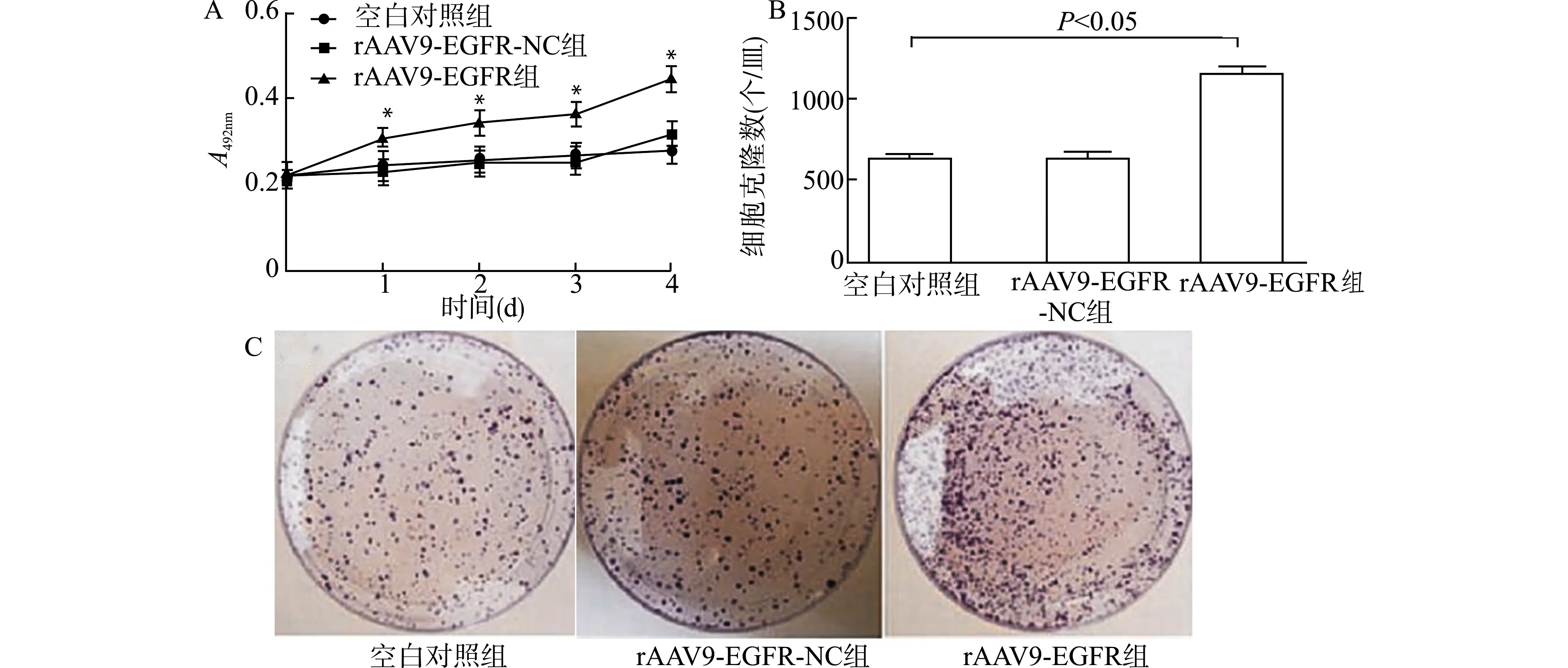
A:CCK-8检测各组细胞的增殖,与空白对照组比较,*P<0.05;B:各组细胞平板克隆结果;C:平板克隆检测细胞增殖图3 CCK-8法和平板克隆实验检测各组HCT116细胞的增殖Fig.3 The proliferation of HCT116 cells in each group detected by cell counting kit-8 and plate cloning assay
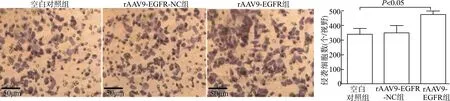
图4 Transwell小室检测各组HCT116细胞的侵袭能力Fig.4 The invasion of HCT116 cells in each group
2.6 过表达EGFR对HCT116细胞迁移能力的影响
细胞划痕实验结果显示,与空白对照组比较,过表达EGFR的rAAV9-EGFR组细胞迁移能力明显增强,差异具有统计学意义(P<0.05)。见图5。
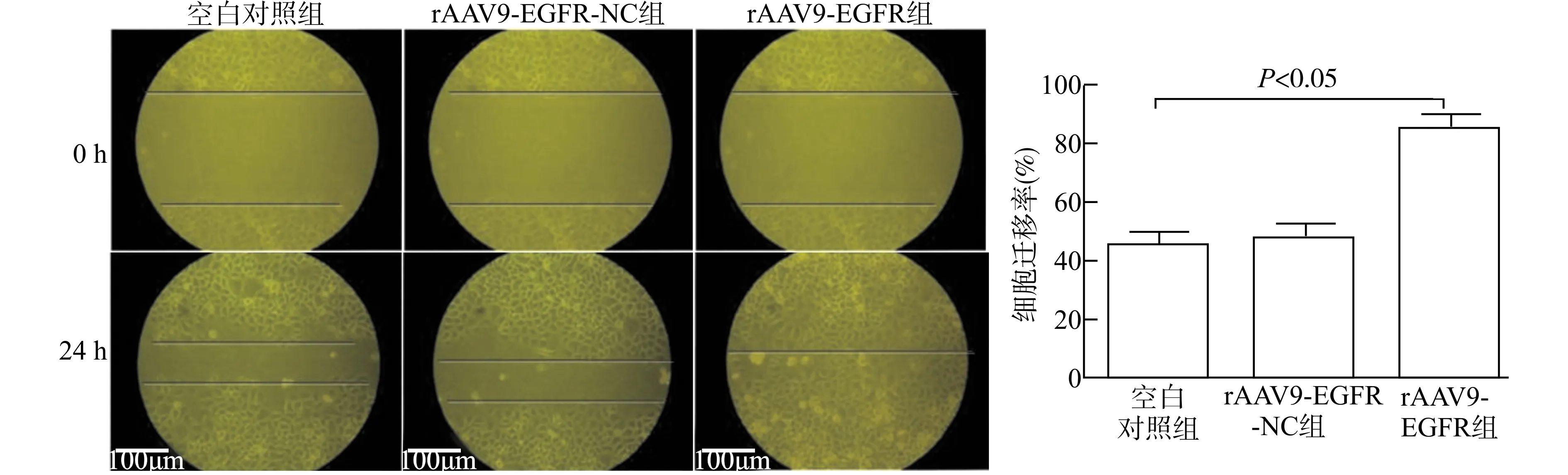
图5 划痕实验检测各组HCT116细胞的迁移能力Fig.5 The migration of HCT116 cells in each group
2.7 过表达EGFR对HCT116细胞EGFR、ITGB6表达水平的影响
ITGB6是广泛存在于生物细胞表面的特异性粘附分子,主要调节细胞的粘附、生长、迁移、侵袭以及诱导血管新生。本研究首先在http://genemania.org上查询了EGFR的和ITGB6的相互作用关系(图6)。采用Western blot检测HCT116细胞中EGFR、ITGB6的表达水平(图7),与空白对照组相比,过表达EGFR后,rAAV9-EGFR组细胞中ITGB6的表达水平明显上升(P<0.05)。
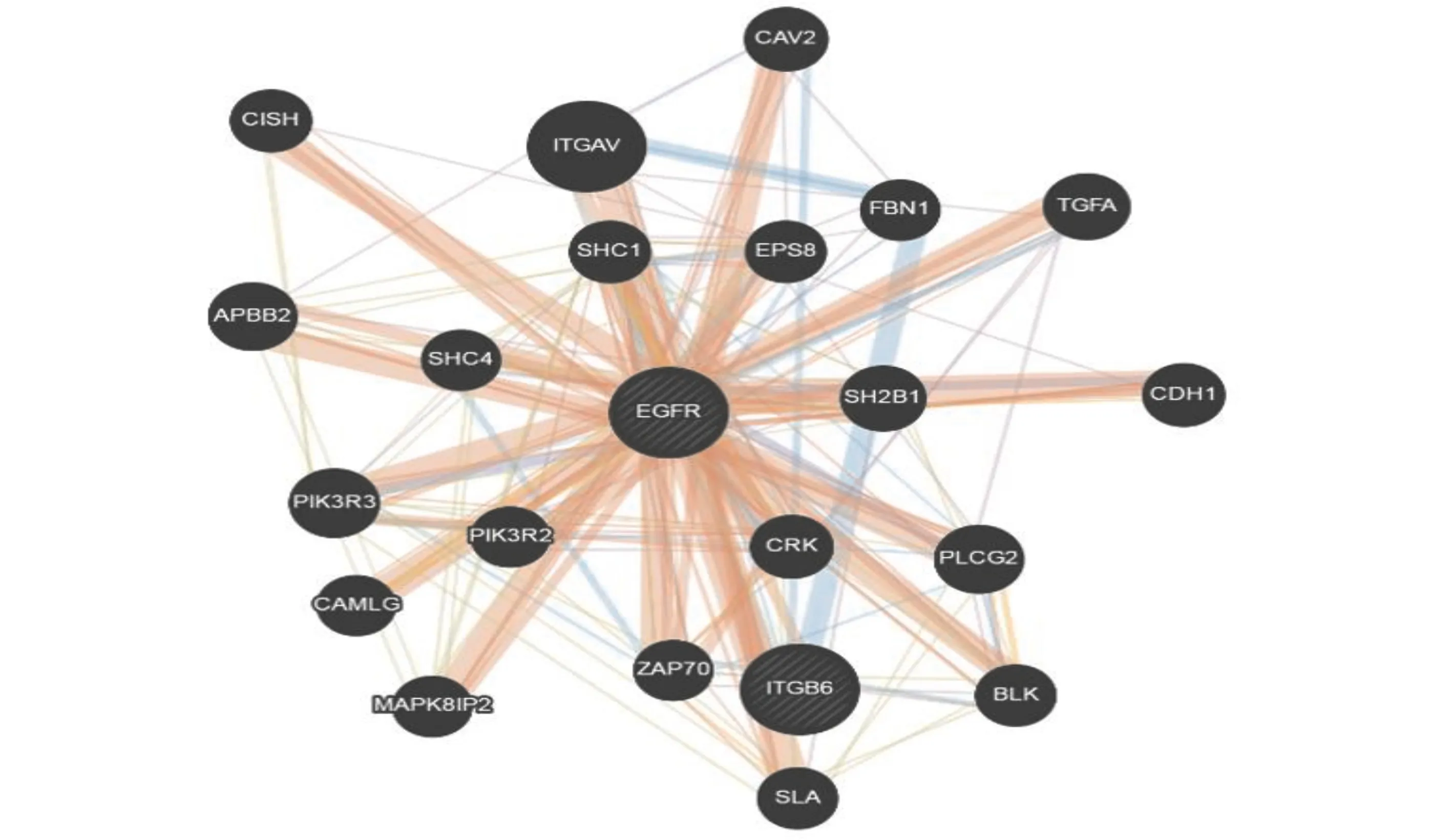
图6 预测EGFR的和ITGB6的相互作用关系Fig.6 The interaction between EGFR and ITGB6
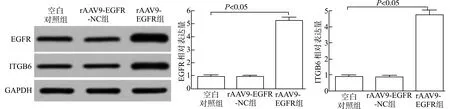
图7 各组细胞中EGFR、ITGB6的表达水平Fig.7 The expression of EGFR and ITGB6 in the cells of different groups
3 讨论
近年来,由于环境和日常膳食结构的变化,结肠癌的发病率和致死率不断攀升,严重危害人类的健康。目前缺乏根治性治疗的外科手段[8],而结肠癌的靶向治疗尚处于起步阶段[9]。已有研究证实[10]细胞内多种信号分子调控或参与结肠癌细胞的发生及癌细胞的侵袭和迁移,因此从分子生物学角度出发寻找结肠癌的发生、侵袭和转移的标志物,为患者提供有效的治疗方法有着重要的意义。
EGFR位于7号染色体上,在大多数组织和细胞中广泛存在,并且EGFR能通过多种途径如PI3K/AKT通路、RAS/RAF/ErK通路直接影响细胞的增殖和迁移[11]。有报道称EGFR可与Ral-GTPase结合激活原癌基因,导致细胞癌变的发生[12]。在对大量前列腺癌、大肠癌、乳腺癌临床标本的研究中发现[13],EGFR信号通路异常表达所引起的恶性肿瘤占很大比重。另外,Chen等[14]在对小鼠肝癌模型的研究中发现人参皂苷Rh2可通过抑制EGFR的表达发挥抗肿瘤效用;Xu等[15]研究发现上调EGFR的表达能明显抑制前列腺癌细胞的生长、侵袭以及迁移。目前尚无明确关于EGFR表达与结肠癌侵袭转移关系的研究报道。
本研究首先检测EGFR在结肠癌组织和癌旁组织中的mRNA表达水平,发现EGFR mRNA在结肠癌组织中的表达水平明显高于癌旁组织(P<0.05)。免疫组化结果显示EGFR蛋白主要存在于细胞膜及细胞质中。在收集的120例结肠癌组织中EGFR的阳性表达率为66.7%(80/120),而在癌旁组织中仅为8.3%(10/120),前者明显高于后者(P<0.05)。接下来对EGFR的表达水平与结肠癌患者临床病理特征进行相关性分析,发现性别、年龄、肿瘤大小、组织分化程度以及T分期与EGFR的表达无显著相关(均P>0.05);而淋巴结转移、浸润深度、临床医学分期与EGFR阳性表达有相关性(P<0.01)。这提示EGFR的高表达可能在结肠癌的发生、发展、侵袭、转移中起着重要的作用。
为进一步研究EGFR在结肠癌中的作用,本研究构建上调EGFR表达的病毒载体rAAV9-EGFR,转染高侵袭性结肠癌细胞株HCT116,通过CCK-8和分子克隆实验检测发现HCT116细胞增殖能力明显升高,Transwell小室和划痕实验结果显示,过表达EGFR后HCT116细胞的侵袭和迁移能力明显增强。
整合素ITGB6是一种跨膜二聚体糖蛋白,主要通过特异性的蛋白识别来介导细胞间以及细胞与周围外基质的粘附,维系细胞形态,与细胞的粘附、运动、侵袭、转移关系密切[16]。已有研究证实ITGB6的粘附作用依靠EGFR的进一步活化[17];何松原等[18]研究发现EGFR能影响ITGB6的表达,从而影响A549细胞的体外血管生成能力。本研究利用生物信息网站预测到EGFR和ITGB6可能存在相互作用;Western blot检测结果表明,与空白对照组和阴性对照rAAV9-EGFR-NC组比较,转染rAAV9-EGFR后,HCT116细胞中EGFR、ITGB6的表达水平明显上升(P<0.05)。
本研究证明EGFR在结肠癌的发展以及癌细胞转移中起着重要的作用,为结肠癌的治疗提供了一个关键性靶向位点。未来有望通过针对EGFR分子的生物学特性来设计结肠癌的分子靶向治疗手段[19](如EGFR的特异性抑制剂或EGFR的单克隆抗体),以抑制EGFR信号通路的激活或者抑制其信号传导。但是患者是否适合靶向治疗,如何将靶向治疗跟化疗药物联用,以及怎样将多种靶向药物联合使用,以达到更好的治疗效果,还需要更深入的研究。
综合上述,本研究提示EGFR在结肠癌组织中存在高表达的现象,并且可能在结肠癌的侵袭、转移中发挥重要的作用,为未来开启结肠癌的个体化靶向治疗提供了新线索。

