再制马苏里拉干酪的玻璃化转变测定及状态图研究
李红娟,秦爱荣,刘婷婷,李丹,李媛,李洪波,于景华*
1(天津科技大学 食品科学与工程学院,天津,300457)2(妙可蓝多(天津)食品科技有限公司,天津,300462)
食品绝大部分是由生物大分子构成的非晶态聚合物,因此都存在玻璃化转变状态[1]。玻璃化转变理论可以很好地解释诸如冷冻、干燥、挤压、焙烤等食品加工贮藏过程中某些食品品质的变化[2]。脱水和冷冻食品基质中经常显示出典型无定形聚合物转变,都是可以借助玻璃化转变温度来解释的物理化学或生化变化[3]。目前,玻璃化转变已经广泛地应用在水果、蔬菜、干燥谷物、粉末状食品的贮藏及加工稳定性分析中。食物的稳定性受成分、玻璃化、贮存温度和相对湿度的影响。如果固体食品的储存温度高于该食品中相关成分的玻璃转化温度(glass transition temperature,Tg),其物理化学性质就可能发生变化。通过测定食品的Tg,构建出该食品的状态图,能够对食品的贮藏稳定性进行预测,并为该产品的适宜加工原料和工艺提供参考[4]。
再制干酪是在原制干酪、乳化盐和其他乳成分的存在下,将配料混合,通过加热和混合乳化,形成的质地均匀的产品,由于存在加热工艺,可以延长干酪保质期。再制干酪除了对原制干酪的风味和质构进行改善外,还能够一定程度上解决原制干酪贮藏条件严格,保质期较短的问题。目前再制干酪可在3~6个月储藏期内保持较好的食用品质[5]。再制干酪也是我国干酪发展的主要品类,但是目前对于再制干酪加工和储藏过程的物理化学基础研究并不深入,而建立再制干酪状态图,能够为我们深入了解干酪贮藏加工性质提供理论基础。因此,本文研究测定了再制马苏里拉干酪玻璃转变温度曲线、冻结曲线、最大冻结浓缩状态等,建立再制马苏里拉干酪的状态图。为评价其贮藏稳定性、加工适宜性提供理论基础。
1 材料与方法
1.1 材料与试剂
实验所用原料:原制马苏里拉奶酪(恒天然贸易有限公司,新西兰),蛋白含量23 g/100 g,脂肪含量23 g/100 g,Na含量 393 mg/100 g;酪蛋白(北京银河路贸易有限公司),蛋白质含量82 g/100g,水分含量9.9 g/100 g;黄油(内蒙古华琳食品有限公司),脂肪含量99.8 g/100g。
实验所用试剂:LiCl、NaCl、NaNO2、P2O5、KNO3,凯玛特(天津)化工科技有限公司;醋酸钾、K2CO3、Mg(NO3)2·6H2O, 天津索罗门生物科技有限公司;MgCl2·6H2O,天津优化生物科技有限公司;KCl,上海阿拉丁生化科技股份有限公司;柠檬酸钠、Na4P2O7, 均为食品级,河南万邦实业有限公司。化学试剂除标明外,其余均为分析纯。
1.2 仪器与设备
DSC 204 F1型差示扫描量热仪,德国NETZSCH公司;MARS 60动态流变仪,德国HAAKE公司;LRH-250F型恒温试验箱,深圳市澳德玛电子科技有限公司;Lab-1B-50E真空冷冻干燥机,北京博医康实验仪器有限公司;GZX-9240MBE电热鼓风干燥箱,上海博迅实业有限公司;ZJR-5干酪融化锅,无锡意凯自动化技术有限公司。
1.3 实验方法
1.3.1 再制马苏里拉干酪的制备
将原制马苏里拉干酪切碎,加入黄油、酪蛋白等其他原料,将原料放入干酪融化锅中,调整融化锅搅拌桨转速为600 r/min,升温至85 ℃,加入乳化盐(柠檬酸钠、焦磷酸钠)水溶液(乳化盐预先溶解在热水中),调整转速至250 r/min,真空设为-600 kPa,搅拌3~5 min,真空恢复默认值,温度降到40 ℃,然后从融化锅中取出再制干酪,冷却成型。再制干酪进行真空包装,置于4 ℃冰箱贮藏。再制干酪成品中脂肪含量为21.3 g/100 g,蛋白含量为15.2 g/100 g,水分含量为62.0 g/100 g。
1.3.2 等温吸附曲线的测定
再制干酪样品含水率测定采用直接干燥法,110 ℃烘箱里干燥24 h,直至恒重。将再制干酪切割成0.5 cm×0.5 cm×0.5 cm的干酪丁,将样品置于-40 ℃冷冻,然后进行冻干。冻干温度-50 ℃,冻干时间16 h,冻干机压力70 Pa。冻干样品研磨成粉末,置于底部装有P2O5粉末的干燥器,干燥14 d,使其达到近似完全干燥。称取干酪粉末(0.5±0.01) g于培养皿中,迅速将其放置在9个不同相对湿度(0.12~0.94)的干燥器中[6],以获得0.12~0.94不同水分活度的样品。然后再将干燥器放在25 ℃的恒温箱中平衡14 d。aw>0.94的样品很难由水分平衡得到,需要将提前计算好的加水量加到对应的培养皿中,放在干燥器中平衡的时间与其他的样品保持一致[7-8]。达到平衡的样品,测定其平衡水分含量,采用Guggenheim-Anderson-de Boer(GAB)模型对等温吸附的数据进行拟合,模型方程如公式(1)所示:
(1)
式中:Mw,物料的平衡干基含水率,g/g;aw,物料的水分活度;Xm,单分子层吸附饱和干基含水率,g/g;C、K,热力学比例常数(方程参数)。
1.3.3 含非冻结水样品及含冻结水样品制备
含非冻结水样品制备:含非冻结水干酪样品由1.3.2方法制备,即干酪完全干燥后,放置于不同水分活度的干燥器中。含非冻结水的再制干酪水分含量为0.008~0.068 g/g(aw为0.12~0.61)。
含冻结水样品制备:当样品水分含量高于0.068时,样品热流曲线出现水熔融峰,一般被认为是含有冻结水样品,含冻结水样品制备是将完全干燥后样品通过计算直接加入相应水分含量的蒸馏水,水分含量在0.23~0.78 g/g之间。
1.3.4 动态流变仪测量含非冻结水样品
由于干酪中含有大量蛋白质和脂肪及其众多聚合物,导致在水分含量极低的干酪样品的差示扫描量热议(differential scanning calorimeter,DSC)热流图出现多而杂乱的熔融峰,不易对干酪玻璃化转变过程做出明确判断,因此采用动态流变仪分析测量此类样品的玻璃化转变温度,具体方法为:将每个样品称量(0.3±0.01) g,用模具压片,直径与流变仪加热底座一致,控制每次压片时间在30 s,将压成片的样品放在样品台上,用直径为20 mm的转子以恒力(30 N)压缩,以3 ℃/min的速度对样品进行热扫描,温度范围在20~100 ℃。在10~80 ℃范围内,以3 ℃/min的速率对样品进行热扫描,记录样品法向力。得到法向力-温度的动态流变仪RA曲线。由于法向力下降开始于试样底部温度达到Tg的点,所以力开始下降的温度可以视为试样的Tg[9]。测量3次结果,取平均值。
1.3.5 DSC测量含冻结水样品
首先用DSC扫描程序对样品热流曲线进行检测绘制,得出到玻璃化转变发生的温度区间。热流曲线采用二次扫描法。初步扫描程序为:样品从室温以5 ℃/min降至-60 ℃,保持10 min,然后再以5 ℃/min从-60 ℃升至40 ℃。第2步扫描(退火)程序为:样品从室温以5 ℃/min降至-60 ℃,再以5 ℃/min升至熔融温度(melting temperature,Tm)(-1 ℃),保持20 min;然后以5 ℃/min降至-60 ℃,再以5 ℃/min升至60 ℃[10]。确定最终的样品温度参数Tm′和冻结温度(frozen temperature,TF)。
1.3.6 数据的拟合和处理
不同水分含量干酪样品玻璃化转变温度可以采用Gordon-Taylor 方程来拟合,如公式(2)所示:
(2)
式中:W1,固形物湿基质量分数,g/g;W2,湿基含水率,g/g;Tg,混合物的玻璃化转变温度,℃;Tg1,固体的玻璃化转变温度,℃;Tg2,水的玻璃化转变温度,为135 ℃;K,Gordon-Taylor参数。
不同水分含量的干酪粉对应的TF用Clausius-Clapeyron 方程拟合,如公式(3)所示:
(3)

1.4 数据统计与分析
本实验中样品指标均重复3次,并计算平均值。绘图及非线性回归分析采用Origin 9.0软件进行。
2 结果与分析
2.1 干酪的吸附等温线
本实验中再制干酪的湿基含水率为0.62 g/g。图1为干酪样品在25 ℃的吸附等温线,为典型的“J”型曲线,对数据进行拟合后得到相关系数和模型参数见表1。从R2可知,实验数据拟合程度较好。表1列出了其他蛋白的Xm、模型参数以及相关系数[11]。在低水分活度时,干酪中含有的水能与某些化合物的极性基团结合,主要是NH3+和COO—蛋白质基团,还包括一些矿物盐的结晶水,即结合水,较难除去,属于非冻结水[12]。aw为0.2~0.6是曲线的线性部分,对应的是氢键较弱的附加水层或多分子层,说明随着aw的增加,自由水越来越多[13]。aw>0.6时水分为孔隙中凝结的水,此阶段干酪吸附的干基含水率明显增大,这种水可以溶解可溶性元素(特别是矿物盐),可以作为酶和微生物等生物制剂的载体[14]。

图1 干酪的吸附等温线(25 ℃)Fig.1 Adsorption isotherm of cheese (25 ℃)
2.2 含非冻结水干酪样品的玻璃化转变
由于干酪中含有大量蛋白质和脂肪及其他物质,导致在水分含量极低的干酪样品的DSC热流图出现多而杂乱的熔融峰,结果如图2所示,不易进行干酪玻璃化转变分析及判断,因此用热流变仪分析测量此类样品的玻璃化转变温度,结果如图3。
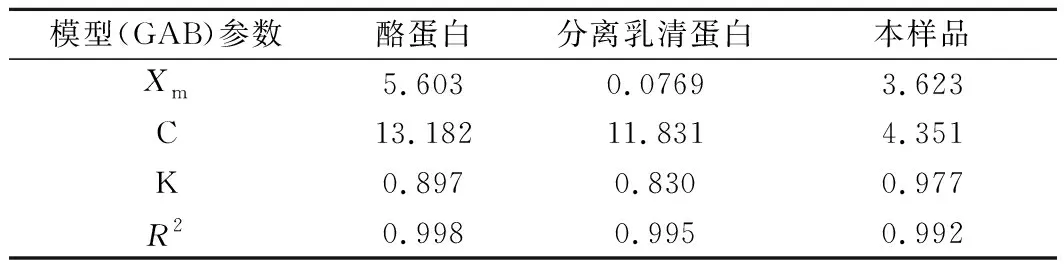
表1 吸附实验数据的模型拟合Table 1 Model fitting of adsorption experimental data

图2 含有非冻结水干酪样品的 DSC 热流图Fig.2 DSC heat flow diagram of cheese samples containing non-frozen water

图3 含有非冻结水干酪样品的动态流变仪测试Fig.3 Dynamic rheometer analysis for cheese samples containing non-frozen water

表2 含有非冻结水干酪样品的玻璃化转变温度Table 2 Glass transition temperature containing of cheese samples non-frozen water
食品的玻璃化转变温度一般来说与食品中溶质的成分、食品总分子量和食品的含水率相关[15]。由表2可知,随着湿基含水率从0.008 g/g增大到0.068 g/g,干酪的Tg从71.2 ℃降低至20.6 ℃。随着含水率增大,干酪样品玻璃化转变温度逐渐减小,这主要由于水的塑化作用引起。水是最基础的塑化剂,水塑化是低摩尔质量碳水化合物、低聚糖、多糖和蛋白质的典型特征,含水量增加可导致分子自由体积增大,局部黏度降低,同时增加分子迁移率[16-17]。
2.3 含冻结水干酪样品的玻璃化转变与冻结点
由DSC热流曲线(图4)测量得到含有冻结水、湿基含水率0.40 g/g的干酪初始冻结温度TF(-5.3 ℃)和冻结终点温度Tm′(-16.4 ℃),最后升温阶段如图4所示,TF定义为冰融化过程吸热峰的峰值温度,即冻结温度,最大冻结浓缩过程的Tm′是冰晶熔融吸热曲线的基线与吸热曲线左边的交点而得到[18]。TF与食品的种类和食品中的可冻结水的含量有关,随冻结水含量的增加而增加。采用Clausius-Clapeyron模型对不同水分含量的干酪粉的冻结温度进行拟合,得到拟合参数E=0.049 45,通过E值可估算干酪中总固形物的分子量364.01,根据文献报道,初乳清蛋白E值为0.054 7[16]。
图5为含有冻结水干酪样品玻璃化转变温度测量DSC热流图,干酪样品的玻璃化转变过程主要有转变初始点Tgi、转变中点Tg、拐点Tgm及终点Tge。

图4 含有冻结水的干酪典型 DSC 热流图(湿基含水率 0.40 g/g)Fig.4 Typical DSC heat flow diagram of chese samles containing frozen water

图5 含有冻结水的干酪 DSC 热流图的玻璃化转变温度测量(湿基含水率0.40 g/g)Fig.5 Glass transition temperature measurement of the DSC heat flow chart of chese samples containing frozen water
由表3实验结果可知,Tm′随着固形物质量分数增加而降低,当固形物湿基质量分数大于50%时,Tm′接近于常数,故固形物湿基质量分数在50%~77%时,最大冻结浓缩状态的Tm′平均值是-27.4 ℃。

表3 含有冻结水干酪的玻璃化转变温度与冻结点Table 3 Glass transition temperature and freezing point of cheese samples containing frozen water
2.4 状态图
状态图代表了食物的不同状态,它是水或固体含量以及温度的函数,为产品的配方、加工、包装、储存提供了重要的信息[19],根据状态图对食物进行贮藏能够避免食品从玻璃状态转化到橡胶状态,从而使得食品可以保存较长时间[18,20]。图7为本文通过实验数据最终建立的再制干酪状态图,该图包含了干酪样品的玻璃化转变温度曲线(D-G)、冻结曲线(A-M)及最大冻结浓缩状态的玻璃化转变温度曲线,其中冻结曲线、冻结温度与固形物质量分数曲线是由Clausius-Clapeyron方程模拟得出。图中的M点对应的冻结终点温度Tm′,为-27.4 ℃。根据计算可得干酪固形物湿基质量分数Xs′值为79%,此时Xs值对应非冻结水含水率,即0.21 g/g。利用Gordon-Taylor方程对玻璃化转变温度同含水率进行分析描述,并进行非线性拟合,得到GT方程。参数Tg1和K分别为75.02 ℃和4.20。参考其他文献的K值,酪蛋白为4.97,初乳清粉为7.89,大豆蛋白为4.22,干酪的K值更接近酪蛋白,这跟干酪的成分有直接关系[21]。GT方程拟合得到的完全干燥干酪样品玻璃化转变温度75.02 ℃,实验测得干燥干酪粉的玻璃化转变温度Tgm为80 ℃,差异小于5 ℃,拟合值基本符合实际测量值。
食品玻璃转化温度测定的意义在于将食品贮藏温度降低至玻璃转化温度以下时,能够最大程度地减少食品在贮藏过程中发生的品质劣变,Tg′即为冻结食品在贮藏过程中不发生质量变化的温度最高点。但是由于实际贮藏条件及成本所限,只能在尽量接近Tg′的温度下贮藏样品[22-23]。再制干酪最大冻结浓缩状态的玻璃化转变温度Tg′确定,在固形物湿基质量分数Xs′=79%的情况下,从M点做垂线,与玻璃化转变温度曲线DG相交,交点N即为干酪最大冻结浓缩状态的玻璃化转变温度Tg′,为-35.5 ℃。
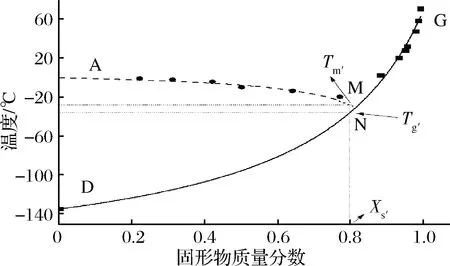
曲线A-M为冻结曲线;曲线D-G为玻璃转变温度曲线图6 干酪的状态图Fig.6 Status diagram of cheese
3 结论
本研究采用差示扫描量热仪作为热分析手段,动态流变分析作为机械分析手段,测量并分析绘制再制干酪的冻结曲线、最大冻结浓缩条件和玻璃化转变曲线和冻结曲线,构建再制奶酪的状态图,通过试验和分析得到以下结论:
(1)再制干酪水分吸附等温线呈典型“J”型曲线,GAB模型能够较好的对再制干酪的吸附等温线进行拟合。由冻结曲线、最大冻结浓缩条件和玻璃化转变线组成再制干酪的初步状态图。Gordon-Taylor方程、Clausius-Clapeyron方程能较好地拟合干酪的玻璃化转变线和冻结曲线。
(2)再制干酪玻璃转化温度同含水率呈负相关,随含水率增加而降低:含有非冻结水干酪样品随着湿基含水率从0.008 g/g增大到0.068 g/g,干酪样品的玻璃转化温度从71.2 ℃降低至20.6 ℃;含有冻结水干酪随着湿基含水率从0.22 g/g增大到0.77 g/g,干酪样品的玻璃转化温度从-19.7 ℃降低至-29.7 ℃,GT模型能够有效预测不同含水率下的玻璃转化温度。
(3)通过再制干酪状态图可知,再制干酪最大冻结浓缩状态的玻璃转化温度为-35.5 ℃,玻璃转化温度较低,-18 ℃的冷冻贮存方式仍高于其最大冻结浓缩状态的玻璃转化温度,在-18 ℃下贮存仍然会发生品质劣变。
再制干酪的最大冻结浓缩融化温度Tm′和玻璃化温度Tg′分别为-27.4 ℃和-35.5 ℃,这2个温度对于干酪样品的贮藏具有重要的指导意义。虽然,目前大部分干酪贮存条件都不能够降低到-35.5 ℃,但是在干酪加工工业中,研究者可以通过调整基础配方或加工工艺,在不影响品质的基础上尽量提高再制干酪的玻璃转化温度,保证干酪在贮藏过程中能够维持良好的品质。同时,再制干酪的状态图对确定最适的再制干酪的贮藏条件和加工条件以及对以后进行常温再制干酪的研究具有很重要的意义,在再制干酪加工中,通过状态图分析能够有效判断食品稳态及亚稳态,对样品的贮藏期进行有效预测判断。下一步实验中将结合干酪状态图及方程,对不同干酪样品进行货架期预测,并结合实际产品质量检测,建立再制干酪货架期模型,为再制干酪加工贮藏提供更有价值的理论指导。

