“四步法”应对情景方程式的书写
四川 王梦林
一、考频统计及分析
全国卷非选择题必考部分三道题的题型一般为无机化工流程题、化学反应原理、化学实验,两道选考题有机化学基础和物质结构与性质中二选一。化工流程题主要侧重无机物性质的考查。2017—2019年9套全国卷化工流程题考查角度及历年考频统计如下表:

方程式书写计算电化学化学实验物质的推断物质性质2019·全国卷Ⅰ22222019·全国卷Ⅱ311112019·全国卷Ⅲ21232018·全国卷Ⅰ312112018·全国卷Ⅱ32122018·全国卷Ⅲ241112017·全国卷Ⅰ2222017·全国卷Ⅱ11422017·全国卷Ⅲ21221
三年各考查角度考频统计如下:

由考查角度考频统计图可以看出:
(1)工业流程题中考频最高的是方程式的书写,每年、每套全国卷必考,89%的工业流程题考查方程式书写的频次在两次及以上。方程式书写的考查主要为在给定情境中的陌生方程式书写,类型分为化学方程式、离子方程式、电极方程式。
(2)物质的推断及物质性质的考查频次也较高。主要是流程中加入的试剂和流程生成物的判断,以及对流程步骤和加入试剂原理的解释,在流程分析过程中会加入一定的实验操作考查。
(3)电化学内容主要在2018年全国卷进行了考查,在2017年和2019年全国卷中并未在工业流程题中考查电化学部分,而将考查设置在了化学反应原理部分。原电池和电解池是在选修四《化学反应原理》中进行系统学习的,在原理部分考查更为合理。
(4)化学计算考频也较高。主要设置在最后一小题,考查形式为滴定法测定含量(2019年全国卷Ⅱ、2018年全国卷Ⅰ、2017年全国卷Ⅱ)、溶度积有关计算(2017年全国卷Ⅰ)、物质组成计算(2019年全国卷Ⅲ)、产率计算(2017年全国卷Ⅲ)。
二、教学中的方程式
六个常见考查角度中方程式的书写出现频次最高,足见其重要性,而方程式的书写一直以来都是教学过程中的难题之一。
1.方程式之难
初中化学接触过一些简单的方程式,因为少和简单所以记忆起来也比较简单,学生并未体会到它的“难处”。《必修一》第二章离子反应和氧化还原反应部分开始接触更多的方程式,第三、四章金属、非金属及其化合物部分方程式的数量急剧上升,学生也深刻体会到了难之所在:①难在量多,第三章和第四章介绍了钠、铝、铁、铜、硅、氯、硫、氮等元素的单质及其化合物,种类多、性质不一,对应的方程式数不胜数;②难在记忆,每个方程式都不一样,但是在高一阶段的学习中比较重要,所以方程式的记忆一直困扰着学生,更有同学出现“今天记住明天忘”的情况;③难在使用,肯花些时间来记忆方程式并不是难事,但是在什么题中应该使用哪些方程式就变得困难了,学生不能准确使用方程式也是一个难题。
2.方程式的意义
化学是一门以实验为基础的学科,化学实验目的一般为验证或探究一些物质的性质,而方程式则是反应性质的最直观的表达。
基于宏观辨识的化学反应描述出了宏观物质的变化,伴随着可观察到的现象和可感觉到的能量变化。基于微观探析的化学反应指的是有新物质生成的反应,即为原子的重新组合过程,反应前后原子种类、数目和性质都保持不变。
化学反应是宏观物质变化与微观原子重新组合的直接体现,理解方程式的本质可提高学生对方程式的认识,方程式不是简单的化学符号的组合,而是反应物中旧化学键断裂和生成物新化学键形成过程的体现。
3.高一阶段方程式教学建议
(1)重视物质性质。强化物质的性质,而不是强化方程式本身。高一学习阶段元素化合物性质教学主要可以分为两大类:物质分类教学法和化合价教学法。
物质分类教学法。以二氧化硅教学为例:二氧化硅属于酸性氧化物,即可联系酸性氧化物的性质——与水、碱、碱性氧化物的反应。

(2)重视配平与守恒。方程式的配平也是学生遇到的一个难题,而配平的基本依据则是守恒:化合价升降守恒(得失电子守恒)、电荷守恒、元素守恒。配平顺序为化合价升降守恒→电荷守恒→元素守恒。
以铜和稀硝酸反应的离子方程式为例:

三、全国卷真题分类剖析
1.化学方程式
【例1】(2019·全国卷Ⅱ·26节选)(2)以重晶石(BaSO4)为原料,可按如下工艺生产立德粉:
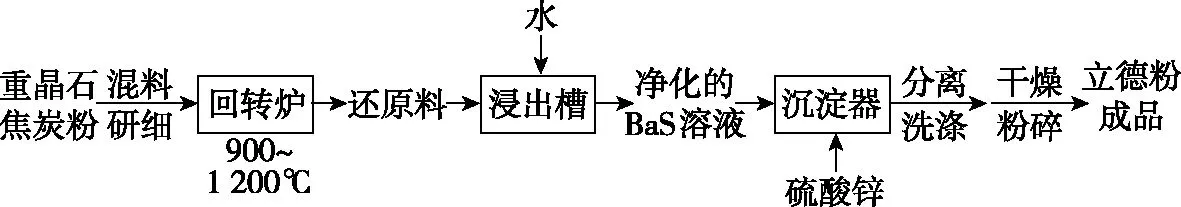
①在回转炉中重晶石被过量焦炭还原为可溶性硫化钡,该过程的化学方程式为_________________
回转炉尾气中含有有毒气体,生产上可通过水蒸气变换反应将其转化为CO2和一种清洁能源气体,该反应的化学方程式为______________________________。


【解析】进入回转炉的反应物为重晶石和焦炭粉,题干指出“重晶石被过量焦炭还原为可溶性硫化钡”,正因为焦炭过量,氧化产物应为CO,故可按照以下流程写出:


【试题解读】两个方程式难度不大,关键在于对题干信息的有效分析,要学会“瞻前顾后”:回转炉中的反应物已经明确给出,题干描述中指出了过量焦炭将硫酸钡还原为硫化钡,在分析氧化产物时不少同学如果没有认真分析题干就会将氧化产物认为是CO2,所以此时应对焦炭的过量引起重视,若重视了这个信息就可以正确判断氧化产物为CO。同时,此空之后提出“回转炉中含有有毒气体”,这个信息也验证了氧化产物是CO而不是CO2,从而写出正确的化学方程式。
【例2】(2019·全国卷Ⅰ·26节选)硼酸(H3BO3)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工业。一种以硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸及轻质氧化镁的工艺流程如下:
回答下列问题:
(1)在95℃“溶浸”硼镁矿粉,产生的气体在“吸收”中反应的化学方程式为______________________________。

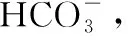

2.离子方程式
【例3】(2017·全国卷Ⅰ·27节选)Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备。工艺流程如下:
回答下列问题:

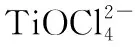

【试题解读】本题是离子方程式的书写,题目给出了主要的反应物和生成物,离子方程式的书写步骤和化学方程式是一致的,只是加入了电荷守恒,而配平电荷时的离子需要从题意来判断,酸性溶液用H+配平,碱性溶液用OH-配平。
【例4】(2018·全国卷Ⅰ·27节选)(4)Na2S2O5可用作食品的抗氧化剂。在测定某葡萄酒中Na2S2O5残留量时,取50.00 mL葡萄酒样品,用0.010 00 mol·L-1的碘标准液滴定至终点,消耗10.00 mL。滴定反应的离子方程式为______________________________。

【解析】Na2S2O5可作抗氧化剂,则说明容易被氧化,碘单质的作用是与Na2S2O5反应将其氧化。Na2S2O5中硫元素化合价为+4,被碘单质氧化为+6价,可按照以下步骤书写:

【试题解读】本题以滴定实验为载体书写氧化还原反应的离子方程式,在例3基础上加入了化合价升降守恒,学生需要分析焦亚硫酸钠中各元素的化合价,判断氧化产物和还原产物。配平电荷选用的是H+,配平原子守恒依然用H2O。
四、方法归纳
陌生方程式的书写只要按照一定的步骤,就能化繁为简,逐个攻破,以下是方程式书写步骤的建议:
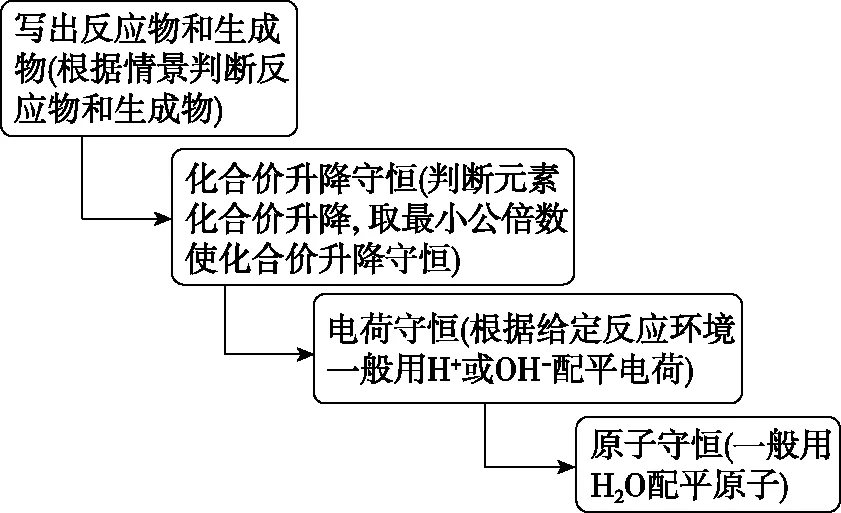
五、复习备考建议
如何能让学生在高考中不受方程式书写困扰是作为教师需要思考的,我们可以从以下几点协助学生:
1.重理解:方程式是宏观现象的微观解释,物质发生了变化但是原子并未改变,体现的是典型的守恒思想。因此在高一和高二的日常教学中我们要重视方程式的意义教学,让学生理解反应、理解方程式。
2.辨情景:工艺流程题中的方程式书写考查重点之一是写出反应物和生成物,部分题干会直接给出重要的反应物和生成物,有的题干则只给部分物质,学生需要从流程和题干描述中自主分析得出物质。
常用的物质判断方法有:(1)箭头法,进入箭头为反应物,出去箭头为生成物;(2)瞻前顾后法,流程前后共同分析,根据前后物质的变化判断反应物和生成物。
3.知守恒:学生可以写出主要物质但不能配平的主要原因就是不会用守恒,多数学生的方程式配平仅限于观察法,而对于守恒不够了解,因此我们要在日常的教学和复习过程中加强守恒思想的灌输,让学生了解守恒在配平方程式中的重要性。
4.肯放手:在遇到情景方程式书写题时,给够学生自主思考和分析的时间,让学生养成独立解决问题的能力,教师只需要在学生遇到无法解决的困难时给予适当的指导即可。

