COVID-19合并肝功能异常的临床研究进展
刘晓菲, 陈丽萍, 程计林
上海市(复旦大学附属)公共卫生临床中心消化内科,上海 201508
新型冠状病毒肺炎(COVID-19)的爆发已经成为国际共同关注的突发公共卫生事件,世界卫生组织将新型冠状病毒命名为SARS-CoV-2(severe acute respiratory syndrome coronavirus 2),其最重要的攻击靶标是肺,而后诸多研究发现,COVID-19患者存在不同程度的肝功能异常,主要表现为肝功能酶、胆红素的升高,尤其是天冬氨酸转氨酶(AST)和丙氨酸转氨酶(ALT)升高常见,特别是重症患者的肝酶升高更为明显,但具体机制尚不明确,本文将针对其发生原因、临床特点及如何应对目前的研究状况作进一步的概述,以供临床诊治工作参考。
1 COVID-19合并肝功能异常的临床特点
COVID-19合并肝功能异常主要表现为肝功能酶的升高,在COVID-19死亡病例中,肝损伤的发生率高达58.6%[1]。此外也有研究指出,COVID-19合并肝损伤的分布存在一定的规律性[2],这样的患者普遍分布于武汉,且主要集中于男性,同时年龄因素也占据着不可忽视的地位,年老者COVID-19合并肝功能异常占多数,但具体机制仍不明确。
最近关于COVID-19的研究显示,COVID-19合并肝功能异常的发生率为14%~53%[3],主要表现为ALT和AST水平升高[1,4-11],部分患者还会出现胆红素、乳酸脱氢酶(lactate dehydrogenase,LDH)升高,但黄疸较少见;有时会出现由于肝功能损伤造成肝脏合成白蛋白减少而形成的低蛋白血症,但这并不排除由于患者营养不良伴随着蛋白丢失过少的可能;凝血酶原时间(prothrombin time,PT)延长的情况也会在重症患者身上发生,碱性磷酸酶(ALP)及谷氨酸转肽酶(GGT)一般不会有明显变化,只有在少数病例中可见其明显升高。近期关于COVID-19合并肝损伤的研究总结如表1所示。
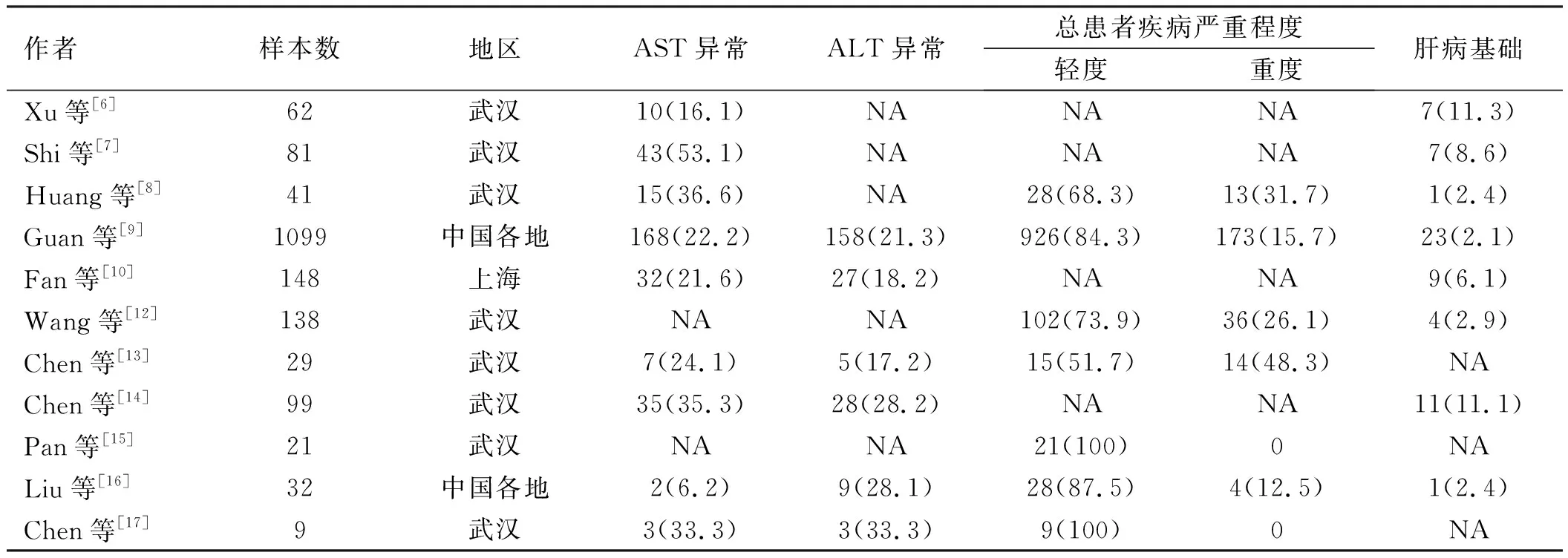
表1 COVID-19合并肝损伤的情况[例数(%)]Tab 1 COVID-19 patients with liver injury [n(%)]
一项来自31个省522所医院涵盖1 099例COVID-19患者的研究[3]发现,肝功能损伤多发于重症患者,是由于这类患者伴有基础性的病变。处于进展病程中的COVID-19患者肝功能损伤占比远高于轻症患者[8-11]。有研究认为,肝功能损伤程度较重的群体多合并肝脏基础性疾病,与无慢性肝病的COVID-19患者相比,合并慢性肝病的COVID-19患者的疾病进展率显著较高[18],考虑到这类具有基础肝脏疾病的患者系统免疫低下的状况,其影响SARS-CoV-2对肝脏的损伤的可能性还是很大的,且这类患者更易发展成重症患者[19]。然而,我们的研究[20]发现,SARS-CoV-2合并HBV感染的患者在肝功能及病情严重程度上并无太大差异,这可能与纳入的COVID-19患者合并感染的患者均与HBV携带者有一定关联。至于代谢相关脂肪肝是否会影响疾病的进展,一项涉及202例COVID-19患者的调查研究[21]指出,非酒精性脂肪肝与COVID-19患者的呼吸困难、低氧血症有一定关系,且这类患者的排毒期会更长。但Biquard等[22]声明,非酒精性脂肪肝患者的肝组织中与SARS-CoV-2感染相关蛋白的基因表达并不高,其具体机制有待进一步研究。可以确定的是肝硬化是影响COVID-19患者预后的一个重要危险因素[23]。
2 潜在机制
2.1 病毒直接攻击肝脏Puelles等[24]通过尸检22例死亡患者发现SARS-CoV-2存在于肝脏的组织学或病理学证据,这就为SARS-CoV-2攻击肝脏提供了直接的证据。而早前,石正丽团队[25]的研究发现,SARS-CoV-2和SARS-CoV有79.5%的高度同源性,均可通过血管紧张素转化酶-2(angiotensin-coverting enzyme-2,ACE2)受体侵入人体。胆管中ACE2受体表达量与肺泡2型细胞表达量相当(肺泡2型细胞是SARS-CoV-2在肺里的靶细胞),而肝细胞中ACE2受体表达量只有胆管细胞中的1/20[26]。胆管细胞在肝脏再生和免疫反应中起到至关重要的作用,因此便有不少研究人员认为SARS-CoV-2很可能通过感染胆管细胞造成胆汁淤积进而侵害肝细胞造成肝损伤。但国内大量临床样本的数据分析显示,早期肝功能异常主要表现为AST、ALT升高,且均比较轻,只有在重症患者中才会有明显的升高,而表示胆管功能的ALP、GGT升高却很少见,只有极个别死亡的病例才会出现黄疸,这些均提示了胆管损伤在COVID-19合并肝损伤中并不常见。另外,有学者认为,有包膜的SARS-CoV-2对胆汁极为敏感,这就为其通过胆管上皮细胞又设置了一道屏障。因此,关于SARS-CoV-2通过感染胆管细胞造成胆管细胞损伤进而损伤肝细胞的研究有待进一步考证。另有研究[27]推测,胆管上皮细胞来源的肝实质细胞的代偿性增生所致病毒受体ACE2在肝组织中的表达上调,可能是SARS-CoV-2感染肝细胞造成肝组织损伤的可能机制。这可能为在肝脏中找到病原体提供了理论依据[24]。
2.2 免疫反应人体对于病毒、细菌等的入侵自有一套防御系统以抵御外界的侵害,保证自身各个系统处于平衡状态。免疫系统在人体抵抗外界有害物质的入侵中扮演了重要的角色,部分COVID-19患者在早期还处于轻症表现,一般在2周后能够检测到肝功能损伤变化[27],肝功能酶升高。这可能与SARS-CoV-2在入侵的时候激活体内的免疫炎症反应,免疫细胞释放大量的炎症因子有关。虽然许多COVID-19患者早期状况良好,但在一些患者中这种感染会导致突发的多器官功能衰竭。多数专家认为,这种突发的多器官功能衰竭主要与重症患者体内的炎症分子风暴的激活有关。事实上,这种病毒能够直接通过TLRs和T杀伤细胞激活炎症信号通路,激活的T细胞然后攻击感染的体细胞,致使其凋亡和坏死,直至T细胞耗竭,有研究[10]表明,COVID-19患者外周血中CD4+淋巴细胞和CD8+淋巴细胞较之正常人少。而由死亡的感染细胞释放的损伤相关分子又可以进一步放大炎症信号通路。同时,由于T细胞的耗尽而不能抵抗病毒和细菌的感染,因此便激活多条炎症信号通路,激活巨噬细胞和二次炎症反应。随着越来越多的炎症分子被释放,损伤和坏死也便成了常态。这一循环可导致多器官的衰竭,肝脏便成了被攻击的靶器官之一,另有免疫组化结果[28]显示,肝窦区弥漫大量的CD68+细胞,表明枯否细胞被激活。
2.3 药物毒性肝脏是人体代谢药物的主要器官,COVID-19患者在治疗过程中使用的药物(包括发热初期的解热退烧药、抗病毒药物、抗生素甚至中药)均会对肝脏造成损伤。用药种类越杂,用药时间越长,发生肝损伤的几率便会越大。根据对于上海市公共卫生临床中心确诊的148例COVID-19患者的各项临床特征、实验室检查及用药和住院时间长短进行分析[10],入院后发生肝功能异常的患者服用洛匹那韦/利托那韦的比例高于入院后肝功能正常者。因此,需要把药物造成的肝损伤纳入考量,综合各方面因素的考虑,对于有基础性肝脏病变的患者要慎重考虑其用法用量,以免造成不必要的肝损伤进而增加临床治疗不必要的负担。
2.4 缺血缺氧再灌注损伤COVID-19患者由于病毒入侵肺泡2型细胞出现广泛的肺部炎症,影响肺部气体的交换,导致肺的氧和能力下降,致使机体处于缺氧状态,酸性物质积聚,重型患者甚至会出现全身炎症反应综合征、呼吸窘迫综合征和多器官功能衰竭,呼吸性细支气管的纤维性坏死和炎症反应也会影响血液的回流,心脏的前负荷增加,进一步影响肝静脉血的回流,使门静脉压力升高,致使肝脏处于一种缺血缺氧的状态,而肝脏对于缺氧又极为敏感,低氧状态下,肝脏细胞凋亡和坏死几率大幅增加。已有肝活组织检查[29]显示,中度的微血管脂肪样变性及轻度的肝小叶汇管区活动性炎症,可能与其缺血缺氧有关。
2.5 其他除了肺泡上皮大量表达ACE2受体外,ACE2受体同样在消化道系统食管上皮、回肠及结肠等有大量表达,这也就为肠源性感染提供了可能性[30]。基于COVID-19患者出现腹泻,且血液和粪便中均能检测出病毒,故不能排除病毒直接侵袭肝脏细胞的可能[19]。此外,有基础肝脏疾病及代谢性疾病可能是感染后致肝损伤的因素之一。如在前述各项调查肝损伤的研究中,发现与肝功能密切相关的代谢性疾病如糖尿病、高血压等,在合并COVID-19时更易发展为重症患者,因此不排除代谢性疾病激发的肝脏继发性损伤。
3 预防及治疗
目前尚未研究出针对COVID-19的特异性药物,疫苗的研发也正在开展,具体效果未知。因此,对于COVID-19患者最主要的措施是患者隔离和改善肺通气功能,抑制潜在的炎症分子风暴反应及支持治疗。目前《新型冠状病毒肺炎合并肝脏损伤的预防及诊疗方案》[31]不建议预防性使用保肝降酶药物,但注重对于基础性肝病例如病毒性肝炎、酒精性脂肪肝、肝硬化等的治疗,要监测肝功能的变化以便能及时发现肝损伤。
ACE2受体抑制剂能够激活ACE2/Ang(1-7)/Mas信号通路或抑制ACE/Ang/AT1R通路可能是治疗COVID-19的重要途径,但已有体外实验证明ACE2受体对心肺有着很大的保护作用,因此也具有其局限性。针对SARS-CoV-2感染者,在严密检测血压的情况下可以考虑应用ACEI及AT1R抑制剂以减轻全身炎症反应,降低患者病死率[32],也是目前可以考虑的措施之一。
4 小结
尽管目前以肝脏受损为首发的病例少见,但不能忽视COVID-19患者可能合并的肝功能异常,基于COVID-19引起的肝损伤是多种机制造成的,其可能的机制包括SARS-CoV-2感染的直接损伤、免疫异常导致的免疫损伤、合并用药导致的药物性损伤、炎症因子风暴引起的炎性损伤及合并基础性疾病导致的其他肝脏损伤等。因此,除了重视对原发病变的治疗外,对于其他可能诱发COVID-19患者肝功能异常的因素也应加强警惕,避免严重肝损伤的发生。

