食品接触用硅橡胶中3种环硅氧烷的测定及迁移规律
刘宜奇,胡长鹰,*,商贵芹,张 泓,曾 莹,贝荣华,朱 蕾,钟怀宁
(1.暨南大学,食品科学与工程系,广东广州 510632;2.常州进出口工业及消费品安全检测中心,江苏常州 213000;3.国家食品安全风险评估中心,北京 100022;4.广州海关技术中心,国家食品接触材料检测重点实验室,广东广州 510070)
硅橡胶是低分子环硅氧烷开环聚合形成高摩尔质量的聚硅氧烷后,经补强、成型、硫化等工序制成的有机硅弹性体,其主链为交替的Si-O键,相对分子质量较大(一般超过1.5×105)[1],而Si-O键的键能比C-C键的键能高,故硅橡胶的热稳定性比一般合成的橡胶高。硅橡胶因具有良好的耐热性和柔顺性,故广泛地应用于食品接触材料,如高压锅密封圈、烤盘、蛋糕模具、蒸垫以及婴儿奶嘴等。D4~D6等小分子环硅氧烷可能具有致癌性和生物富集毒性[2-5]。D4是一种低分子量环硅氧烷,具有高亲脂性[6-7],可在小鼠子宫中引发雌激素活性,高浓度的D4会降低血清E2的水平[8-9]。此外,D5可作为多巴胺受体激动剂,对人体神经系统产生不利影响[10]。D5可通过多巴胺受体激动剂的机制来改变垂体对大鼠的动情周期的控制[11]。Warner等[12]发现北极地区的海豹脂油样品有D6,这表明D6具有生物富集性。对于环硅氧烷的安全性,目前主要关注的是其生物和环境样品、医药产品、医疗器械、化妆品和个人护理产品中存在硅氧烷状况[13-14],但对食品接触用硅橡胶中环硅氧烷的安全性重视还不够。
固相微萃取-气质联用法[15-16]、吹扫捕集-气质联用法[17-18]和溶剂提取-气质联用法[19]主要用于对硅橡胶中挥发性物质的高通量筛选分析和低分子量硅氧烷的定量分析,但对潜在危害性较大的D4~D6的定量分析研究不多,以及其在油性食品模拟物中的迁移规律有待进一步研究。杨建平等[20]发现上海市的30批次烘焙用硅橡胶制品中有83.3%的样品中的挥发性物质的含量都大于0.5%,且80%样品中挥发性物质含量都超出参考值的3~5倍。这表明硅橡胶制品中含有较多的挥发性物质,其产品质量有待进一步提高。郑春翠等[21]发现硅橡胶密封垫圈中低聚物单体在油性食品模拟物正己烷中的迁移力特别强。该迁移试验是以全浸泡的方法,而硅橡胶制品与食品通常是单面接触的,为了更客观反映硅橡胶中环硅氧烷D4-D6向食品迁移的过程,需要进行硅橡胶制品的单面迁移试验。因此,本文通过建立溶剂提取-气相质谱法测定硅橡胶制品中D4~D6含量,并研究硅橡胶制品中D4-D6向油性食品模拟物95%乙醇的单面迁移规律,为相关法律法规的修订提供参考。
1 材料与方法
1.1 材料与仪器
3种奶嘴样品分别标记为A1、A2和A3,3种高压锅密封圈样品分别标记为B1、B2和B3,3种烤盘样品分别标记为C1、C2和C3 购于淘宝;八甲基环四硅氧烷(纯度≥98.0%)、十甲基环五硅氧烷(纯度≥99.0%) 上海阿拉丁有限公司;十二甲基环六硅氧烷(纯度≥97%) 上海源叶生物科技有限公司;二氯甲烷、甲醇和正己烷 色谱纯,美国Fisher 公司;乙酸乙酯(AR)、丙酮(AR) 广州化学试剂厂;无水乙醇(GR) 天津市科密欧化学试剂有限公司;一级超纯水 德国Merck公司Milli-Q型超纯水仪制备;高纯氦气(纯度≥99.999%) 空气化工气体(东莞)有限公司。
7890A-5975C气相色谱-质谱联用仪 美国Agilent公司;iS50傅里叶红外分析仪 赛默飞世尔科技(中国)有限公司;EL104电子分析天平(0~120 g,精度0.0001 g) 梅特勒-托利多仪器(上海)有限公司;KB3漩涡仪 海门市其林贝尔仪器制造有限公司;SK250LH 超声波清洗器 上海导超声仪器有限公司;尼龙滤膜(孔径0.45 μm) 天津津腾实验设备有限公司;移液器(20~200 μL;100~1000 μL;2.5~25 mL) 德国Brand Transferpette公司。
1.2 实验方法
1.2.1 样品前处理 用无水乙醇擦拭食品接触用硅橡胶产品,除去表面杂质,晾干后,在铝箔上剪成碎片(约3 mm×3 mm)。
1.2.2 衰减全反射-傅里叶变换红外光谱分析鉴定硅橡胶的结构 通过衰减全反射-傅里叶变换红外光谱分析[22],判断样品是否为硅橡胶材质。ATR-FTIR的相关参数:分辨率为8.000,采集增益为8.0,扫描次数为32次。
1.2.3 提取溶剂的优化 硅橡胶的交联度高,在溶剂中可发生溶胀,但不溶解[23]。取0.5000 g剪碎的硅橡胶样品于25 mL具塞试管中,分别加入10.0 mL甲醇、丙酮、乙酸乙酯、二氯甲烷、正己烷、正己烷/丙酮(1∶1)、正己烷/乙酸乙酯(1∶1)和正己烷/二氯甲烷(1∶1),这些溶剂分别标记为1号、2号、3号、4号、5号、6号、7号和8号溶剂,在漩涡仪上振荡15 s,使硅橡胶完全浸泡在提取液中,以选择对D4~D6提取能力最佳的溶剂。为避免在持续超声下引起的高温使D4~D6挥发,通过添加冰袋使超声温度控制在(16±2) ℃,超声30 min后取出振荡15 s,取1 mL提取液过0.45 μm有机滤膜后置于气质进样瓶中,上GC/MS检测。
1.2.4 超声时间的优化 取0.5000 g剪碎的硅橡胶于25 mL具塞试管中,加入10.0 mL正己烷,在漩涡仪上振荡15 s,使硅橡胶完全浸泡在正己烷中,分别在(16±2) ℃下超声15、30、45、60、75和90 min,取出振荡15 s后,取1 mL提取液过0.45 μm有机滤膜后置于气质进样瓶中,上GC/MS检测。
1.2.5 色谱条件 GC/MS条件:HP-5MS色谱柱(30 m×250 μm×0.25 μm,美国Agilent公司);载气为高纯氦气,纯度≥99.999%;载气流速为1.5 mL/min,进样口温度为230 ℃;分流比为2∶1;升温程序为40 ℃保持1 min,以20 ℃/min升温至315 ℃,保持4 min。离子源为电子轰击(EI);电子能量为70 ev;四极杆温度为150 ℃;离子源温度为230 ℃,传输线温度为230 ℃;采用离子检测(SIM)模式,其中D4的m/z为281.00,282.00,133.00;D5的m/z为355.0,267.00,73.00;D6的m/z为341.00,429.00,325.00,73.00;溶剂延迟4.5 min。
1.2.6 D4~D6在正己烷溶剂中的标准曲线 分别称取7.2886 mg的D4、7.2150 mg的D5和7.3638 mg的D6于10 mL容量瓶中,用正己烷定容,分别配制成质量浓度为714.3 μg/mL的D4~D6的单标,再从D4~D6单标中分别取2.800 mL于10 mL容量瓶中,用正己烷定容配制成200.0 μg/mL的D4~D6混合标准储备液,保藏于4 ℃的冰箱中。通过正己烷稀释后,配制成0.5、1.0、5.0、10.0和20.0 μg/mL的D4~D6混标的标准曲线溶液。
1.2.7 方法回收率及精确度的测定 扣除色谱图中的空白背景后,以信噪比为3作为D4~D6在仪器中的检出限,信噪比为10作为D4~D6在仪器中的定量限。由于硅橡胶制品在制备过程中不可避免残留硅氧烷低聚物,没有空白样品,故选择含量最低的样品进行加标试验。向B3号样品加入2.5、5.0和10.0 μg/mL三个不同浓度的D4~D6标准溶液,按优化后的方法进行处理,平行测定6次,计算其回收率和精密度。
1.2.8 硅橡胶样品中D4~D6的含量 3种不同用途的9个食品接触用硅橡胶产品,按照优化后的方法进行检测,平行3次。若提取液浓度大于20.0 μg/mL,则进行稀释,使稀释后的提取液浓度在标准曲线范围内。
式(1)
其中:C:硅橡胶样品中D4~D6的初始含量(mg/kg);N:由标准曲线计算出的D4~D6浓度(μg/mL);W:所称取硅橡胶样品的质量(g);n:为提取液稀释倍数;10.0:为提取溶剂体积(mL)。
1.2.9 迁移实验 由于《GB 4806.11-2016食品安全国家标准 食品接触用橡胶材料及制品》[24]中只明确了总迁移条件,对特定物质的迁移条件尚未有规定,结合《GB 310604.1-2015 食品安全国家标准 食品接触材料及制品迁移试验通则》[25],以及硅橡胶烤盘在实际应用中接触的食品属于高脂性食品,同时在预试验中发现硅橡胶在油性食品模拟物异辛烷、正己烷和正庚烷会出现溶胀现象,而在95%乙醇中未发现溶胀现象,故选择95%乙醇作为油性食品模拟物在60 ℃中进行迁移试验。
由《GB 5009.156-2016 食品安全国家标准 食品接触材料及制品迁移试验预处理方法通则》[26]的要求,选择迁移测试池对硅橡胶进行单面迁移试验。把烤盘C3剪成6.50 cm×6.50 cm大小,将样品放置迁移测试池夹板中间,安装迁移测试池,并以铝箔作为空白迁移样。由于硅橡胶烤盘在迁移测试池内的接触面积为0.1256 dm2,该接触面积对应硅橡胶烤盘的质量为1.6317 g,根据《GB 310604.1-2015》中认为食品接触材料及制品的接触面积与食品或食品模拟物体积之比为6[25],故模拟液的体积为21.00 mL。为使模拟液的初始温度更接近迁移时的温度,将95%乙醇在(60±1) ℃恒温水浴锅预热3 h后,取21.00 mL 95%乙醇倒入迁移测试池中,拧紧螺帽,迅速将迁移测试池放置在(60±1) ℃的电热鼓风干燥箱中。在迁移时间为15、30、60、90、120、150、180、210和240 min时(每个时间段3个平行,每个试样都是独立的),趁热将迁移测试池中95%乙醇全部转移出来,冷却至室温后,混匀,稀释后取1 mL模拟物过0.45 μm有机滤膜后置于气质进样瓶中,上GC/MS检测。
式(2)
其中:M:为D4~D6的迁移率(%);C:硅橡胶样品中D4~D6的初始含量(mg/kg);c:为95%乙醇食品模拟物中D4~D6的浓度(μg/mL);n:为提取液稀释倍数;21.00:为食品模拟物的体积(mL);1.6317:为硅橡胶烤盘面积为0.1256 dm2时的质量(g)。
1.2.10 D4~D6在95%乙醇中的标准曲线及精密度 分别称取7.2886 mg的D4、7.2150 mg的D5和7.3638 mg的D6于10 mL容量瓶中,用95%乙醇定容,分别配制成质量浓度为714.3 μg/mL的D4~D6单标,再从D4~D6单标中分别取2.800 mL于10 mL容量瓶中,用95%乙醇定容配制成200.0 μg/mL的D4~D6混合标准储备液,保藏于4 ℃的冰箱中。通过95%乙醇稀释后,配制成0.5、1.0、3.0、7.0和15.0 μg/mL的D4~D6混标的标准曲线溶液。
以95%乙醇中D4~D6混标的三个不同质量浓度0.5、3.0和15.0 μg/mL来检验仪器的精密度。
1.3 数据处理
使用Origin 2018作图,Minitab 17.0进行统计学分析。
2 结果与讨论
2.1 硅橡胶产品的衰减全反射-傅里叶变换红外光谱分析
由ATR-FTIR法可以判断橡胶产品的材质。由图1可知,2962 cm-1是CH3中C-H的对称振动吸收峰,1260 cm-1是CH3的不对称振动吸收峰,1008 cm-1是O-Si-O的对称振动吸收峰,788 cm-1是Si-C对称振动吸收峰[27],且3种类型的硅橡胶产品的红外谱图基本一致,可确认这些产品均为硅橡胶产品。
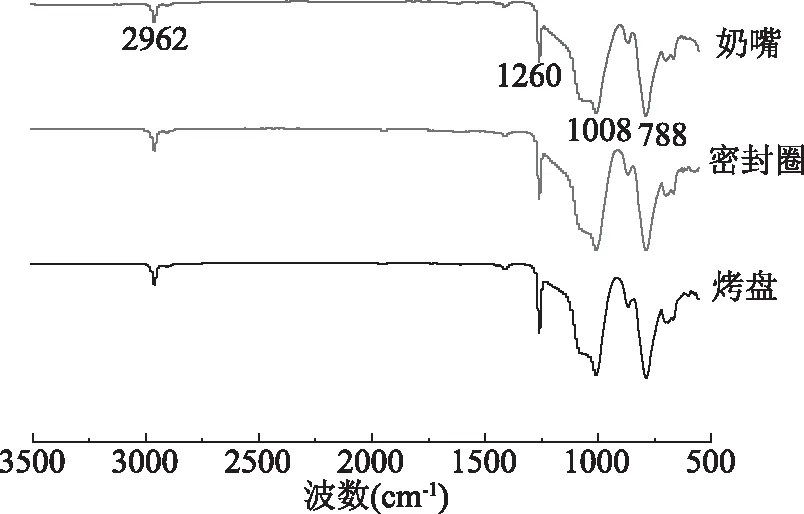
图1 硅橡胶产品的衰减全反射-傅里叶变换红外光谱图Fig.1 ATR-FTIR of silicone rubber products
根据提取溶剂的极性大小,选择甲醇、丙酮、乙酸乙酯、二氯甲烷、正己烷、正己烷/丙酮(1∶1)、正己烷/乙酸乙酯(1∶1)和正己烷/二氯甲烷(1∶1)作为提取溶剂。由图2可知,5号溶剂(正己烷)对硅橡胶中D4~D6的提取能力最好,其次是3号溶剂(乙酸乙酯)和2号溶剂(丙酮),而4号溶剂(二氯甲烷)对硅橡胶中D4~D6的提取能力最弱。故选择5号溶剂(正己烷)作为硅橡胶中D4~D6的提取溶剂。
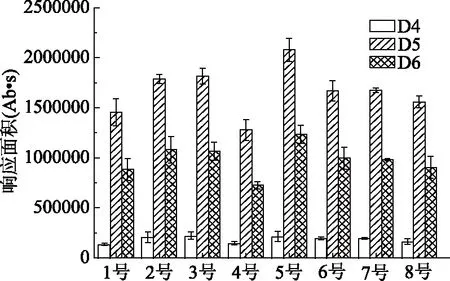
图2 溶剂对D4~D6的提取效果的影响Fig.2 Extraction effect of solvents on D4~D6
2.3 超声时间的优化
由图3可知,超声提取时间为15~30 min时,D4~D6的响应峰面积均随着提取时间的延长而增加;提取时间为30 min时,D4~D6的响应丰度均达到最大值,具有极显著性差异(P<0.01);随后,D4~D6的峰面积均随着时间的延长而呈下降趋势。长时间的提取可充分萃取出硅橡胶中的D4~D6,但是随着提取时间的过长,溶出的部分会被硅橡胶再吸附,造成损失[28],同时,随着超声时间的延长,超声温度升高,会加快D4~D6的分子运动,进而导致部分硅氧烷挥发,造成溶剂中D4~D6的损失,进而导致D4~D6的提取效果降低。故试验选择超声提取时间为30 min。
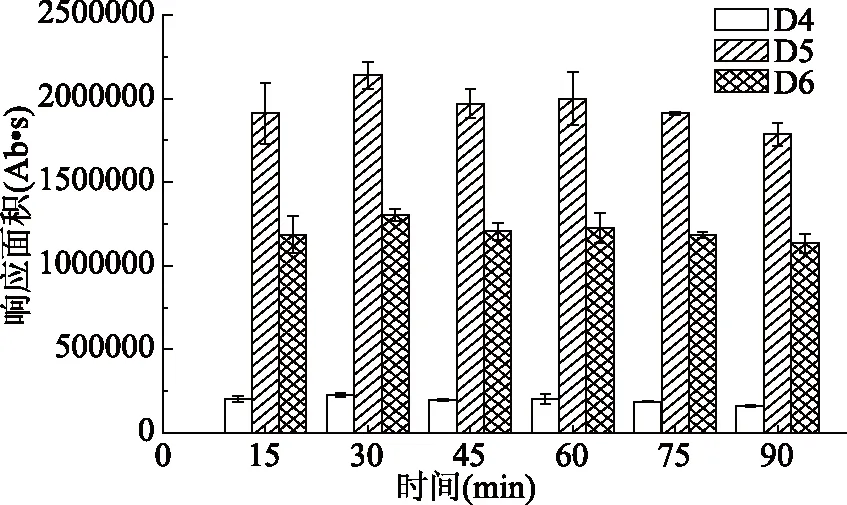
图3 超声时间对D4~D6的提取效果的影响Fig.3 Extraction effect of ultrasonic time on D4~D6
2.4 方法的验证
D4~D6的质量浓度均在0.5~20.0 μg/mL范围内与其峰面积呈线性关系,线性回归方程曲线和相关系数,以及方法的检出限和定量限见表1。在加标回收试验中,D4~D6的回收率为85.20%~98.12%,相对标准偏差(RSD)为2.17%~4.27%,这表明该方法对硅橡胶中D4~D6的定量具有较好的可信度。
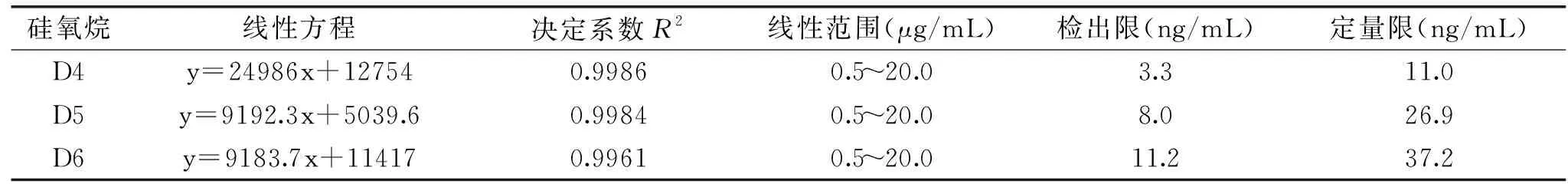
表1 D4~D6在正己烷中的线性参数、检出限及定量限Table 1 Linear parameters,detection limit and quantitative limit of D4~D6 in n-hexane
2.5 迁移实验用硅橡胶样品的确定
本试验收集了3种不同类型的9个品牌食品接触用硅橡胶产品,经ATR-FTIR确定其材质为硅橡胶,通过上述优化的提取条件和检测方法对其D4~D6的含量进行测定。从表2看出,D4~D6的检出率为100%,不同类型的硅橡胶中的D4~D6含量相差较大。奶嘴和高压锅密封圈中的D4~D6含量较低,其D4的含量范围分别为53.27~113.07和12.32~101.81 mg/kg,均值分别为82.71和68.38 mg/kg;其D5的含量范围分别为82.20~146.87和23.11~266.65 mg/kg,均值分别为114.82和131.57 mg/kg;其D6的含量范围分别为53.57~93.40和37.11~259.46 mg/kg,均值分别为71.74和134.65 mg/kg。而烤盘类硅橡胶中D4~D6的含量较大,D4的含量范围分别是91.51~341.45 mg/kg,均值是175.08 mg/kg;D5的含量范围是514.22~1376.68 mg/kg,均值是824.12 mg/kg;D6的含量范围是696.24~1183.69 mg/kg,均值是901.17 mg/kg。
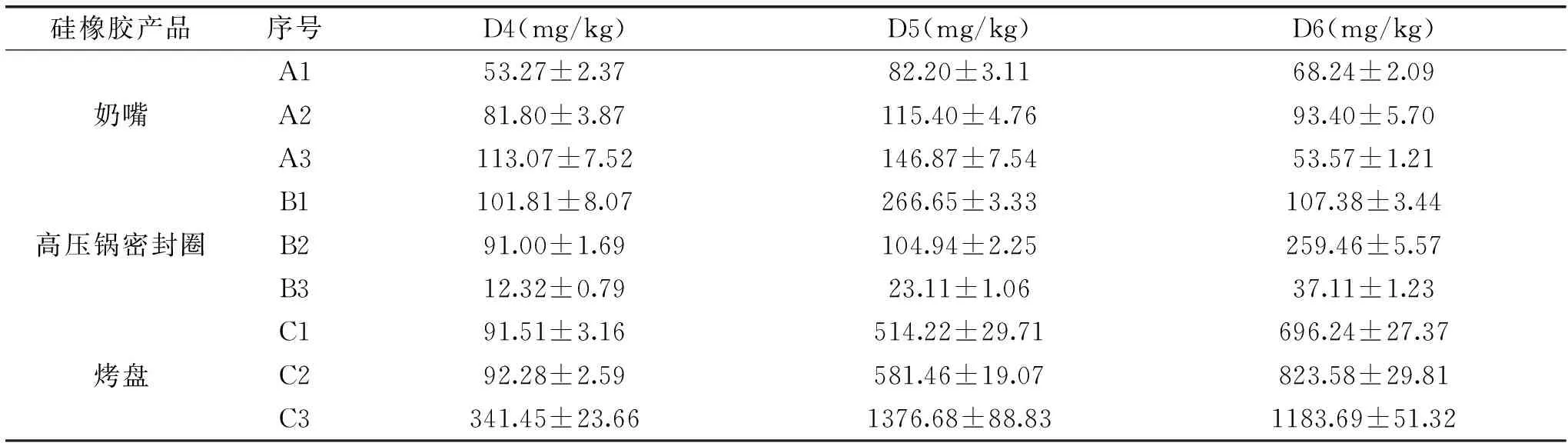
表2 不同类型和不同品牌硅橡胶中D4~D6的含量(n=3)Table 2 Contents of D4~D6 in different types and brands of silicone rubber products(n=3)
相关研究[29]表明,使用硅橡胶烘烤模具焙烤蛋糕时,环硅氧烷会迁移到蛋糕中。由此可猜测,烤盘类硅橡胶中高含量的D4~D6可能在焙烤蛋糕时,更容易迁移至蛋糕中,对人体健康存在一定的风险,故选择高D4~D6含量的烤盘C3作为迁移样品。
2.6 油性食品模拟物对D4~D6迁移的影响
硅氧烷的迁移取决于温度、食品中油脂含量、接触时间、食品接触材料硅橡胶中硅氧烷的含量、硅氧烷的分子量以及食品模拟物和接触材料硅橡胶之间硅氧烷的分配系数[30]。因D4~D6具有亲脂性[6],且在预试验中发现烤盘C3中的D4~D6基本不向水性和酸性食品模拟物中发生迁移,故本文主要研究硅橡胶烤盘C3中D4~D6向油性食品模拟物95%乙醇的迁移状况。
在95%乙醇体系中,D4~D6在0.5~15.0 μg/mL质量浓度范围内线性良好,回归方程分别为:y=111532x-34284、y=51318x-15446和y=45341x-14477,相关系数均大于0.9963,扣除空白背景后,其检出限(信噪比为3)分别为5.5、11.8和15.8 ng/mL,定量限(信噪比为10)分别为18.5、39.4和52.6 ng/mL。其相对标准偏差(RSD)为1.54%~8.74%,表明该方法可有效检测95%乙醇中D4~D6的含量。
图4展示了硅橡胶烤盘C3中D4~D6在60 ℃的95%乙醇油性食品模拟物中的迁移行为,符合一般迁移规律。D4~D6在迁移时间为150 min实现了迁移平衡,迁移率分别为71.36%、57.03%和49.31%。这说明了硅橡胶烤盘中D4在60 ℃的95%乙醇中最易于迁出,D5次之,D6最小,这与它们的分子量大小有关。上述结果也表明了硅橡胶烤盘中D4~D6易向油性食品发生迁移。
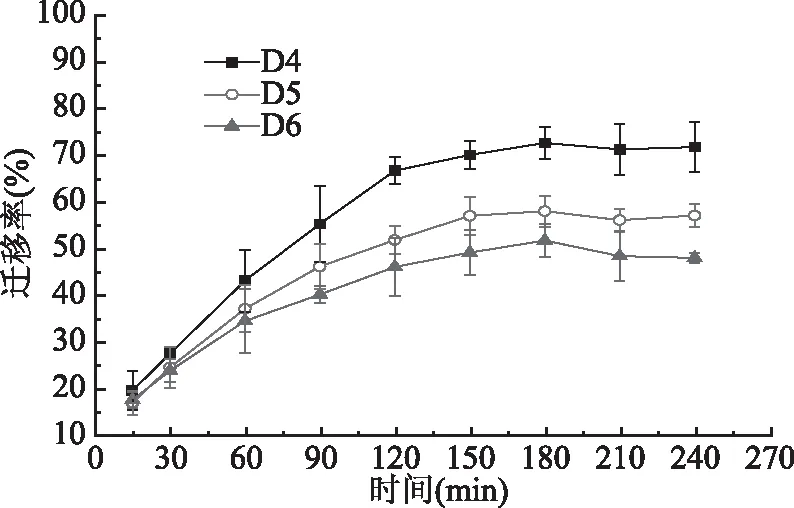
图4 硅橡胶烤盘中D4~D6在60 ℃的95%乙醇中的迁移率Fig.4 The migration rate of D4~D6from silicone rubber baking tray to 95% ethanol at 60 ℃
3 结论
本文通过衰减全反射-傅里叶变换红外光谱确定样品是否为硅橡胶材质;采用溶剂提取-气质联用法,在优化提取溶剂为正己烷和超声提取时间为30 min下,建立对食品接触用硅橡胶中D4~D6含量的简便快速检测方法。采用本文建立的方法检测食品接触用硅橡胶产品,发现烤盘类硅橡胶中D4~D6的含量最高,其D4~D6的均值分别为175.08、824.12和901.17 mg/kg,可能对人体健康有隐患。通过迁移试验,发现硅橡胶烤盘中D4~D6在60 ℃油性食品模拟物95%乙醇中实现迁移平衡时,D4~D6的迁移率分别为71.36%、57.03%和49.31%。接下来将对烤盘类硅橡胶中的D4~D6在油性食品模拟物橄榄油和固体食品模拟物Tenax®中的迁移以及在真实食品加工过程中迁移作进一步研究。

