荧光猝灭法测定维生素C片和果汁饮料中抗坏血酸的含量
张爱菊,张小林
(甘肃医学院,平凉744000)
抗坏血酸(AA)又称为维生素C(Vc),结构中的烯二醇使其具有还原性。抗坏血酸不能在人体中合成,只能从外界获取,获取途径有两条,一是水果和蔬菜;二是药剂。抗坏血酸的测定方法主要有滴定法[1-2]、光谱法[3-5]、电化学分析法[6-7]和色谱法[8-9]等。滴定法灵敏度低,且标准溶液不稳定,不适合低含量抗坏血酸的测定。荧光法[10-11]具有检出限低,抗干扰能力强等特点。
罗丹明B(RB)具有荧光特性,其阳离子与I3-通过静电引力形成离子缔合物,可使其荧光消失,基于碘化钾-罗丹明B体系荧光猝灭法测定氧化性物质的研究已有报道[12-18],但尚未见碘化钾-罗丹明B荧光反猝灭法用于还原性药物测定的研究报道。研究发现[19-20],在弱酸性条件下将碘溶液和罗丹明B混合即可使罗丹明B发生荧光猝灭,但在碘化钾-罗丹明B缔合物形成前加入抗坏血酸,溶液重新发出荧光,其荧光强度与抗坏血酸的浓度在一定范围内呈线性关系。本工作基于氧化还原和缔合反应原理,在不需催化、加热及长时间等待的情况下完成药剂和果汁中抗坏血酸的快速测定,其过程不受样品浑浊度和色度的影响,准确度高且检出限较低(5.6×10-9mol·L-1)。目前,类似方法尚无相关报道。
1 试验部分
1.1 仪器与试剂
930N型荧光光度计;FA 2004N型分析天平;pHS-3C型精密pH计。
罗丹明B标准储备溶液:1.0×10-3mol·L-1,称取0.119 8 g罗丹明B固体,加水溶解并稀释至250.0 mL,混合均匀。
罗丹明B标准溶液:1.0×10-4mol·L-1,称取10.00 mL罗丹明B标准储备溶液于100 mL容量瓶中,用水定容,混合均匀。
抗坏血酸标准储备溶液:5.00×10-2mol·L-1,称取0.880 0 g抗坏血酸,用水溶解并稀释至100.0 mL,混合均匀。
抗坏血酸标准溶液:5.00×10-4mol·L-1,移取抗坏血酸标准储备溶液1.00 mL于100 mL容量瓶中,用水定容,混合均匀。
抗坏血酸标准溶液系列:分别移取抗坏血酸标准 溶 液 0,0.50,1.00,2.00,3.00,4.00,5.00 mL 于6个不同的50 mL容量瓶中,用水定容,配制成0,5,10,20,30,40,50μmol·L-1的抗坏血酸标准溶液系列。
乙酸-乙酸钠缓冲溶液:0.1 mol·L-1,pH 为4.7。
碘标准溶液[21]:1.0×10-3mol·L-1。
所用试剂均为分析纯,试验用水为二次蒸馏水。
1.2 试验方法
移取一定体积的样品稀释液(含抗坏血酸约0~0.35 mg)于50 mL容量瓶中,加入1.0×10-3mol·L-1碘标准溶液2.0 mL,混合摇匀,再依次加入罗丹明B标准溶液5.00 mL,乙酸-乙酸钠缓冲溶液(pH为4.7)5.0 mL,用水定容,混合摇匀后静置10 min。以1.0×10-6mol·L-1罗丹明B标准溶液作为灵敏度调试液,按照仪器工作条件对其进行测定。
2 结果与讨论
2.1 荧光光谱
按照试验方法对罗丹明B溶液、罗丹明B-I3--抗坏血酸和罗丹明B-I3-溶液在455~655 nm内进行扫描,并绘制不同体系的荧光光谱,见图1。其中罗丹明B、I3-和抗坏血酸的浓度分别为1.0×10-5,4.0×10-5,2.0×10-5mol·L-1。
结果表明:当激发波长为365 nm时,罗丹明B在580 nm处有最大荧光强度;向罗丹明B溶液中加入I3-溶液后,罗丹明B溶液的荧光猝灭,荧光发射波长未发生改变;在I3--罗丹明B缔合物形成之前加入一定量的抗坏血酸后,荧光得以重现,且荧光强度与抗坏血酸加入量有关。
2.2 试验条件的选择
2.2.1 罗丹明B的浓度及其用量

图1 荧光光谱Fig.1 Fluorescence spectra
罗丹明B的荧光特性与其浓度息息相关[22]。当罗丹明B的浓度不小于1.5×10-5mol·L-1时,罗丹明B会形成二聚体或多聚体,激发波长和发射波长逐渐红移,自熄灭作用增强,罗丹明B的浓度与其对应的荧光强度之间的线性消失,为了保证样品测定过程中有足够宽度的线性范围和更低的检出限,试验选择1.0×10-4mol·L-1的罗丹明B溶液的用量为5.00 mL,此时反应液中罗丹明B的浓度为1.0×10-5mol·L-1。
2.2.2 碘标准溶液的体积
在不含抗坏血酸的情况下,试验考察了碘标准溶液的体积对罗丹明B荧光强度的影响,结果见图2。

图2 碘标准溶液的体积对罗丹明B荧光强度的影响Fig.2 Effect of volume of iodine standard solution added on fluorescence intensity of rhodamine B
由图2可知:随着碘标准溶液体积的增加,罗丹明B的荧光强度逐渐降低;当碘标准溶液体积为0~2.0 mL时,线性度较高;当碘标准溶液体积增加至4.0 mL时,罗丹明B的荧光强度开始趋于稳定;当碘标准溶液体积增加至6.0 mL时,罗丹明B的荧光强度几乎不再发生变化。为了得到较为准确的测定结果,试验选择的碘标准溶液体积为2.0 mL。
2.2.3 体系的酸度
罗丹明B的荧光强度体现在羧基上[22],抗坏血酸在酸性条件下相对稳定。取抗坏血酸标准溶液2.00 mL,固定其他条件,在溶液中加入不同体积的0.1 mol·L-1HCl和0.1 mol·L-1NaOH 溶液,按试验方法考察了在不同酸度体系下罗丹明B的荧光强度,结果见图3。
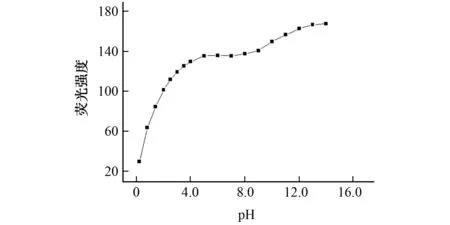
图3 体系的酸度对罗丹明B荧光强度的影响Fig.3 Effect of acidity of the system on fluorescence intensity of rhodamine B
由图3可知:随着体系pH的增加,游离态罗丹明B的羧基开始电离,并且电离程度逐渐增大,吸电子能力逐渐减弱,荧光强度逐渐增大;当体系pH为4.0~8.0时,罗丹明B的荧光强度趋于稳定;当体系的pH大于9.0时,缔合物中的碘发生歧化,罗丹明B的荧光强度继续增大。这说明pH为4.0~8.0时,有利于罗丹明B和I3-发生缔合,也有利于抗坏血酸氧化,试验选择了pH为4.7的乙酸-乙酸钠缓冲溶液作为反应介质。
2.2.4 反应温度与反应时间
移取抗坏血酸标准液2.00 mL进行试验,试验考察了反应温度与反应时间对罗丹明B荧光强度的影响。结果发现:当反应温度为20~35℃时,罗丹明B的荧光强度较大且变化幅度较小。试验选择的反应温度为常温(25℃)。
抗坏血酸与I3-反应速率较快,加入罗丹明B标准溶液后黄色瞬间变浅以至消失。在室温下,罗丹明B与I3-在8 min内反应完全,且其荧光强度在40 min内保持稳定。试验选择加入罗丹明B静置10 min后测定体系的荧光强度。
2.2.5 试剂的加入顺序
试验考察了抗坏血酸、碘和罗丹明B等3种试剂的加入顺序对体系荧光强度的影响。结果发现:以抗坏血酸、碘和罗丹明B的顺序加入时,体系最稳定,且荧光强度相对较高,这是由于I3-和缔合物罗丹明B-I3-与抗坏血酸之间的反应速率存在差异,I3-与罗丹明B形成的离子缔合物是疏水的,在溶液中很快沉淀[23],抗坏血酸无法与其完全反应。试验选择以抗坏血酸、碘和罗丹明B的顺序加入这3种物质。
2.3 共存离子的影响
针对药物中经常使用的赋形剂、添加剂及水果中的共存物质,试验选择了淀粉、葡萄糖、糊精、乳糖和硬脂酸等干扰物质以及Ca2+、Mg2+和Al3+等阳离子进行干扰试验。固定抗坏血酸用量,在优化条件下进行干扰试验。结果表明:测定误差在±5%内时,50倍的乳糖、硬脂酸、淀粉、糊精及100倍的上述3种金属阳离子对测定结果均无干扰。
2.4 标准曲线和检出限
按照试验方法对抗坏血酸标准溶液系列进行测定,以抗坏血酸的浓度为横坐标,与其对应的荧光强度为纵坐标绘制标准曲线。结果表明:抗坏血酸的浓度在40μmol·L-1内与其对应的荧光强度之间呈线性关系,线性回归方程为y=5.330x+33.81,相关系数为0.995 3。
以3倍的标准偏差与标准曲线斜率的比值计算方法的检出限(3s/k)为5.6×10-9mol·L-1。
2.5 样品分析
2.5.1 药剂分析
取标示量为50 mg/片的抗坏血酸片(维生素C片)5片,研磨后混合均匀,取其十分之一(相当于25 mg)药粉于小烧杯中,用水溶解并转移至250 mL容量瓶中,用水定容,所得溶液过滤后,取1.00 mL滤液,按照试验方法进行测定,结果见表1。
取抗坏血酸注射液(2 mL,0.5 g/支)0.10 mL于250 mL容量瓶中,用水稀释至刻度,混合摇匀。移取上述溶液1.00 mL,按照试验方法进行测定,结果见表1。
试验进一步对上述抗坏血酸片剂和抗坏血酸针剂样品进行加标回收试验,每个加标样品平行测定6次,计算回收率和测定值的相对标准偏差(RSD),结果见表1。

表1 实际样品中抗坏血酸的分析结果(n=6)Tab.1 Analytical results of ascorbic acid in substantial samples(n=6)
由表1可知:抗坏血酸片剂样品和抗坏血酸针剂中抗坏血酸的加标回收率分别为97.4%,98.4%,测定值的RSD分别为2.3%,1.7%,说明方法具有良好的精密度。根据测定结果推算出样品中抗坏血酸的含量,片剂抗坏血酸为49.63 mg/片,针剂抗坏血酸为0.51 g/支,与其标示量基本一致,说明方法具有良好的准确度。
2.5.2 果汁分析
分别采用本法和碘量法对橙汁味、蜜桃味和葡萄味等3种果汁饮料样品进行测定,计算2种不同分析方法测定结果的相对误差,结果见表2。

表2 抗坏血酸的测定结果Tab.2 Results of determination of ascorbic acid
由表2可知:所有样品中实际测得抗坏血酸含量均在商品标示含量范围内,且相对误差均小于5%。
罗丹明B-碘溶液体系间接测定抗坏血酸反应现象明显,操作步骤简便,所得结果准确,检出限低,建立了一种灵敏度高、选择性好、线性范围较宽的测定抗坏血酸的方法。该方法在测定过程不使用任何有毒溶剂,相对于其他相关抗坏血酸的测定方法更环保。

