PAA/PEG复合水凝胶膜的制备及其性能
杨 珊,王 琳,王 鹏,党民团
(1. 渭南师范学院 化学与材料学院,陕西省煤基低碳醇转化工程研究中心,陕西省渭南市 714099;2. 渭南师范学院 附属医院,陕西省渭南市 714099)
水凝胶是一种能在水中溶胀、保持大量水分但却不溶于水的具有三维网状结构的高分子材料[1]。水凝胶是最早用于人体的生物材料,具有良好的生物相容性、生物降解性,低毒或无毒、易成型加工等特点[1],被广泛应用于生产、生活和医疗领域[2-3]。然而,由于水凝胶机械强度较低,极大限制了其作为生物材料在医疗领域的应用[1]。提高水凝胶的机械强度是近些年国内外众多研究者关注的问题[2,4]。由于高分子材料的强度上限取决于主链化学键力和分子链间的作用力,在一般情况下,增加高分子的极性或形成氢键可以提高其强度[5]。目前,已报道的提高水凝胶强度的方法有:适度化学交联、形成互穿网络、氢键作用、与纳米粒子复合、纤维增强、冷冻-解冻法、自组装、共聚等[1-2,4,6-9]。聚丙烯酸(PAA)是一种亲水性较强的聚合物,具有优良的力学性能和生物相容性,被广泛用于制备水凝胶的生物医用材料[10-11],由于其含有羧基,因此容易形成分子间氢键。聚乙二醇(PEG)具有高亲水性和良好的生物相容性,被美国食品药品管理局批准可制备用于人体的组织工程材料和药物控释材料[3,6,12-14]。本工作拟通过适度化学交联和分子间氢键提高水凝胶的机械强度,采用自由基溶液聚合法原位聚合制备了PAA/PEG复合水凝胶膜,研究了PEG用量对复合水凝胶膜性能的影响。
1 实验部分
1.1 主要试剂与仪器
丙烯酸(AA),天津市天大化学试剂厂生产;PEG1000,分子式HO(CH2CH2O)nH,相对分子质量为900~1 100,成都市科龙化工试剂厂;N,N-亚甲基双丙烯酰胺(BIS),天津市科密欧化学试剂有限公司;过硫酸铵(APS),天津市福晨化学试剂厂:均为分析纯。实验用水为超纯水,电阻率18.25 MΩ·cm,自制。
90-2型集热式恒温磁力搅拌器,郑州长城科工贸有限公司;GZY-P60-V型超纯水机,湖南克尔顿水务有限公司;KH-100E型超声波清洗器,昆山禾创超声仪器有限公司;Tensor Ⅱ型红外光谱仪,德国Bruker公司;RGM6000型微机控制电子万能材料试验机,深圳市瑞格尔仪器有限公司;STA449F5型同步DSC&TG热分析仪,德国Netzsch公司;Sigma500型扫描电子显微镜,德国Zeiss公司。
1.2 水凝胶膜的制备
按表1配方制备PAA/PEG复合水凝胶膜。在10 mL离心管中加入定量AA和PEG,加入AA质量0.75%的交联剂BIS以及AA质量2.00%的APS,超声混匀后置于60 ℃恒温水浴中反应30 min,得到有一定黏度的液体。将该黏稠液体倾倒在玻璃板上使其均匀铺展,然后在60 ℃烘箱中保温反应5 h成膜,膜自然冷却后放入纯水中浸泡、脱膜同时纯化除杂,随后自然晾干,得到透明、致密的浅黄色PAA/PEG复合水凝胶膜,膜厚0.2 mm。为方便比较,同时制备PAA水凝胶膜,除了不加PEG外,其余步骤同PAA/PEG复合水凝胶膜的制备过程。
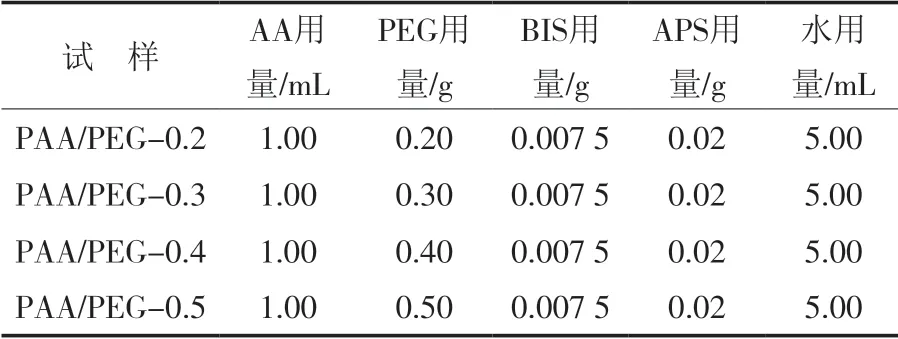
表1 PAA/PEG复合水凝胶膜的配方Tab.1 Formula of PAA/PEG composite hydrogel films
1.3 测试与表征
红外光谱(IR)分析:采用衰减全反射模式测试PAA水凝胶膜、4种干燥的PAA/PEG复合水凝胶膜以及纯PEG的IR,波数为600~4 000 cm-1,扫描16次。
热稳定性:采用热分析仪测定PAA/PEG复合水凝胶膜的受热行为。取试样5~10 mg,Al2O3坩埚,参比为空坩埚,N2气氛,流量为30 mL/min,升温速率为10 ℃/min,温度为20~600 ℃。
扫描电子显微镜(SEM)观察:裁切干燥的PAA/PEG复合水凝胶膜小片,用导电胶黏在铝制试样台上,喷金100 s,观察其表面形貌,工作电压4 kV,图片信号为SE2。
溶胀性能:采取称重法测定PAA/PEG复合水凝胶膜对水的溶胀性能。准确称量干燥的复合水凝胶膜并置于纯水中浸泡,每隔一定时间取出并称质量,计算溶胀比(SR),绘制溶胀速率曲线并求取平衡溶胀比(ESR),计算方法同文献[15]。
力学性能:用万能材料试验机对晾干后的PAA/PEG复合水凝胶膜按GB/T 1040.3—2006进行拉伸性能测试,试样按DIN-53504 S3裁剪,总长度35 mm,总宽度6 mm,标距长度10 mm,标距宽度2 mm,厚度0.2 mm。测试条件:室温,预加张力0.05 N,以80 mm/min拉伸薄膜直至断裂。应力(σ)和应变(ε)分别按式(1)和式(2)计算[2]。

式中:F为拉伸力,N;b,d分别为水凝胶膜的初始宽度和厚度,m;l0,l分别为水凝胶膜的初始长度和拉伸后的长度,m。
作σ-ε曲线,计算拉伸强度和断裂标称应变[2,5]。
2 结果与讨论
2.1 成膜性分析
当PEG与AA质量比接近1.0时,不能形成水凝胶膜。改变PEG与AA的配比、其他成膜条件按表1所列。结果表明:当AA用量较大时,容易形成均匀、透明的水凝胶膜,这与白晴文等[2]对聚乙烯醇-PAA凝胶膜成膜条件的研究结论一致。在成膜过程中,水凝胶膜极易发生卷曲,这与薄膜干燥过程中水蒸发引起的表面张力以及聚合物柔性大分子链的链段运动有关。当PEG与AA质量比为0.4,BIS和APS用量分别为AA质量的0.75%和2.00%时,60 ℃预聚合30 min后的体系成膜性最佳。纯PAA水凝胶膜很脆、易碎,PAA/PEG复合水凝胶膜则为柔性膜。
2.2 IR分析
结合文献[16]对PEG和PAA膜的IR曲线上各峰的归属,从图1可看出:3 380~3 500 cm-1为羧基上O—H和交联剂BIS中氨基N—H的伸缩振动峰的叠加;2 926,2 918 cm-1处为饱和亚甲基C—H的不对称伸缩振动峰;1 710 cm-1处为AA中羧基C=O的伸缩振动峰;1 157 cm-1处为C—O的伸缩振动峰,该峰的相对强度较纯PAA水凝胶膜的大;1 077 cm-1处为PEG中C—O—C的伸缩振动峰(1 096 cm-1)发生了位移;1 012 cm-1处则应为AA中C—O的变形振动峰(1 041 cm-1)发生了位移,这两个峰向低波数发生位移应与PEG,PAA间通过氢键复合有关[6,17-19];而815 cm-1处应为C—H的变形振动峰,是PEG中842 cm-1处峰和AA中796 cm-1处峰的合并出峰。比较可见,PAA/PEG复合水凝胶膜的IR曲线与PEG的IR曲线完全不同,与PAA的IR曲线在690~1 540 cm-1的吸收峰的峰形和相对强弱也明显不同,表明PAA/PEG复合水凝胶膜中同时含有PAA链段和PEG链段,即PAA/PEG复合水凝胶膜制备成功。同时,以815 cm-1处吸收峰为基准,随着PEG用量的增加,1 077,1 012 cm-1处峰的强度明显增大,说明PAA/PEG复合水凝胶膜中PEG含量随之增加。结合文献[2]可知,PAA/PEG复合水凝胶膜是通过PAA链间交联、PEG与PAA链间氢键以及链间物理缠结紧密结合在一起的三维网状结构(见图2)。
2.3 热稳定性
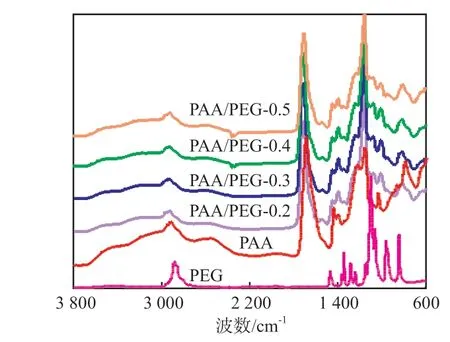
图1 PEG,PAA水凝胶膜和PAA/PEG复合水凝胶膜的IRFig.1 IR spectra of PEG,PAA hydrogel film and PAA/PEG composite hydrogel films

图2 PAA/PEG复合水凝胶膜的结构示意Fig.2 Structure of PAA/PEG composite hydrogel films
从图3看出:PAA/PEG复合水凝胶膜的热重曲线形状基本相同,都存在两段明显的质量损失,对应差示扫描量热法(DSC)曲线上有2个大的吸热峰,说明复合水凝胶膜的分解是分步进行的。PAA/PEG-0.2,PAA/PEG-0.3,PAA/PEG-0.4,PAA/PEG-0.5的初始分解温度分别为167,170,174,175 ℃,分解前约有1.3%~2.8%质量损失源于失去少量吸附水,第一步分解最快的温度分别为245,252,255,257 ℃,第二步分解最快的温度分别为413,429,427,424 ℃,600 ℃时的残炭率分别为7%,5%,2%,4%。水凝胶膜的分解包括了链裂解、取代基分解以及炭化过程[16]。由此可见,PAA/PEG复合水凝胶膜的分解温度不同,且随着PEG用量的增加而略有升高,说明PAA/PEG复合水凝胶膜被成功制备;在测试范围内,未检测出水凝胶膜发生玻璃化转变,说明在室温至分解前,水凝胶膜处于高弹态,链段运动相对自由。
2.4 SEM观察
从图4可以看出:PAA/PEG复合水凝胶膜的表面都比较平整,不存在孔结构;相比之下,PAA/PEG-0.3的平整性最差,PAA/PEG-0.4和PAA/PEG-0.5较好。4种水凝胶膜的表面或多或少存在0.4~1.0 μm的白色棒状物,推测是PEG链聚集引起的。4种水凝胶膜的SEM照片表面都存在明显的黑框,这是由于水凝胶膜比较软,在聚焦过程中有部分链受高能电子束激发分解所致。
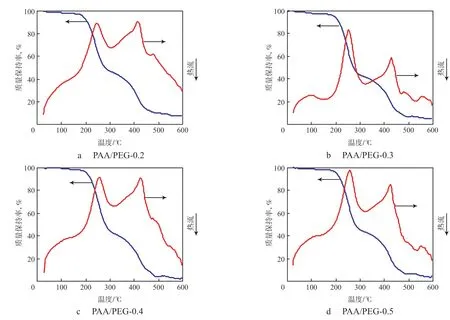
图3 PAA/PEG复合水凝胶膜的DSC和热重曲线Fig.3 DSC and TG curves of PAA/PEG composite hydrogel films

图4 PAA/PEG复合水凝胶膜的SEM照片(×2 000)Fig.4 SEM photos of PAA/PEG composite hydrogel films
2.5 溶胀行为
从图5可以看出:PAA/PEG-0.2,PAA/PEG-0.3,PAA/PEG-0.4,PAA/PEG-0.5的ESR都不大,分别为2.2,2.1,1.5,1.9,且平衡时间皆较长(10~12 h)。由于复合水凝胶膜很薄(厚度仅0.2 mm),且其表面并无孔结构(见图4),所以吸水溶胀性较差。比较4种水凝胶膜的ESR可知,虽然PEG亲水性好,但随着其用量的增大,水凝胶膜的吸水溶胀性反而变差。这是由于在水凝胶膜中,PEG链与PAA链间通过氢键结合,PEG用量的增加导致氢键数目增多、交联度增大,从而使吸水性变差,故PAA/PEG-0.4的ESR最低;而PAA/PEG-0.5的ESR又有所增大,推测是由于PEG用量过多导致PEG链与PAA链间的氢键数目反而有所减少。
2.6 力学性能

图5 PAA/PEG复合水凝胶膜的水溶胀行为Fig.5 Swelling kinetics of PAA/PEG composite hydrogel films in water
据报道[2],纯PAA水凝胶膜也具有一定的机械强度和较好的拉伸性能(拉伸强度为0.35 MPa,断裂标称应变为2 000%)。本工作制备的纯PAA水凝胶膜很薄、很脆,无法进行拉伸性能测试。然而,加入适量PEG的PAA/PEG复合水凝胶膜的力学性能明显提高。从图6和表2可以看出:4种PAA/PEG复合水凝胶膜的拉伸强度皆很小,远小于常见塑料[5],但断裂标称应变较大,故皆属于软而韧的橡胶类材料;4种水凝胶膜中,PAA/PEG-0.4的拉伸强度和断裂标称应变皆最大(分别为1.58 MPa,414%)。由此可见,适量PEG的加入有助于提高PAA水凝胶膜的强度和韧性。与白晴文等[2]制备的聚乙烯醇-PAA水凝胶膜相比,本工作制备的PAA/PEG-0.4复合水凝胶膜的断裂标称应变要小得多,但拉伸强度明显大得多。这是由于制备过程中加入交联剂导致交联点增多所致,该水凝胶膜的吸水溶胀性最差也证明了这一点。
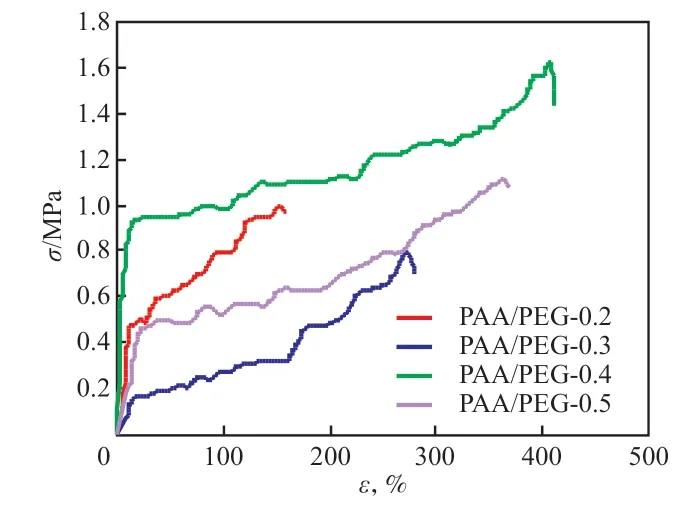
图6 PAA/PEG水凝胶膜的σ-ε曲线Fig.6 Stress-strain curves of PAA/PEG composite hydrogel films
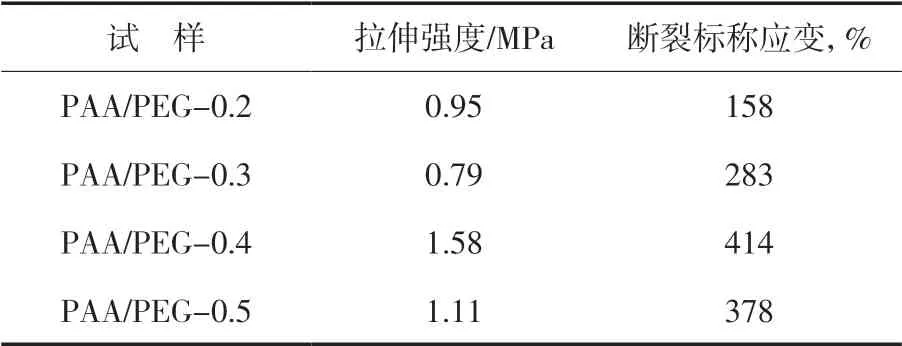
表2 PAA/PEG复合水凝胶膜的拉伸性能Tab.2 Tensile properties of PAA/PEG composite hydrogel films
3 结论
a)以AA为单体、PEG为大分子模板,通过原位聚合制备了PAA/PEG复合水凝胶膜。
b)当PEG与AA质量比为0.4,BIS与APS用量分别为单体AA质量的0.75%,2.00%时,于60 ℃预聚合30 min后的体系成膜性最好,该复合水凝胶膜的热稳定性良好,表面平整、无孔,水溶胀性较差,但拉伸强度和断裂标称应变分别为1.58 MPa,414%,是软而韧的薄膜材料。
——以高中化学“氢键”的教学为例

