[npb—SiO2—(Pb)S—Fe PP]催化性能研究
周志富,黄冠,袁广平,赵树凯,莫林强,李佩兰,刘鹏,韦柳进,韦丽萍
(广西大学 化学化工学院,广西 南宁 530004)
0 引言
目前,许多高效催化氧化环己烷制备环己醇和环己酮(KA油)的研究方法逐渐被发掘,但是因为过多使用有机溶剂[1-3]或者采用PhIO、NaIO4和n-Bu4NIO等氧化剂[1-2,4],将对环境造成较大的污染,不符合全球目前的绿色发展理念。为此,科学家们更青睐于绿色仿生催化体系的金属卟啉,在较温和反应条件下催化氧化环己烷生成KA油[5-7]。然而,由于金属卟啉价格昂贵以及在均相催化氧化反应体系中容易发生二聚而失活,或被氧化而难以回收等问题,以至于在应用中带来了一系列的问题[8]。科学家在不断研究中发现:将金属卟啉的中心金属离子与载体通过配位方式结合,能够较好地解决上述问题[9-10]。例如,宁星星等[11]利用硫化锌配位负载锰卟啉催化环己烷氧化,在相同条件下,相对Mn TCPP而言,Mn TCPP/ZnS催化氧化环己烷的转化率、转化数和醇酮产率分别提高了94.5 %、81.8 %和36.8 %,这表明配位固载作用的确能提高金属卟啉的催化活性和效率。
为了能够充分利用廉价的血红素于催化环己烷氧化生产KA油的实际中,拟将血红素配位固载到具有较大比表面积、稳定性良好且具有规则纳米孔的[npb—SiO2—(Pb)S]载体上,形成[npb—SiO2—(Pb)S—Fe PP]催化材料,试图有效地模拟P 450酶中巯基硫原子轴向配位原卟啉及其空腔结构的催化作用功能,以提高血红素催化氧气氧化环己烷形成环己醇和环己酮的能力。为合理开发利用从猪、牛等动物血液中容易提取廉价的血红素,提供一条应用的新途径。
1 实验
1.1 试剂和仪器
试剂:血红素(Sinopharm Chemical Reagent Co., Ltd);硅酸四乙酯、环己烷、氯苯和硝酸铅(上海阿拉丁生化科技股份有限公司);N,N-二甲基甲酰胺、氢氧化钠和环己醇(西陇化工股份有限公司);无水乙醇、盐酸和酚酞(成都市科龙化工试剂厂);邻苯二甲酸氢钾(天津市科密欧化学试剂有限公司),无水碳酸钠(天津市科密欧化学试剂有限公司)。所用实验试剂均为分析纯。
实验主要使用的测试仪器:紫外-可见分光光度计(型号:UV-1800,岛津仪器(苏州)有限公司),气相色谱仪(型号:GC-7900),高压反应釜(型号:WDF-05),傅里叶红外光谱仪(型号:Nexus 470,美国尼高力公司),热重分析仪(型号:Netzsch TG 209 F3),扫描透射电子显微镜(TEM,型号:Titan G2 ETEM),多站比表面积测试系统(型号:ASAP 2460),离心机(型号:TG16-WS),X射线光电子能谱学(XPS,型号:ESCALAB 250XI )。
1.2 催化剂的合成
1.2.1 硫铅官能团化的纳米多孔二氧化硅棒固载血红素
① 巯基官能团化的纳米多孔二氧化硅棒(npb—SiO2—SH)的制备[12-13]:首先,称取十六烷基三甲基溴化铵(CTAB,7×10-4mol)和氢氧化钠(NaOH,1.75×10-3mol)溶解于120 mL的去离子水中。室温下搅拌40 min,将混合溶液升温至80 ℃,然后将硅酸四乙酯(TEOS,5.07×10-3mol)逐滴加入到CTAB溶液中,逐渐滴加(3-巯基丙基)三甲氧基硅烷(MPTMS,1.02×10-3mol)。在80 ℃条件下搅拌反应2 h,自然冷却至室温,得到白色沉淀物,在离心机以6 500 r/min得到未除CTAB产物。其次,在50 ℃下,将未除CTAB的产物用5.0 %(v/v)的盐酸乙醇溶液萃取5 h,离心分离萃取液,得到已除CTAB的(npb—SiO2—SH),此过程重复2次,以彻底除去CTAB。最后经洗涤并干燥后得到(npb—SiO2—SH)。经有机元素分析,碳、氢和硫元素含量分别为8.09 %、1.89 %和7.09 %(质量百分比)。
② 硫铅官能团化的纳米多孔二氧化硅棒[npb—SiO2—(Pb)S]的制备[14]:称取巯基官能团化的纳米多孔二氧化硅棒0.2 g,投入到40 ℃的1 000 mL去离子水中搅拌,向其中加入0.36 mol/L 30 mL的Pb(NO3)2溶液,然后用0.1 mol/L的NaOH溶液和0.1 mol/L的HNO3溶液调节至溶液pH=6.0。继续搅拌4 h后,过滤、洗涤并干燥滤饼得到[npb—SiO2—(Pb)S]。
③ 硫铅官能团化的纳米多孔二氧化硅棒固载血红素[npb—SiO2—(Pb)S—Fe PP]的制备:称0.5 g的[npb—SiO2—(Pb)S]置于烧瓶中,加入200 mL去离子水,搅拌并加热至50 ℃。逐滴加入2.0 mL 1.53 ×10-3mol/L血红素的DMF溶液,反应7 h。自然冷却后抽滤,用去离子水洗涤,在85 ℃干燥24 h,得到[npb—SiO2—(Pb)S—Fe PP]催化材料。用紫外-可见分光光度法对滤出液中的金属卟啉的含量进行测定,由此计算出[Fe PP]固载量为4.0 mg/g(6.14×10-6mol)。采用ICP-OES技术测定得到[Fe PP]固载量为4.15 mg/g(6.37×10-6mol)。
1.2.2 [npb—SiO2—(Pb)S—Fe PP]催化氧化环己烷
向高压反应釜(WDF-05)倒入200 mL环己烷,投入相应的[npb—SiO2—(Pb)S—Fe PP]催化材料。加热至所需反应温度,并持续通入氧气使其达到所需反应压力。控制搅拌速度为200 r/min ,尾气流量为0.04 m3/h,反应时间为4 h。在催化氧化反应过程中,每30 min取样1次。将取得的液体样品,以氯苯为内标物,采用气相色谱法测定主要产物的质量百分质量;采用酸碱滴定法测定副产物含量。实验结束后,将反应混合液进行抽滤、洗涤和干燥,并回收催化材料,便于再次循环使用。[npb—SiO2—(Pb)S—Fe PP]催化氧化环己烷的反应如图1所示:
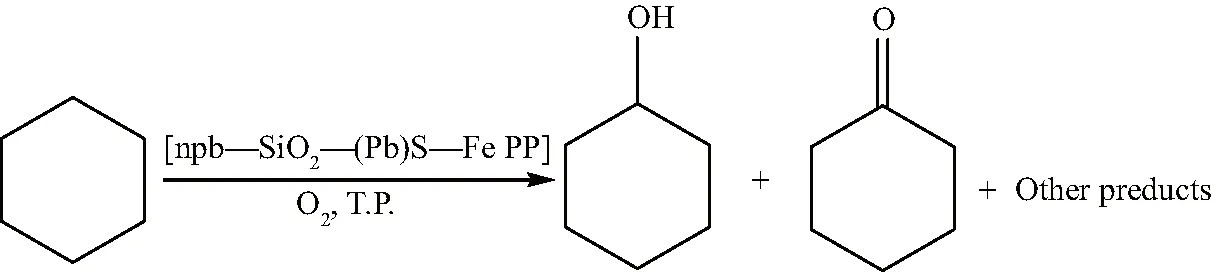
图1 [npb—SiO2—(Pb)S—Fe PP]催化环己烷氧化反应Fig.1 Cyclohexane oxidation reaction catalyzed by [npb—SiO2—(Pb)S—Fe PP]
2 结果与讨论
2.1 催化剂的表征
2.1.1 紫外可见光谱表征
图2为[Fe PP][摩尔吸光系数ε=1.00×105L/(mol·cm)]的DMF溶液和[npb—SiO2—(Pb)S—Fe PP][ε=9.57×104L/(mol·cm)]的DMF悬浊液紫外光谱。从图2可以看出,[Fe PP]的Soret峰分布在395 nm处,Q峰主要出现在544 nm处,[Fe PP]固载到[npb—SiO2—(Pb)S]之后,Soret峰已经红移6 nm,即401 nm处,并且Q带峰已经消失,与文献[16]相一致,说明[Fe PP]和[npb—SiO2—(Pb)S]成功配位固载[8]。
2.1.2 红外光谱表征
图 3中的(a)、(b)、(c)和(d)曲线分别是(npb- SiO2-SH),[npb—SiO2—(Pb)S],[npb—SiO2—(Pb)S—Fe PP]和[Fe PP]的红外光谱。(npb—SiO2—SH)的巯基特征峰在2 569 cm-1处[14],当(npb—SiO2—SH)吸附铅离子形成[npb—SiO2—(Pb)S]之后,2 569 cm-1处的巯基峰消失,说明(npb—SiO2—SH)成功吸附铅离子生成了[npb—SiO2—(Pb)S]载体。1 699 cm-1是血红素中的羧基峰[17],1 222 cm-1为C—H弯曲振动峰,1 119 cm-1和1 079 cm-1是C—N伸缩振动峰和C—O伸缩振动峰[18-19]。与[npb—SiO2—(Pb)S]对比,[Fe PP]固载到[npb—SiO2—(Pb)S]后,C—S吸收峰从685 cm-1红移至679 cm-1处[20],这说明血红素已经成功固载到[npb—SiO2—(Pb)S]。
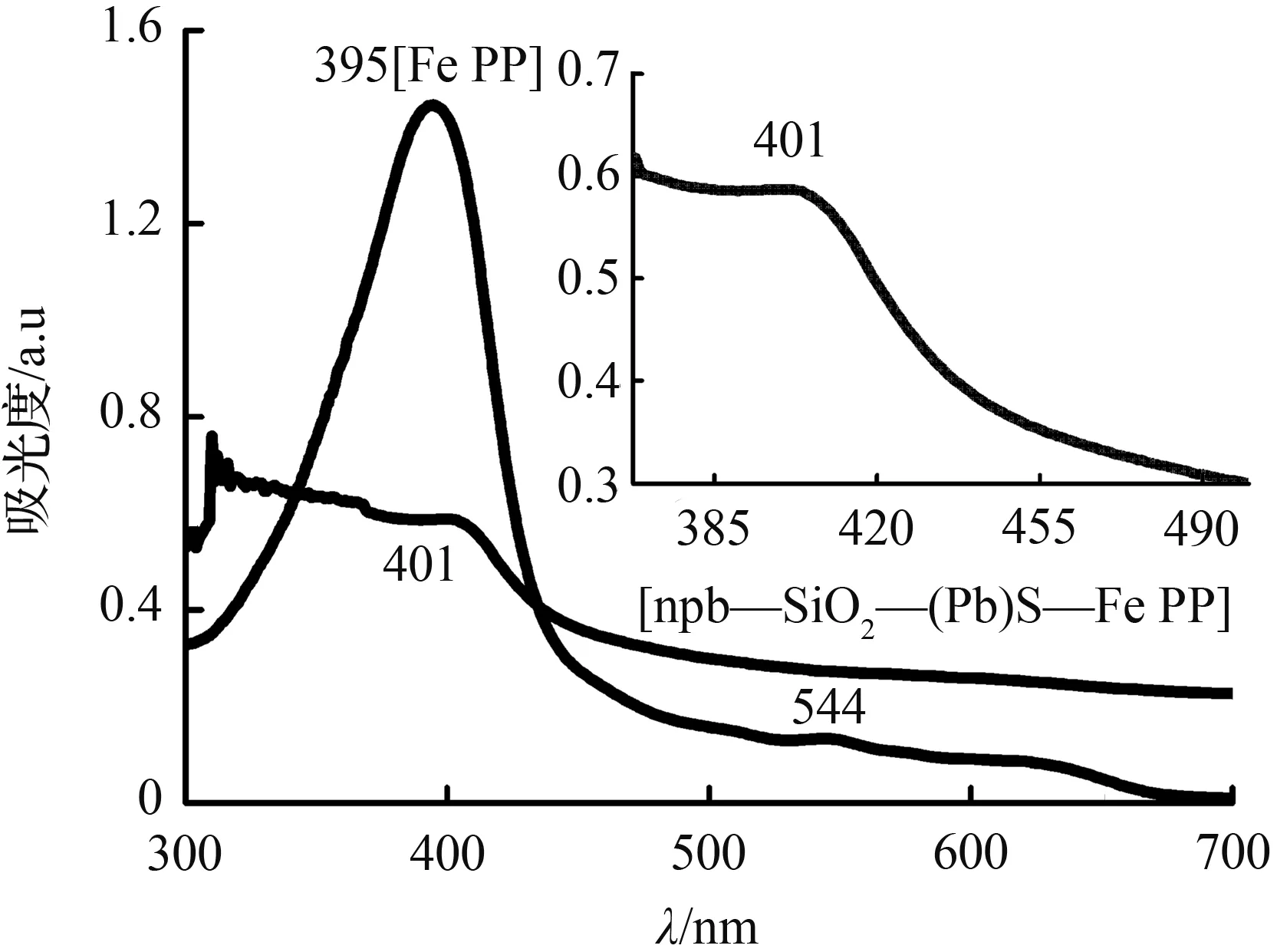
图2 [Fe PP]的DMF溶液和[npb—SiO2—(Pb)S—Fe PP]的DMF悬浊液紫外光谱Fig.2 UV-Vis spectra for the DMF solution of [Fe PP],and for the DMF suspension of [npb—SiO2—(Pb)S—Fe PP]
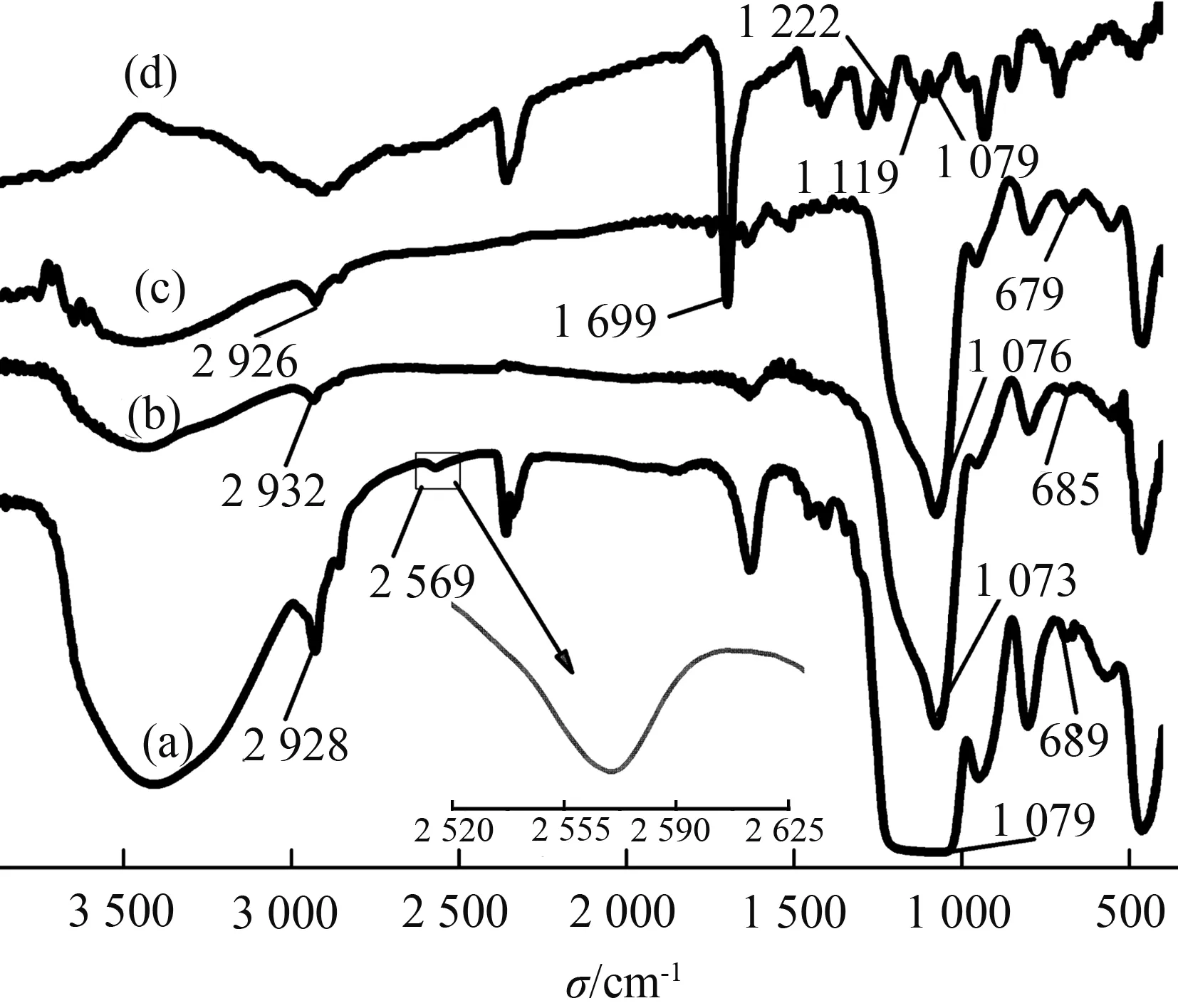
图3 (npb—SiO2—SH)(a),[npb—SiO2—(Pb)S](b), [npb—SiO2—(Pb)S—Fe PP](c)和[Fe PP](d)的傅里叶红外光谱,波数范围为4000~400 cm-1Fig.3 FTIR spectra for (npb—SiO2—SH)(a), [npb—SiO2—(Pb)S](b),[npb—SiO2—(Pb)S—Fe PP](c) and [Fe PP](d), with an effective frequency range of 4000~400 cm-1
2.1.3 BET和TEM表征
图4是[npb—SiO2—(Pb)S—Fe PP]的氮气吸脱附等温曲线和孔径分布图。[npb—SiO2—(Pb)S—Fe PP]的BET表面积约为268.0 m2/g,孔径主要分布在1.5~2.5 nm。这种大比表面积有利于[Fe PP]分子的分散从而避免其发生二聚失活,并且[Fe PP]在催化过程中能够充分与氧分子接触,增强催化活性[21]。
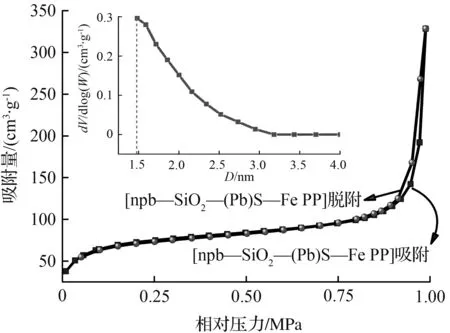
图4 [npb—SiO2—(Pb)S—Fe PP]的氮气吸脱附等温线和孔径分布图Fig.4 N2 adsorption/desorption isotherm and pore-size distribution curves of [npb—SiO2—(Pb)S—Fe PP]
图5为[npb—SiO2—(Pb)S]和[npb—SiO2—(Pb)S—Fe PP]的TEM图,从图5可见:[npb—SiO2—(Pb)S]和[npb—SiO2—(Pb)S—Fe PP]均为纳米孔棒状材料,且表面均有相似的黑点,笔者利用ImageJ 软件对上述两个TEM图中黑点的粒径进行统计计算分析,载体[npb—SiO2—(Pb)S]表面黑点粒径大小约为0.91 nm,而催化材料[npb—SiO2—(Pb)S—Fe PP]表面黑点粒径大小则约为1.9 nm,后者与血红素分子直径(约为1.7 nm[22])相近。其中,载体中的黑点可能是铅离子取代巯基中的氢原子所引起的,而催化材料的黑点则可能是血红素分散配位固载到载体上所造成的。这表明血红素已成功地配位固载到载体上,形成了[npb—SiO2—(Pb)S—Fe PP]催化材料。

(a) [npb—SiO2—(Pb)S]

(b) [npb—SiO2—(Pb)S—Fe PP]
2.1.4 X射线光电子能谱分析
图6是[Fe PP], [npb—SiO2—(Pb)S]和[npb—SiO2—(Pb)S—Fe PP]的全谱图和关键元素(S、Fe、N)的XPS能谱图,表1是固载前后关键元素结合能的具体变化值。从图6(b)可以看出,[npb—SiO2—(Pb)S]固载[Fe PP]之后,硫原子的结合能从164.07 eV和162.76 eV[14]变为164.97 eV和163.70 eV。在这一固载过程中,硫原子结合能增大,说明硫原子的电子云密度是降低的。这意味着硫原子与中心金属离子间发生了配位作用。这种配位作用引起中心金属离子及其邻近的氮原子的结合能也发生变化:首先,如图6(c)所示,[Fe PP]固载后,铁离子的Fe3+2p3/2和2p1/2结合能由709.93 eV和724.21 eV变为710.59 eV和729.95 eV;然而,715.60、729.95、717.33、730.06 eV则是Fe3+固载前后的卫星峰[23-28]。可见,铁离子结合能是增大的,即中心金属离子电子云密度下降,导致中心金属离子正电性增强[29-31],而硫原子结合能的变化说明[npb—SiO2—(Pb)S]的硫原子已经与[Fe PP]中心铁离子轴向配位,这种轴向配位是有利于催化活性的提高[11]。其次,也导致了血红素中氮原子结合能变化,血红素存在着两种化学环境氮原子,其中一种以配位形式存在,另外一种则是共价键存在[32]。根据图6(d),[Fe PP]固载到[npb—SiO2—(Pb)S]之后,[Fe PP]的氮原子(N→Fe)的结合能从400.03 eV升高至400.13 eV,说明N电子云密度降低,对铁离子的配位能力增强,使得[Fe PP]中的铁离子固载更加牢固,更利于催化中心的回收和重复利用。从以上关键元素结合能的变化说明:[Fe PP]已经通过配位作用固载到了[npb—SiO2—(Pb)S]之上,这样的固载方式更有利于在催化过程中催化剂的稳定和重复使用,以及提升催化剂的催化性能和催化效率。
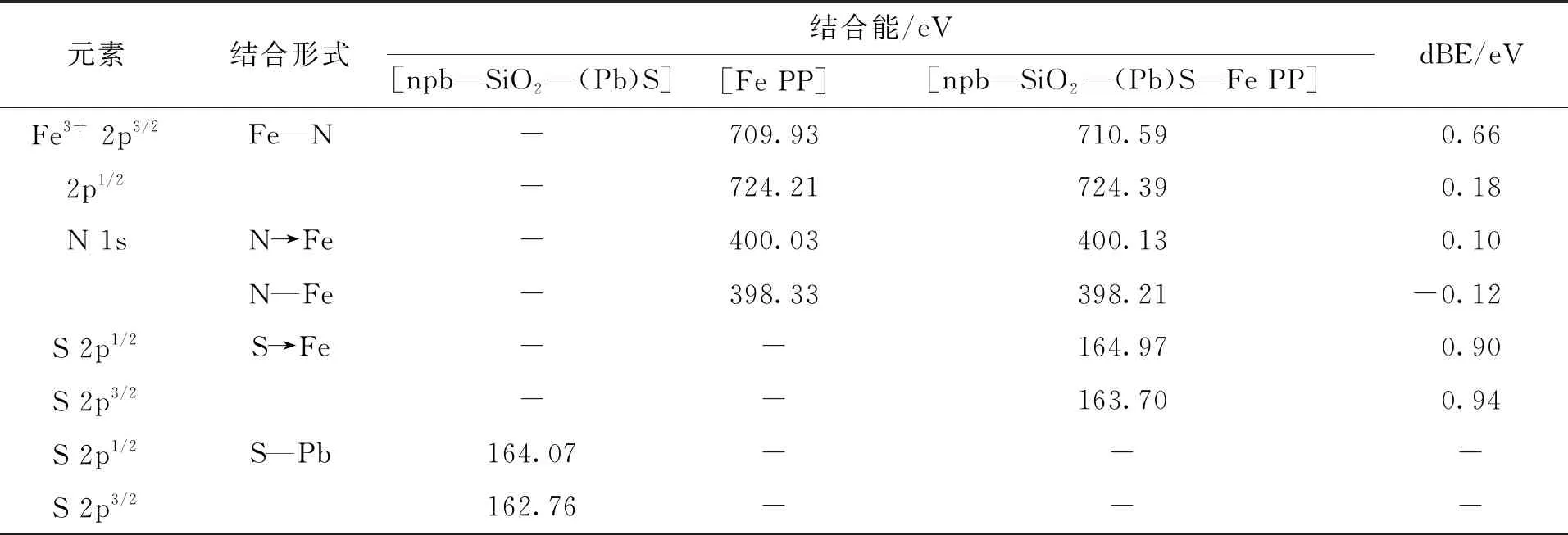
表1 [Fe PP], [npb—SiO2—(Pb)S]和[npb—SiO2—(Pb)S—Fe PP]中关键元素的内层电子结合能Tab.1 Binding energy of the key elements in [Fe PP], [npb—SiO2—(Pb)S], and [npb—SiO2—(Pb)S—Fe PP]

(a) XPS全谱
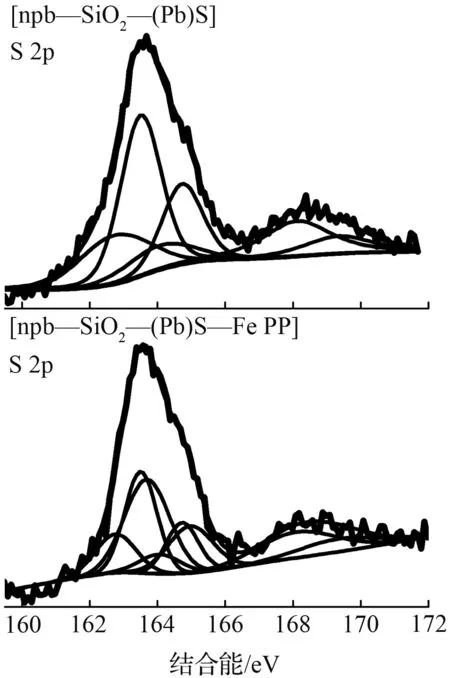
(b) S元素的XPS能谱
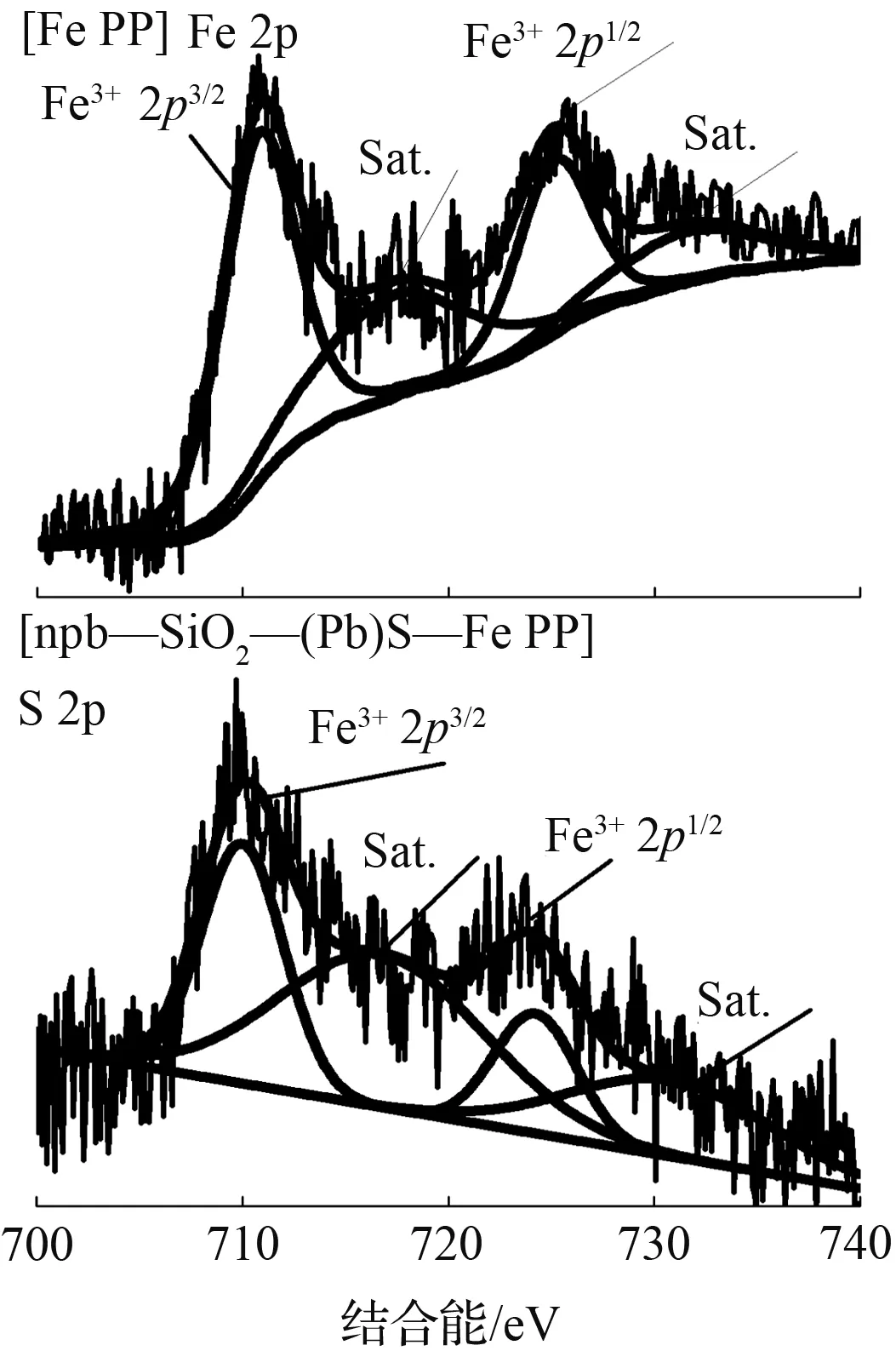
(c) Fe元素的XPS能谱
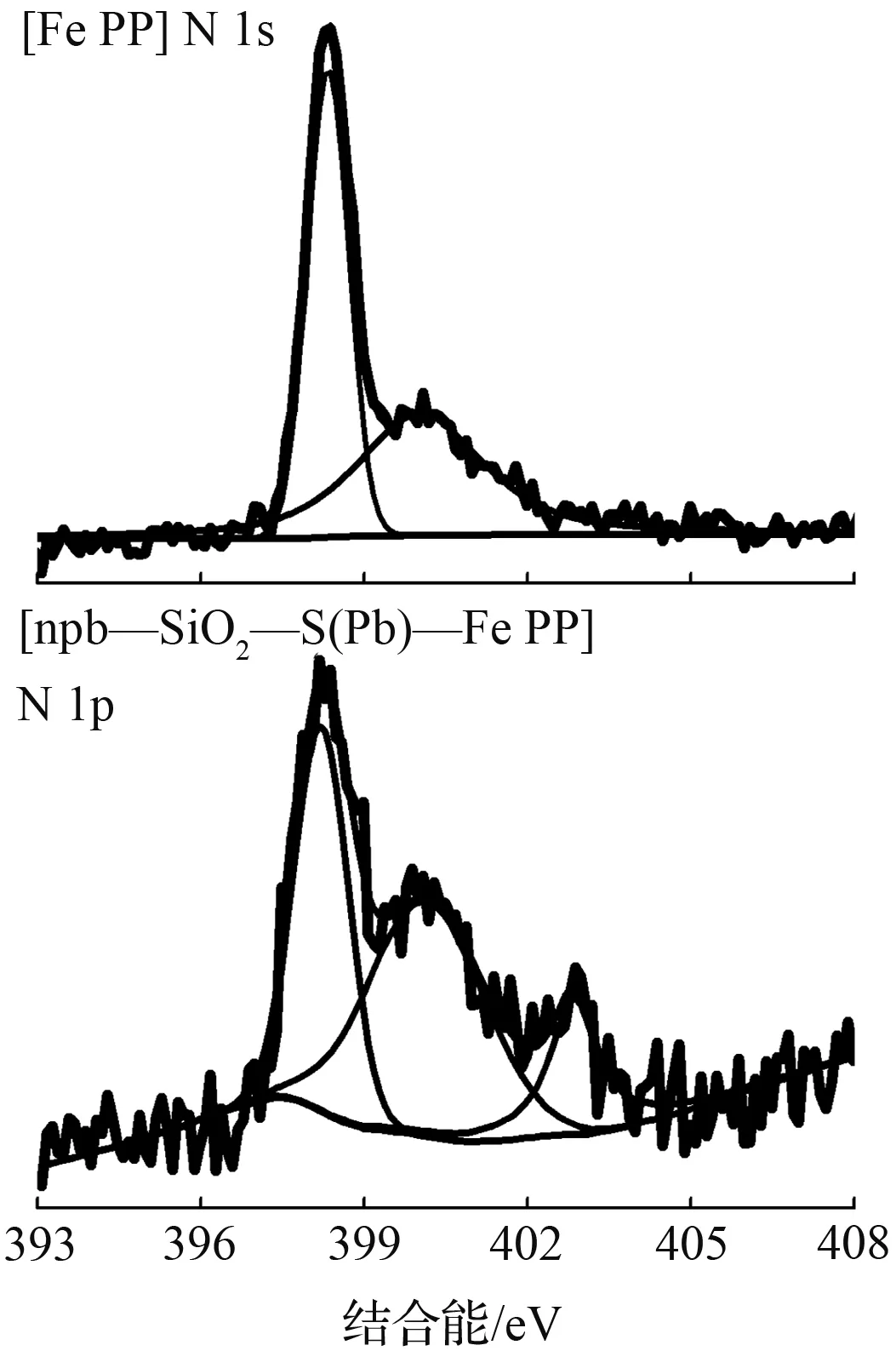
(d) N元素的XPS能谱
2.2 [npb—SiO2—(Pb)S—Fe PP]催化氧化环己烷
2.2.1 [npb—SiO2—(Pb)S—Fe PP]催化氧化环己烷的反应条件探索
[npb—SiO2—(Pb)S—Fe PP]催化氧化环己烷的结果见图7。从图 7(a)可见,表示[npb—SiO2—(Pb)S—Fe PP]在反应压力为0.9 MPa,催化剂用量为0.5 mg和反应时间为第4 h的反应条件下,转化率和醇酮产率均随着温度的升高而增大,并且以160 ℃为最佳反应温度;随之温度越高,转化率和醇酮产率反之降低。以上实验结果可能是反应温度过高导致血红素分子的结构受到破坏[29],从而失去活性。图7(b)表示相应催化剂用量和时间条件下,转化率和醇酮产率均随着压力的增大而增大,并且以0.9 MPa为最佳反应压力;随之压力增大,转化率和醇酮产率反之降低。这主要是在高浓度的氧气条件下,导致少部分固载在硫铅官能团化的纳米多孔二氧化硅棒上的血红素被氧化而失活[29]。图7(c)表示催化剂在最佳温度、压力和反应时间在第4 h反应条件下,转化率和醇酮产率均随着催化剂用量的增加而增大,并且以0.5 mg为最佳反应用量;催化剂用量增多,催化效果明显下降。这可能是催化剂用量超过一定量时引起的催化剂抑制作用[33]。图7(d)是在最佳温度、压力和催化剂用量条件下,催化剂催化环己烷氧化反应随反应时间的变化情况。在前3.5 h内醇酮产率和转化率都是随着反应时间的增加而增加,但是在3.5~4 h所得到的结果是醇酮产率增长缓慢,而转化率继续增加。考虑实际工业生产的效果和成本及催化剂的使用寿命,较佳的反应时间初步定为4 h。综上所述,[npb-SiO2-(Pb)S-Fe PP]催化氧气氧化环己烷的较佳反应条件为: 反应温度为160 ℃、反应压力是0.9 MPa、催化剂用量0.5 mg和反应时间为4 h。

(a) 反应温度对催化性能的影响
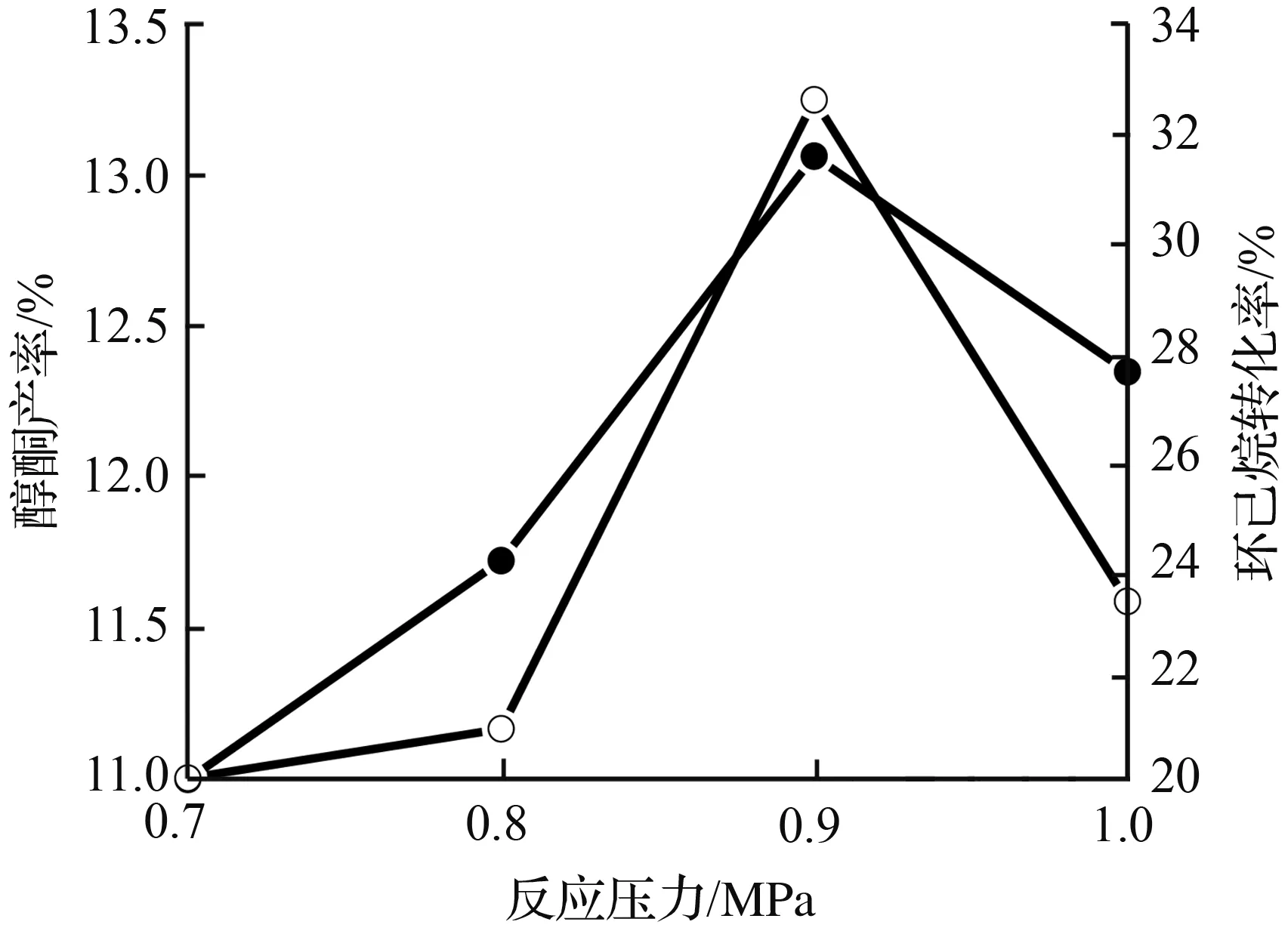
(b) 反应压力对催化性能的影响
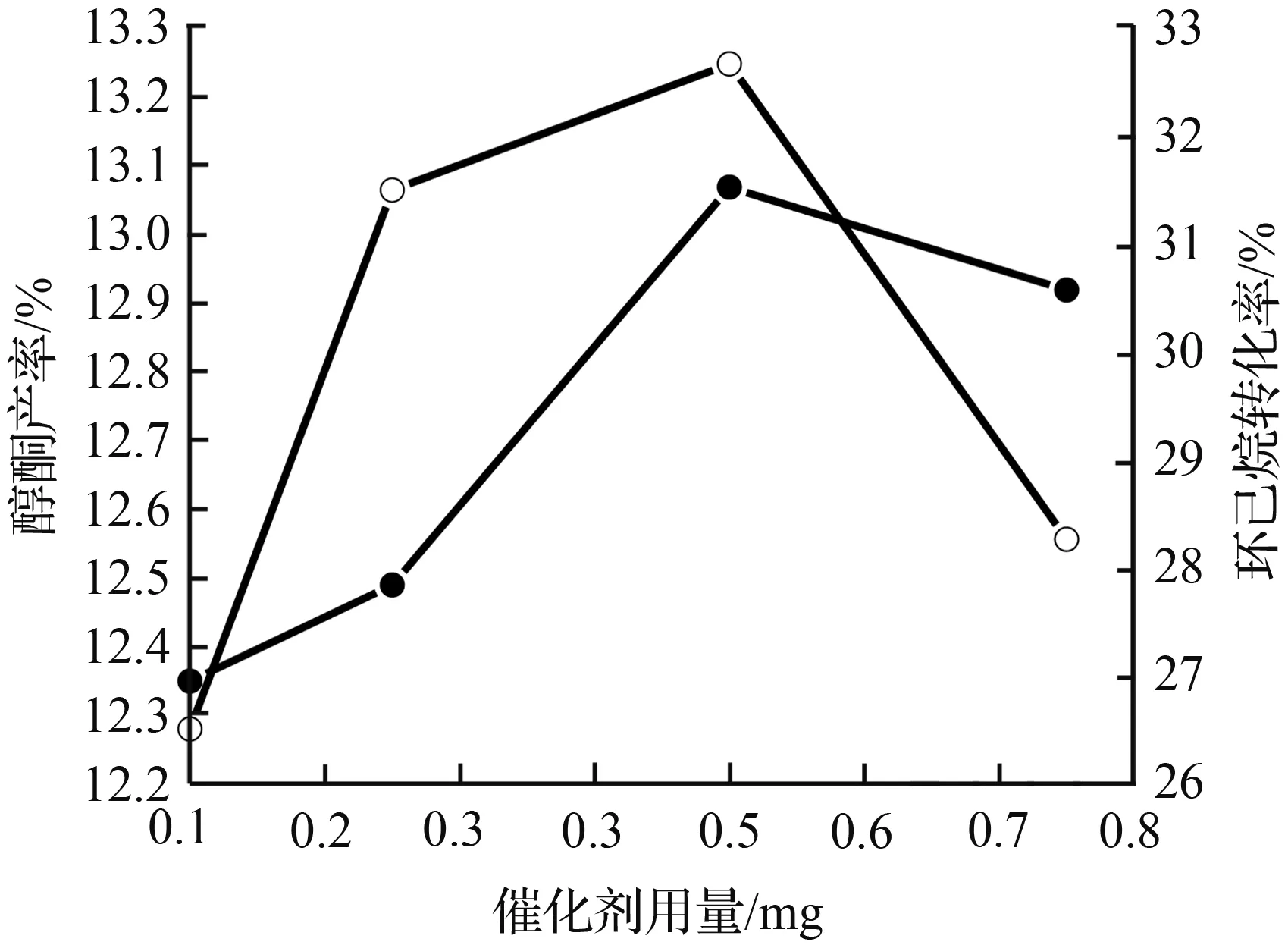
(c) 催化剂用量对催化性能的影响

(d) 反应时间对催化性能的影响

图7 [npb—SiO2—(Pb)S—Fe PP]催化氧化环己烷的结果Fig.7 Results of cyclohexane oxidation over [npb—SiO2—(Pb)S—Fe PP]
2.2.2 [npb—SiO2—(Pb)S—Fe PP]与[Fe PP]催化性能的比较
催化剂[npb—SiO2—(Pb)S—Fe PP]可以重复使用5次(表2),并且催化环己烷的平均转化频次、转化率和醇酮产率分别为1.93×105h-1、29.43 %和12.13 %,与[Fe PP]相比,[npb—SiO2—(Pb)S—Fe PP]催化氧化环己烷的平均转化频次,转化率和醇酮产率分别提高了19.88 %,22.27 %和14.98 %。引起这些催化性能差异的可能主要原因是:第一,[npb—SiO2—(Pb)S]与[Fe PP]配位作用提高了中心金属离子的正电性,有利于氧分子的活化,提高[npb—SiO2—(Pb)S—Fe PP]的催化性能;第二,[npb—SiO2—(Pb)S]的大比表面积及空腔结构有利于血红素的高度分散,避免血红素二聚而失活,充分发挥其应有的催化效能。
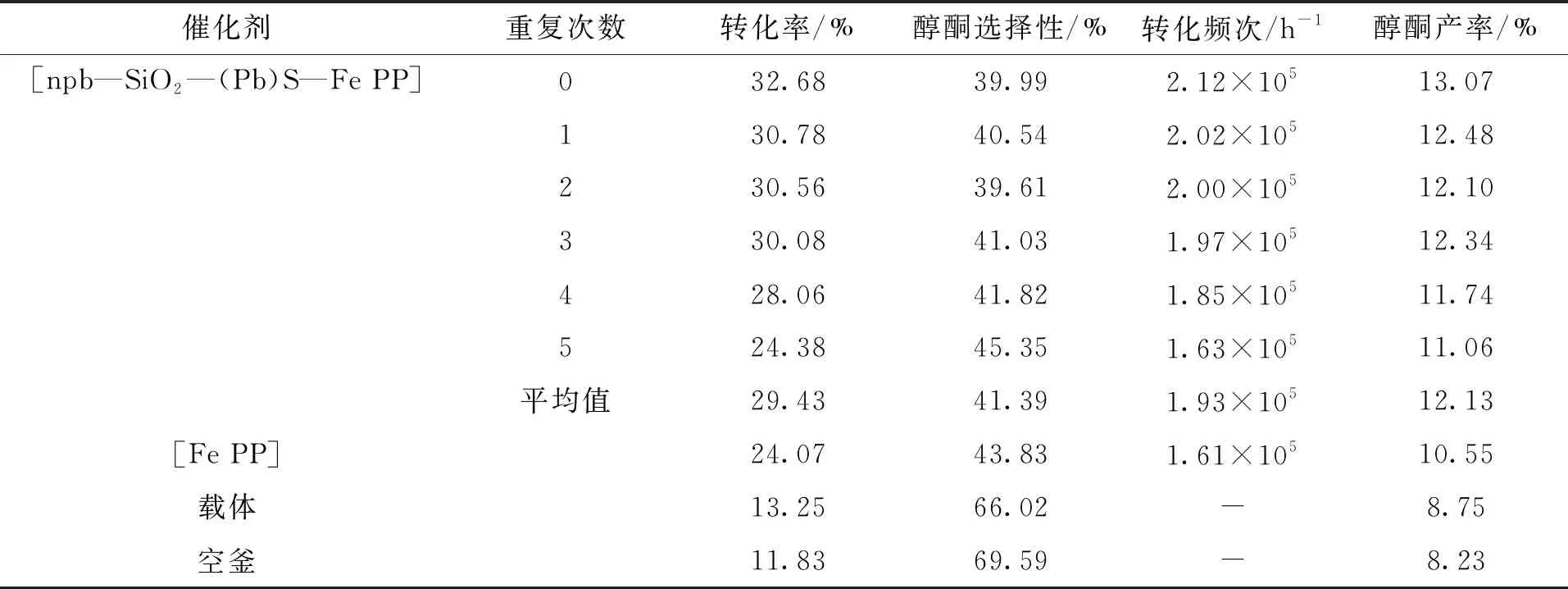
表2 最佳催化反应条件下,[npb—SiO2—(Pb)S—Fe PP]和[Fe PP]催化氧化环己烷的结果比较Tab.2 Comparison of the catalysis results forcyclohexane oxidation by [npb—SiO2—(Pb)S—Fe PP] with [Fe PP] under the optimum reaction conditions
3 结论
血红素是一种廉价易得的天然产物,利用其中心金属离子与[npb—SiO2—(Pb)S]中的硫原子轴向配位,模拟P-450酶的半胱氨酸巯基的轴向配位调节催化性能作用;同时,以[npb—SiO2—(Pb)S]的纳米空腔结构模拟P-450酶天然空腔结构的功能。通过硫原子与血红素中心铁离子的配位作用,改变血红素中心铁离子的结合能,增强其正电性。由此,有效避免了[Fe PP]在催化过程中二聚而失活,并提高催化剂的催化活性、催化效率和循环使用次数:[npb—SiO2—(Pb)S—Fe PP]催化氧化环己烷平均转化频次、环己烷转化率和醇酮产率分别为1.93×105h-1、29.43 %和12.13 %;与[Fe PP]相比,催化氧化环己烷的转化频次提高了19.88 %,转化率提高了22.27 %,醇酮产率提高了14.98 %;此外,4 mg/g血红素固载量的[npb—SiO2—(Pb)S—Fe PP]催化材料可以重复使用5次。所以,[npb—SiO2—(Pb)S—Fe PP]可能是一种具有潜在应用价值的催化材料。

