RSPE-UPLC-MS/MS法测定禽蛋中氯羟吡啶残留
梁飞燕,林小莹,辛丽娜,叶勇,陈圣杰,王捷*
(1.广西-东盟食品检验检测中心,广西 南宁 530021; 2.广西医科大学 药学院,广西 南宁 530021)
0 引言
氯羟吡啶又称二氯二甲吡啶酚、克球酚,对鸡9种艾美耳球虫均有良好的防治效果,是目前国内使用最广泛的抗球虫药之一,在国际上使用也较多。氯羟吡啶有一定的致畸作用和胚胎毒作用。不遵守休药期规定、超剂量使用、饲料中非法添加等操作,均有可能导致氯羟吡啶在鸡体内和鸡蛋中的残留。中华人民共和国农业部第235号公告及2019年9月6日发布并于2020年4月1日实施的《食品安全国家标准》(GB 31650—2019)中对鸡/火鸡的肌肉、肝、肾的兽药残留做出了限量要求,却没有对鸡蛋中氯羟吡啶的残留量做出规定。2019年4月,农业农村部官网发布了《2019年动物及动物产品兽药残留监控计划》中指出鸡蛋中不得检出氯羟吡啶。为此,考察和研究氯羟吡啶在禽蛋中的残留水平和现状,对制定禽蛋中氯羟吡啶的残留限量标准、保障禽蛋质量安全均具有重要意义。
关于鸡蛋中氯羟吡啶的检验方法,我国目前现行有效的标准有《鸡蛋中氯羟吡啶残留量的检测方法 高效液相色谱法》(GB/T 20362—2006)、《出口动物源食品中抗球虫药物残留量检测方法 液相色谱-质谱/质谱法》(SN/T 3144—2011)。《鸡蛋中氯羟吡啶残留量的检测方法 高效液相色谱法》采用色谱法进行测定,专属性差,灵敏度低,已不适应当前痕量组分分析的仪器设备要求;《出口动物源食品中抗球虫药物残留量检测方法 液相色谱-质谱/质谱法》采用液相色谱-质谱/质谱法进行测定,仪器灵敏度高,但净化过程采用常规的固相萃取法,要经过活化、平衡、上样、淋洗、洗脱共5个步骤,操作复杂、耗时长。目前,关于禽蛋中氯羟吡啶残留检测方法的文献报道甚少,而且大都采用了高效液相色谱法[1-2]或常规的固相萃取法[3]。为此,笔者研究了一种样品前处理简单、快速、灵敏、专属性强、准确度高的禽蛋中氯羟吡啶残留的反相固相萃取(RSPE)-超高效液相色谱(UPLC)-串联质谱(MS/MS)的检测方法,并对当前鸡蛋中氯羟吡啶的残留现状进行了考察。
1 实验
1.1 仪器与试剂
ExionLC液相色谱-AB 6500三重四级杆液质联用仪(美国AB SCIEX公司);ML204电子天平(梅特勒-托利多国际有限公司);KS 260涡旋振荡仪(德国IKA集团);ST 40R高速冷冻离心机(赛默飞世尔科技有限公司);AutoVap S60氮吹仪(美国ATR公司)。
乙腈、甲醇、甲酸均为色谱纯(美国默克公司);水为Millipore超纯水;Oasis PRIME HLB固相萃取小柱(500 mg,6 cc,沃特世科技有限公司);氯羟吡啶标准品含量98.85 %(美国Stanford Chemicals公司)。
1.2 标准溶液的制备
标准储备液:准确称取氯羟吡啶标准品适量至棕色瓶中,用甲醇溶解,配制成浓度为1 000 μg/mL的溶液。
标准溶液:精密量取标准储备液适量,用甲醇稀释成100 μg/mL的溶液。
1.3 样品前处理
取禽蛋样品去壳后均质,称取2.50 g(精确到0.01 g)置于50 mL离心管中,用乙腈∶水(90∶10,v/v)定容至10.0 mL,于涡旋振荡器中涡旋10 min,10 000 r/min 5 ℃离心5min。取上清液置于Oasis PRIME HLB固相萃取柱(500 mg,6 cc)中,待其自然流出,收集流出液4.0 mL于15 mL离心管中,40 ℃水浴氮气吹至近干,残渣用乙腈∶水(10∶90,v/v)定容至1.0 mL,涡旋震荡2 min复溶,过0.22 μm滤膜后待上机测定。
1.4 基质标准工作曲线溶液的制备
精密量取标准使用液适量,氮气吹干,加入按1.3节样品前处理得到的空白基质溶液1.0 mL,得到浓度为0.5~20 ng/mL的系列基质标准工作曲线溶液。
1.5 色谱-质谱条件
1.5.1 色谱条件
CAPCELL PAK C18MGⅢ-H色谱柱(3 μm,2.0 mm×100 mm);流动相为0.1 %甲酸溶液A-乙腈B,梯度洗脱程序见表1;流速为0.4 mL/min;柱温为40 ℃;进样量为20 μL。

表1 流动相梯度洗脱程序Tab.1 Mobile phase gradient elution procedure
1.5.2 质谱条件
电离方式为电喷雾离子源(ESI),正离子扫描;采集模式为多反应监测模式(MRM);电喷雾电压(IS)为5 500 V,离子源温度(TEM)为400 ℃,气帘气流速为35 L/min,雾化气流速为55 L/min,辅助加热气流速为55 L/min,射入电压为10 V。氯羟吡啶的相关质谱参数见表2,氯羟吡啶总离子流图见图1。

表2 氯羟吡啶质谱采集参数Tab.2 MS acquisition parameters of clopidol
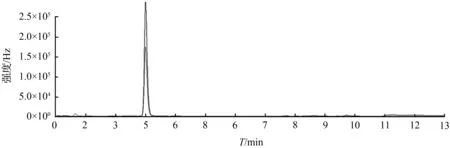
图1 氯羟吡啶总离子流图Fig.1 Total ion current of clopidol
2 结果和讨论
2.1 提取溶剂的选择
合理选择提取溶剂,不仅能有效提取待测组分,还可以阻止干扰组分进入提取液中,降低基质干扰。氯羟吡啶为吡啶类化合物,在甲醇或乙醇中极微溶,在水、丙酮、乙醚、苯中不溶,在氢氧化钠中溶解。鸡蛋含有大量的脂肪和蛋白质,乙腈可沉淀蛋白。通过查阅相关标准和文献[4-7],氯羟吡啶的检测均采用乙腈做为提取溶剂。为此,本研究考察了不同比例的乙腈溶液[无水乙腈、乙腈∶水(90∶10,v/v)、乙腈∶水(80∶20,v/v)、乙腈∶水(70∶30,v/v)]对氯羟吡啶的提取效率和基质干扰程度,结果表明乙腈含量越高,沉淀蛋白能力越强;同时因鸡蛋中含有丰富脂溶性物质(叶黄素和玉米黄素等),乙腈含量越高,进入提取液的脂溶性物质越多,为此得到的提取液显示的黄色越深,基质干扰也越大。通过比较得出,采用乙腈∶水为90∶10(v/v)时提取回收率较高,峰形较好,所以本研究选择乙腈∶水为90∶10(v/v)作为提取溶剂。
2.2 固相萃取柱的选择
PRiME HLB固相萃取柱[8-11]是一种新型的反相固相萃取吸附剂,可以吸附样品中的非极性干扰物但不影响目标物的回收率,尤其是对于造成基质干扰的脂肪和磷脂,去除效率高达95 %以上,从而达到最简单的过滤式样品制备流程,实现样品纯化的目的。为此,笔者考察了PRiME HLB固相萃取柱对样品的净化效果,通过与含HLB和MCX吸附剂的固相萃取柱比较发现:PRiME HLB固相萃取柱纯化速度快、操作简单、基质干扰小,氯羟吡啶的峰型和回收率均优于使用HLB和MCX吸附剂的固相萃取柱。故采用PRiME HLB固相萃取柱作为纯化柱。
2.3 方法学验证
2.3.1 线性范围、检出限和定量限
按照1.4节配制系列基质标准工作曲线溶液,以1.5节的色谱、质谱条件进行测定,考察氯羟吡啶的线性。结果以目标物质量浓度为横坐标,定量离子峰面积响应值为纵坐标,绘制工作曲线。测得氯羟吡啶在0.5~20 ng/mL内线性关系良好,详见图2,线性方程为y=3.689 0×105x+15 990,相关系数为0.999 2。在空白鸡蛋中添加适量的氯羟吡啶标准溶液,按1.3节配制检出限溶液和定量限溶液,以定量离子的信噪比S/N=3、S/N=10分别计算检出限和定量限,得到本方法氯羟吡啶的检出限为0.001 3 μg/kg,定量限为0.004 5 μg/kg。

图2 氯羟吡啶工作曲线Fig.2 Working curve of clopidol
2.3.2 回收率和精密度
采用加标回收法,在鸡蛋空白样品中添加3种不同浓度水平的标准溶液:0.4、1.0、4.0 μg/kg,一式3份,按拟定的方法和条件进行前处理,得到回收率溶液上机测定回收率和精密度。结果显示,3种浓度水平的回收率分别为105.90 %、106.82 %、101.65 %,RSD分别为1.53 %、1.11 %、2.91 %,详见表3,符合国家标准《实验室质量控制规范 食品理化检验》(GB/T 27404—2008)附录F 检测方法确认的技术要求中的相关规定。

表3 方法回收率及精密度Tab.3 Result of tests for recovery and precision (n=3)
3 禽蛋中氯羟吡啶残留现状的考察
本次考察从流通环节共采集禽蛋样本82批次,采用具体方法对氯羟吡啶的残留进行了筛查检测,结果3批次禽蛋检出氯羟吡啶的检出率为3.66 %,样品检出氯羟吡啶的测定值见表4。

表4 氯羟吡啶测定结果Tab.4 Determination results of clopidol
氯羟吡啶为广泛用于家禽球虫病的药物,中华人民共和国农业部第278号公告中规定氯羟吡啶预混剂在产蛋期为禁用药物,本研究检出禽蛋中氯羟吡啶的残留,可能为养殖户在养殖过程没有遵守休药期规定而造成。为此,指导养殖户科学、合理用药,提高养殖户的安全和风险意识,对于降低兽药残留风险、提高禽蛋质量具有重要意义。
4 结论
本次研究建立的禽蛋中氯羟吡啶残留的RSPE-UPLC-MS/MS方法,具有操作简单快速、方法准确度高、灵敏等优点,满足食品检测方法的技术要求,可用于禽蛋中氯羟吡啶残留的筛查检验,为监管部门实施风险监测提供了技术支持,对禽蛋质量风险监控和质量安全的提高具有重要价值。

