尼可地尔对梗阻性冠心病患者冠状动脉微循环障碍的影响
官 兵,苏 杨,韦旭斌,张 莹
(昆明医科大学第二附属医院心内科三病区,昆明云南 650101)
近40 余a 来,随着循证医学和冠状动脉有创性、无创性诊断技术的迅速发展,冠状动脉微循环功能异常的临床现象受到人们的高度重视。为此,2013 年欧洲心脏病学会(ESC)在《稳定性冠状动脉疾病治疗指南》(以下称《指南》)中正式将此病命名为冠状动脉微循环功能障碍(coronary microvascular dysfunction,CMD)[1];我国为了在该领域能更加深入的开展基础和临床研究,于2017 年5 月由中华医学会心血管病学分会多个专业学术组的,在该领域具有深厚造诣的资深专家,首次在世界范围内编订了《冠状动脉微血管疾病诊断和治疗的中国专家共识》(以下称《中国专家共识》)[2],明确将本类病变定义为冠状动脉微血管疾病(coronary microvascular disease,CMVD),并给出了治疗建议,但对合并阻塞性稳定型冠状动脉疾病的CMVD 诊断及治疗,仍是值得探索的领域。尼可地尔被推荐为冠状动脉微血管心绞痛的首选药物[3]。所以,本研究通过有创冠状动脉造影检出梗阻型冠心病伴CMVD,测定腺苷负荷心肌微循环阻力指数(index of microcirculatory resistance,IMR)及腺苷负荷心脏磁共振(cardiac magnetic resonance,CMR)心肌灌注储备指数(myocardial perfusion reserve index,MPRI)作为观测微循环障碍的指标,观察、评价尼可地尔治疗冠心病患者CMVD 的效果。
1 资料与方法
1.1 资料
1.1.1 研究对象入选标准:连续选取2016 年10 月至2018 年9 月因缺血性症状和体征而入住昆明医科大学第二附属医院心内科患者21 例,经冠状动脉介入造影显示梗阻性冠心病(≥1 支心外膜冠状动脉血管,管径狭窄≥50%、冠脉血流储备分数(FFR)≤0.8 为阻塞性冠心病)[4],同时以冠状动脉内压力/温敏导丝系统测定IMR,并依据IMR确定伴有CMD。梗阻性冠心病伴CMD 诊断是异常的冠脉容量血流储备(coronary volumetric flow reserve,CFR),即腺苷负荷的CFR <2.3[5];IMR >23,EER <0.8[6]。同时期行腺苷负荷CMR 及静息状态成像检查。而非CMD 排除标准即:IMR <22。
1.1.2 一般临床资料研究筛选完成冠状动脉内生理学评估符合FFR<0.8、CFR<2.3、IMR≥23的CMVD 患者入选该试验,分组及相关的临床资料特征见表1,两组患者临床资料比较,差异无统计学意义(P<0.05),具有可比性。
1.2 方法
1.2.1 IMR 的检测冠状动脉造影按常规方法进行,运用0.014 英寸压力/温敏导丝系统测量冠脉血流储备分数(fraction flow reserve,FFR)及IMR。先在体外将压力导丝水平放置,使压力导丝前端感应器放置于室温生理盐水中进行校零。后经6F 的引导管将压力导丝的压力感应器推送至导管开口处,然后调制EQUALIZE 值在-10~+10 之间,再将压力导丝送入到病变血管远端(距导管口>5 cm)。然后将Radi Analyzer 系统调至测定CFR界面,测量远端冠脉血管内压力(Pd)。测定IMR之前首先从导引导管内弹丸式预推1 次3 mL 室温生理盐水,如压力导丝感应器显示温度下降>2℃,则以140 μg/(kg·min)的速度静脉泵入ATP(系沈阳光大制药有限公司生产),使冠脉达到最大充血状态,ATP 泵入90 s 后,分3 次每次抽取3 mL 室温生理盐水快速(<0.25 s)推入至冠脉远端,并在基线水平重复测定3 次平均传输时间(TmnHyp),IMR 值采用公式Pd×Tmn 计算[7]。心外膜冠脉存在侧支循环,则引入动脉内崁压放置预扩球囊阻塞冠脉近端,测量的压力数值是Pw,来矫正狭窄所造成的血流动力学影响,校正公式为IMR=Pa×Tmn×[(Pd-Pw)/(Pa-Pw)],其中Pa 为导管测得的主动脉内压力,Pw 代表冠状动脉内球囊充气完全封堵管腔后冠状动脉内压。FFR 值在IMR 测定过程中同时检测出来,CFR 由最大充血时血流的平均峰值速度(APV)与静止时APV 的比值导出。给药结束后继续记录30 s,取最低FFR 值为最终测量结果(图1)。给药过程中应注意观察患者不良反应,如房室传导阻滞、低血压、心悸、呼吸困难、胸闷等。
本例68 岁男性心绞痛患者静息心电图正常,运动心电图因严重心绞痛提前终止。其被转做侵入性冠状动脉造影,见图2A、2B,前降支及对角支狭窄60%~70%。3-T CMR 血管造影(正常射血分数60%;无局部壁运动异常),无明显的局部可逆灌注缺损,晚期Gadoliniumenhancement(LGE)成像无心肌梗死,提示梗阻性心外膜CAD。行腺苷负荷MR 检查,见图2C 心肌灌注减低,见图2D中间层面各节段波峰上升一致,上升缓慢,Segment1、2、3、4、5、6 峰值信号约为左心室血池峰值信号的20%(>50%正常),为低灌注节段MPRI=1.32 整体受损(<1.4),与2 条冠脉IMR >25 U 升高的阻塞性冠状动脉相对应。本病例表明,CMR 可以为微血管缺血提供客观的一站式评估,潜在地避免了多次检测和侵入性操作。

图1 2 组患者治疗前后IMR 压力曲线图Fig.1 IMR pressure curves before and after treatment in the two groups
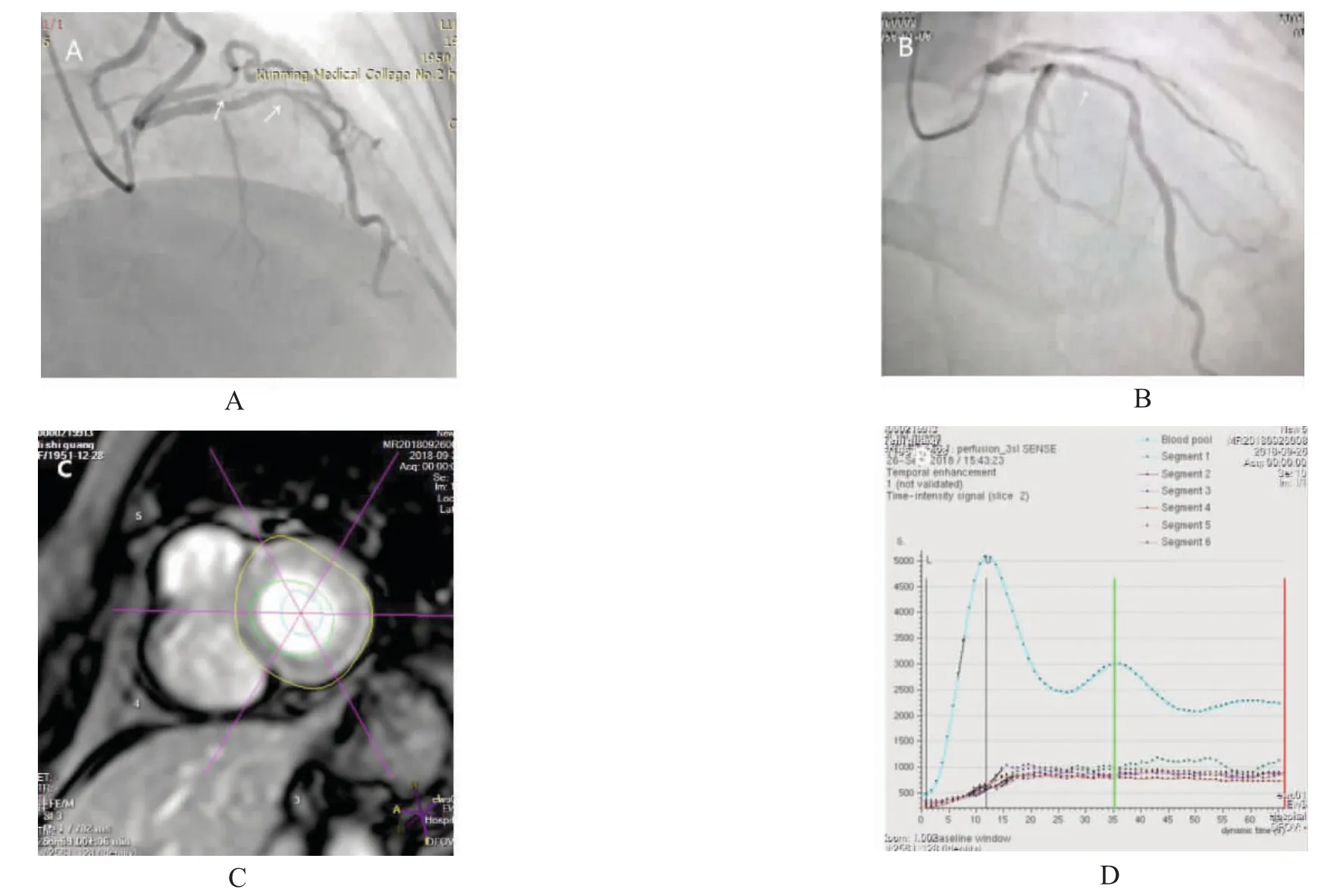
图2 应用腺苷负荷冠状动脉介入造影和腺苷负荷CMR 评价微血管诱导缺血Fig.2 Application of load interventional angiography and load CMR to evaluate microvascular induced ischemia
1.2.2 磁共振心肌腺苷负荷和(或)静态灌注成像采用Philip 公司Achieva 3.0T,TX 多源发射磁共振仪扫描仪。心脏腺苷负荷和(或)静态灌注显像,采用动态成像技术,以电影方式记录对比剂钆喷酸葡胺注射液(Gd-DTPA)首次通过左心室灌注心肌的过程。首先持续静脉注射ATP 注射液,剂量为140 μg/(kg·min)。用药时间为6 min,静滴3 min 后注射对比剂并采集图像,做心肌首过灌注扫描,在3 个左心室(LV)短轴成像切片(基底、中和远端LV 切片)中获得灌注图像。
灌注扫描结束后,再经高压注射器给予2 次注入造影剂Gd-DTPA 液,剂量为140 μg/(kg·min)。以TrueFISP 扫描成像在对比剂注入10 min 后行延迟增强扫描;延迟扫描结束后,再次注射对比剂,记录静态图像,用来测定FFR、左心室容量(LV)和质量,均使用标准化方法进行[8]。
采集的MRI 图像使用飞利浦Achieva 3.0T TX多源发射磁共振仪配套工作站(EWS)后处理心脏软件包进行分析、计算、处理,包括左心室心肌灌注CMRI 评价、左心室心肌DE-MRI 评价及心脏电影对心功能的评价。对MR 扫描图像由2 名以上诊断医师在双盲情况下进行分析判读。
CMR 图像上选定感兴趣区域(ROI),ROI 的LV 空腔区域被手动调节以包括空腔内的最大信号强度区域。MPRI 定义为:MPRI=RUstress/RUrest。RU 被定义为第1 次心肌灌注时间-强度曲线的最大上斜率与第一遍LV 腔时间-强度曲线的最大上斜率之间的比值,即采用半定量分析由研究者对标准化后的信号强度用图像分析软件绘制各节段心肌及对应层面LV 血池时间-信号强度也肌灌注曲线,根据各节段灌注曲线的特点,在不同心肌灌注等级的区域内选择不同位置的ROI 并绘制各个ROI 的时间-信号强度(T-SI)(SI-T)心肌灌注曲线,用各个ROI 峰值信号强度除以该ROI 所在层面左也室血池获得相对峰值信号强度,分别记录不同心肌灌注等级区域内各个ROI 的相对峰值信号强度(SImax)、最大上升叙率Slopmax,S=(SImax-SImin)/△T。使用AHA 16 段模型(心尖未成像),在2 张图像数据由于高应力心率获得的情况下,数据被记录12 段,平均MPRI 是12 段的平均值,计算跨壁MPRI[9],见图2 C、2D 显示了1位使用CMR MPRI 评估微血管性心绞痛的患者。
冠状动脉介入造影及心脏核磁共振检查前,长效硝酸盐、短效钙通道阻滞剂、α-阻滞剂、β-阻滞剂和ACE-I/血管紧张素II 受体拮抗剂在24小时内停用,长效钙通道阻滞剂在IMR 和CMRI测试前保持48 h。在测试前4 h 内不服用舌下硝酸甘油。
1.3 统计学处理
2 结果
2.1 一般临床资料
研究筛选完成冠状动脉内生理学评估符合FFR<0.8、CFR<2.3、IMR≥23 的CMVD 患者入选该试验,分组及相关的临床资料特征见表1。21例梗阻性心外膜CAD 患者冠脉造影定量分析的冠脉造影显示有显著性狭窄(66±9)%。
2.2 试验完成后两组患者比较
2.2.1 尼可地尔治疗两组患者冠状动脉造影结果比较入选阻塞性冠心病(远端血管FFR≤0.8、IMR≥25)的两组患者尼可地尔治疗前CFR、IMR比较差异无统计学意义(P>0.05);并且两组均有CMD 受损心肌的MPRI<1.4(P>0.05),见表2。尼可地尔组治疗后CFR、MPRI、Pd/mmHg 显著高于对照组(P<0.01),也显著高于本组治疗前(P<0.05);尼可地尔组治疗后IMR 显著低于对照组(P<0.01),也显著低于本组治疗前(P<0.05);FFR 值尼可地尔组治疗后与本组治疗前以及对照组治疗后无差异(P>0.05),见表2。
2.2.2 尼可地尔治疗后两组患者CMR 检查对照组负荷腺苷灌注心肌呈低灌注区表现(图3),治疗组其峰值信号强度,曲线上升斜率及对达峰时间改善(缩短)信号对比增强率均明显高于本组治疗前(P<0.05),见表2,其心肌信号强度-时间曲线的峰值信号增强约40%,见图3;尼可地尔治疗后其峰值信号强度,曲线上升斜率及信号对比增强率也明显高于治疗期(P<0.05),见表2,心肌信号强度-时间曲线的峰值信号增强约60%(图4)。仅通过检测心室中短轴节段,尼可地尔治疗后,治疗组比较对照组的平均跨壁MPRI 显著增高(P<0.01),见表2。
3 讨论
因为CMD 在临床中广泛存在,并且CMD 是冠心病远期预后及心血管事件发生的独立预测指标[10],所以CMD 的临床治疗也必须引起高度重视。CMD 被定义为冠状动脉微循环异常导致斑片状、广泛性心内膜下心肌缺血,而非梗阻性冠心病心外膜冠脉狭窄引起的心肌缺血[11]。超过60%阻塞性冠心病患者共存微血管病变[12]。阻塞性冠心病患者的CMVD,主要病理表现为内皮细胞和平滑肌细胞功能障碍,以及血管腔阻塞[13];许多因素被认为是CMVD 的致病因素,包括动脉粥样硬化性疾病的危险因素、激素和结构因素[2]等。所以,在心绞痛的阻塞性冠心病患者中,确认其伴随CMD,并引起的症状仍然具有挑战性,其引起的心肌缺血仍然是临床心脏病学实践中的一个诊断难题,而且对这类患者的治疗也是临床实践中非常值得探讨的。
诊断CMVD 目前仍然没有统一标准,2003 年Fearon 等[14]提出了IMR 的概念,术者在冠状动脉介入治疗时直接测定,IMR 可量化冠脉微循环功能障碍的严重程度,测定时不依赖心外膜动脉狭窄程度[15],避免侧支循环对狭窄远端血流的影响是植入近端阻塞球囊,反映的是冠脉微循环的病变,所以IMR被认为是目前最敏感、最准确的评估冠脉微循环损害程度的指标[16]。合并阻塞性冠状动脉疾病的CMVD 的诊断,在稳定性心绞痛和CMD 女性的患者中,CMD 可以通过IMR 阈值≥25 U[17-18]来识别。而且升高的IMR 则与较低的Duke 大学运动负荷缺血分数[18]相关,具有预测长期重大心脏不良事件的价值[19]。
表1 两组患者临床资料比较()Tab.1 A comparison of the clinical data of the two groups()

表1 两组患者临床资料比较()Tab.1 A comparison of the clinical data of the two groups()
表2 尼可地尔治疗后两组FFR 值、IMR 值、MPRI 值比较()Tab.2 Comparisons of FFR、IMR and MPRI values between the two groups after nicodil treatment()

表2 尼可地尔治疗后两组FFR 值、IMR 值、MPRI 值比较()Tab.2 Comparisons of FFR、IMR and MPRI values between the two groups after nicodil treatment()
与治疗前比较,*P<0.05;与治疗后对照组比较,##P<0.01。

图3 对照组腺苷负荷后心肌灌注储备成像Fig.3 Myocardial perfusion reserve imaging after adenosine loading in the control group

图4 尼可地尔治疗后腺苷负荷后心肌灌注储备成像Fig.4 Myocardial perfusion reserve imaging after adenosine loading after nicordil treatment
对合并阻塞性冠状动脉疾病的CMVD 的诊断,《中国专家共识》的建议[2]:在PCI 治疗解除心外膜冠状动脉狭窄病变后,如注射腺苷后测量的CFR <2.0,可确诊合并阻塞性冠状动脉病变存在的CMD[20];CMR 显像显示心肌灌注缺损或钆延迟显像增强,可诊断为CMVD。
心肌缺血诊断的金标准是核素扫描,但随着磁共振技术可获得高分辨力图像等的发展,其已逐渐成为无创评估心脏结构、功能、心肌缺血[21]的金标准,并且无创性CMR 测定MPRI 可用于检测有创性负荷冠状动脉造影所确定的CMD[9]。
正常情况下心肌的耗氧量和氧供保持平衡状态,为了反映冠状动脉在负荷状态下增加血流量的能力,用冠状动脉最大能力扩张时(充血状态)和静息状态下的心肌血流量之比来表示,即MPRI,即CMR 能通过延迟增强扫描显像心肌灌注来反映心肌微循环的状态。在心绞痛患者中,已取得临床验证的CMR 检测可以诊断冠心病,并能够客观地评估心外膜和微血管心绞痛,即测出CMRI[22];Pepine C J 等[23]研究,对女性X 综合征的患者,经CMR 腺苷首次灌注,平均跨壁心肌MPRI 为1.83±0.5 诊断出CMD。所以CMRI 可以用作诊断CMD 的一种非侵入性工具。基于此,我们纳入标准是通过冠状动脉介入检查,经温敏/压力导丝系统测定CFR、IMR 值,检出梗阻性冠心病的CMVD,在冠状动脉二级治疗的基础上给予尼可地尔口服治疗六个月以上受试者,对照不用尼可地尔为参考组,复查IMR、MPRI,观察尼可地尔治疗梗阻性冠心病伴CMVD 效果。本研究的结果:在稳定型梗阻性冠心病患者,伴有由创伤性IMP所定义的CMVD 在尼可地尔治疗后,首次CMR 灌注时降低了MPRI,改善了冠状动脉微循环障碍。
Alexander L 等[22]的研究,MPRI 阈值1.4 是检测阻塞性冠心病(FFR≤0.8)诱发心肌缺血的最佳阈值(AUC:0.95;95%置信区间0.85~0.99,P<0.001),其阻塞性冠心病远端心肌缺血为真阳性;对照组正常心肌为真阴性;而MPRI 阈值为1.6时,阴性预测值较高(95% CI:79%~99%;95%CI:77%~99%)用于排除CMD 引起的明显诱导性缺血[27]。我们测定尼可地尔治疗前两组MPRI(1.42±0.68 vs 1.48±0.7)低于1.6 诊断这组冠心病患者伴有CMVD。另外De Bruyne 等[24],以梗阻性心外膜CAD 下游心肌为代表的MPRI 截止阈值,采用FFR(≤0.8)方法[24]确定MPRI 截止阈值,得到MPRI 阈值也是1.4。
《中国专家共识》依据冠状动脉微血管功能为终点的随机临床研究或非随机观察研究[25],推荐了对CMVD 治疗[2],其中以急性ST 段抬高型心肌梗死合并CMVD 的治疗给出了综合各种药物的治疗,而本研究是探讨对稳定性梗阻型冠心病合并CMVD治疗。尼可地尔是三磷酸腺苷(ATP)敏感性钾通道开放剂,在结构上属于硝酸盐类可开放血管平滑肌ATP 敏感性钾通道(ATP-sensitive potassium channel),加速钾离子从细胞内流出,从而减少钙离子内流,扩张冠脉微循环的小血管,改善冠脉微循环功能[26];同时减轻心脏前负荷;还可增加环磷鸟苷(cGMP)合成而扩张微循环血管。可有效扩张心外膜下冠状动脉和冠状小动脉,因此尼可地尔应作为冠状动脉微血管心绞痛的首选推荐药物[27]。尼可地尔对于患者CMVD 长期预后的影响尚不明了[2],本研究初步观察到尼可地尔长期治疗合并阻塞性冠心病降低了IMR(P<0.01)、MPRI(P<0.01),取得了治疗CMVD 良好效果。
总之,本研究验证了6 个月长期口服尼可地尔可有效治疗阻塞性冠心病患者伴发的CMVD。但这项研究也有几个潜在的局限性:入选的病例是冠状动脉造影定义的梗阻性冠心病,阻塞性冠心病可能与较低的平均MPRI 的血管区域变化和节段性视觉灌注异常有关;尽管磁共振能够通过心肌灌注成像间接反应冠状动脉微循环变化,但仍需要扩大病例,额外的长期随访,以确定心肌灌注储备的无创性和有创性措施之间的关系;以及进一步确认CMR 衍生的MPRI 测试导致改善心血管结果。

