MALDI-TOFMS在药物基因组学检测中的应用及展望
曹书娟 刘彬 朱安娜
药物基因组学是近年来由药物遗传学发展而来的临床基因检测新兴领域,其研究目的是阐明基因多态性对药物效应和毒性的影响以及对药物作用靶点的确定。不同个体的药物遗传多态性是药物基因组学的基础,表现为药物代谢酶的多态性、药物受体的多态性以及药物靶标的多态性等。在药物代谢相关途径中的细胞色素P450(Cytochrome P450proteins,CYP)酶系是最主要的药物代谢酶,目前已发现的CYP基因至少有53个,其中的CYP3A4、CYP2D6、CYP2C19、CYP1A2、CYP2E的编码基因具有较为显著的遗传多态性意义[1]。在药物受体基因多态性的研究中最为重要的药物受体是G蛋白偶联受体,目前研究较多的是β2-肾上腺素受体[2],另外5-羟色胺(5-hydroxytryptamine,5-HT)载体[3]、维生素D受体(Vitamin D receptor,VDR)[4]和血管紧张素转换酶等基因多态性[5]对药物的作用也密切相关。药物转运基因及相关疾病通路基因如ApoE基因[6]、编码P-糖蛋白的基因[7]、VKORC1基因的多态性研究[8]也证实了药物转运基因和疾病通路上的靶点基因与药效之间的密切关系。药物基因组信息是当前个体化精准医疗的一个重要部分,药物基因组学的临床实施可以实现个性化医学,提高治疗的功效,安全性和成本效益。另一方面,通过区分有效适用人群,使得更多的新药能够有效通过临床试验,为治疗提供更多可能。
随着基因检测技术的发展,目前已有多种分子检测平台可应用于药物基因组学的研究,包括基于聚合酶链式反应(Polymerase Chain Reaction,PCR)技术的荧光定量PCR[9]、突变扩增阻滞系统荧光定量PCR[10]、微滴式数字PCR[11]、生物芯片技术[12]、Sanger测序技术[13]和二代测序技术[14]等。这些技术各具特点,也各有局限性。基质辅助激光解吸附电离飞行时间质谱(Matrix-Assisted Laser Desorption/Ionization Time of Flight Mass Spectrometry,MALDI-TOFMS)技术的出现和发展克服了PCR技术多重扩增能力不足的问题,解决了药物基因组检测中多个变异位点同时检测的需求;其不依赖于荧光探针和荧光类试剂的检测流程,质谱技术的高准确性和高灵敏度保证了检测的高准确度和重复性;同时其检测成本相比二代测序技术具备更高的性价比。
越来越多的研究者在MALDI-TOFMS技术平台上取得了大量的研究成果,MALDI-TOFMS已经成为分子检测的又一有力工具。本文将系统性的介绍MALDI-TOFMS技术原理和使用该技术开展的药物基因组相关的研究进展。
1 MALDI-TOFMS技术原理
MALDI-TOFMS出现于20世纪80年代,该技术突破了传统质谱仅可以进行小分子物质分析的局限,使得核酸、蛋白质等生物大分子也可以应用质谱进行研究[15],极大推进了基因组学和蛋白质组学的发展,为生物和医学领域带来革命性突破。
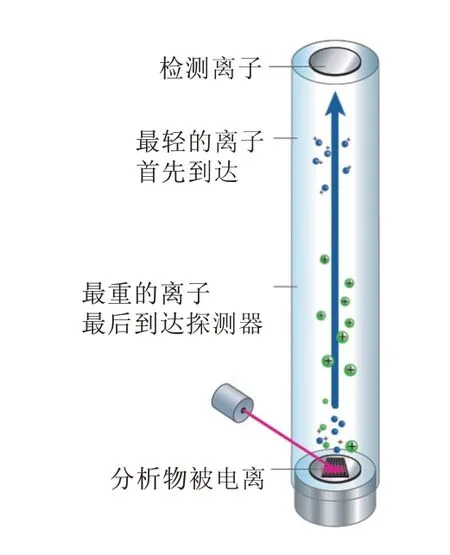
图1 MALDI-TOF质谱系统原理图示(绘制)Figure1 Schematic representation of the MALDI-TOF mass spectrometry system
质谱技术的基本原理是通过将待测样品离子化,产生一系列不同质荷比的离子,质量分析器能够测定该样品中不同种类离子的分子量,按照从小到大的顺序依次排列从而得到一张分子量峰图。质谱仪器可以通过样品进样方式、离子源、质量分析器的类型等方面进行分类。其中,MALDI-TOF MS采用的是样品与基质混合进样,激光解吸附电离作为离子源以及飞行时间法进行质量分析。
首先,MALDI-TOFMS的电离过程需要基质参与。基质多采用有机酸[16],因其具有很强的激光能量吸收能力,能够增强样品对激光的吸收,同时降低激光对样品的破坏,对样品起到保护作用。样品与基质混合后发生共结晶,经激光照射,基质迅速蒸发,其与样品之间的分子间作用力快速减弱,样品分子进而得以释放。与此同时,基质将吸收到的激光能量传递至样品分子并使其带上正电荷。该技术灵敏度极高,仅需pmol-fmol级别的微量样本即可进行检测[17]。随后,离子化的样品分子进入飞行时间质量分析器,通过脉冲电场对离子化的样品进行加速,不同分子量的离子在真空飞行管内以各自不同的恒定速度向离子检测器飞行,从而可以区分出样品中不同分子量的离子(图1)。在核酸检测的应用中,分子量的检测范围多限制在1000-10000D这个分子量区间内[18]。在现有的成熟应用中,MALDI-TOF能够检测的变异类型包括单核苷酸多态性(Single Nucleotide Polymorphism,SNP)、拷贝数变异(Copy Number Variations,CNVs)、甲基化、插入缺失突变(In/Del)等。
对于药物基因组学检测中常见的变异类型:SNP和CNV的检测,MALDI-TOF主要通过基于多重PCR、单碱基延伸及质谱检测相结合的技术来实现。例如在SNP检测中,首先通过PCR的方法将含有待测SNP的目的片段进行扩增,扩增结束后利用虾碱性磷酸酶(Shrimp Alkaline Phosphatase,SAP)将体系中的剩余的dNTP去磷酸化不能够继续与模板结合。然后在反应体系中继续加入SNP多态性碱基所对应的单碱基延伸引物(Unlined base Extension Primer,UEP)和双脱氧核糖核苷(Dideoxynucleotide,ddNTP)等相关成分进行单碱基延伸反应。在这个过程中,UEP可与待测SNP的5′端结合且只延伸一个碱基,根据模板中不同的SNP序列即可得到不同的延伸产物。经离子交换树脂脱去反应体系中的Na+、K+、Mg2+等离子后,即可将反应液进点样至MALDI-TOF MS专用芯片上进行质谱检测并得到延伸产物的分子量图谱(图2)。

图2 MALDI-TOFMS检测实验流程Figure2 MALDI-TOFMSworkflow
核酸质谱能够实现在同一个反应孔中对多个不同位点同时进行扩增和延伸,单孔反应最多高达40重。因同一SNP位点上不同基因型(纯和型或杂合型)对应的碱基不同,且各个SNP位点上所设计的引物序列不同,即可在结果中以分子量图谱的形式显示出同一位点上的不同基因型,并区分出不同位点上的延伸产物峰(图3)。同样的原理在检测基因突变时,在突变位点上检出的不同碱基即为野生型和突变型。除了基因突变的定性检测,根据质谱图谱中检测峰的峰面积与该分子量核酸片段的含量成正比的关系,还能够计算出样本中野生型和突变型在该位点上的比例。目前MALDI-TOFMS能够检出最低0.1%的突变比例。
一次质谱可以同时分析多至几十个位点的基因分型,图为9个位点同时检测的结果示例[19]。
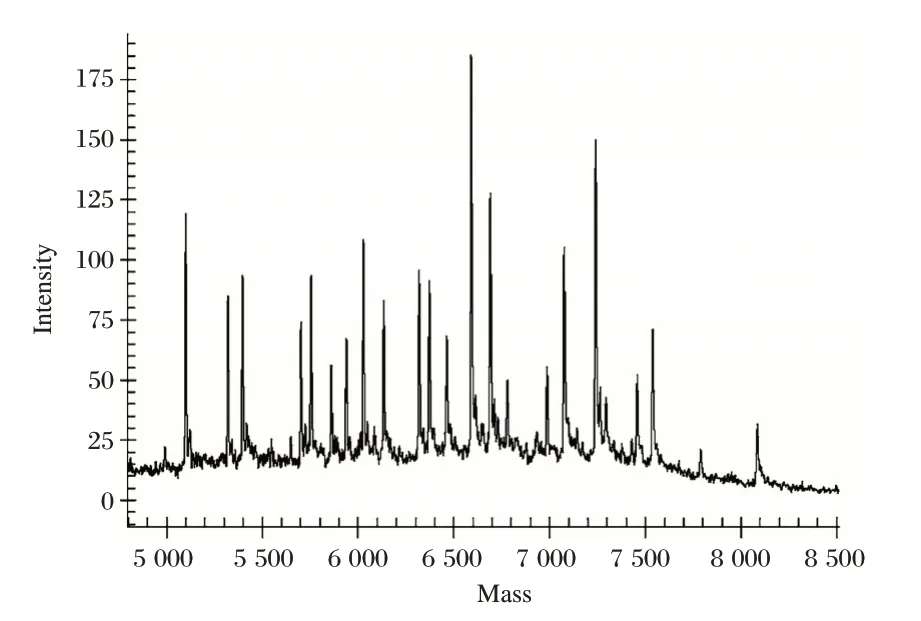
图3 MALDI-TOFMS原始数据Figure3 MALDI-TOFMS rawdata
2 MALDI-TOFMS在药物基因组相关分子标记检测中的应用
Liu等研究者为研究相关基因位点对氯吡格雷用药的影响,在MassARRAY核酸质谱和焦磷酸测序两种技术平台上,在458位中国汉族心血管患者群体中,对CYP2C19(*2,*3,*4,*5,*17)和ABCB1C3435T基因上共6个SNP进行了基因分型检测,并使用Sanger测序作为验证技术。其中有6份样本在两种方法中呈现不同结果。经Sanger测序验证,MassARRAY平台的检测结果与Sanger测序结果完全一致,6个SNP的次等位基因频率在该患者群体中分别为27.1%(CYP2C19*2),5.9%(CYP2C19*3),0%(CYP2C19*4),0%(CYP2C19*5),1.1%(CYP2C19*17),40.9%(ABCB1)。该项研究的研究者认为MassARRAY核酸质谱技术平台能够为氯吡格雷相关药物基因组检测提供精准的检测结果,同时相比于焦磷酸测序MassARRAY能够实现高性价比、快速出具报告和更高的检测通量[20]。奥氮平作为二代抗精神疾病药物,在精神分裂症的治疗中起到非常重要的作用。但不同患者对奥氮平的应答反应个体差异巨大。Zhou等研究者使用MALDI-TOF技术对两个独立的实验组进行12个与奥氮平药物反应相关的SNP检测,结果显示其中有2个SNP在两个实验组中均与奥氮平的药物应答反应显著相关。并指出这2个SNP在后续临床开展的奥氮平治疗中起到重要参考作用[21]。
CYP2D6基因的CNV也是药物基因组学研究中常见的一种多态性形式。常见的CNV检测方法只能对CYP2D6基因的单一区域进行检测,以确定拷贝数,而人类CYP2D6基因常为与CYP2D7假基因的杂交型基因,因此这些常规方法的单一区域检测很可能得到不准确的拷贝数或药物代谢信息。使用MALDI-TOFMS通过对CYP2D6基因中不同区域设计多个检测位点同时进行检测,深度覆盖杂交型CYP2D6基因,能够获得更为精准的拷贝数变异信息,通过设计CNV,SNP以及In/del的检测组合,可以实现对一系列药物基因组基因位点的同时检测,提供一套快速,经济,准确的检测方案。实验数据表明MALDI-TOF质谱能够准确进行CYP2D6基因多态性分型,是一种经济有效的药物基因组检测方案[22]。同时MassARRAY核酸质谱技术也常常作为其他分子检测技术的验证标准,Liu等研究者设计了一套基于荧光定量PCR技术的含32个SNP的CYP450家族基因分型和拷贝数变异panel,并使用Mass ARRAY核酸质谱以及数字PCR(Droplet Digital PCR,ddPCR)技术对该panel检测结果进行验证,结果证明核酸质谱技术具备与ddPCR一致的灵敏度和准确性[23]。美国Assurex公司针对精神类疾病用药制定了一套基于MassARRAY核酸质谱平台的检测方案,和参考方法的平行比较结果具有100%的一致性[24],基于此Assurex使用该平台开发的GenesightPGx检测pane l覆盖55种常见药物,检测量每年超过50万人次。国内的第三方检测机构和医院也逐渐基于此平台开展高血压、精神分裂、抑郁症等疾病用药基因检测。
3 展望
现有的可用于药物基因组学相关研究的技术和平台,如荧光定量PCR、微滴式数字PCR,生物芯片技术,Sanger测序技术和二代测序技术等,这些技术在实验操作难度、检测时间的长短、检测成本的控制、数据分析难度等方面各有利弊。相比之下,已有大量研究证明MALDI-TOFMS利用多重PCR技术,在同一个反应中同时检测高达40个变异位点,不但能够对药物基因组学中相关SNP进行检测,还能够在同一panel中同时检测CNV和Indel,极大的提高了检测效率,节约了样本用量,同时其基于分子量的质谱检测方式提供了不依赖于荧光信号的检测准确度,以极高的性价比满足了药物基因组分子检测的需求。美国食品药品监督管理局(U.S.Food and Drug Administration,FDA)已于2018年批准美国Agena Bioscience公司的MassARRAY®MALDI-TOFMS可用于临床核酸检测[25]。在中国,达瑞生物的DR MassARRAY飞行时间质谱系统通过了国家药品监督管理 局(National Medical Products Administration,NMPA)审核,成为国内第一台获批IVD核酸质谱检测系统,批准其SNP方面的应用,如耳聋基因检测等。
随着全基因组关联分析(Genome-wide association analysis,GWAS)生物统计/信息平台的建立和发展,越来越多的基因多态性信息被发现与药物在体内的代谢、转运、和作用靶点密切关联。自2007年FDA批准了第一种遗传分子检测,根据CYP2C9和VKORC1基因多态性预测抗凝药华法林的敏感性[26-28],标志着药物基因组学已经开始由实验室研究走向实际应用。到目前为止已有140余种药物经FDA批准,在说明书中附上其药物基因组信息,用于指示不同基因型的临床患者在应用该药物时对疗效和毒性的预测作用[28],其中涵盖了高血压、内分泌、哮喘、高血脂、精神类、肿瘤等疾病的药物治疗。在我国,为进一步推进合理用药、安全用药,中华人民共和国国家卫生健康委员会于2015年7月颁布了《药物代谢酶和药物作用靶点基因检测技术试行指南》(国卫医医护便函〔2015〕240号)[29]。在指南中明确指出药物代谢酶和药物作用靶点相关的药物种类及其对应基因,进一步提高了药物基因组学检测的重要性并作出规范化的要求。
基于MALDI-TOFMS的核酸检测平台具备了独特的多重PCR技术,稳定且准确的检测结果,经济的检测成本和快速的周转时间,能够满足临床上越来越多的对中高通量SNP、CNV及Indel变异的定性和定量检测需求,这些优势也使得核酸质谱技术在基因检测领域显示出强大的竞争力。伴随全球对药物基因组研究日益增长的关注度和更多遗传标记的发现,以及对核酸质谱技术的了解与应用不断深入,该检测平台将成为分子检测实验室不可或缺的标准装备。

