Mg和Zr共掺杂TiO2对光催化还原CO2的影响
王杰,汪莉,贺拴玲,董新月,张晴
(北京科技大学 能源与环境工程学院,北京 100083)
人工光合成是CO2转化和利用的创新技术。TiO2对太阳光能的利用率极低[1],因此对TiO2进行改性研究成为了光催化还原CO2领域的研究热点,尤其对过渡金属、稀土元素及非金属研究颇多[2-5]。有研究者指出[6-8],利用金属Zr掺杂TiO2不仅可以保持TiO2和ZrO2原有的特殊性能,还能克服两者各自的缺点,具有更大的比表面积和热稳定性。碱金属改性TiO2后,催化剂表面容易形成碱性位点,这对于CO2在催化剂表面的吸附极为有利[9-11]。本文采用溶胶凝胶法制备了Mg-Zr共掺杂TiO2光催化剂,通过XRD、SEM、XPS、UV-vis、BET对催化剂进行表征,采用气-固相反应器对Mg/Zr-TiO2光催化还原CO2产生CO和CH4的性能进行了实验研究。
1 实验部分
1.1 材料与仪器
氯化镁、氧氯化锆、钛酸丁酯均为分析纯。
CD-1400X马弗炉;PL203电子天平;DF-101Z集热式恒温加热磁力搅拌器;XMTD-20485-2数显恒温磁力搅拌器;HG101-1A电热鼓风干燥箱;HSX系列氙灯光源;GC9790型气相色谱仪;Ultima-IV 3KW X射线衍射仪;Quanta 3D FEG型扫描电子显微镜;STA449F3型热天平。
1.2 催化剂的制备
1.2.1 Mg/Zr-TiO2催化剂的制备 采用溶胶凝胶法制备Mg和Zr共掺杂TiO2催化剂。量取一定量的钛酸丁酯和一定量的乙醇混合,搅拌1 h得到混合溶液A;称取一定质量的MgCl2·6H2O和氧氯化锆(控制Zr/Ti的摩尔比为0.25),溶解于醋酸、水和乙醇的混合溶液,形成溶液B;将B溶液缓慢滴加至A溶液中,搅拌得到透明均匀的溶胶;溶胶在50 ℃条件下陈化一段时间,然后在110 ℃条件下干燥;最后将干凝胶颗粒放入马弗炉中350 ℃下煅烧2 h,即得Mg/Zr-TiO2粉体。按照掺杂Mg含量的不同将所得催化剂标记为(m)Mg/0.25Zr-TiO2(m为Mg/Ti摩尔比)。
1.3 光催化实验
光催化还原CO2实验系统由供气系统、反应系统和检测系统三部分组成,气相实验装置见图1。
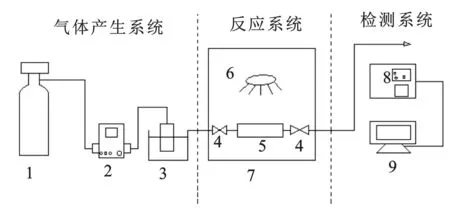
图1 光催化还原反应试验装置示意图Fig.1 Schematic profile of photocatalytic reduction reaction experimental apparatus
1.CO2气瓶;2.质量流量计;3.水浴锅;4.阀门;5.光反应器;6.光源;7.光化学反应仪;8.气相色谱;9.电脑显示仪
光催化还原CO2的性能测试反应在自制的反应器中进行。反应器体积约为140 mL,催化剂平铺在玻片上,催化剂用量约为0.100 g,氙灯置于反应器的正上方,光源功率约为300 W。本实验采用高纯CO2(99.999%),先将其以15 mL/min的流量通过水浴锅,形成含35%水蒸气的混合气体后再通入光催化反应器,通气20 min后达到吸附饱和状态后关闭出气口,再将流量减小至10 mL/min,10 min后停止通气。然后打开光源,光照10 h。光照结束后关闭光源,使用气相色谱仪分析产物生成量。本实验采用手动进样方式,检测反应产物为CO和CH4。
1.4 催化剂的表征
1.4.1 X射线衍射分析(XRD) 采用Rigaku Ultima-IV 3KW X射线衍射仪分析催化剂颗粒的物相。在40 mA的电流强度、40 kV加速电压下,采用铜靶(波长为0.154 06 nm),并以20(°)/min的速度扫描,其扫描角度是2θ=10~100°。
1.4.2 扫描电镜分析(SEM) 采用Quanta 3D FEG,在10 kV的条件下,进行电镜扫描,观察催化剂的表面形貌。
1.4.3 比表面积分析(BET) 采用TriStar II 3020比表面积和孔径测试仪通过静态氮物理吸附法测试催化剂比表面积、孔容及孔结构参数。
1.4.4 X射线光电子能谱分析(XPS) 采用Thermo SCIENTIFIC ESCALAB 250xi X射线光电子能谱仪对催化剂表面化学结构进行分析。
1.4.5 紫外-可见漫反射光谱分析(UV-Vis DRS) 采用UV3150紫外可见光近红外分光光度计分析样品对光的吸收情况,以标准白板调零,硫酸钡为参比,扫描范围 200~800 nm,采样间隔1 nm。
2 结果与讨论
2.1 微晶结构
图2为Zr/Ti的摩尔比为0.25时350 ℃煅烧的不同Mg含量的(m)Mg/0.25Zr-TiO2复合催化剂的XRD谱图。

图2 不同Mg掺杂量催化剂的XRD图谱Fig.2 XRD pattems of catalysts with different Mg doping amount
a.TiO2;b.0.25Zr-TiO2;c.0.5%Mg/0.25Zr-TiO2;d.0.75%Mg/0.25Zr-TiO2;e.1%Mg/0.25Zr-TiO2;f.1.5%Mg/0.25Zr-TiO2
由图2可知,TiO2在2θ=25.460,38.000,48.200,54.200,55.260,62.960,69.060,70.439,75.280°和82.978°出现了较强的衍射峰,分别对应锐钛矿型TiO2的(101)面、(004)面、(200)面、(105)面、(211)面、(204)面、(116)面、(220)面、(215)面和(224)面,说明TiO2在350 ℃煅烧2 h后所制备的催化剂为纯锐钛矿型TiO2。0.25Zr-TiO2也出现上述锐钛矿型 TiO2的晶面,其特征衍射峰峰位全部向小角度偏移,如0.25Zr-TiO2的(101)晶面位于2θ=25.240,无ZrO2相出现,说明 Zr4+进入TiO2的晶格取代了Ti4+,且由于Zr4+半径(0.072 nm)比Ti4+半径(0.064 nm)大,Zr4+掺杂后引起TiO2晶格畸变,从而导致晶格膨胀。掺入Mg后无ZrO2和MgO出现,TiO2的晶型仍然没有改变,Mg2+掺杂到TiO2中取代晶格位置上的Ti4+,这样TiO2晶格中原来Ti4+结点处将缺少2个电子,为了平衡电价,必然在近邻形成带正电的氧空位,且各个晶面的衍射峰峰位与TiO2相比也均向小角度偏移,与0.25Zr-TiO2相比,(m)Mg/0.25Zr-TiO2在各个晶面的衍射峰峰位均向大角度偏移,这归因于Mg2+(0.057 nm)比Ti4+半径(0.064 nm)小,引入Mg后,TiO2(101)晶面的峰变得尖锐,这说明TiO2的结晶度增大。
2.2 微观形貌
图3为煅烧温度为350 ℃,不同Mg掺杂量的(m)Mg/0.25Zr-TiO2(350 ℃)光催化剂的SEM图。如上显示,颗粒粒径均为纳米级,粒径大小约在20 nm左右,与根据谢乐公式计算出的晶粒粒径大小相吻合。当Mg的掺杂量为1%时,(m)Mg,Zr/TiO2颗粒的分散性最好。随着Mg含量的增加,纳米颗粒分散性会变差,从Mg掺杂量为1.5%的SEM图中可以看到颗粒之间越来越紧密,形成团聚。


a.0.5%Mg/0.25Zr-TiO2(350 ℃) b.0.75%Mg/0.25Zr-TiO2(350 ℃) c.1%Mg/0.25Zr-TiO2(350 ℃) d.1.5%Mg/0.25Zr-TiO2(350 ℃)图3 不同Mg掺杂量催化剂的SEM谱图Fig.3 SEM spectra of catalysts with different Mg doping amounts
2.3 表面组成
为了研究1%Mg/0.25Zr-TiO2复合材料表面各元素的化学形态,对复合材料进行了XPS检测,进一步确定其Mg、O、Ti和Zr的存在状态。图4为1%Mg/0.25Zr-TiO2复合材料的XPS能谱,结合能以C在284.8 eV处的1s峰为参考值。复合材料中仅存在Ti、Zr、O、Mg和C五种元素,C元素可能是有机物未完全焙烧干净或者仪器本身偶尔带有的碳氢化合物所致。从Ti2p的 XPS图谱中可以看到,Ti2p3/2和Ti2p1/2的平均结合能分别为458.4 eV和464.2 eV,由 Ti2p谱峰拟合的结果分析,458.6,458.1 eV应分别归属于TiO2和Zr0.85Ti1.5O4的Ti2p3/2结合能的位置,Zr0.85Ti1.5O4在催化剂表面以无定形态分布,伴峰Ti2p1/2的结合能为 464.1 eV,属于TiO2。O1s 的峰形不对称,说明1%Mg/0.25Zr-TiO2复合材料表面存在多种结合态的氧,对O1s的XPS谱图进行分峰拟合,在结合能529.8 eV和531.06 eV出现了分别属于TiO2和Zr0.85Ti1.5O4中晶格氧的窄谱峰,在结合能532.2 eV处出现了表面羟基(OH-)的谱峰,这也说明了1%Mg/0.25Zr-TiO2复合材料表面有大量的羟基氧。从Zr3d XPS图谱中可以看到,复合材料中Zr在Zr3d5/2和Zr3d3/2的平均结合能分别为181.81 eV和184.20 eV,与X射线光电子标准谱图里的数据基本一致,这说明Zr是以Zr4+的形式存在。Mg l的XPS谱图谱1 303.40 eV处有结合能峰,应归属于Mg掺杂进入TiO2晶格中形成Mg—O—Ti键中的Mg1s峰,诱导O—Ti键上的电子向Ti偏移,从而导致Ti2p3/2的结合能值比TiO2中Ti2p3/2结合(458.8 eV)略微减小,这与文献报道中的一致[12]。
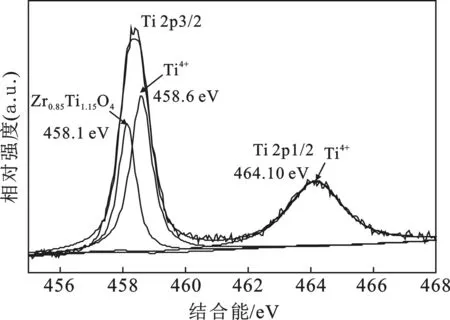
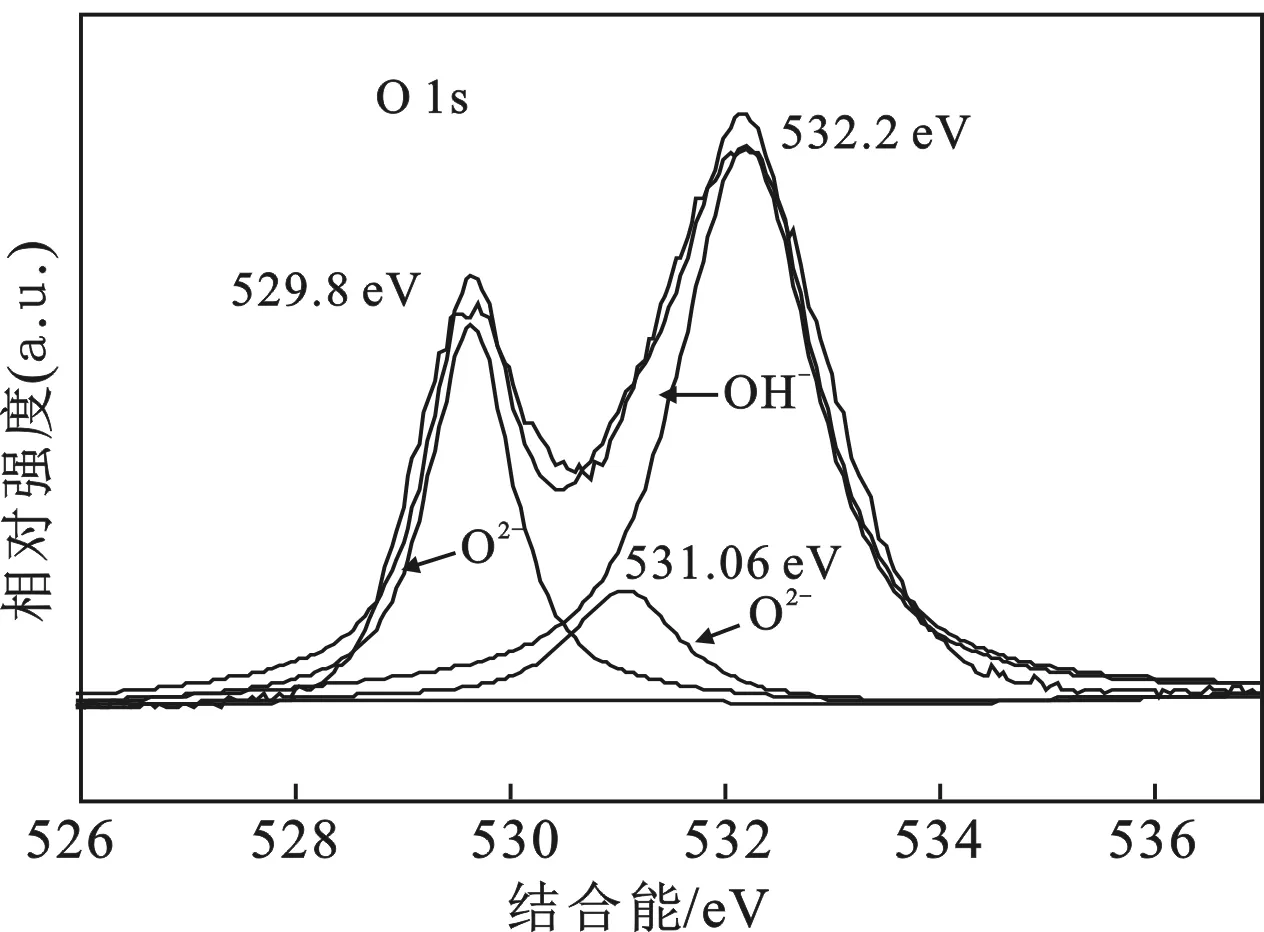


a.Ti2p谱峰拟合图 b.Ols 谱峰拟合图 c.Zr3d 谱峰拟合图 d.Mg1s 谱峰拟合图图4 1%Mg/0.25Zr-TiO2复合材料的XPS能谱图Fig.4 XPS image of 1%Mg/0.25Zr-TiO2 composites
2.4 比表面积
TiO2、0.25Zr-TiO2以及不同Mg掺杂量的Mg/Zr-TiO2几种催化剂的比表面积对比见表1。可以发现Zr和Mg的单掺杂以及Zr、Mg共掺杂都能提高TiO2的比表面积,这将为光催化还原CO2提供更多的反应位点,有利于提高光催化活性,其中1%Mg/0.25Zr-TiO2(350 ℃)的比表面积最大,为76.906 m2/g,这也是其光催化活性最高的一个因素。

表1 Mg/Zr-TiO2掺杂TiO2样品的比表面积Table 1 BET of Mg/Zr-TiO2 samples
2.5 紫外-可见漫反射分析
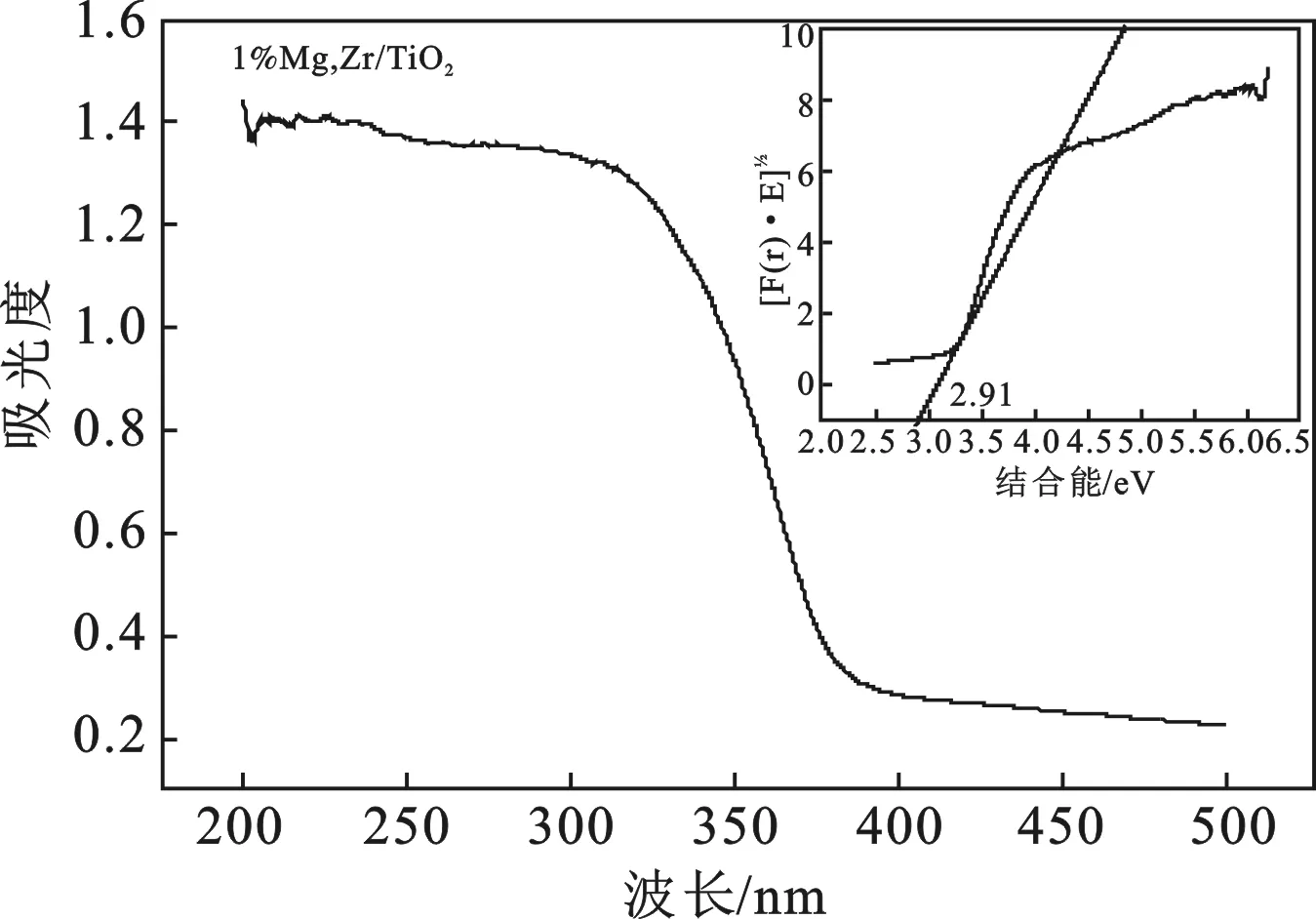
图5 1%Mg/0.25Zr-TiO2的UV-Vis DRS图谱Fig.5 UV-Vis DRS of 1%Mg/0.25Zr-TiO2 samples
使用Kubelka-Munk(KM)方程和Tauc绘图方法从反射[F(R)]光谱确定样品的UV-Vis吸收边和带隙能。图5显示的是1%Mg/0.25Zr-TiO2(350 ℃)的UV-Vis DRS图谱,其光吸收带红移至400 nm,且其光吸收范围相比纯TiO2的光吸收范围更宽,1%Mg/0.25Zr-TiO2(350 ℃)的带隙能为2.91 eV,与锐钛矿TiO2的禁带宽度3.20 eV相比明显减小,说明其在接受光照后,更容易形成激发态发生光催化反应。Mg和Zr的引入,二者起到协同作用,既能够提高TiO2在紫外光下的光催化活性又能够提高在可见光照射下的光催化活性。
2.6 光催化还原CO2的性能
图6显示了不同Mg掺杂量的Mg/0.25Zr-TiO2(350 ℃)光催化还原CO2时CO和CH4产率,其中1%Mg/0.25Zr-TiO2在紫外光照射10 h时后光催化效率最高,光催化还原CO2的产物CO和CH4的生成量分别为54.89 μmol/g和0.73 μmol/g。
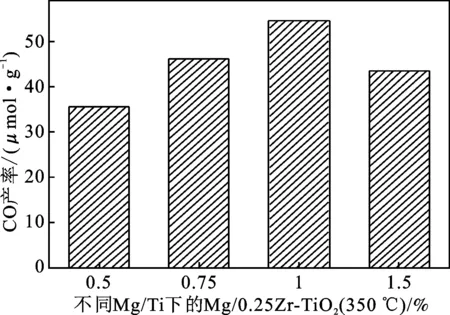
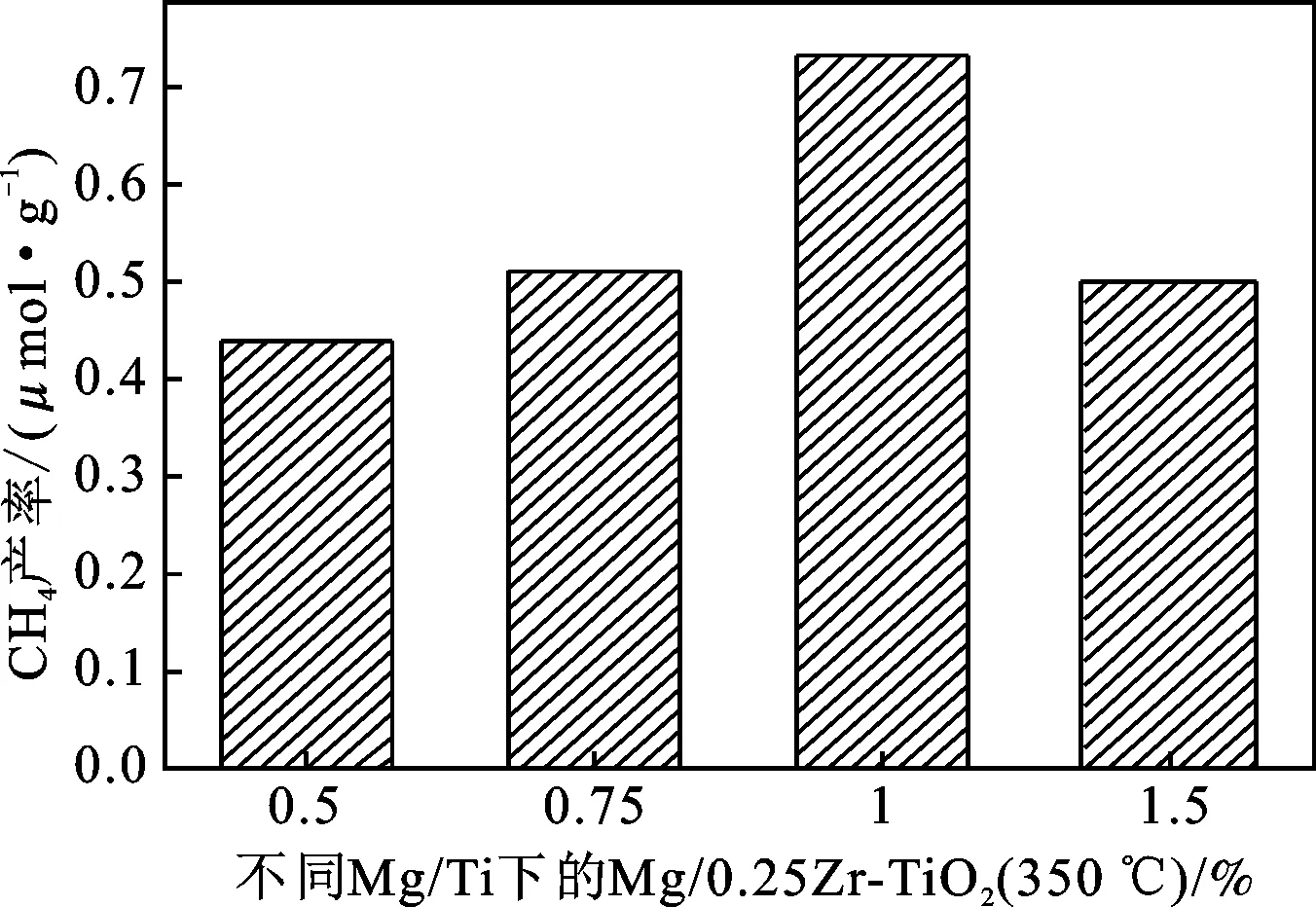
图6 不同Mg/Ti比的(m)Mg/0.25Zr-TiO2(350 ℃) 紫外光下光催化还原CO2的性能Fig.6 Photocatalytic reduction of CO2 under ultraviolet light at (m) Mg/0.25Zr-TiO2 (350 ℃) with different Mg/Ti
图7显示纯TiO2、Mg/TiO2、Zr/TiO2作为光催化剂紫外光照10 h还原CO2时CO的累积产生量分别为 14.19 ,18.34,40.46 μmol/g,CH4的累积产生量分别为0.51,0.65,0.54 μmol/g。Mg和Zr的引入都能提高TiO2的光催化还原CO2的催化效率,Zr的单掺杂改性TiO2比Mg改性TiO2更有利于提高CO的产量,而Mg改性TiO2相比于Zr的单掺杂改性TiO2其对CH4产率提高更为明显。Mg和Zr共掺杂改性TiO2对光催化还原CO2的产物CO和CH4都有明显的提升。Zr4+进入TiO2的晶格中取代Ti4+,Zr4+比Ti4+能有效的捕获电子,使晶格发生畸变,产生结构缺陷,抑制光生电子-空穴对的复合,有利于提高光催化活性,Mg2+掺杂到TiO2中倾向于取代晶格位置上的Ti4+,这样TiO2晶格中原来Ti4+结点处将缺少2个电子,为了平衡电价,必然在近邻形成带正电的氧空位。添加适量的Mg和Zr(Zr∶Ti=0.25)制得Mg、Zr共掺杂改性的Mg/Zr-TiO2复合光催化剂相比于单掺杂的Mg/TiO2、Zr/TiO2光催化活性有了明显提高,说明Mg和Zr共同引入TiO2对其光催化还原CO2起到了协同作用,能进一步提高光催化还原CO2活性。最佳Mg的掺杂比为Mg∶Ti=1%。
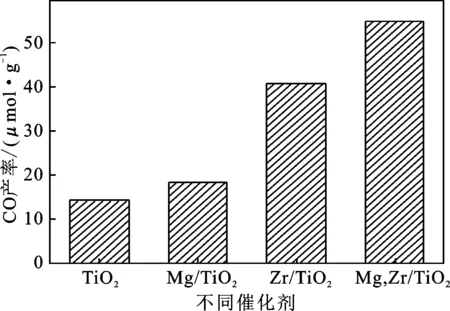
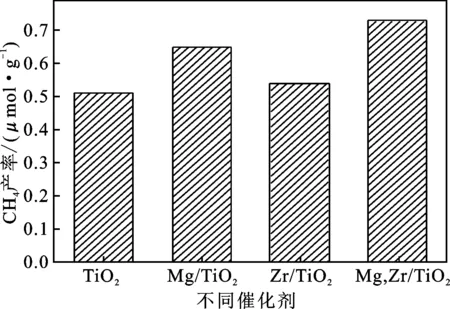
图7 TiO2、1%Mg-TiO2、0.25Zr-TiO2和 1%Mg/0.25Zr-TiO2紫外光下光催化还原CO2性能Fig.7 Performance of photocatalytic reduction of CO2 over TiO2,1%Mg-TiO2,0.25Zr-TiO2 and 1%Mg/0.25Zr-TiO2
图8显示了TiO2、1%Mg/TiO2(350 ℃)、1%Mg/0.25Zr-TiO2(350 ℃)三种催化剂在可见光照射10 h后CO和CH4的生成量。由图8可知,可见光照射10 h后三种催化剂光催化还原CO2产生的CO的量分别为10.59,17.17 μmol/g和 42.47 μmol/g,CH4的产生量分别为0.32,0.53 μmol/g和0.56 μmol/g。可以明显的看到Mg和Zr的引入能够明显提高TiO2在可见光下的光催化还原CO2的催化性能。单独的纯TiO2作为光催化剂时,由于其带隙能(3.2 eV)的原因,在光子能量较大的紫外光照射下更容易达到激发态以产生电子-空穴对,发生光催化反应,而光子能量较小的可见光不容易使其达到激发态,因此纯TiO2在可见光下的光催化活性不高。通过引入Mg和Zr能够拓宽其光吸收范围,降低其带隙能,提高在可见光和紫外光下的光催化还原CO2性能。
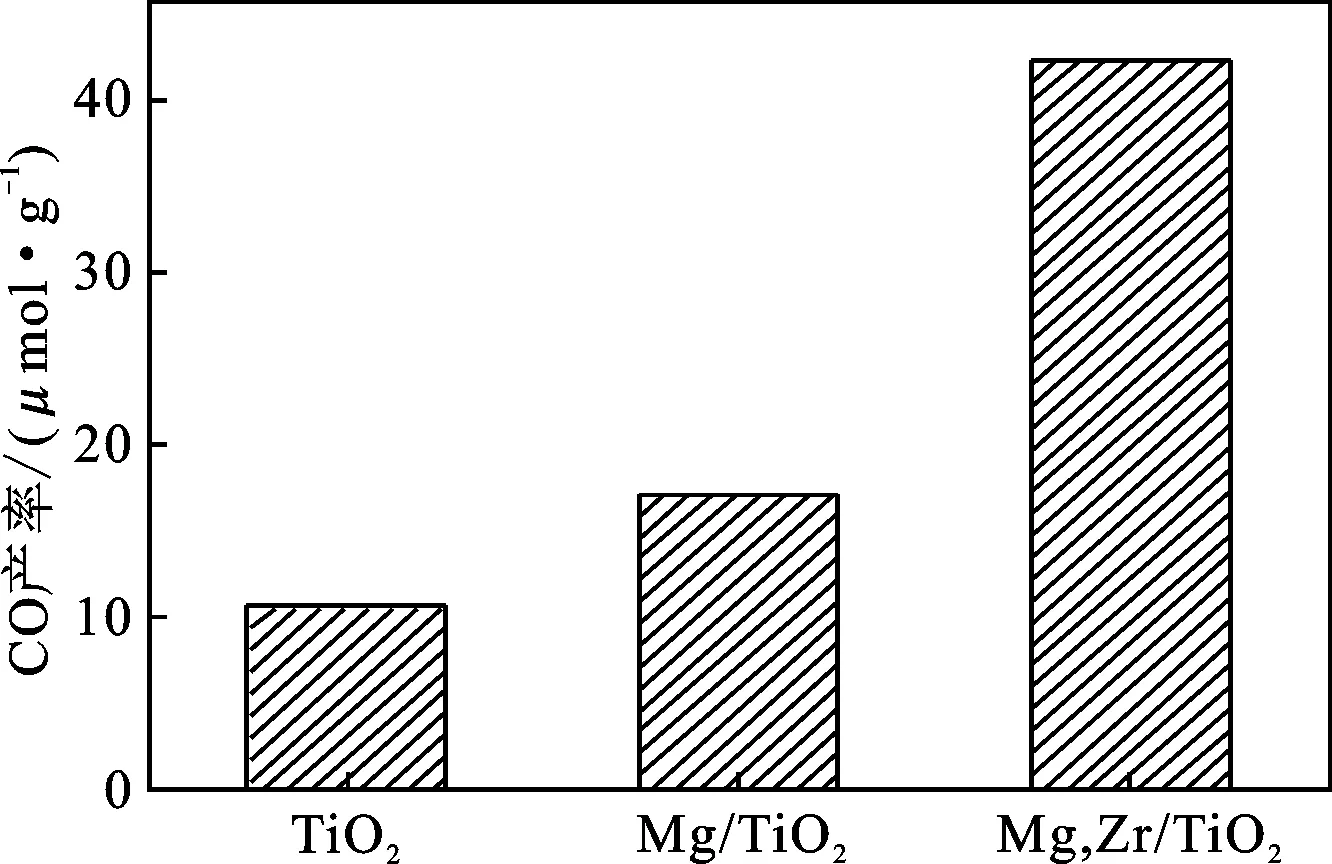
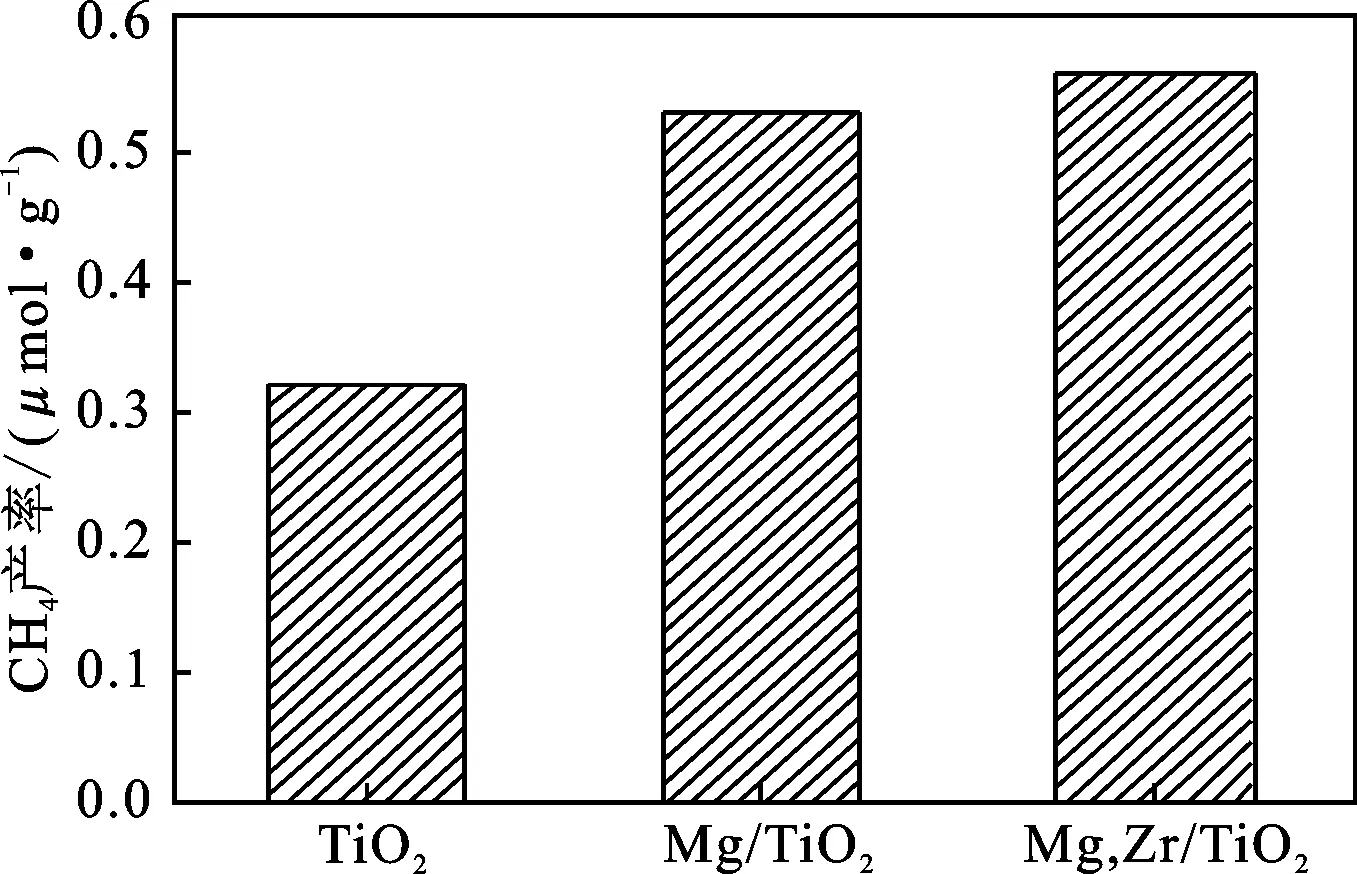
图8 TiO2、1%Mg-TiO2和1%Mg/0.25Zr-TiO2 可见光催化还原CO2性能Fig.8 Performance of visible light catalytic reduction of CO2 by TiO2,1% Mg-TiO2 and 1% Mg/0.25Zr-TiO2
由以上分析可得,碱金属Mg和金属Zr对TiO2进行共掺杂后,Zr4+进入TiO2的晶格中取代Ti4+,Zr4+比Ti4+更能有效的捕获电子,使晶格发生畸变,产生结构缺陷,抑制光生电子-空穴对的复合,有利于提高光催化活性。Mg2+进入TiO2的晶格间隙中取代Ti4+,形成氧空位,并且在催化剂表面形成了大量的碱性位点,这有利于CO2在催化剂表面的吸附,同时Mg2+的掺杂在TiO2晶格中产生杂质能级,这也在一定程度上抑制了光生载流子的复合。Mg和Zr的共掺杂同时能够拓宽TiO2光吸收范围,降低其带隙能,从而提高了可见光下的光催化活性,Mg和Zr的共掺杂可以起到协同作用,进一步提高TiO2的光催化性能。
3 结论
(1)本文采用溶胶凝胶法制备了TiO2、Zr-TiO2和(m)Mg/0.25Zr-TiO2复合催化剂。光催化还原CO2实验结果表明,Mg和Zr的共掺杂可以起到协同作用,明显提高TiO2的光催化性能。在气相反应器中,紫外光照10 h后,最佳掺杂量的1%Mg/0.25 Zr-TiO2复合催化剂催化还原CO2生成CO和CH4的产量为54.89 μmol/g和0.73 μmol/g,是纯TiO2的3.87倍和1.43倍。
(2)通过SEM、XRD、BET及XPS等表征分析可知,(m) Mg/0.25Zr-TiO2复合催化剂的表面形貌为纳米级颗粒。Zr4+掺杂进入TiO2的晶格取代Ti4+,使得TiO2晶格发生畸变,产生晶格缺陷,有效抑制光生电子-空穴对的复合。Mg和Zr共掺杂使TiO2的结晶度明显增大,Mg2+进入TiO2的晶格取代Ti4+形成 Mg—O—Ti键结构,产生氧空位,同时在催化剂表面产生大量碱性位点。
(3)通过UV-Vis DRS表征分析可知,1%Mg/0.25 Zr-TiO2复合催化剂的禁带宽度为2.91 eV,比TiO2的禁带宽度要小,说明Mg和Zr的共掺杂降低了TiO2的带隙能,扩展了可见光响应范围,1%Mg/0.25 Zr-TiO2复合催化剂可见光下10 h生成CO和CH4量分别为42.47 μmol/g和0.56 μmol/g,是纯TiO2的4.01倍和1.75倍。

