不分泌型多发性骨髓瘤并间变性浆细胞瘤1例
谢静 关军 杨航 覃双来 王兵 胡作为
作者单位:430065 武汉 湖北中医药大学第一临床学院
不分泌型多发性骨髓瘤(non-secretory multiple myeloma,NSMM)是以恶性浆细胞增生伴血和尿中缺乏可检测的单克隆免疫球蛋白(M-成分)为特征,占骨髓瘤的1%~5%[1],临床罕见,诊断困难,易漏诊或误诊。本文报道不分泌型多发性骨髓瘤并间变性浆细胞瘤1例,以期提高对该病的认识。
1 临床资料
患者,女性,64岁。2014年6月因“全身乏力、心慌、浮肿进行性加重半年余”于外院住院治疗,发现胸骨、双侧髂骨压痛,诊断为冠状动脉粥样硬化性心脏病(心绞痛型),给予抗血小板聚集、改善冠脉血供、延缓心室重塑、利尿等治疗,症状未缓解。2014年8月本院收治入院,患者胸骨、双侧髂骨疼痛症状明显。查体:胸骨、双侧髂骨压痛阳性。既往有脑梗塞、冠心病、高血压病史,2009年L5腰椎压缩性骨折,2014年再次出现腰椎压缩性骨折,饮食、睡眠欠佳,体力较前明显下降。辅助检查:血红蛋白67g/L,尿素氮11.2 mmol/L,β2微球蛋白 4.00 mg/L,血沉40 mm/h。诊断为多发性骨髓瘤,骨髓增生异常综合征。完善免疫固定电泳、肿瘤标志物、骨髓细胞学、流式细胞学、骨髓瘤全套等检查。血清KAP游离轻链(尿)水平(96.46 mg/dL)升高,比值(8.6125)明显异常。体液免疫功能:IgG<4.72 g/L,IgA<0.26 g/L,IgM<0.16 g/L。骨髓细胞学检查示细胞增生活跃,浆细胞约占31.5%;可见原幼浆,约占16.5%,胞体稍大,大小不一,核仁1~2个,清楚,胞浆嗜碱性;可见双核浆细胞,细胞有成簇聚集现象(图1)。流式细胞学检测示骨髓中可见Kappa单克隆增生的浆细胞,约占有核细胞的21.08%,考虑为浆细胞骨髓瘤。X线检查示肋骨、骼骨、颅骨等多处扁骨骨质破坏(图2)。患者有典型骨髓改变(浆细胞>15%)及广泛性骨质破坏等2处损害,无异常免疫球蛋白血症,尿中无本一周氏蛋白,免疫固定电泳(尿、血)示阴性,符合NSMM诊断标准。随后行5个周期TCD方案化疗(环磷酰胺0.4 g,d1、d8、d15;地塞米松 10 mg,d1~2、d8~9、d15~16、d22~23)及3个周期VCMP方案化疗(长春新碱2 mg,d1;环磷酰胺 600 mg,d1;马法兰 8 mg,d1~4;强的松 60 mg,d1~14),化疗结束后评估骨髓达微小缓解。
2016年11月患者因腰痛行CT检查,左腰部及髂骨旁见软组织肿块影,行左臀部实性包块穿刺术。包块穿刺标本活检免疫分型示细胞以淋巴细胞为主,浆细胞约占全部有核细胞的8.48%,表达CD38、ckappa,部分表达 CD56dim、CD138dim,不表达 CD19、CD20、clambda,不能排除单克隆性异常浆细胞可能,表型异常(图3)。病理诊断:(臀部)间变性浆细胞瘤。免疫组化检查示:LCA(-),CD138(+),CD38(部分+),MUMI(+),PIasma(-),CD3(-),CD20(-),Kappa(±),Lambda(-),Ki-67(LI:67%),CyclinD1(+),CD56(-)。异常免疫球蛋白检测未见异常M带,游离轻链比值为12.29。流式免疫分型检查示约9.65%细胞考虑为单克隆性异常浆细胞,表型不正常。骨髓活检示异常浆细胞约占40%,提示疾病进展。患者及其家属因无条件行含硼替佐米的方案治疗,拟服用雷利度胺、地塞米松降低肿瘤负荷。最终患者因多发髓外骨髓瘤浸润合并肺部感染于2017年3月22日死亡。

图1 骨髓穿刺涂片(HE×1000)Fig.1 Bone marrow smear(HE×1000)
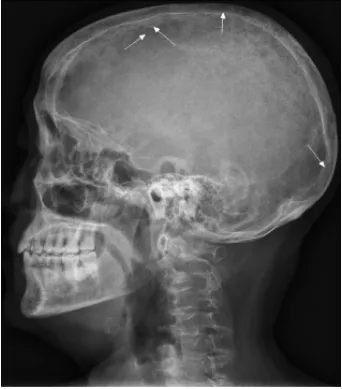
图2 患者颅脑X线片检查图片Fig.2 Patient's brain X-ray examination picture

图3 包块穿刺活检流式免疫分型细胞图Fig.3 Block puncture biopsy flow immunophenotyping cell diagram
2 讨论
多发性骨髓瘤国际骨髓瘤工作组诊断标准:⑴高钙血症(血钙浓度>11.5 mg/dL)、肾功能不全(肌酸酐>2 mg/dL 或肌酐清除率<40 mL/min)、贫血(血红蛋白<10 g/dL或比正常值低2 g/dL以上);⑵生物标志物包括:骨髓中克隆性浆细胞≥60%,受累区和非受累区FLC比值为100或以上,受累区FLC≥100 mg/L或MRI发现一个以上局灶性病变(累及骨或骨髓)中的一种或多种;⑶伴骨病变(在X线骨骼摄片、全身MRI或全身PET/CT检查中发现存在的一处或多处溶骨性病变)。其中有一种特殊分型,即NSMM,患者外周血、尿检查未见单克隆免疫球蛋白。回顾国内外文献,发现多数接受此类转换的NSMM患者预后不良,建议行免疫组化或流式细胞仪检测,以区分不生产型和不分泌型,然后行免疫固定电泳和血清游离轻链检测,以检测早期复发[2]。根据细胞质内免疫球蛋白的发现,非分泌型骨髓瘤被分为不产生和不分泌两种类型,其中不产生型约占15%,且浆细胞不能产生免疫球蛋白;而85%为不分泌型,可产生免疫球蛋白,但不将其分泌出细胞[3]。本例患者尿中无本一周氏蛋白,免疫固定电泳(尿、血)检查示阴性,骨髓细胞学检查亦未见异常免疫球蛋白血症,流式细胞学检查可见增生的浆细胞,属于不分泌型。
NSMM常为多系统受累,且缺乏特异性临床症状,50%~70%的患者因溶骨性病变出现骨性疼痛[4]。本例患者以不明原因贫血(血红蛋白67 g/L)就诊,无明显肾损害、高钙血症、反复感染、高黏滞综合征等。提示对于首发症状不明的患者,应深入分析其阳性体征(如患者查体胸骨、双侧髂骨压痛阳性)及既往病史,并鉴别溶骨性病变及冠心病,以防误诊或漏诊[5]。本例患者后因臀部包块疼痛症状明显,考虑骨髓瘤髓外浸润,诊断为(臀部)间变性浆细胞瘤。由于NSMM的M蛋白阴性,疗效不能根据M蛋白水平进行判断,只能根据骨痛、贫血及高钙血症的程度,以及髓外浆细胞的体积、数量,骨髓及活检中浆细胞的比例[6],考虑疾病进展。目前国内仅见唐大寒等[7]报告的1例“无分泌型”多发性骨髓瘤合并髓外浆细胞瘤。文献报道约80%的NSMM患者对初始化疗有反应[8],对目前的治疗药物耐药率极高[9]。本例患者先后予TCD方案和VCMP方案化疗,化疗后骨髓细胞学检查显示达微小缓解,提示化疗有效。后期合并间变性浆细胞瘤,同时肺部感染,说明患者免疫功能严重低下。
多发性骨髓瘤是一种常见的血液系统恶性肿瘤,表现为浆细胞异常增生,中位生存时间为3~4 年[10]。BOURANTAS[11]报道 NSMM 的预后与多发性骨髓瘤无显著差异。吴学宾等[12]报道NSMM的生存期为6个月至12年,平均45个月。NSMM合并间变性浆细胞瘤的预后及治疗尚未有文献报道,本例患者行雷利度胺和地塞米松治疗未明显缓解,因多发髓外骨髓瘤浸润合并肺部感染死亡,生存时间为3年余,与上述研究报道一致。目前该病的发生机制及治疗均未明确,仍有待进一步探索。

