多次扩创 负压吸引治疗软组织社区获得性MRSA感染
张燕平 韩叶萍 艾进伟 李光辉 杜晨飞
作者单位:1.450046 郑州,河南中医药大学;2.450002 郑州,河南省中医院
自1961年首次发现耐甲氧西林金黄色葡萄球菌(MRSA)以来,MRSA已经成为重要的医院感染病原菌[1],因其致病力强、传播范围广,且易产生多重耐药成为当前困扰临床治疗的一大难题[2]。随着MRSA感染区域向院外扩散日益明显,临床中将医院外因素引起的、近1年内无医源性感染高危因素,于门诊或入院48 h内细菌培养分离出MRSA病菌等感染称为社区获得性MRSA(CA-MRSA),多为皮肤关节软组织的感染[3]。近年来CA-MRSA的发生率呈上升趋势,鉴于院内MRSA耐药性的不断升级及其面对的治疗困境,对于CA-MRSA的治疗方案应谨慎选择,结合多种手段降低或减少抗生素的使用,规范临床用药。2017年1月—2018年6月,我科通过多次清创、VSD负压吸引、皮肤减张缝合,联合敏感抗生素,治疗20例发生于皮肤软组织及骨的社区获得性MRSA感染患者,临床治疗效果满意。现报告如下。
1 资料与方法
1.1 一般资料选取2017年1月—2018年6月我科收治的20例软组织CA-MRSA感染者,其中男 8例、女12例;年龄40~85岁,平均62岁;手部4例、足部5例、背部5例,小腿4例、大腿2例;12例感染范围局限,8例感染范围较大、界限不明显,其中2例合并胫骨骨髓炎。除1例为4年前胫骨骨折手术钛板内固定外,其余病例身体健康,无外伤手术史,无激素、免疫抑制剂及抗生素使用史。主要表现为皮肤、软组织、骨的化脓、皮肤溃破、坏死渗出等感染症状,创面软组织炎症感染范围为:4 cm×6 cm~12 cm× 25 cm,2例出现脓毒症症状,无脓毒性休克发生。
1.2 CA-MRSA的诊断标准①在门诊或入院 48 h内,创面分泌物细菌培养结果为MRSA感染;②近1年内无医源性感染高危因素接触或住院经历;③无严重复杂基础病史;④CT、磁共振(MRI)检查显示病灶部位、范围、深度及是否波及骨髓。
1.3 治疗方法尽早彻底扩创、VSD负压吸引:完善检查后,均在入院48 h内在合适麻醉下对创面进行彻底扩创、清除创面分泌物、坏死无活力的筋膜肌肉组织(尽量保留皮肤),露出新鲜创面,以创面微渗血为清创标准,合并骨髓炎者行皮质开窗扩创减压;大量双氧水、生理盐水、碘附冲洗创面后止血。皮肤褥式缝合但缝线不打结、敞开创面。将负压敷料进行修剪,使其完全覆盖创面,创面较深呈深腔者先用负压敷料充填创面再用一层敷料覆盖,半透膜边缘超过敷料3~5 cm封闭创面,连接负压引流及冲洗装置,生理盐水500 mL+庆大霉素16万U持续引流冲洗,1次/d。3~4 d后去除负压敷料,创面先做细菌培养和药敏试验,观察创面变化情况,如创面仍有脓性渗出或坏死组织,再次扩创;若创面干净、肉芽组织新鲜,皮肤减张缝合,将原缝线拉紧打结,以不影响皮肤血运为度(若皮肤发白、表明缝线太紧),再次负压敷料封闭持续冲洗引流。3~4 d后再次皮肤减张缝合、更换负压敷料,待创面皮肤拉拢闭合后,常规换药,至伤愈拆线。根据药敏结果选择抗生素,根据创面情况决定抗生素使用时间,加强营养,纠正贫血、低蛋白血症、电解质紊乱。
2 结果
12例感染范围局限病例,选用较低级别的敏感抗生素,单独静脉滴注环丙沙星、左氧氟沙星或者克林霉素,1周后停用;8例感染范围较大、界限不明显者,生理盐水250 mL+万古霉素0.5 g静脉滴注,1次/8 h,其中7例万古霉素使用1周后改为上述低级别抗生素再使用1周,1例万古霉素使用2周后改为上述低级别抗生素再使用1周。
创面情况及细菌培养:19例在第1次更换负压敷料时(术后3~4 d),创面已干净、组织鲜红、无脓性分泌物,创面培养无细菌生长;1例第2次更换负压敷料时细菌培养转为阴性。18例在经过2次扩创、减张缝合、负压吸引后闭合创面,2例经过 3次更换负压敷料后创面闭合。所有患者创面均在3~4周内愈合,创面瘢痕不严重,肢体功能恢复良好。所有病例随访均超过半年,无复发病例。
3 典型病例
患者女,85岁,4年前右胫骨骨折钛板内固定,术后骨折愈合,正常行走,之后身体状况良好,无住院、抗生素使用史。半年前无明显原因出现右小腿原手术区域皮肤溃破、流脓。入院急查伤口分泌物细菌培养+药敏试验,结果显示为MRSA,对利福平、庆大霉素、左氧氟沙星、环丙沙星、复方新诺明、万古霉素、利奈唑胺、替加环素敏感,其中万古霉素的最小抑菌浓度(MIC)为1;红霉素、苄唑西林、克林霉素耐药。腰硬联合麻醉下去除内固定,清除皮下及钉道脓液,大量冲洗后,创面缝合、不打结,持续负压吸引,生理盐水500 mL+庆大霉素16万U冲洗,3次/d;生理盐水250 mL+万古霉素0.5 g静脉滴注, 1次/8 h;第4天去除负压敷料,创面新鲜,再次细菌培养已为阴性;皮肤减张缝合,继续负压吸引;术后第7天去除负压敷料,再次减张缝合后皮肤闭合,普通敷料包扎换药,并停用万古霉素;第24天创面愈合,下地行走正常。术后随访半年,无复发。患者术中及术后创面恢复情况见图1。
4 讨论
对于皮肤关节软组织的社区获得性MRSA感染,外科扩创引流是第一步,以往的治疗方法是彻底扩创、油纱或者碘附纱布填塞换药,换药次数多,患者痛苦,创面易污染且愈合较慢,可遗留较重的瘢痕。我们采用扩创后敞开创面、负压吸引方法,负压敷料覆盖并封闭原化脓性感染部位,使创面避免与空气中的病原菌及其他医源性感染因素接触,保护创面,减少污染;负压敷料填塞扩创后的深腔,起到占位效应,减少血肿、减少细菌繁殖机会。生理盐水联合庆大霉素持续灌注冲洗给药,既可促进伤口分泌物及坏死失活组织及时排出,又可使药物有针对性地直接作用于局部炎症感染创面,使炎症迅速消退,减少抗生素通过静脉全身给药的不良反应,一定程度上降低耐药性产生[4]。术后3~4 d更换负压敷料,方便根据创面情况判定抗生素及临床治疗方法是否有效,如创面干净、分泌物较少、肉芽组织新鲜、细菌培养阴性提示治疗措施得当,可停用抗生素,否则需要更换抗生素甚至治疗方案。扩创后创面敞开、缝线不打结,便于创面分泌物的及时排出,又有利于二期闭合创面。减张缝合时逐步收紧伤口,以不影响创面皮肤血运为度。通过多次减张缝合,既不会导致皮肤软组织的缺血、坏死,又可待肿胀减轻、皮肤张力降低后利用原位皮肤实现创面闭合,避免植皮或皮瓣手术[5]。
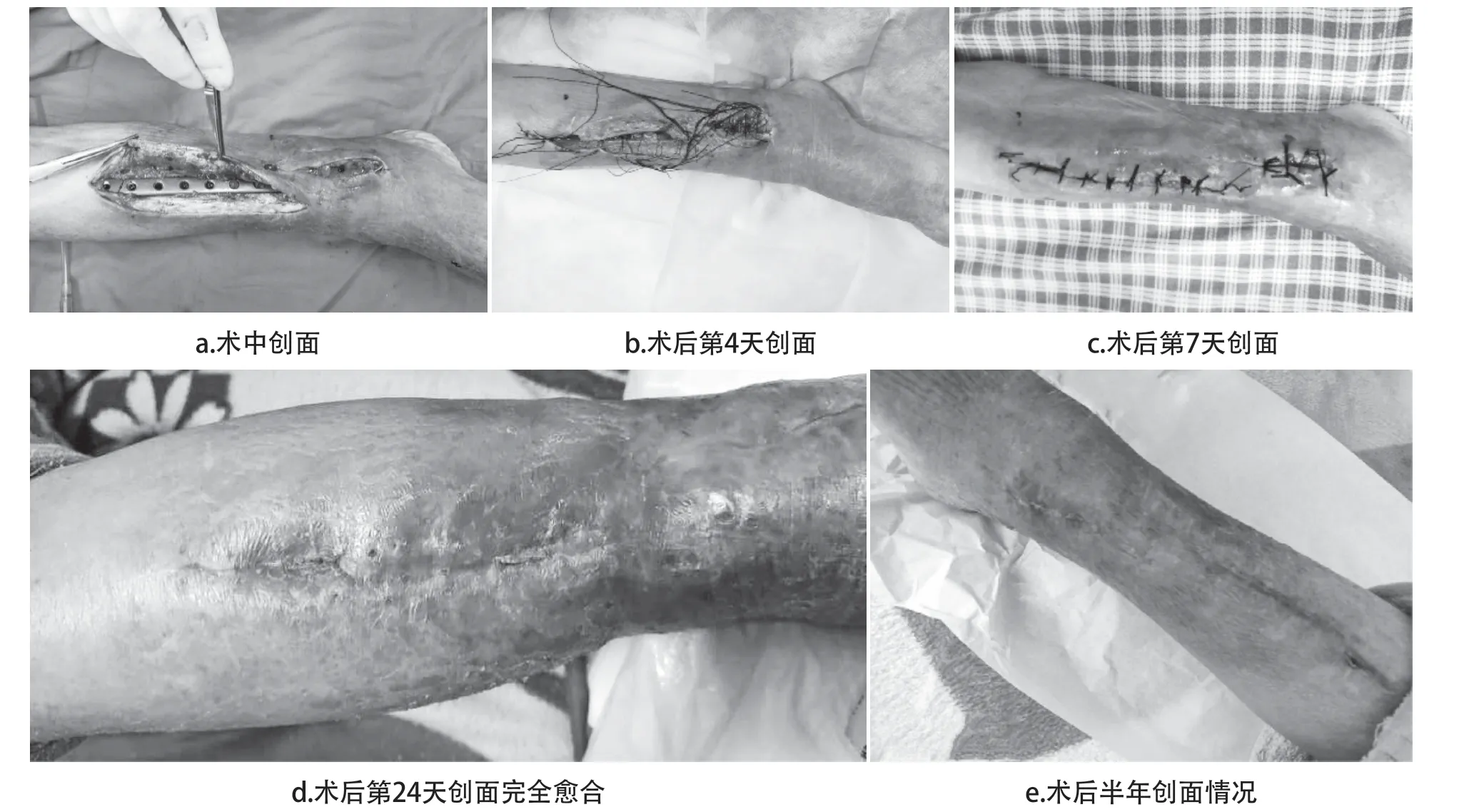
图1 患者MRSA感染创面术中及术后愈合情况
医院获得性MRSA(HA-MRSA)在ICU、呼吸科等常见,患者多具有基础病复杂、长期住院、侵入性有创操作、反复抗生素应用等病史[6]。HAMRSA对庆大霉素、环丙沙星、四环素、亚胺培南、美罗培南等多种抗菌药物均具有高度耐药性,比较难治。且近年来,随着抗生素的广泛应用,造成MRSA多重耐药现象的不断升级,进一步加剧了HA-MRSA感染的治疗难度。虽然万古霉素是治疗MRSA的首选药,但随着万古霉素应用增多,万古霉素耐药的金黄色葡萄球菌(VRSA)增多。一些欧洲国家治疗MRSA的指南规定,万古霉素限用于严重的MRSA患者。只有减少万古霉素的应用,才能降低VRSA的发生。而社区获得性MRSA耐药性较HA-MRSA耐药性低,相对来说有较多的抗生素选择。我们针对CA-MRSA引起的软组织感染,在外科彻底扩创、负压吸引基础上选择敏感抗生素。对于不严重的软组织感染,选择低级别的抗生素如克林霉素、左氧氟沙星、环丙沙星等,只有对严重的软组织感染,才用万古霉素。应用时参考药敏试验结果,万古霉素MIC值越低,治疗效果越好;MIC值≥2 μg/mL时应改用其他抗生素,使用过程中注意肾毒性和耳毒性的发生以及血小板减少不良事件。本组病例,万古霉素使用最长不超过2周。临床疗效满意,一定程度上减少了万古霉素的应用。
综上所述,对于软组织社区获得性MRSA感染创面,采用多次清创、负压吸引、皮肤减张缝合基础上,配合敏感抗生素,能有效地缩短病程,临床疗效满意。随访半年以上,未见复发病例,远期效果有待进一步观察。

