超声造影对原发性腹膜后神经鞘瘤的诊断价值
徐亚丹, 武文卿, 韩 红, 闻捷先, 季正标, 王文平
复旦大学附属中山医院超声科,上海 200032
神经鞘瘤又称施旺细胞瘤,起源于神经纤维鞘的Schwann细胞,多为良性、少部分为恶性[1-2]。神经鞘瘤多发生于脑神经的鞘膜、外周运动神经和感觉神经,有完整包膜,常为孤立肿块,与相关神经粘连在一起,呈偏心性生长,其长轴与神经干方向一致[3]。神经鞘瘤常位于头颈部及四肢,较少发生于腹膜后[4-5],原发性腹膜后神经鞘瘤(primary retroperitoneal schwannoma,PRS)占所有神经鞘瘤的0.7%~3%[6-7]。目前关于PRS的CT/MRI报道较多,而关于其超声表现较少[8],尤其是超声造影(contrast-enhanced ultrasound,CEUS)研究更少。因此,本研究收集了14例PRS的CEUS图像,旨在提高对此类患者的临床诊治。
1 资料与方法
1.1 一般资料 回顾性收集2013年1月至2018年11月在复旦大学附属中山医院经手术或穿刺病理证实为PRS的14例患者的临床资料。所有患者均行常规超声及CEUS检查。其中男性8例、女性6例,年龄33~74岁,中位年龄为52岁。5例患者表现为腰痛、腹痛等腰腹部不适,2例表现为尿频尿急,1例触及肿块,6例体检时发现肿块。实验室检查无特殊;甲胎蛋白(AFP)、癌胚抗原(CEA)、癌抗原199(CA199)、CA125等常见肿瘤标志物无特殊。9例患者经手术证实,5例患者经穿刺证实。本研究经医院伦理委员会审核批准。
1.2 仪器与造影剂
1.2.1 仪 器 选用Mindray Dc 8、Toshiba Aplio500、GE Logiq E9彩色多普勒超声诊断仪,探头频率为1~5 MHz,均配有实时灰阶谐波CEUS软件。
1.2.2 CEUS造影剂 造影剂采用Sono Vue(Bracco公司),由磷酯包裹的六氟化硫微气泡组成,微泡的平均直径为2.5 μm。造影前将24.98 mg粉剂和5 mL 0.9%氯化钠溶液混合并振荡混匀,制成造影剂,以气体容积计算,其浓度为8 μL/mL。每次造影时抽取2.0 mL溶液,经肘静脉呈弹丸式注射,随即快速推入5 mL 0.9%氯化钠溶液冲管。
1.3 超声图像评价 所有患者在CEUS前先行常规超声检查,对病灶进行观察,并记录其位置、数目、大小、内部回声、边界、形态、有无钙化;在进行超声多普勒血流成像时,记录血流信号及其位置、形状,记录阻力指数及收缩期峰值流速等。在多发病灶患者中选择目标病灶,对其合适切面后进行造影,注射造影剂2.0 mL;启动造影程序并开始计时,在造影模式下观察所选取病灶的增强表现,包括肿块增强起始时间、达峰时间、开始减退时间、增强方式及增强特点等。每次持续造影并观察5~10 min,录像记录造影全过程。根据病灶回声与腹部周围肌肉回声之间的对比,在各个时相中将病灶的增强程度分为高、低、等3种情况。造影过程中用超声仪器同步录像并存盘。如须重复造影,则2次造影间隔时间需大于15 min。最后将造影影像全程回放,并由2位高年资腹部超声医师分别进行分析并判断。
2 结 果
2.1 常规超声影像特征 14例肿瘤多位于腹部中轴线近脊柱处,其中4例位于腹部中轴线处、5例位于脊柱偏右侧、5例位于脊柱偏左侧。10例患者为单发,4例患者为多发,病灶直径大小49~174 mm,平均为(107.3±42.8) mm。14例患者共选取14个病灶,有7个表现为不均匀低回声、3个表现为均匀低回声、3个表现为混合回声、1个表现为无回声。13个病灶边界清晰,1个病灶边界不清晰。13个病灶形态规则,呈圆形或椭圆形;1个病灶形态不规则。9个病灶内部出现囊变区(图1),其中1个病灶为完全囊变。2个病灶内部出现钙化。
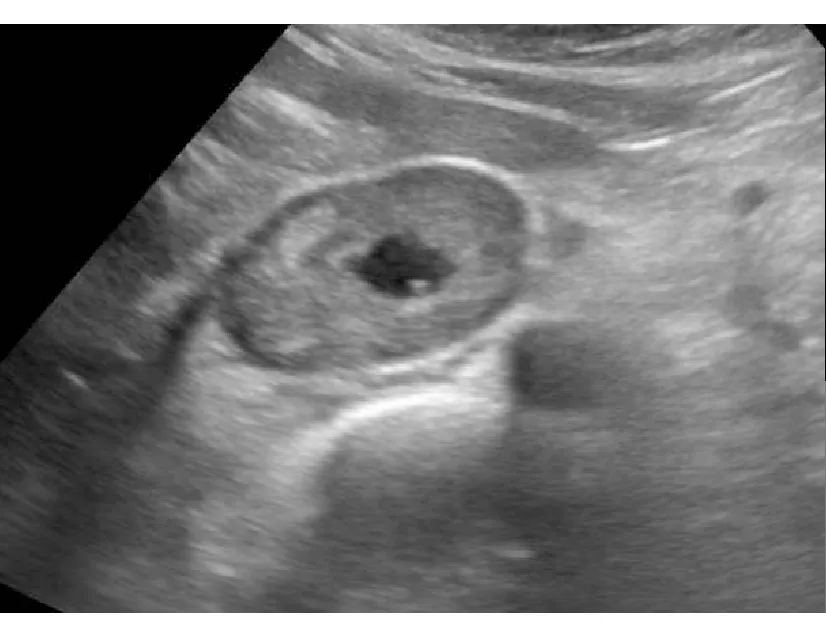
图1 患者女性,74岁,病灶呈低回声、形态规则、边界清,中间出现典型囊变区
在彩色多普勒血流显像上,5例患者的病灶周边及内部均有彩色血流信号,4例仅内部有彩色血流信号,1例周边有血流信号,4例未见明显血流信号。在有血流信号的10例患者中,8例表现为短线状彩色血流、2例表现为分枝状血流(图2);9例患者为动脉血流,1例患者为静脉血流,收缩期病灶最大流速(PSV)平均为(0.24±0.07) m/s,血流阻力指数(RI)平均为0.67±0.1。
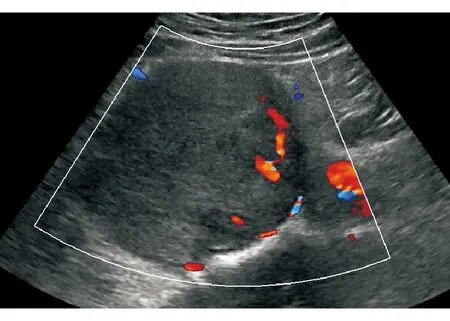
图2 患者男性,41岁,病灶内部血流丰富
2.2 CEUS影像特征 14个病灶均行CEUS,除1个病灶不增强外,余13个病灶均在增强早期快速增强,平均开始增强时间为(17.6±3.3) s、达峰时间为(30.9±6.1) s、开始减退时间为(42.9±9.8) s。肿瘤增强方式:弥散整体不均匀增强6例(图3A),分枝状整体增强5例(图3B),分隔增强2例(图3C),完全不增强1例(图3D)。分枝状增强中,2例均匀增强、3例不均匀增强。11个病灶内部出现始终不增强区(图3C),其中2个病灶内部出现小片状不增强区、8个病灶内部出现大片状不增强区、1个病灶为完全不增强。

图3 CEUS下PRS的增强特征
A:患者男性,63岁,不均匀低回声病灶增强后早期呈弥散整体增强;B:患者女性,44岁,病灶在常规超声上呈低回声,注射造影剂后出现分枝状整体增强,即病灶早期呈分枝状增强、后期整体增强(箭头);C:患者男性,59岁,病灶大部分为囊变区,仅见少数分隔,与左肾关系密切,增强后仅分隔部分增强、内可见不增强区;D:患者女性,33岁,病灶在常规超声上无回声,注射造影剂后始终不增强
3 讨 论
3.1 临床特征 PRS大多为良性肿瘤,生长缓慢,而腹膜后间隙组织疏松,给肿瘤的生长提供了较大的空间。PRS多发生于腹部中轴线近脊柱处,由于位置较深不易被发现,就诊时病灶往往已较大[9-10]。本组病例的病灶大小约107 mm。肿瘤长到一定程度可引起不典型的临床症状,如腹痛、腰痛等[11],而肿瘤较小时多为体检发现。PRS可发生于任何年龄, 35~50岁多发,男性多于女性[12]。神经鞘瘤虽为常见肿瘤,目前影像学研究较多,但PRS不易诊断。曲腾飞等[6]研究的59例PRS患者中,明确诊断者仅2例,13例增强CT提示为神经源性肿瘤,其余患者均未明确诊断。
3.2 常规超声特征 本组14例PRS均经病理证实,且均未提示恶性。在常规超声上,14例病灶大多为单发、多发者少见,往往表现为低回声,与以往报道[13]一致。病理上PRS可见Antoni A区和Antoni B区2种组织类型。由于Antoni B区容易发生变性,导致大多数肿瘤回声不均匀,甚至少数病灶表现为混合回声。本组3个病灶呈混合回声。由于大部分PRS为良性肿瘤且有完整包膜,因此病灶大多边界清楚、形态规则,呈圆形或椭圆形。本研究中仅1例病灶形态不规则,经穿刺证实为PRS。典型的PRS可出现囊性变,本组病例中64.3%(9/14)出现囊性变,其中2例病灶内部仅可见数条分隔,另1例完全囊变。Kim等[14]认为,囊性变对于本病的诊断具有重要意义。PRS可出现钙化,但概率较低,本组仅2例患者出现钙化;李忠明等[15]报道的22例PRS中,仅3例出现钙化,提示钙化不能作为提示PRS的征象。
彩色多普勒血流显像在71.4%(10/14)患者中检测到血流信号,且血流信号较丰富。虽然PRS为良性肿瘤,但其阻力指数较高,平均约0.67,与之前报道[16]一致。然而,之前研究[16]纳入的神经鞘瘤大多分布于外周,位于腹膜后者少见,而本研究病例全为腹膜后,说明PRS与外周神经鞘瘤具有相同的生物学特征。PRS与浅表神经鞘瘤的表现不完全相同,由于肿瘤位置较深及腹腔脏器结构复杂,典型的鼠尾征较难发现,本组病例未发现该征象。
3.3 CEUS特征 PRS的Antoni A区呈灰白色,细胞密集排列呈条索状、旋涡状或栅栏状;Antoni B区细胞稀疏,间隙有较多液体存在,可出现多种变性,如脂肪变、囊性变、黏液样变等[15]。CEUS时增强区对应肿瘤细胞丰富的Antoni A区,而不增强区对应为出血或囊变的Antoni B区,因此Antoni A区和Antoni B区的比例及Antoni B区的性质决定了增强方式及特点。目前关于PRS的CEUS表现报道罕见。本组PRS均在早期快速增强,且增强方式多样,其中弥散整体不均匀增强6例、分枝状整体增强5例、分隔增强2例、不增强1例。分枝状增强中,2例均匀增强、3例不均匀增强。弥散整体不均匀增强表现为早期整个病灶弥散增强,峰值时整体增强,但局部增强程度不一;分枝状整体增强表现为病灶早期呈分枝状增强,峰值时形成一个类似于整体增强的病灶;分隔增强表现为病灶囊变,仅分隔部分增强,其余部分不增强。本组病例增强过程中有78.6%(11/14)出现不增强区,其中2个病灶内部出现小片状不增强区、8个病灶内部出现大片状不增强区、1个病灶表现为完全不增强。本研究结果提示, PRS在CEUS时,多在峰值时表现为整体不均匀增强。而其增强CT主要表现为渐进性延迟轻中度强化,且多强化不均匀[15],这与PRS CEUS的强化方式相似,但CEUS是一个动态的增强过程,可观察的动态增强细节内容较CT更丰富。
3.4 超声诊断价值 本组病例中,2例误诊为恶性肿瘤,1例患者因左侧睾丸缺如考虑为精原细胞瘤,1例因完全囊变考虑为囊肿,2例诊断为神经鞘瘤,8例诊断为神经来源性肿瘤。2例误诊病例中,1例肿瘤呈不规则形状、边界不清,其高阻血流和增强后出现的出血、坏死、囊变区与恶性肿瘤相似;另1例为分隔增强的病灶,因其位置与左肾中下部关系密切,误诊为肾脏来源的囊性恶性肿瘤。因此,当PRS超声表现不典型时,诊断困难较大,容易误诊,而目前国内关于PRS的CEUS的研究仅有少数个案报道。本研究的主要不足亦为病例数较少,因此需要更大样本的研究来验证其CEUS表现,以提高超声对于PRS的术前诊断正确率。
综上所述,PRS好发于中青年,多发生于腹部中轴线近脊柱处,病灶体积较大。PRS常规超声多为不均匀低回声,单发多见,边界清楚,形态呈圆形或椭圆形,病灶内出现囊变区具有较大的诊断意义;彩色多普勒超声多可测及丰富血流,且多为高阻血流。PRS的CEUS表现多为早期增强,可呈整体不均匀增强或分枝状整体增强,增强后期常出现不增强区,囊变者表现为分隔增强或不增强;若出现以上较多征象,应考虑PRS。

