顶空气相色谱法测定Selexipag合成中间体的残留溶剂
齐海娟 崔浩亮 邓晓晴 王洪朋 高双双 哈婧

摘要:为了更好地控制Selexipag的产品质量,保证用药安全,建立了顶空气相色谱法,对Selexipag两个中间体4-[(5,6-二苯基吡嗪-2基)(异丙基)氨基]-1-丁醇(S5)和N-(2-氯乙酰基)甲基磺酰胺(S7)合成过程中残留的溶剂量进行检测。色谱柱为Kromat PC-624(V)(30.0 m×0.32 mm×18 μm)毛细管柱,程序升温方式,FID检测器温度为250 ℃,进样口温度为200 ℃,顶空瓶平衡温度为80 ℃,顶空瓶平衡时间为30 min,两个中间体所涉及的溶剂包括甲醇、乙醇、二氯甲烷、丙酮、乙酸异丙酯、甲苯及四氢呋喃。结果表明,在此色谱条件下被测溶剂完全分离,各溶剂标准曲线相关系数r2均大于0.997,平均回收率为 95.1%~106.2%,精密度、稳定性及重复性的RSD值范围为1.78%~4.60%。气相色谱法操作简单,准确度、灵敏度高,可用于检测Selexipag 原料药中残留的有机溶剂,为其中间体的质量控制提供科学依据。
关键词:色谱分析;顶空气相色谱;残留溶剂;Selexipag;中间体;含量测定
中图分类号:TQ4607;R9272文献标志码:A
QI Haijuan,CUI Haoliang,DENG Xiaoqing,et al.Determination of residual solvents in synthetic intermediate of Selexipag by headspace gas chromatograhy[J].Journal of Hebei University of Science and Technology,2019,40(3):226-232.Determination of residual solvents in synthetic intermediate of
Selexipag by headspace gas chromatograhy
QI Haijuan, CUI Haoliang, DENG Xiaoqing, WANG Hongpeng, GAO Shuangshuang, HA Jing
(School of Chemical and Pharmaceutical Engineering,Hebei University of Science and Technology, Shijiazhuang, Hebei 050018, China)
Abstract:In order to better control the quality of Selexipag products and ensure drug safety,headspace gas chromatography is established to detect the amount of solvent remaining in the synthesis of Selexipag intermediates 4-\[(5, 6-diphenylpyrazin -2-yl) (isopropyl) amino\]-1-butanol (S5) and N-(2-chloroacetyl) methyl sulfonamide (S7). Gas chromatography is adopted with Kromat PC-624(V) capillary column (30.0 m×0.32 mm×18 μm). The FID detector temperature and injection port temperature are 250 ℃ and 200 ℃, respectively. The headspace sampling is used at temperature 80 ℃ for 30 min. The solvents revolved are methanol, ethanol, acetone, dichloromethane, isopropylacetate, tetrahydrofuran and methylbenzene. The tested component could be completely separated under the chromatographic conditions. The correlation coefficient of each solvent standard curve is greater than 0.997 and the mean recoveries of all components are in range of 95.1%~106.2%. The RSD values of precision, stability and repeatability range from 1.78% to 4.60%. The analytical method is simple, accurate and sensitive, and it can be used for the determination of residual solvents in Selexipag, which provides scientific basis for the quality control of intermediates.
Keywords:chromatographic analysis;headspace gas chromatography;residual solvent;Selexipag;intermediate;content determination
賽乐西帕(Selexipag,商品名为Uptravi)是一种口服前列环素受体(IP受体)激动剂,在人体内被羧酸酯酶水解为活性代谢物,Selexipag及其活性代谢产物对IP受体的选择性优于其他前列腺素受体[1-3],可有效降低肺动脉压力,用于治疗成人肺动脉高压症[4-5]。2015年12月21日,Selexipag经美国食品药品监督管理局标准审评批准后上市,具有良好的市场前景[6-7]。目前,已有研究大多是关于Selexipag药理及合成方面的,在质量控制方面,虽有关于Selexipag原料药残留溶剂检测的相关方法,但并未涉及对其中间体合成过程中残留溶剂的检测。
河北科技大学学报2019年第3期齐海娟,等:顶空气相色谱法测定Selexipag合成中间体的残留溶剂Selexipag的合成路线较短,4-[(5,6-二苯基吡嗪-2基)(异丙基)氨基]-1-丁醇(S5)和N-(2-氯乙酰基)甲基磺酰胺(S7)是Selexipag合成过程中的2个重要中间体。依据药品审批要求,为了更好地控制Selexipag最终产品质量,必须对2个中间体合成过程中所涉及的残留溶剂进行检测,并进行方法学验证[8-10]。根据文献[11]可知:Selexipag合成中的中间体S5在合成、纯化及精制过程中涉及到甲醇、乙醇、二氯甲烷、丙酮、乙酸异丙酯等有机溶剂;S7涉及到甲苯、四氢呋喃等有机溶剂。根据《中华人民共和国药典》(2015年版)第四部分“残留溶剂测定法”项下残留溶剂及限度规定,二氯甲烷、四氢呋喃、甲醇、甲苯为二类溶剂(限度分别为0.06%,0.072%,0.3%和0.089%),乙醇、丙酮及乙酸异丙酯为三类溶剂(限度均为0.5%)[12]。笔者采用顶空气相色谱法,建立了7种有机溶剂的测定方法,并对3批样品进行了检测,以期为Selexipag中间体的质量控制提供参考。
1主要仪器与试剂
GC7900气相色谱仪,中国天美科学仪器有限公司提供;DK3001A顶空进样器,中国北京中兴分析仪器新技术研究所提供;GH20高纯氢发生器、GA2000A低噪音空气泵,中国北京中兴汇利科技发展有限公司提供;AL 204万分之一电子天平,瑞士Mettler公司提供。
S5与S7为河北省药用分子重点实验室自制产品,S5的批号分别为20180301,20180401及20180415,S7批号分别为20180417,20180501及20180519。试验所用试剂甲醇、乙酸异丙酯及二氯甲烷,天津市大茂化学试剂厂提供;四氢呋喃、N,N二甲基甲酰胺(DMF)、二甲基亚砜(DMSO)及乙醇,天津市永大化学试剂有限公司提供;甲苯及丙酮,洛阳市化学试剂厂提供。所用试剂均为分析纯。
2方法与结果
2.1色谱条件
顶空进样,平衡温度为80 ℃,平衡时间为30 min,阀箱温度为100 ℃,传输线温度为110 ℃,定量环的体积为1 mL。
色谱柱为Kromat PC-624(V)(30.0 m×0.32 mm×18 μm),固定相为6%(体积分数,下同)氰丙基苯基-94%二甲基聚硅氧烷。采用程序升温,初始温度为40 ℃,保持5 min,以20 ℃/min升至180 ℃,保持5 min。FID检测器温度为250 ℃,进样口温度为200 ℃,分流比为20∶1,载气为N2。
2.2溶液的配制
2.2.1对照品溶液的配制
精密称取各对照品适量,配制成每1 mL中含有甲醇30 mg、二氯甲烷6 mg、丙酮50 mg、乙醇50 mg、乙酸異丙酯50 mg的对照品溶液,用DMSO溶解,作为对照品储备液1。然后逐级稀释成每1 mL含甲醇120 μg、二氯甲烷24 μg、丙酮200 μg、乙醇200 μg、乙酸异丙酯200 μg的溶液,作为混合对照品溶液2。
2.2.2供试品溶液的配制
精密称取0.2 g的供试品S5于20 mL顶空瓶中,精密加入5 mL DMSO,超声溶解,密封。精密称取0.2 g的供试品S7于20 mL顶空瓶中,精密加入5 mL DMF,超声溶解,密封。
2.2.3标准曲线溶液的配制
精密移取10,30,50,70,100 μL的对照品储备液1,分别置于10 mL的容量瓶中,用DMSO定容,即得S5残留溶剂系列质量浓度的对照品溶液。S7残留溶剂系列质量浓度的对照品溶液配制过程同S5,定容溶液改用DMF。
2.3系统适用性
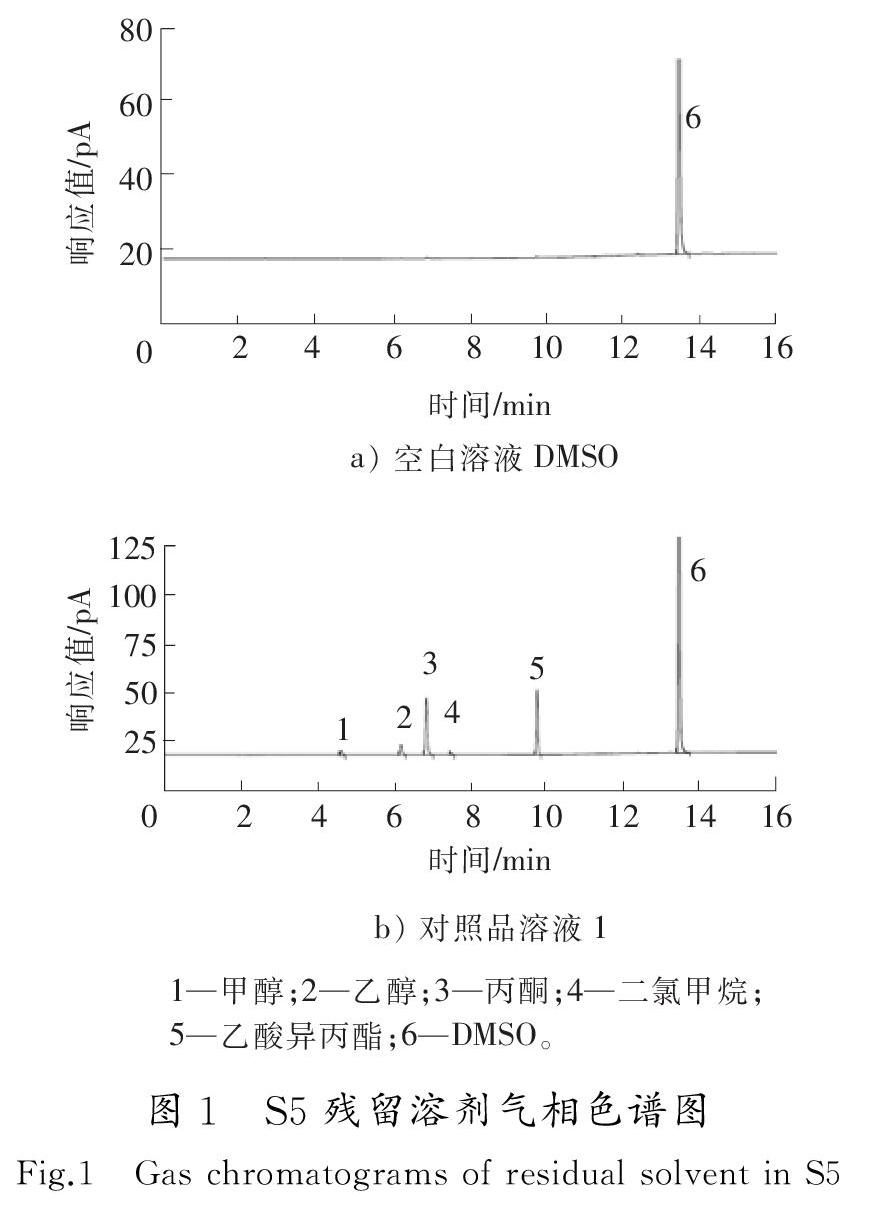
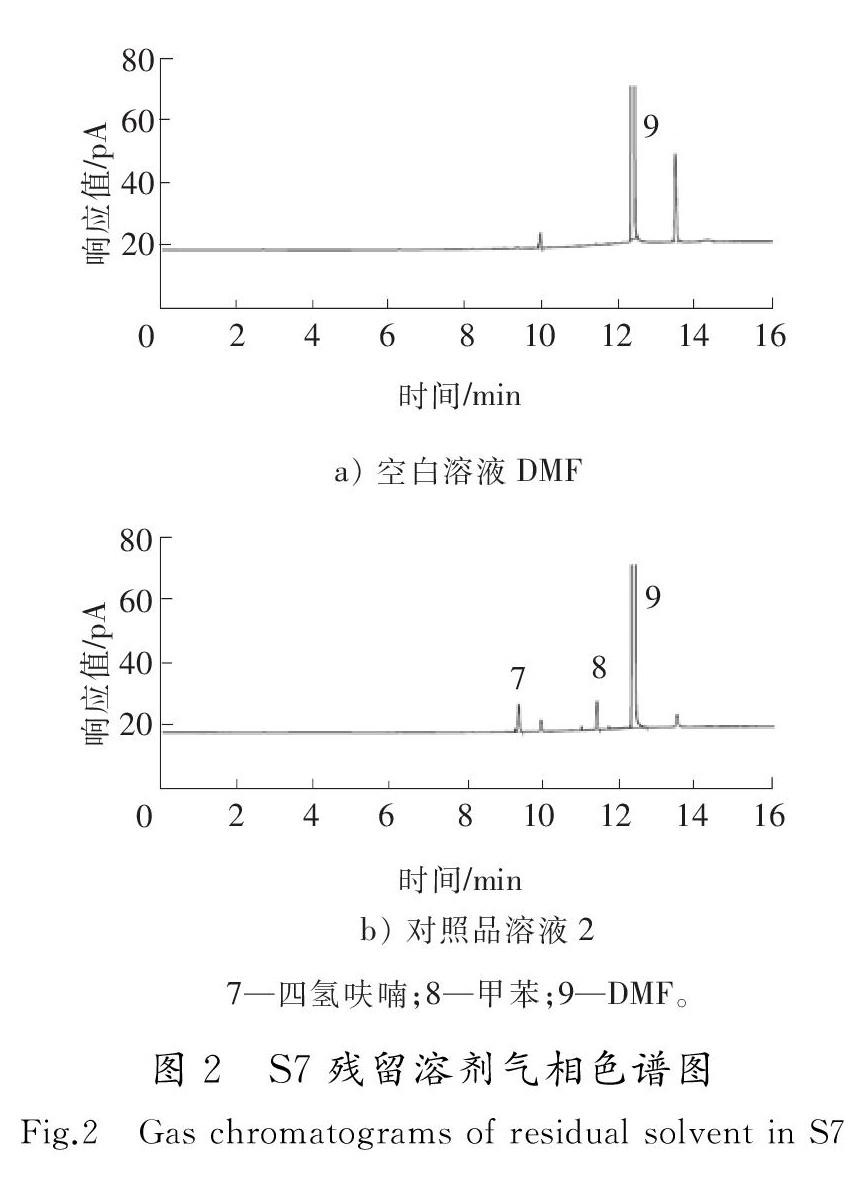
精密移取对照品溶液1、对照品溶液2、空白溶液DMF及DMSO各5 mL,放入20 mL的顶空瓶中,密封。在前述色谱条件下进行测定,记录气相色谱图,见图1和图2。在所得的色谱图中,各组分峰的理论塔板数均大于6 000,各个相邻峰的分离度均大于1.5,空白溶剂对样品测定无干扰。
2.4线性关系
精密移取系列质量浓度的对照品溶液各5 mL,置于20 mL顶空瓶中,按2.1项色谱条件进行测定,记录各峰面积。以峰面积为纵坐标,以各对照品的质量浓度为横坐标,进行线性回归,分别得到S5及S7残留溶剂的线性方程及线性范围,结果见表1。
表1残留溶剂线性测定结果
Tab.1Result of linearity test for the residual solvent
中间体溶剂线性方程r2线性范围/ (μg·mL-1)甲醇y=0.057x+0.2820.998 032.07~320.7乙醇y=0.475x +0.8400.997 951.2~512.0S5二氯甲烷y=0.093x +0.2830.997 56.1~61.0丙酮y=0.475x +2.7200.997 552.0~520.0乙酸异丙酯y=0.394x +4.8000.997 052.4~524.0
S7甲苯y=0.825x +1.8430.997 67.2~72.0四氢呋喃y=0.455x +1.6110.997 010.1~101.02.5精密度
精密移取对照品溶液1与混合对照品溶液2各5 mL,放入20 mL的顶空瓶中,平行制备6份,按21项色谱条件进行测定,记录各峰面积,计算各残留溶剂峰面积的RSD值,结果见表2。由表2可以看出,RSD值均小于4.0%,表明该方法的精密度良好。
2.6重复性
取批号为20180301(S5)及20180417(S7)供试品,
中间体溶剂RSD值/%甲醇2.8乙醇1.8S5二氯甲烷2.9丙酮3.1乙酸异丙酯3.6
S7甲苯1.8四氢呋喃3.4采用2.2.2项方法配制供试品溶液,平行制备6份,按2.1项的色谱条件进行检测,记录色谱峰图。S5的残留溶剂中的甲醇、乙醇、丙酮、二氯甲烷及乙酸异丙酯均未检出,S7残留溶剂中的甲苯未检出,四氢呋喃的平均含量为0.032%,RSD值为4.6%,表明该方法重复性良好,结果见表3。
2.7稳定性
取批号为20180301(S5)及20180417(S7)供试品,按2.2.2项方法配制供试品溶液,平行制备5份,分别在0,2,4,6,8 h采用2.1项的试验条件进行检测,记录色谱图。S5残留溶剂中甲醇、乙醇、丙酮、二氯甲烷及乙酸异丙酯均未检出,S7残留溶剂中甲苯未检出,四氢呋喃的平均含量为0.037%,RSD值为4.2%,结果见表4,表明2个中间体溶液在8 h内稳定性良好。
2.8回收率
精密称取批号为20180301(S5)的供试品0.2 g,置于20 mL顶空瓶中,共9份。由对照品储备液1配制低、中、高3种浓度(各溶剂限度的80%,100%,120%)的混合对照品溶液,分别精密加入3种不同浓度的混合对照品5.0 mL,每种浓度各制备3份。按2.1项色谱条件进行测定,记录各峰面积,按外标法进行计算,中间体S7的试验过程同上(样品批号为20180417),结果见表5。
2.9检测限与定量限
将2.2.1项混合对照品溶液逐级稀释,分别以信噪比为3和10时的质量浓度作为检测限和定量限。进样分析,记录气相色谱图,见图3和图4,测得甲醇、乙醇、二氯甲烷、丙酮、乙酸异丙酯、甲苯及四氢呋喃的检测限分别为4.5,7.5,0.9,7.5,7.5,3.0和2.4 μg /mL,定量限分别为15,25,3,25,25,10和8 μg /mL,定量限的精密度RSD值分别为4.3%,2.9%,3.6%,2.8%,3.0%,4.5%和4.6%,表明定量限的精密度良好。
2.10样品的测定
精密称取S5(编号为20180301,20180401及20180415)和S7(编号为20180417,20180501及20180519)各3批样品,按照2.2.2项方法制备供试品溶液,每批2份,按“2.1”项色谱条件进行分析,甲醇、乙醇、二氯甲烷、乙酸异丙酯及丙酮均未检出,S7的3批样品中甲苯未检出,四氢呋喃的质量分数分别为0040%,0050%和0.050%。
3讨论
3.1进样方式的选择
气相的进样方式有直接进样及顶空进样,直接进样快速方便、精密度好,顶空进样温度较低,可避免样品热解损失以及非挥发性物质对进样口和毛细管柱的污染[13-16],同时顶空进样对于低沸点组分的检测灵敏度高[17-21],适用于对挥发性物质的测定,故选择顶空进样方式检测残留溶剂。
3.2溶剂的选择
顶空气相色谱法选用的溶剂一般为水,但由于2个中间体不溶于水,故先后考察了DMSO及DMF溶剂。DMSO对于2个中间体具有良好的溶解性,但由于DMSO中存在杂质,会影响S7残留溶剂中甲苯的测定,故对于S5的溶剂选用DMSO,S7的溶剂选用DMF。
3.3顶空条件的选择
采用单因素考察方法确定了最佳平衡时间和平衡温度。固定平衡时间,考察不同平衡温度(75,80,100 ℃)下待测物响应值的变化。发现随着温度的升高,待测物响应值增加,但由于80 ℃与100 ℃的响应值无差异,考虑温度过高会使样品发生热解,故选择平衡温度为80 ℃。固定平衡温度,考察不同平衡时间(30,35,40 min)对待测物响应值的影响。发现随着时间的延长,待测物的响应值并无明显增加,故选择平衡时间为30 min。
3.4顶空瓶溶剂体积的选择
分别考察了溶剂体积为3,4,5,6 mL时响应值的变化情况。发现随着溶剂体积的增加,响应值增加,当溶剂体积为6 mL时响应值有所下降,可能是因为溶剂体积过大会导致顶空瓶密封性下降,所以将溶剂体积确定为5 mL。
4结语
通过对溶剂及其体积和平衡时间等条件的优化实验,建立了顶空毛细管气相色谱法,对Selexipag两个中间体4-[(5,6-二苯基吡嗪-2基)(异丙基)氨基]-1-丁醇和N-(2-氯乙酰基)甲基磺酰胺合成过程中7种有机溶剂的残留量进行了检测。方法操作简便,灵敏度高(定量限低于2015年版《中华人民共和国药典》中规定的残留溶剂限度),准确度高(回收率为95.1%~106.2%),重复性好,分离度符合要求。但本研究仅对Selexipag中间体中的甲醇、乙醇、二氯甲烷、丙酮、乙酸异丙酯、甲苯及四氢呋喃7种溶剂进行了检测,尚未对中间体中的其他物质进行研究。为了保证用药安全,未来还需对中间体中的相关物质做进一步的研究。
参考文献/References:
[1]US FDA.Full Prescribing Information: UPTRAVI (Selexipag) Tablets[EB/OL].http://www.accessdata.fda.gov/drugsatfda-docs/label/2015 /207947s000lbl.pdf,2015-12-01.
[2]錢清华,桂玉梅,高慧.治疗肺动脉高压新药Selexipag的研究进展[J].连云港职业技术学院学报,2018,31(2):1-6.
QIAN Qinghua,GUI Yumei,GAO Hui.Advances in research on Selexipag, a new drug for pulmonary hypertension[J].Journal of Lianyungang Vocational and Technical College,2018,31(2):1-6.
[3]夏训明.美国FDA批准Uptravi(Selexipag)片剂治疗肺动脉高压[J].广东药学院学报,2016,32(1):35.
[4]张新房,孙慧娟,祝美华,等.新型前列环素受体激动剂Selexipag[J].中国新药杂志,2016,25(19):2161-2164.
ZHANG Xinfang, SUN Huijuan,ZHU Meihua,et al.A novel prostacyclin receptor agonist, Selexipag [J]. Chinese Journal of New Drugs,2016,25(19):2161-2164.
[5]王艳,张四喜,闫荟羽,等.治疗肺动脉高压新药——Selexipag研究进展[J].中国医院药学杂志,2017,37(15):1540-1545.
WANG Yan,ZHANG Sixi,YAN Huiyu,et al.Advances in research of pulmonary hypertension:Selexipag[J]. Chinese Journal of Hospital Pharmacy,2017,37(15):1540-1545.
[6]佚名.美国FDA批准治疗肺动脉高压药物Selexipag上市[J].中国执业药师,2016,13(3):54.
[7]李兴民.一种塞乐西帕的合成方法[P].中国专利:CN 105949135,2016-09-21.
[8]ICH指导委员会.药品注册的国际技术要求[M].北京:人民卫生出版社,2006.
[9]李眉,马玉楠. 简介ICH关于药品中溶剂残留量的指导原则[J].中国药师,1998,1(3):119-120.
[10]李丽丽,王洪朋,田海伟,等.顶空气相色谱法测定Selexipag中6种有机溶剂残留量[J].中国药科大学学报,2018,49(1):93-96.
LI Lili,WANG Hongpeng,TIAN Haiwei,et al.Determination of 6 residual solvents in Selexipag by headspace gas chromatography[J].Journal of China Pharmaeutical University,2018,49(1):93-96.
[11]方倩,王辉,尚振华.赛乐西帕的合成工艺[J].中国新药杂志,2018,27(7):822-826.
FANG Qian,WANG Hui,SHANG Zhenhua,et al.Synthetic process of Selexipag [J].Chinese Journal of New Drugs, 2018, 27(7):822-826.
[12]国家药典委员会.中华人民共和国药典[M].北京:中国医药科技出版社,2015.
[13]张小妮,刘雪峰,王嫦鹤,等.顶空气相色谱法测定盐酸罗匹尼罗原料药的溶剂残留[J].西北药学杂志,2015,30(6):699-701.
ZHANG Xiaoni,LIU Xuefeng,WANG Changhe et al. Determination of residual solvents in ropinirole hydrochloride by headspace gas chromatography [J].Northwest Pharmaceutical Journal,2015,30(6):699-701.
[14]张丽姝,佘东来,王淼,等.顶空毛细管气相色谱法同时测定罗库溴铵起始物料LK-7中的8种残留溶剂[J].沈阳药科大学学报,2018,35(7):547-551.
ZHANG Lishu,SHE Donglai,WANG Miao, et al. Determination of eight residual solvents in the starting material of rocuronium bromide by headspace capillary gas chromatography [J]. Journal of Shenyang Pharmaceutical University, 2018,35(7):547-551.
[15]孙鹏振,付素珍,董敏,等.顶空气相色谱法测定盐酸安舒法辛原料药中5种残留溶剂[J].烟台大学学报(自然科学与工程版),2018,31(2):177-182.
SUN Pengzhen,FU Suzhen,DONG Min, et al. Headspace gas chromatography determination of five residual solvents in ansofaxine hydrochloride[J]. Journal of Yantai University (Natural Science and Engineering Edition),2018,31(2):177-182.
[16]王建明,曹曉玲,曹旺华.顶空气相色谱法测定丹参酮ⅡA磺酸钠原料药中的溶剂残留量[J].河北工业科技,2006,23(5):267-268.
WANG Jianming,CAO Xiaoling,CAO Wanghua. Determination of residual solvents in sodium tanshinonⅡA silate by headspace GC[J].Hebei Journal of Industrial Science and Technology,2006,23(5):267-268.
[17]余秋丽,黄琦,于秋洋,等.顶空毛细管气相色谱法测定帕瑞昔布钠中的残留溶剂含量[J].沈阳药科大学学报,2017,34(10):889-892.
YU Qiuli,HUANG Qi,YU Qiuyang,et al.Determination of five residual solvents in parecoxib sodium by gas chromatography with head-space sampling[J].Journal of Shenyang Pharmaceutical University,2017,34(10):889-892.
[18]韓月,李成文,刘秀鹏,等.埃索美拉唑钠中七种残留溶剂的测定[J].承德医学院学报,2017,34(2):140-142.
[19]罗毅,姜建彪,常青.顶空-气相色谱法与吹扫捕集-气质联用法测定水中乙醛、丙烯醛、丙烯腈、吡啶的方法比较[J].河北工业科技,2017,34(3):208-213.
LUO Yi,JIANG Jianbiao,CHANG Qing.Comparison of headspace-GC with purge and trap-GC/MS methods in determination of acetaldehyde, acrolein, acrylonitrile and pyridine [J]. Hebei Journal of Industrial Science and Technology,2017,34(3):208-213.
[20]刘英,刘葵葵,邓玉晓,等.顶空气相色谱法同时测定硫酸沃拉帕沙原料药中7种有机溶剂的残留量[J].中国药房,2018,29(16):2224-2227.
LIU Ying,LIU Kuikui,DENG Yuxiao, et al. Simultaneous determination of 7 residual solvents in vorapaxar sulfate raw material by headspace GC[J]. Chinese Pharmacy ,2018,29(16):2224-2227.
[21]黄卫娟,杨丽玲,王淑芬,等.顶空气相色谱法同时测定醒脑静注射液中6种有机溶剂的残留量[J].中国药房,2017,28(27):3868-3871.
HUANG Weijuan,YANG Liling,WANG Shufen, et al. Simultaneous determination of 6 residual organic solvents in Xingnaojing injection by headspace GC [J].Chinese Pharmacy,2017,28(27):3868-3871.第40卷第3期河北科技大学学报Vol.40,No.3
2019年6月Journal of Hebei University of Science and TechnologyJune 2019

