基于核心素养视角的化学“催化剂”教学探讨
王卫军

摘要:从学生核心素养培养的角度,对化学催化剂教育教学内容、价值与意义进行了剖析和探讨,认为适当挖掘和理顺中学化学催化剂的教学,能深化与完善学生化学知识体系,能指导和激励学生发展,并培养学生社会责任意识与担当。
关键词:核心素养;催化剂;概念教学;中学化学
文章编号:1008-0546(2019)06-0002-06 中图分类号:G632.41 文献标识码:B
doi:10.3969/j.issn.1008-0546.2019.06.001
一、中学化学“催化剂”教学现状概述
“催化剂”是在中学化学教材中高频出现的名词,但呈现较为零碎,也没有得到师生足够重视,有关催化剂的教学,大都只是陈述了其作为单一影响因素对反应影响的结果,而极少讨论其作用机理,以及与其他相关因素的综合影响。最终以一种结论性知识让学生识记,较少涉及思维和能力方面的要求。
综观各阶段化学教材对催化剂的介绍,其实是推崇备至的,不仅介绍了催化剂的定义、工作原理和实践价值,还对学生情感、态度与价值观方面作出了积极的影响和指导。以人教版化学教材为例,较为具体介绍催化剂的有三处(表1):
教材以“定性→半定量→机理”的方式逐步深入介绍催化剂。初中阶段给出了催化剂定义,让学生从宏观和结果上认识了催化剂,当然,这里催化剂只是众多化学反应条件中的一个,并没有涉及其影响的过程和原理。在高中必修2教材中,催化剂以“科学视野”的形式呈现,讲述了催化剂在工业生产中的广泛应用,半定量陈述了催化剂对化学反应速率的影响结果,以及简要介绍了催化剂发展历史及前景。这里充分展示了催化剂对人类生活、生产的实践意义和价值,并刻意对学生的情感和志趣进行了引导。到选修4,教材结合有效碰撞理论对催化剂催化机理进行了介绍,虽然不是特别具体和深入,但还是较为深刻地解析出化学反应本质和机理,它让学生对化学反应的动力学和热力学有了理解的角度和眉目,并由此建立化学反应控制思想和意识。
通过对教材的分析,可以发现,催化剂有很大的教学潜在价值,非常值得研究和挖掘。但在实际教学中,它却不是教学重点,不属于核心概念范畴。因此,它总是被有意或无意地忽视,甚至在初中阶段,有些教师为了让学生理解课本上“催化剂的质量和化学性质在反应前后都没有发生变化”的说法,肆意地简化和错化催化剂催化机理,告诉学生催化剂是不参与化学反应的。于是,催化剂在学生心目中就成了化学反应的“围观群众”,是置身于反应之外的。那么,它的“不变化”就可以轻易地被学生接受了。在高中阶段,催化剂似乎也只是一个简单的结论:“催化剂能加快化学反应速率,但不能改变化学平衡常数,也不能改变平衡转化率。”而对催化剂的高效性、选择性、以及研究的价值与意义极少探讨。所以,催化剂在整个中学阶段,都是一个知识碎片,既不深刻也不系统,在学生能力培养上没有发挥出应有的价值。
当然,在中学阶段对催化剂教学内容的理顺与挖掘,并不是没有边界和止境的,我们不可能将足以作为一门化学学科分支的催化剂,全面纳入到中学化学教学中来,超脱了教学实际必然是不可取的。为此,笔者就如何在中学阶段,适切挖掘和组织催化剂教学内容,帮助学生深入认识化学反应本质,提升学生思维与思想品质,构建化学核心素养体系等方面,做一下尝试性梳理,并阐述些个人看法。
二、中学化学“催化剂”教育教学内容、价值与意义探讨
催化剂在实践生产中的作用与价值日益凸显,有关催化剂的研究也是方兴未艾,催化剂自然不能在中学化学教学中缺席。一方面是由催化剂自身价值决定的,既然要培养学生“具备能够适应终身发展和社会发展需要的必备品格和关键能力”,学生就不应该对催化剂一无所知;一方面催化剂概念、催化剂工作原理,有助于学生更清晰和详实地认识化学反应过程;三是催化剂应用现状和发展前景,对学生情感与志向具有激励和导向作用。
1.对催化剂概念的再认识
早在1901年,物理化学之父奥斯特瓦尔德(F.w.Ostwald)就对催化剂和催化作用作了定义:“凡能改变化学反应的速率,而本身不形成化学反应的最终产物,就叫做催化剂。”到1977年,国际纯粹化学及应用化学联合会建议,将催化剂定义为:“存在较少量就能显著的加速反应。而其本身最后并无损耗的物质称为该反应的催化剂。”之问虽然历经了76年的研究,对催化剂的定义表述稍有不同,但其核心意义是一致的,都是“能加快反應,但自身不变”,只是后面定义中涉及了催化剂催化效能及专一性方面的内容。结合当前中学化学教材对催化剂的定义,我们可以发现,定义中对“不变”的描述,从“不形成化学反应的最终产物”到“本身最后无损耗”再到“本身质量和化学性质没有发生变化”,这反映出,人们对催化剂的认识是不断发展的,进而推知,当前我们所学的化学概念并不一定是恒成立的,而是会随着研究和认识的深入,不断地得到修正和完善。
催化剂的“不变”,让很多人误以为催化剂拥有永久的寿命,似乎一旦制成就能永远的使用下去。但事实上,催化剂并非长生不老,而是在使用的过程中,有一个由弱到强再衰退的过程,就如同生命一样,有成长期、成熟期、衰老期,直至消亡(失去催化活性)。也就是说,催化剂在催化过程中并非真的不变。其“不变”结论是在摒弃了其他因素影响(副反应等),对被催化反应进行单一研究而得出的一种理想状态下的结论。事实上,催化剂在催化过程中,其状态、结构均会发生变化,而结构发生变化势必改变化学性质,而且催化剂即便在成熟期,也会由于接触到某些杂质而降低或失去催化活性,这种现象称之为催化剂中毒。所以,在实际生产中,催化剂需要定期更换和补充,而非我们想象的那样,加入一次催化剂就一劳永逸了。为此,在工业生产中,我们不得不考虑如何延长催化剂的寿命,而设法去净化原料,排除毒物,并进行催化剂抗毒能力方面的研究。
2.催化剂一定程度上揭开了化学反应过程的面纱
我们对化学反应的研究,已经不满足于知道反应的结果,而是希望掌握化学反应的过程。而过程的发现,就需要对化学反应过程进行干涉,即通过改变反应过程中的某些因素,而改变反应的结果,从而揭示出化学反应的真实过程。
(1)催化剂从化学键的角度改变了反应历程
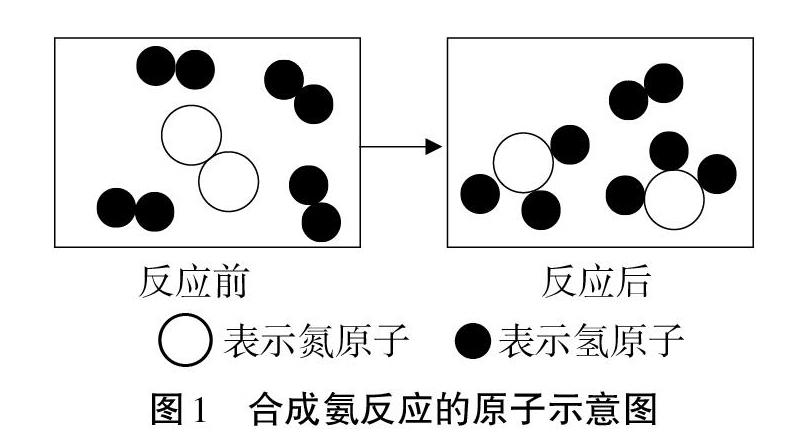
在初中阶段,我们常用原子示意图(如图1)表示化学反应的过程,从中得出的结论也只是反应的结果,即化学反应就是元素原子重新组合的过程,故而其反应前后原子的种类和个数不变(质量守恒定律)。这里化学反应只是原子的“重新组合”过程,没有涉及到为什么要这样或那样组合的问题。
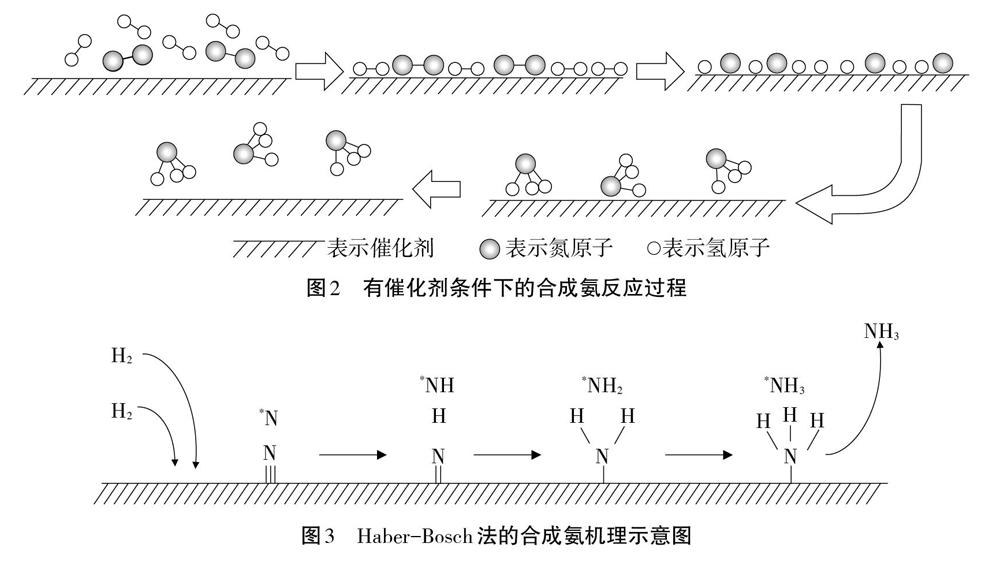
到高中阶段,通过催化剂,让学生对化学反应过程有了更进一步的了解。如合成氨反应,从反应的吉布斯自由能来看,该反应有极大自发进行的趋势,但事实上其反应发生极为困难,从第一次实验室研制到工业化投产,大约经历了150年的时间,由此可见,合成氨理论与生产实践之间存在着巨大沟壑,而催化剂成为了跨越此问障碍的功臣。合成氨反应在没有催化剂的条件下,即便是高温高压,它也几乎不发生。但在催化剂作用下,发生了图2的过程,催化剂参与并有效地帮助了N2、H2的解离,从而使得合成氨反应顺利发生。
Haber-Bosch法合成氨中催化剂催化机理(图3)有如下解释:首先N2在铁催化剂表面上进行化学吸附,使氮原子问的化学键减弱。接着是化学吸附的氢原子不断地跟表面上的氮分子作用,在催化剂表面上逐步生成-NH、-NH2和NH5,最后氨分子在表面上脱吸而生成气态的茸氨。可见,催化剂在反应中主要是帮助克服N=N键断裂的困难。常温常压下N=N的键能高达946kJ/mol,键能很大,使得N2离解需要极高的温度,但温度过高又会造成NH3分解,温度上的冲突难以调和,使合成氨工业化生产困难重重。而催化剂的介入,大幅度地减弱了N=N键能,让其断开无需很高的温度,从而让合成氨的工业化生产成为可能。
这个事实从另一个角度告诉我们,化学反应过程的确存在着化学键的断裂和形成,同时也说明化学反应的路径并不是唯一的,有多种可能,并在一定条件下是可以改变和选择的。这就意味着,化学反应在一定条件下是可控的,这为我们合理地利用化学反应提供了思路。这对化学教学而言,有如下意义:①将“暗箱式”反应过程“明朗化”,由于“可视”而让化学反应变得更易理解和接受;②反应从“封闭”走向“开放”,化学反应路径不唯一,并受着反应条件的影响,故而化学反应是可控的,人力不仅可以介入,还能进行控制和选择,驾驭反应朝着我们所期望的方向和方式去发生,即让学生从“学化学”走向“参与化学”,由被动转向主动;③催化剂让有价值的反应从可能走向真实,不仅彰显了化学学科的意义与价值,还能将其扩大化,即可以指导人们更有效地去开发和利用化学反应,从而让某些有价值的化学反应由期待转变成现实,这无疑为学生学习化学提供了动力。
(2)催化剂从能量的角度改变了反应速率
任何化学反应均伴随着能量的变化。不管是化学反应中化学键的断裂和形成,或是有效碰撞理论,均与能量转化有关。在有效碰撞理论中,反应物分子只有吸收到足够的能量才能转化为活化分子,才有几率发生有效碰撞,导致反应发生。
在高中选修4教材中,有如图4的示意图,展示了催化剂对反应活化能的影响,从图中可以看出,催化剂参与了化学反应,改变了化学反应的历程,降低了反应的活化能(E1→E3),从而减少了化学反应对温度的要求,但却不影响反应最终的能量转化结果,即改变了反应对能量的需求,却没有改变反应的能量转化量。课本的结论是:催化剂只是同等程度的改变正逆反应速率,而不改变平衡状态及平衡转化率。这结果不仅适用于物质层面,在能量层面也是适用的。
图4对学生来说,不仅有抽象的化学意义,也颇为形象。化学反应过程类似于“翻山越岭”,催化剂能另辟蹊径地避开了高山险阻,而找到了一条相对容易却能到达同样终点的道路。当然,从严格意义上来讲,图4并不是非常合理,从催化剂的变化来看,化学反应必定包括着催化剂反应消耗与再生的过程。因此,有催化剂参与的反应路线至少有两个峰,就如图5所示。
催化剂從能量角度揭示了反应的过程,揭示了反应热力学与动力学之间的本质联系,可有效解决学生将化学反应动力学与热力学截然分开又各自为政的现象,解决了学生由于机理理解不透彻、不贯通而思维受阻或不严密的情况。再者,通过催化剂的介入,可以发现,能量贯穿着反应的始终,它不仅是反应的起因,还是决定反应路径与方向选择的因素,更是反应必然的结果(热效应),反应的整个过程都与能量息息相关,为此,由能量人手来控制和利用化学反应应该是个不错的选择。
3.催化剂在工业生产中具有化腐朽为神奇的力量
科学家致力于对化学反应的研究,不仅是为了探究化学反应事实,更在于如何利用化学反应、控制化学反应,乃至创造化学反应。催化剂能改变反应历程、改变反应速率,这对我们控制和利用化学反应来说,意义是非凡的。一个化学反应若要造福于人类,就必须投入工业化生产,而工业化生产就不可避免地要考虑生产效率与效益。
(1)催化剂是提高生产效率最有力的手段
在化工生产中,我们一定会思考:如何选择反应条件才能让生产效率和效益达到最佳。就拿合成氨来说,影响合成氨反应速率的主要因素有浓度(压强)、温度、催化剂,它们对反应速率的影响结果如表2:
表中数据可以看出,物质浓度对反应速率的综合级数为1.5,也就是说,物质浓度对化学反应速率的影响微乎其微,而在工业生产中,提高气体浓度,就意味着提高压强,意味要增加能耗及设备的抗压成本,这对提高生产效率和效益意义并不大。从提高温度角度而言,温度从700K升高到800K,反应速率才提高3个数量级。但温度升高100K,反应器的材质就必须提高二个档次(一般温度每升高50K,材质就要提高一个档次),能耗也大幅度提高,从投入和产出的效益来看,升到更高的反应温度,仍然是不可取的。但是在700K条件下,使用催化剂和没有催化剂相比较,其反应速率常数增加了12个数量级,催化剂对反应速率的影响非常巨大,再加上催化剂成本相对低廉,它所带来的收益远远不是其它因素可以比拟的。因此,使用催化剂是合成氨工艺必然的选择。
合成氨最终选择的反应条件为:以铁触媒作催化剂,压强在20MPa-50MPa之间,温度在500°C左右。其中之所以选择500°c,不是因为在该温度下生产成本与反应速率达成统一,也不是因为在该温度下生产成本与平衡转化率达成一致,而是因为在该温度下,催化剂的活性最高。催化剂改变反应速率的高效能,让催化剂理所当然地成为了生产实践中首要考虑的因素。
控制化学反应的手段很多,但不同手段的成本与效果是不同的,也就是说,很多方法理论上或许可行,但实际上却行不通。就如反应温度、浓度、压强等因素,理论上非常容易控制,但实际上却受到诸多掣肘,当然催化剂也是如此,但单纯考虑生产成本和反应速率的话,催化剂的确是最经济、最有效的提效措施。为此,研究新型、高效催化剂是提升生产效益最科学、最有前途的方法之一。
(2)催化剂改变了化工生产的“产率”,从而提高了效益
尽管课本上反复强调,催化剂只能改变反应速率,而不能改变化学平衡常数,不能改变平衡转化率。但在实际生产中,它却是能改变“产率”的。在合成氨工艺中,从合成塔出来的反应气体是没有达到化学平衡状态的,催化剂让反应更接近化学平衡状态,使得氨气在产出气体中占有了更高的比例。如图6,t2是无催化剂条件达到平衡的时间,但实际生产的反应时间为t1。由于催化剂提高了反应速率,故而一定程度上提高了合成氨的原料转化率。
再者催化剂具有选择性,它的选择性在实际生产中也能提高原料的转化率。在选修4教材中,有这样一句话:“对于在给定条件下反应物之间能够同时发生多个反应的情况,理想的催化剂还可以大幅度提高目标产物在最终产物中的比率。”由于催化剂选择性地加快了目标反应的速率,从而提高了目标反应在众多副反应中的比率。目标产物增多,副产物减少,原料的利用率无疑就得到了提高。所以,催化剂虽然不能改变化学平衡常数,但并不意味着在实际生产中不能改变原料的转化率。
这个事实告诉我们,化学理论与生产实践有吻合的地方,但并不完全一致。化学理论所预设的各种前提条件毕竟不能囊括所有的实际因素,所以,学习化学理论,不能只是读懂文字上的意思,更需要变通,最好能将化学理论置于实践角度加以审视和理解,这样才能更准确和全面地掌握化学理论的基本内涵。化学理论或许可以告诉我们实践的方法和思路,但绝无法提供实践的最终方案或结果。只有将知识与实践充分融合,学习所获才不是只有知识,而是更有力量的智慧与能力。
4.催化剂有助于学生深刻领会化学精神,树立化学志向
催化剂让很多反应从实验室走进社会,走进人们的生活。如果没有催化剂,合成氨也许至今还停留在科学家设计的图纸上,人类可能至今还无法摆脱依靠天然氮肥的被动局面。可以说,催化剂改变了人类的历史和进程,而且在将来会有更大的影响力。
(1)催化剂记录着科学家奋斗的历史,改变了人类的命运
哈伯与博施为了找到合成氨高效稳定的催化剂,在两年的时问里,他们进行了6500多次实验,测试了2500种不同的配方,最后才选定含铅镁促进剂的铁催化剂。从而在1913年成功建立了年产7000t规模的合成氨工厂。合成氨的工业化生产,在人类历史上具有划时代的意义,从某种角度而言,它让人类走出了食不果腹、衣不遮体的窘境。哈伯也因此被人们高度赞誉:“他是天使,他为人类带来了丰收和喜悦,他是用空气制造面包的圣人。”合成氨发展历史给予我们三点启示:一是催化剂的研究就如同其它科学研究一样,要经历无数次的实验,也经历了无数次的挫折和失败,但科学家坚韧不拔、孜孜以求的科学精神,最终战胜了一切而如愿以偿;二是催化剂对人类有着非凡的意义,一个似乎并不起眼的铁触媒催化剂,却是让合成氨从梦想走进现实,彻底地改变了人类生存的状态,即化学的“小”研究却有大意义;三是投身化学事业,不仅能充分发挥个人才智,而且还能实现人生价值。或许人们对哈伯有褒贬不一的看法,但他确确实实是“解救世界粮食危机”的科学天使,是“用空气制造面包”的圣人,人们必将永远记住并感激他。在1920年,瑞典皇家科学院特意为哈伯举行了诺贝尔化学奖的授奖仪式,尽管这是迟到的仪式,但它再次证明了人们是不会忘记为人类做出巨大贡献的科学家的。
(2)催化剂研究需要更多有志之士参与
人教版九年级化学教材阐述了催化剂的重要性:“催化剂在化工生产中具有重要而广泛的应用,生产化肥、农药、多种化工原料等都要用到催化剂。”人教版高中必修2教材中,着重介绍了特殊催化剂——酶,并如是说:“催化剂的神奇面纱至今尚未完全揭开,因此,催化剂的研究和应用将是21世纪化学的一个极具魅力和应用前景的重大主题。”在人教版高中选修4教材中,又这样说道:“在现代化学工业中催化剂的应用十分普遍,这方面的研究成果多次获得诺贝尔化学奖。但遗憾的是,催化剂的设计和选择,目前主要还是依靠经验和筛选的方法。由于催化剂可以为化学工业带来巨大的经济效益,而且选择性极高的酶的生物催化作用,有助于加深对生命过程的认识和模拟,所以催化剂作用的研究一直是受到高度重视的高科技领域。”从课本的描述中,我们可以体会得到,催化剂在工业生产和社会发展中,发挥着越来越重要的作用,但催化剂的研究还不够完善,仍有很多空白领域,投身催化剂研究将大有可为。教材字里行间无不透露出对学子殷切的希望,希望学生能有志于催化剂方面的研究,以此实现人生的价值与意义。
三、基于催化剂概念教学的反思
核心素养的建构,是对“能力人”和“高尚人”的期望。教学要以超脱知识积累走向能力培养,就需要更深刻和全面地理顺知识之来龙去脉,积极构建指向思维能力发展的知识呈现和接受方式,并充分挖掘知识背后的人文属性,激发情感共鸣,唤醒责任意识和对生命价值的诉求,让学生之于自己或之于社会都更有存在意义与价值。
纵观每个化学概念的背后,其实都有一系列的事实和理论,反映着某些化学规律与规则,如科学家研究它的历程和实践应用它的故事。不管是概念本身,还是其生成的背景、形成的过程,以及实践应用的事实,都有着不可忽视的教育价值,都是值得深入挖掘和探讨的内容。具体说来,概念教学的基本思路有以下几点:
(1)概念教学要厘清概念的内涵,并将概念置于化学知识体系中进行系统的呈现,概念不是化学知识中的孤岛,而是一个枢纽,一个关键的节点,它可以让学生建构的化学知识体系更加稳固。
(2)概念教学要结合实践应用,概念不能是純粹和静态的,而需要在实践中彰显它的价值,读万卷书,行万里路,不只是学习的方式,更是检验、完善和发展概念的基本途径。
(3)概念教学要重视概念生成的背景和发展的历程,因为这些可以反映出人类文明进步的情况,概念的进化演变可以告诫学生,概念的学习必须要用审视和发展的眼光去看待,而不能将其固化,更不能固步自封,拒绝进步与改变。
(4)概念教学要展现概念研究的现状和发展的前景。概念之所以得到传承,就是因为它对人类发展有极其重要的作用,概念所涉及的理论、思想、技术与方法或许当前已经发挥出巨大的价值,但它绝对不是完美的,需要进一步发展和完善。因此,在科学文明与社会需求的召唤下,需要激励学生责无旁贷地挺身而出。
(5)概念教学要重视科学家在此过程中多付出的努力和所获得的成就。科学家对化学的研究和践行,记录着科学家们对科学的热爱和执著,他们百折不饶的科学精神、恪尽职守的责任担当、深刻厚重的家国情怀都非常值得师生效仿和发扬。

