利胆颗粒质量标准的研究
吕凌岳,梁大连,张岱州,李 敏,郭 琪,王 芳,张 伟
(1.山东中医药大学,山东 济南 250355;2.山东省药学科学院 山东省化学药物重点实验室,山东 济南 250101;3.青岛市中医院,山东 青岛 266033)
利胆颗粒由青皮、白芍、姜黄、大黄、郁金等10味中药组成,有疏肝利胆,行气止痛,清热解毒排石的功效,可用于治疗慢性胆囊炎、胆囊结石、胆管炎、胆囊手术后综合征及胆道功能性疾病。其中青皮、白芍和姜黄为君药。芍药苷作为白芍的主要有效成分,有解痉镇痛、解热降温、抗炎、抗氧化、抗溃疡及调节血脂等作用[1];姜黄素(curcumin)是姜黄中的一种天然活性物质,有抗氧化、抗炎等作用[2]。橙皮苷是青皮的主要有效成分,有抗炎、抗氧化、祛痰平喘、延缓衰老等作用[3]。为了有效控制自制制剂的质量,本研究参照文献,建立了定性鉴别芍药苷和姜黄素的薄层色谱法和定量测定橙皮苷含量的高效液相色谱法,经结果验证,所建立的方法准确可靠,可用来有效控制利胆颗粒的质量。为后续该新药质量标准的制订奠定基础。
1 仪器与试药
1.1 仪器
Agilent 1260 高效液相色谱仪(美国安捷伦)、SB-5200DTD超声波清洗机(宁波新芝)、 XA105电子分析天平(德国梅特勒)、紫外光谱仪:UV-2550PC 型。硅胶G薄层板(默克化工)。
1.2 试药与试剂
芍药苷对照品(批号110721-201617)、姜黄素对照品(批号110736-201640)、橙皮苷对照品(批号110820-201607)、姜黄对照药材(批号121188-200502)、白芍对照药材(批号120905-201610),均由中国食品药品检定研究院提供。
利胆颗粒:将青皮、白芍、姜黄、大黄、郁金等10味中药(济南建联中药店)按处方比例加入圆底烧瓶中,分别加入8倍量、6倍量、6倍量水回流提取3次,提取时间分别为1.5,1.5,1 h,合并提取液,静置过夜,将上清浓缩至相对密度为1.30~1.35的清膏,60 ℃减压干燥后,粉碎过80目筛,加入配比淀粉混合均匀。用乙醇制软材,过12 目筛制湿颗粒,烘箱干燥,即得。
乙腈为色谱纯(盛世萨格),水为纯净水(娃哈哈);其他试剂均为分析纯(西陇科学)。
2 方法
2.1 薄层鉴别
2.1.1 芍药苷鉴别
2.1.1.1 溶液制备 对照品溶液 取芍药苷对照品适量,精密称取,加乙醇制成每1 ml含1 mg溶液,作为芍药苷对照品溶液。
药材对照溶液 取0.5 g白芍对照药材置入锥形瓶,加甲醇20 ml,超声提取20 min,滤过,取续滤液5 ml,浓缩至1 ml,作为白芍药材对照溶液。
阴性对照溶液 将利胆颗粒处方去除白芍一味药材,按照1.2项下相同的制备方法制得颗粒,精密称取1 g置入锥形瓶,加入甲醇20 ml,超声提取20 min,滤过,取续滤液5 ml,浓缩至1 ml,作为阴性对照溶液。
供试品溶液 取利胆颗粒1 g置锥形瓶中,加入甲醇20 ml,超声提取20 min,滤过,取续滤液5 ml,浓缩至1 ml,作为供试品溶液。
2.1.1.2 薄层鉴别 吸取阴性对照溶液、药材对照溶液、对照品溶液、供试品溶液各8 μl,点于同一硅胶G薄层板上,室温下以乙酸乙酯-甲醇-冰醋酸-水(15:2:1:3)于10 ℃下放置过夜的上层溶液为展开剂,展开,取出,晾干,喷以5%香草醛硫酸溶液,在105 ℃加热至斑点显色清晰。对照药材溶液与对照品溶液在相同位置出现斑点,相应的位置上,供试品溶液出现斑点而阴性对照溶液则没有。结果见图1。

图1 芍药苷薄层色谱鉴别
2.1.2 姜黄素鉴别
2.1.2.1 溶液的制备 对照品溶液 取姜黄素对照品适量,精密称取,加甲醇制成每1 ml含1 mg的溶液,作为对照品溶液。
药材对照溶液 取0.5 g姜黄对照药材置锥形瓶中,加甲醇20 ml,超声提取20 min,滤过,取续滤液5 ml,浓缩至1 ml,稀释25倍作为药材对照溶液。
阴性对照溶液 将利胆颗粒处方去除姜黄一味药材,按照1.2项下相同的制备方法制得颗粒,精密称取1 g置入锥形瓶,加入甲醇20 ml,超声提取20 min,滤过,取续滤液5 ml,浓缩至1 ml,作为阴性对照溶液。
供试品溶液的制备 取利胆颗粒1 g置锥形瓶中,加入甲醇20 ml,超声提取20 min,滤过,取续滤液5 ml,浓缩至1 ml,作为供试品溶液。
2.1.2.2 薄层鉴别 吸取阴性对照溶液6 µl、药材对照溶液2 µl、对照品溶液1 µl、供试品6 µl,点于同一硅胶G薄层板上,室温下以二氯甲烷-甲醇-甲酸(96:4:0.7)为展开剂,展开,取出,晾干,分别置日光和紫外灯(365 nm)下检视。对照药材溶液与对照品溶液在相同位置出现斑点,相应的位置上,供试品溶液出现斑点而阴性对照溶液则没有。结果见图2、图3。
图2 姜黄素薄层色谱鉴别(日光下)

图3 姜黄素薄层色谱鉴别(紫外灯下)
2.2 橙皮苷含量测定
2.2.1 溶液制备 对照品溶液 取橙皮苷对照品适量,精密称定,加甲醇制成每l ml含50 μg溶液,即得。
药材对照溶液 取青皮对照药材0.5 g,精密称定,置入50 ml具塞量瓶,加入甲醇适量,超声处理(功率300 W,频率40 Hz)20 min,放冷,用甲醇补足至刻度,摇匀,滤过,精密量取续滤液5 ml,置入10 ml量瓶,用甲醇稀释至刻度,摇匀,即得。
供试品溶液 取利胆颗粒1.0 g,精密称定,置入50 ml具塞量瓶,加入甲醇适量,超声处理(功率300 W,频率40 Hz)20 min,放冷,用甲醇补足至刻度,摇匀,滤过,精密量取续滤液5 ml,置入10 ml量瓶,用甲醇稀释至刻度,摇匀,即得。
阴性对照溶液 按1.2项下处方工艺制备不含青皮的阴性样品,取1.0 g,精密称定,置50 ml具塞量瓶,加入甲醇适量,超声处理(功率300 W,频率40 Hz)20 min,放冷,用甲醇补足至刻度,摇匀,滤过,精密量取续滤液5 ml,置入10 ml量瓶,用甲醇稀释至刻度,摇匀,即得。
2.2.2 色谱条件 色谱柱:Shimadzu VP-ODS C18(250 mm×4.6 mm,5 μm);流动相:以乙腈为流动相A,0.2%磷酸溶液为流动相B,按下表中的规定进行梯度洗脱;流速:1.0 ml/min;柱温:30 ℃;检测波长:283 nm。

表1 梯度洗脱时间表
2.2.3 专属性试验 分别精密吸取阴性对照溶液、对照药材溶液、对照品溶液、供试品溶液各10 μl,按含量测定项下的方法进行测定。结果:供试品溶液和对照品溶液色谱图上有一保留时间几乎相同的特征峰,而阴性对照溶液在此保留时间橙皮苷出峰位置无吸收峰,表明辅料及其他组分不干扰橙皮苷的测定。
2.2.4 定量限 取橙皮苷对照品,用甲醇制成每1 ml中含3.996 μg溶液,取10 μl进样,记录色谱图,按色谱峰信噪比(S/N)=10作为定量限,最低可定量测定的浓度为3.996 μg/ml,定量限为0.03996 μg。

图4 橙皮苷HPLC图
2.2.5 仪器精密度试验 取含量测定项下的橙皮苷对照品溶液10 μl,连续进样6次,记录色谱图,平均峰面积858.9132,计算RSD=0.305%。结果表明,仪器精密度良好。
2.2.6 线性关系的考察 精密称取橙皮苷对照品10.40 mg,置入50 ml量瓶,加甲醇适量溶解,定容至刻度,摇匀,作为橙皮苷对照品储备液(0.1998 mg/m1)。精密量取对照品储备液1.0,2.0,3.0,5.0 ml,分别置入10 ml量瓶,加甲醇至刻度,制成4份不同浓度的对照品溶液;精密吸取上述对照品溶液及储备液各10 μl,分别注入高效液相色谱仪,按照含量测定项下的色谱条件测定,以进样量X(μg)为横坐标,峰面积Y为纵坐标绘制标准曲线,得回归方程Y= 16 135X-7.8441,R²=0.9999。结果表明,橙皮苷在浓度19.98~199.8 μg/ml范围内进样量与峰面积呈良好线性。
2.2.7 加样回收试验 称取6份已知含量的样品(橙皮苷含量为5.476 mg/g),每份0.5 g,分别精密加入3 ml橙皮苷对照品溶液(0.806 47 mg/ml),按2.2.1项下所述方法制备供试品溶液,2.2.2项下色谱条件进行含量测定,结果见表2。结果表明,平均回收率为97.41%,RSD为1.696%,结果符合要求。
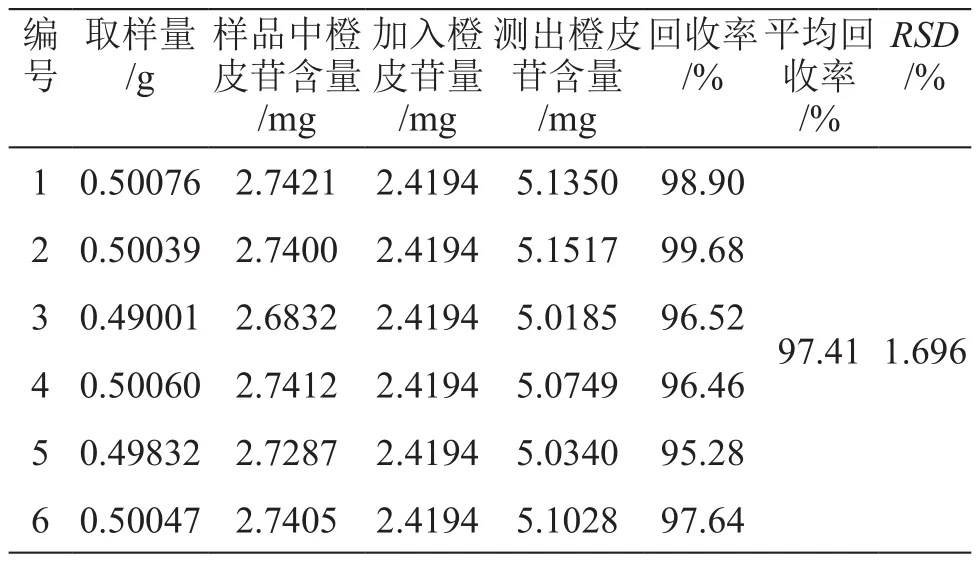
表2 回收率试验结果
2.2.8 重复性试验 精密称取供试品6份各1 g,按2.2.1项下的方法制成6份供试品溶液,按2.2.2项下色谱条件进行测定。结果橙皮苷平均含量为5.4758 mg/g,RSD为1.40%,重复性试验的相对标准偏差<2%,符合试验要求。
2.2.9 仪器精密度试验 精密吸取对照品溶液10 μl,连续进样6次,计算峰面积平均峰面积858.913,RSD为0.30%。仪器精密度试验的RSD<2%,符合试验要求。
2.2.10 溶液稳定性试验 将供试品溶液于室温条件下放置,分别于0,1,2,4,8,12 h取出测定橙皮苷峰面积,计算平均峰面积为878.4155,RSD为0.83%。结果表明,供试品溶液在12 h内基本稳定。
2.2.11 样品含量测定 根据上述建立的橙皮苷含量测定方法测定3批样品,橙皮苷含量为5.2515,5.7799,5.6874 mg/g。
3 讨论
筛选利胆颗粒中白芍TLC鉴别方法,展开剂分别采用了三氯甲烷-乙酸乙酯-甲醇-甲酸(40:5:10:0.2)[4]、二氯甲烷-乙酸乙酯-甲醇-甲酸(40:5:10:0.2)、醋酸乙酯-甲酸-冰醋酸-水(15:1:1:2)[5]、乙酸乙酯-甲醇-冰醋酸-水(15:2:1:3)于10 ℃下放置过夜的上层溶液。结果表明以乙酸乙酯-甲醇-冰醋酸-水(15:2:1:3)于10 ℃下放置过夜的上层溶液为展开剂显色后主斑点更加清晰,各斑点间的分离度较佳。
在姜黄的TLC定性鉴别研究中,展开剂分别选用了三氯甲烷-甲醇-甲酸(96:4:0.7)[6]、二氯甲烷-甲醇-甲酸(96:4:0.7)、环己烷-丙酮(1:1)[7]、氯仿-甲醇-冰醋酸(96:3:1)[8]。结果表明,以二氯甲烷-甲醇-甲酸(96:4:0.7)为展开剂显色后主斑点更清晰;且只有在该展开剂条件下,姜黄对照药材能呈现3个主成分的斑点。
在橙皮苷含量测定的研究中发现,由于橙皮苷具有双氢黄酮氧苷结构,呈弱酸性[9],因此流动相的 pH 对分离有较大影响。流动相条件尝试甲醇-0.1%磷酸(35:65)[10]、甲醇-冰乙酸-水(35:4:61)[11]、甲醇-冰乙酸-水(30:4:66)[12]甲醇-1%乙酸水溶液(50:50)[13]、但分离效果不佳,分离度偏低。改用乙腈磷酸系统,采用乙腈-0.2%磷酸20:80[14]、乙腈0.2%磷酸15:85以及梯度洗脱的液相条件。以分离度、峰形、保留时间作为评价指标,最终确定了2.2.2项下的梯度洗脱色谱条件,分离度远高于其他条件。

