腹腔镜下门静脉高压症巨脾切除术中优先离断脾蒂的效果观察
彭 俊
(广西北海市人民医院普通外科一区,北海市 536000,电子邮箱:nunu839@163.com)
腹腔镜下行脾切除术主要用于治疗各种外伤引起的脾破裂和血液系统疾病导致的脾肿大[1-2]。由肝硬化引起的脾肿大患者存在凝血功能障碍、巨脾导致的血流淤积及与周围组织粘连,手术风险非常大[3]。随着腹腔镜手术技术的不断发展,其手术风险已大大降低,但术中大出血特别是脾蒂出血仍然是最凶险的问题,因此,术中对脾蒂的处理是手术的核心问题[4]。本研究探讨肝硬化并门静脉高压症巨脾患者行腹腔镜下巨脾切除术时先离断脾蒂的效果及安全性,现报告如下。
1 资料与方法
1.1 临床资料 选取2012年1月至2017年1月在我院就诊的80例肝炎性肝硬化并门静脉高压症伴有巨脾患者为研究对象。入组标准:(1)符合2000年中华医学会传染病与寄生虫病学分会修订的《病毒性肝炎防治方案》中肝炎性肝硬化的诊断标准[5],均有不同程度的胃食管静脉曲张;(2)符合《内科学》[6]中巨脾诊断标准:深吸气时触诊脾脏边缘超过脐右及(或)脐水平线以下,长径在22 cm以上;(3)年龄25~68岁。排除标准:有严重心肺功能不全、肾脏功能不全以及恶性肿瘤患者。肝脏储备功能评定标准按Child-Pugh分级标准[7]。按随机数字表法将患者分为观察组和对照组各40例,两组患者的性别、年龄、病程、脾脏长径、肝功能分级、胃食管静脉曲张程度、血红蛋白水平、血小板计数、白细胞计数等资料比较,差异均无统计学意义(均P>0.05),具有可比性。见表1。
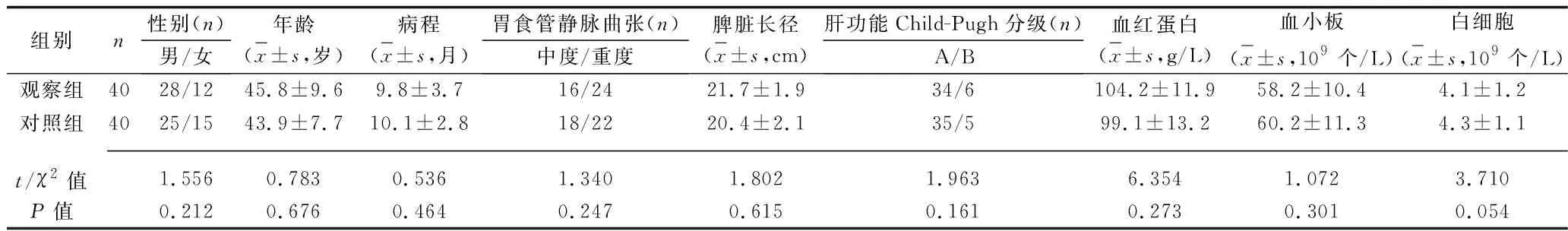
表1 两组患者的一般资料比较
1.2 手术方式
1.2.1 观察组:采用全身麻醉、行气管插管。患者取右侧倾斜位,保持头高足低位。在脐下缘作一1 cm切口,置入气腹针建立气腹,气腹压力为12 mmHg(1 mmHg=0.133 kPa);于同一切口放入1 cm穿刺鞘用于观察脾脏实际大小及其与周围脏器的粘连情况等。分别在右锁骨中线与脐平面、左腋前线肋缘下5 cm以及肋缘下作一切口,分别插入直径为5 mm、12 mm和5 mm的三根穿刺鞘。使用1 cm的腹腔镜下直线切割器从胃大弯向左侧将胃结肠韧带离断,露出脾蒂。然后探查入脾脏后方间隙,钝性分离周围疏松结缔组织后,在此间隙中用Endo-GIA一次性离断器切断脾蒂,然后再分别离断脾脏周围的脾膈韧带、脾胃韧带、脾结肠韧带等,切除脾脏。接着再沿胃壁向上用超声刀分离胃胰皱襞,结扎血管后剪断,于食管右侧将左膈下静脉离断。将贲门及食管下端6 cm充分游离并离断周围血管。用生理盐水充分清洗腹腔,检查术区没有出血灶后将脾脏放入标本袋内切碎后经主操作孔取出,脾窝放置一根双腔引流管。
1.2.2 对照组:术前准备、麻醉方法与观察组相同。手术时先离断胃结肠韧带、脾动脉,随后离断脾脏周围的脾膈韧带、脾胃韧带、脾结肠韧带后切除脾脏,然后再分离出脾蒂,用Endo-GIA一次性离断器切断脾蒂,其他操作方法同观察组。
1.3 观察指标 比较两组手术时间、术中出血量、中转开腹例数、术后下床活动时间、术后肛门排气时间、住院时间、脾窝引流管拔出时间及术后并发症发生率。
1.4 统计学分析 采用SPSS 21.0软件进行统计学分析。计量资料以(x±s)表示,比较采用t检验;计数资料用例数和百分比表示,比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结 果
2.1 两组患者术中和术后情况比较 观察组的手术时间、脾窝引流管拔出时间、术中出血量均短于或少于对照组(均P<0.01),两组术后下床活动时间、术后排气时间及住院时间比较,差异均无统计学意义(均P>0.05),见表2。观察组患者腹腔镜手术均成功,无中转开腹手术患者;对照组有2例中转开腹手术,中转开腹率为5.0%(2/40),两组中转开腹率比较,差异无统计学意义(χ2=0.513,P=0.474)。

表2 两组患者术中和术后情况比较(x±s)
2.2 两组患者术后并发症发生率比较 观察组术后并发感染2例,腹水8例,并发症发生率为25.0%(10/40);对照组术后并发感染4例,肝衰竭1例,胰瘘2例,腹水12例,并发症发生率为47.5%(19/40),观察组并发症发生率低于对照组(χ2=4.381,P=0.036)。
3 讨 论
巨脾可由多种疾病引起,如血液系统疾病、感染性疾病、免疫系统疾病、脾脏恶性肿瘤、囊肿等[8]。但引起巨脾的最常见疾病还是肝炎肝硬化所导致的门静脉高压症[9]。巨脾的治疗方法为外科手术切除,手术方法分为开腹脾切除术和腹腔镜下脾切除术[10-12],由于腹腔镜手术创伤小,有利于患者恢复,因此其在临床的应用越来越多。
由于门静脉高压症患者的脾脏严重充血、肿大,并且常伴有脾功能亢进,脾脏组织脆弱,手术中易破碎出血,加上患者常有凝血功能障碍,腹腔镜手术的风险极高,腹腔镜下脾切除术曾是该类患者的禁忌证[13-15]。随着腹腔镜手术技术的发展,腹腔镜下巨脾切除术已经逐步应用于临床,目前常用的是术式是腹腔镜下脾切除术加贲门血管离断术[16],术中出血是手术最凶险的并发症,尤其是在处理脾蒂过程中[17-18],目前根据脾蒂离断的顺序该术式分为脾蒂一级离断法、二级离断法和优化离断法等[19]。常规的腹腔镜下脾脏切除术首先离断脾脏周围的连接韧带,然后再处理脾蒂,这对于其他疾病导致的脾肿大可行,安全性较高,但是对于门静脉高压伴巨脾患者,因其脾蒂的血管增粗,脾门异常增大,再加上脾上极紧贴胃短动脉,如果在术中处理脾蒂操作不当或离断不完全,则可能导致大出血[20-22]。
本文观察组行腹腔镜下巨脾切除术时,优先处理脾蒂,即结扎动脉后用直线切割吻合器直接切断脾蒂,然后再分别离断脾脏周围的脾膈韧带、脾胃韧带、脾结肠韧带后切除脾脏,结果发现,与行常规腹腔镜下巨脾切除术的对照组比较,观察组手术时间更短,术中出血量减少(P<0.05)。本研究结果还发现,观察组患者术后脾窝引流管拔出时间短于对照组,术后感染、胰瘘、腹水等并发症发生率低于对照组(P<0.05),术后观察组患者无肝衰竭、术后大出血等凶险并发症发生。
综上所述,肝炎性肝硬化并门静脉高压症巨脾患者行腹腔镜下巨脾切除术时先离断脾蒂再切除脾脏的手术效果较好,手术安全性高,术后并发症发生率低,值得临床推广。

