经脾蒂上间隙入路腹腔镜脾切除术的临床应用与分析
田野,刘庆宏,曹晓飞,罗宝洋
(泰州市人民医院 肝胆胰外科,江苏 泰州 225300)
自1991年腹腔镜脾切除术首次报道以来[1],随着腹腔镜外科技术的不断发展,腹腔镜器械的不断改进,腹腔镜脾切除术已经成为普通外科较为常规的手术方式[2]。腹腔镜脾切除术因其创伤小、疤痕小和恢复快等优点而被广泛应用于需要行脾脏切除的患者的治疗中[3]。而在临床实践中发现,控制出血是决定手术成功的关键,以脾蒂前间隙为入路建立脾蒂周围无血管间隙,能更为安全有效地控制出血,成为腹腔镜脾切除术成功的关键点[4-5]。2017年以来泰州市人民医院开始经脾蒂前间隙入路的腹腔镜脾切除术,积累了一定的经验和技巧,现总结报道如下。
1 资料和方法
1.1 一般资料
回顾性收集2017年1月至2019年1月泰州市人民医院肝胆胰外科行腹腔镜脾切除术的患者资料,共28例,其中男10例,女18例;年龄45~65岁,平均(49.80±1.89)岁。其中血液系统疾病所致巨脾患者5例,余23例均为肝硬化合并门静脉高压症,单纯脾大并脾功能亢进的患者。所有患者均无消化道出血病史。
1.2 手术技巧和方法
1.2.1 手术体位:应用多功能床,患者取头高脚低平卧位,头高20°~30°,左侧抬高20°~40°,两腿分开。气腹压维持在10~13 mmHg。显示器置于患者头侧偏左,术者位于患者右侧,一助位于患者左侧,扶镜手位于患者两腿之间。
1.2.2 Troca穿刺点的选择:A孔(探查孔10 mm)位于脐下,B孔(辅助操作孔5 mm)位于剑突与脐连线的中点,C孔(主操作孔12 mm)位于左锁骨中线与左肋缘交点与脐连线的中点,D孔(辅助操作孔5 mm)位于左腋前线与肋缘的交点(依据脾脏大小上下移动),E孔(5 mm)位于剑突下,悬吊胃。
1.2.3 手术操作过程:建立气腹后先探查腹腔,了解脾脏的大小和周围(尤其是膈肌)粘连情况,探查肝脏硬化情况及血管曲张程度,探查腹腔其他脏器有无病变等。
于胃体中点处沿胃大弯向左侧切开胃结肠韧带、胃脾韧带至脾上方,抬起胃体切断胃后血管和胃胰皱襞,切开小网膜囊于E孔置入12#导尿管将胃体悬吊,便于分离处理脾动脉及胃短血管。结合术前影像学检查结果,在胰体尾交界上缘寻找脾动脉并结扎(图1A)。进入脾蒂上缘与胃短血管之间的恒定的无血管区(脾蒂上间隙) (图1B),充分游离并扩大,经此间隙向左上前抬起脾脏处理胃短血管及脾隔韧带。超声刀联合血管夹处理脾下极血管,切断脾肾韧带,分离脾周粘连,将脾脏托起建立脾后隧道(图1C),与脾蒂上间隙会合,建立脾蒂周围无血管间隙。暴露脾门、脾蒂,从C孔置入直线切割闭合器(Endo-GiA)一次性切断脾蒂(图1D)。将脾脏沿长轴方向剪成长条小块置入标本袋,将A孔延长至3~5 cm后将其取出。冲洗腹腔彻底后,脾窝置引流管一根,关闭切口。
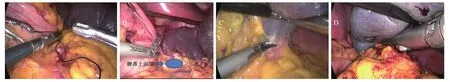
图1 手术操作过程
1.3 术后随访
术后常规随访3个月并复查血常规、肝功能、凝血功能和腹部彩超。
2 结果
28例患者均成功完成腹腔镜脾切除术,最大手术切口约5 cm。平均手术时间为(133.50±4.32)min,平均出血量为(198.00±54.76)mL,平均术后胃肠功能恢复时间为(39.37±4.06)h,无出血、胰漏等并发症发生。所有患者均于术后第7天拔除腹腔引流管,第8天出院。1个月后对所有患者进行随访,发现:1例患者出现门静脉血栓,但无明显症状,给予口服阿司匹林治疗;6例患者出现血小板升高,血小板计数>600×109/L,给予口服羟基尿治疗后血小板控制可;余患者未见明显异常体征。所有患者均无延迟性消化道出血、腹腔出血、胰瘘和腹水等并发症发生,无死亡病例。
3 讨论
脾脏切除术广泛应用于脾脏外伤,血液病,特别是ITP和血栓性血小板减少性紫瘢[6],门静脉高压症合并脾功能亢进等疾病的治疗[7]。由于腹腔镜下操作空间和手术视野的限制,脾脏上极的处理难度相对较大[8]。门脉高压巨脾的患者脾脏往往血运丰富、组织易碎,容易造成术中出血[9]。脾胃韧带处胃短血管压力较大,若此处出现损伤会导致出血迅猛,且此处操作空间较小,暴露困难,无法进行较好的止血[10];出血后往往需中转开腹手术治疗。
目前临床上对于脾脏微创切除手术患者脾蒂的处理方法主要有2种:(1)使用血管闭合器将脾蒂离断,具有较好的止血效果,可广泛应用于脾脏切除患者;但脾蒂未充分游离的情况下会出现脾蒂离断不全导致大出血而被迫中转开腹手术[11]。(2)二级脾蒂离断法脾切除术,对手术医师的要求较高,术中较容易发生出血而中转开腹手术[12]。手术入路主要有腹腔镜下二级脾蒂离断法脾切除术、杂交手术、手辅助腹腔镜脾切除术、术前脾动脉栓塞、脾下级入路法、隧道法脾脏切除术等一些腹腔镜脾切除术的改进方法,但未进行比较,尚不能给出一个最优方案[13]。借助于腹腔镜的放大效果,可在腹腔镜下寻找脾叶血管之间的间隙,通过分离的间隙结扎和离断脾蒂来降低手术难度[2]。在只游离脾下极,脾上极未游离的情况下,若出现离断脾蒂后出血,此时由于脾蒂处空间狭小,无论是寻找出血点还是缝扎出血点均操作受限,而在离断脾蒂前适当的处理脾上级建立脾蒂上间隙的方法,此时即使离断脾蒂出血,由于空间变大,也能从容不迫地处理出血,降低脾蒂大出血的中转开腹手术率及提高手术安全性。
脾蒂上缘与脾上级的胃短血管之间有一个明显而恒定的无血管区,而且此区域随着脾的增大而增大,此无血管区的间隙疏松容易分离不会出现明显出血。经此间隙可将脾蒂与胃短血管分开,处理胃短血管。同时向左上前方抬起脾脏,扩大脾上间隙,能够更容易离断脾膈韧带,控制出血。在充分游离脾肾韧带的基础上,通过脾蒂上间隙,可紧贴脾脏将脾上极上抬后自右向左游离无血管区间隙,顺利地与脾脏外侧的脾后隧道贯通,即可建立脾蒂的无血管隧道。此间隙能够较好地放置切割闭合器,进而达到一次性完整离断脾蒂的效果[13]。但门脉高压患者往往脾蒂较宽,同时合并脾门扭曲,为避免脾蒂闭合不全,应用金手指带7号线结扎悬吊缩小脾蒂。吊起脾脏脾蒂在有张力牵拉的情况下,用腹腔镜下切割闭合器穿过隧道一次性离断脾蒂。73%的患者胰尾部距离脾门不到1 cm,30%的患者胰尾紧贴脾门,因此闭合脾蒂时尽量靠近脾被膜分离,以避免胰瘘。
腔镜技术在脾切除中的微创性、安全性、有效性已得到充分证明及广泛认可。随着外科技术、先进手术设备的不断改进,腹腔镜脾切除术在复杂脾脏处理中的应用越来越广泛。精准的手术入路,是避免腹腔镜脾切除术并发症发生,使患者获得更好预后的关键措施。经脾蒂上间隙入路建立脾蒂周围无血管间隙切除脾脏的微创切除手术是安全、可行的,以期能为临床治疗提供有价值的参考。

