糖尿病前期患者前庭功能损伤及其影响因素分析
孟 岩 庄晓明
(首都医科大学附属复兴医院内分泌科, 北京 100038)
糖尿病(diabetes mellitus,DM)是严重威胁人类健康的世界性公共卫生问题。在全世界范围内发病率均呈上升趋势,近40年来我国的糖尿病发病率从1980年的0.67%[1]上升至2013年10.9%[2],糖尿病前期的比例更高。糖尿病前期是介于正常糖代谢和糖尿病的中间阶段的状态, 美国糖尿病防治计划(Diabetes Prevention Program, DPP)[3]研究结果显示糖尿病微血管合并症不仅发生于糖尿病阶段,早在糖尿病前期阶段已逐渐发生。前庭器官主要由迷路动脉供血,迷路动脉为微血管属于单一终末动脉,在糖尿病患者中约有70%的患者伴有不同程度的前庭功能受损的表现[4],那么糖尿病前期人群是否同样存在前庭功能受损呢?
温度试验是目前临床中用于前庭功能检查最广泛的方法,检测的是水平半规管前庭眼动反射。本研究通过对62例糖尿病前期患者进行前庭温度试验,探讨糖尿病前期与前庭功能损害的关系,并分析前庭功能损害的可能危险因素。
1 对象与方法
1.1 研究对象
根据口服葡萄糖耐量试验(oral glucose tolerance test,OGTT)结果连续入选糖尿病前期患者62例,其中男性30例,女性32例,年龄25~75岁,平均年龄(52.21±9.78)岁。另选同期年龄、性别构成接近、OGTT血糖正常的健康体检者共44名为对照组,其中男性19例,女性25例,年龄39~63岁,平均年龄(49.55±7.20)岁。
糖尿病前期诊断标准:①根据中国2型糖尿病防治指南(2017版)[5]:空腹血糖受损(impaired fasting glucose,IFG): 6.1 mmol/L≤空腹血糖 (fasting blood glucose, FPG)<7.0 mmol/L,餐后2 h血糖(2-hour post blood glucose,2 hPG)<7.8 mmol/L;糖耐量减低(impaired glucose tolerance,IGT): FPG<7.0 mmol/L,7.8≤ 2 hPG<11.1 mmol/L。IFG和IGT统称为糖尿病前期。
纳入标准:①年龄25~75岁;②血糖符合糖尿病前期诊断标准。
排除标准:①妊娠状态;②有其他明确导致内耳损伤病因,如噪音损害、耳毒性药物使用、梅尼尔病、良性阵发性位置性眩晕、前庭神经炎;③耳科检查存在外、中耳疾病者;④耳外伤和(或)手术患者;⑤眼科检查存在眼底病变患者;⑥严重的肝、肾、心脏、神经系统疾病以及其他全身疾病。
1.2 研究方法
1.2.1 一般资料
问卷调查,收集受试者一般临床资料,包括年龄、性别、既往史(高血压、高脂血症等)、耳鸣、眩晕等内容。测量受试者身高、体质量,计算体质量指数(body mass index,BMI)。
1.2.2 内分泌相关检查
OGTT FPG、 2 h PPG、糖化血红蛋白(glycosylated hemoglobin A1c,HbA1c)、三酰甘油(triglyceride,TG)、总胆固醇(total cholesterol,TC)、高密度脂蛋白胆固醇(high density lipoprotein-cholesterol,HDL-C)、低密度脂蛋白胆固醇(low density lipoprotein-cholesterol,LDL-C)、尿白蛋白/肌酐比值(urine albumin to creatinine ratio,UACR)。
1.2.3 前庭功能检查
采用Ulmer公司眼震视图仪(videonystagmography,VNG),测试内容为温度试验。原理为以冷热空气为刺激源,分别刺激左右水平半规管,使迷路的内淋巴因温度变化产生流动,引起终顶偏曲而出现眩晕、眼震等前庭反应。方法为患者取仰卧位,头前倾30°,采用50°和24°气流注入双侧外耳道,刺激持续40 s,两次不同温度实验间隔应>5 min。温度试验以最大慢相角速度(slow phase velocity,SPV)作为检测指标,前庭功能异常标准:①一侧半规管轻瘫(canalparalysis,CP)>16%且另一侧半规管功能正常。②双侧冷热SPV相加结果均<10。
1.3 统计学方法

2 结果
2.1 一般情况
两组受试者在年龄、性别、BMI、TC、TG、LDL-C、和HDL-C方面,差异均无统计学意义,糖尿病前期组耳鸣、眩晕例数高于对照组(P<0.05),详见表1。
2.2 前庭功能检查结果
糖尿病前期组前庭功能异常44例(71.0%),对照组前庭功能异常17例(38.6%),两组比较差异有统计学意义(P<0.05),详见表2。
与对照组比较,糖尿病前期组左、右眼最大慢相角速度SPV均降低,差异有统计学意义,详见图1。
2.3 糖尿病前期患者前庭功能损害的危险因素分析
在糖尿病前期组中根据前庭温度试验结果,以是否存在前庭损害为因变量,以性别、年龄、BMI、血压、耳鸣、眩晕、FPG、糖负荷后2 h PG、HbA1c、UACR、LDL-C、HDL-C、TC、TG作为自变量,进行后退法非条件Logistic回归分析。结果显示年龄、HbA1c进入模型,随着年龄增大,HbA1c浓度升高,糖尿病前期患者出现前庭功能损害的危险性逐渐增大,详见表3。
表1 糖尿病前期组与对照组一般临床资料比较Tab.1 General information of pre-diabetic mellitus patients and controls

表2 糖尿病前期组与对照组前庭功能异常检出情况比较Tab.2 Detection rate of vestibular dysfunction between pre-diabetic mellitus patients and controls
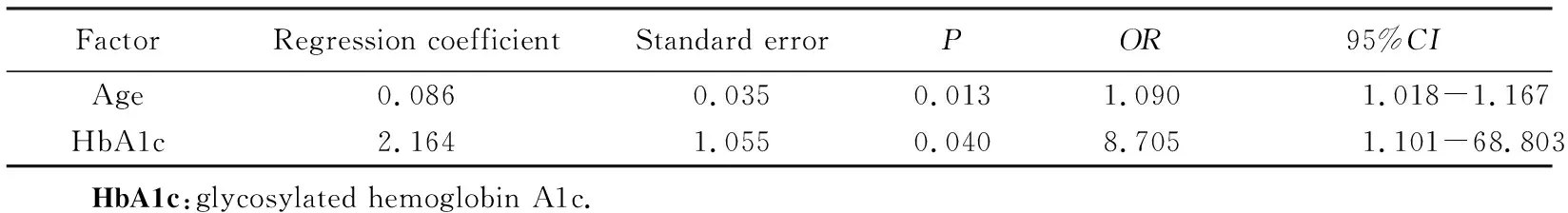
表3 糖尿病前期组前庭功能损害的相关因素分析Tab.3 Risk factors of vestibular dysfunction in pre-diabetic mellitus patients
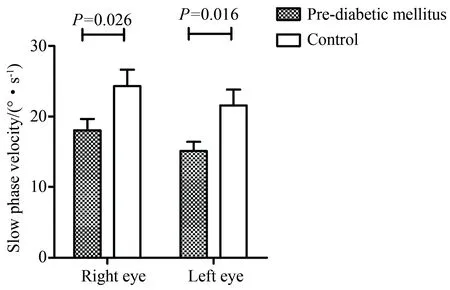
图1 糖尿病前期组与对照组最大慢相角速度比较Fig.1 Comparison of the SPV between the pre-diabetic mellitus patients and controlsSPV:slow phase velocity.
3 讨论
机体的平衡主要依赖于前庭觉、视觉和本体觉的相互作用,又称平衡三联,其中前庭系统在维持平衡中起主导作用[6]。前庭损伤不仅可出现不同程度的眩晕、恶心、呕吐、面色苍白、四肢厥冷等症状,甚至可导致患者定向功能减弱、平衡功能失调[7],因此糖尿病患者前庭功能的研究逐渐引起重视。在临床研究中,李鹃等[8]对76例糖尿病患者行眼震电图检查,68.4%存在前庭功能异常。周芸等[9]对137例糖尿病患者进行前庭功能检查,结果显示有84.4%的患者存在前庭功能障碍。Ward等[10]对病程10年以上的2型糖尿病患者进行前庭功能检查,70%的受试者存在半规管功能减退。本研究中,糖尿病前期组44例(71.0%)存在前庭温度试验异常,明显高于血糖正常者,与上述研究结果相一致,进一步比较发现糖尿病前期组双眼SPV均低于对照组,表现为双侧水平半规管功能受损。推测原因为糖尿病微血管病变可引起内耳微小血管循环障碍,使前庭神经变性过程发生在前庭眼动通路相应的部位,从而引起前庭反应异常[11]。
在发病机制的研究中,Gawron等[12]曾提出,糖尿病前庭功能损伤主要与糖尿病周围神经病变及微血管病变有关,该研究分析认为,由于前庭感受终器仅由迷路动脉供血,且该动脉为微血管,糖尿病微血管病变导致迷路动脉供血不足或闭塞时,就将引起前庭系统的外周性损害。Agrawal等[13]的研究比较了糖尿病合并周围神经病变与单纯糖尿病患者的前庭功能,结果显示糖尿病合并周围神经病变者前庭功能障碍的发生率更高,即糖尿病前庭功能损伤的发病机制可能与糖尿病周围神经病变及微血管病变有关。在前庭形态学研究中,袁艺昕[14]发现糖尿病大鼠前庭下神经从造模后第8周开始出现了结构改变,并且随着病程的延长超微结构破坏更严重,但球囊的前庭毛细胞、支持细胞等结构较对照组未发现明显异常,推测在糖尿病早期前庭功能障碍中前庭神经的损害可能起到更关键的作用,对进一步研究其病理机制提供了一定的理论基础。糖尿病前期是糖尿病发展过程中的重要阶段,是血糖异常的分水岭,已有研究[15]显示糖尿病周围神经病变及微血管病变在部分糖尿病前期患者中既已出现,因此推测糖尿病前期同样存在上述前庭形态学的改变,有待于今后病理学进一步研究证实。
本研究中可见年龄、糖化血红蛋白与前庭功能检查具有相关性。年龄与前庭损害呈正相关,OR=1.090(95%CI:1.018~1.167),表明年龄每增加1岁,前庭损害是原来的1.09倍。分析可能随着年龄的增加,长期的高血糖、胰岛素抵抗及脂质代谢异常等各种危险因素持续累积,加重微血管病变,促进动脉粥样硬化,导致前庭损害。关于血糖控制情况与前庭损害的相关性,目前研究结果不一,有研究[10, 16]显示血糖控制情况与前庭损害无明显相关性,Agrawal等[13]认为糖尿病病程和长期高血糖可增加前庭损害的发生率。本研究结果显示糖化血红蛋白是前庭损害的危险因素(OR=8.706,95%CI:1.101~68.803),高血糖状态通过氧化应激、缺氧和局部缺血、多元醇通路的激活以及糖基化终末产物浓度的提高等多种途径均可对前庭造成损伤。当细胞的抗氧化防御系统减少时,氧化应激会加速前庭器官老化,导致前庭功能减退。
前庭功能损害发生较为隐匿,早期可由视觉、本体觉代偿而维持身体平衡,通过相关研究[17-18]有利于提高患者和临床医生提高对前庭功能损害的认识,目前已有关于血糖与前庭功能的研究,但多为小样本的临床观察,病理学研究较少,有待于今后进一步探索研究。

