在元素化合物教学中巧用问题情境 培养学生核心素养的教学设计
韦骁珉
【摘 要】本文以“硝酸的性质”为例,论述如何通过巧妙的设计,将宏观辨识与微观探析、证据推理与模型认知、科学探究与创新意识等素养融入课堂,以培养学生的化学学科核心素养。
【关键词】高中化学 核心素养 硝酸的性质 实验探究 问题情境
【中图分类号】G 【文献标识码】A
【文章编号】0450-9889(2019)09B-0098-03
自 20 世纪 90 年代起,教学大纲就提出需要培养学生观察能力、思考能力和实验能力的必要性。2013 年,提出培养学生的科学探究能力。2015 年,教育部启动修订普通高中课程标准,提出要发展学生核心素养和学科核心素养。此外,国际科学教育课程文献中也提出学科素养的概念,核心素养和学科能力是国内外共同研究的焦点。
化学学科核心素养包括宏观辨识与微观探析、变化观念与平衡思想、证据推理与模型认知、科学探究与创新意识、科学态度与社会责任五个方面。通过学习硝酸的有关性质,一方面能完善学生元素及其化合物的知识体系,帮助学生逐步掌握学习化学的一些基本方法;另一方面在联系实际内容的基础上巩固氧化还原、离子反应等理论,还能使学生真正认识化学在促进社会发展,改善人类生活条件方面所起的重要作用,也为必修 2 学习物质结构、元素周期律、化学反应与能量等理论知识打下重要的基础。
一、巧用问题情境融入化学学科素养的元素化合物教学
硝酸是必修 1 最后一个内容。学生已经掌握了酸的通性,并熟悉金属活动性顺序表;学习了氧化还原反应、离子反应等原理;储备了很多元素化合物性质的感性材料;具备一定的实验分析能力,可以设计简单的探究实验。然而,学生容易误认为活泼金属与酸反应的产物一定是氢气,以及越活泼的金属与酸反应现象越明显等。教师可以设计巧妙的问题情境,让学生多次在“意外”中发现问题,再运用化学基本思想和方法设计实验方案。
情境一
在本节课中,利用硝酸泄露新闻视频与新制、久置浓硝酸实物进行对比。学生容易得出久置硝酸发生分解反应。这是自然界物质处于不断运动与变化状态的结果,且化学的变化需要一定的条件,加热就是硝酸分解的条件之一。这也是学科素养“变化观念与平衡思想”的体现。利用硝酸泄漏事故的情境作为出发点,介绍硝酸的工业用途以及泄露过程中消防员使用氧化钙处理现场情况。在帮助学生对社会热点问题作出正确的价值判断和提高学生的安全意识的同时,融入“科学态度与社会责任”这一素养。
情境二
让学生在认知冲突中发现硝酸具有强氧化性。学生从酸的通性中归纳出浓硝酸可以使石蕊试剂变红,但在具体分组实验中发现是先变红后变淡。教师创造了这个“突发”的问题情境,并引导学生发现这个有价值的问题。联系已学的二氧化硫、石墨、新制氯水均具有漂白性类比假设出浓硝酸的漂白原理可能是暂时性漂白,也可能是永久性漂白,具有强氧化性。确定研究目的后,学生根据两种不同类型的漂白性设计出特定的探究实验,并从自己设计的实验中找到答案。这鼓励学生在探究中学会合作,正视异常现象,敢于提出自己的看法。值得一提的是,在科学探究的过程中,认识角度和认识方式决定学生探究活动的逻辑起点。因此教师在设计探究实验前并不是突兀地抛出问题,而是从学生已有的“酸的通性”漂白原理总结的角度引导学生探究。探究硝酸氧化性这一部分更是引导学生从分析溶液中存在的离子入手,帮助学生建立思考的逻辑起点。这一环节,从真实问题和假设出发设计对应探究方案,运用化学实验进行实验探究能提高学生“科学探究与创新意识”的素养。
情境三
在探究硝酸氧化性本质的过程中,创设新的问题情境:在过量 Cu 与稀硝酸反应结束后的容器中加入稀硫酸,为什么和 Cu 与稀硝酸反应现象一致?从宏观现象的一致性引导学生推测微观反应的一致性。无论是何种溶液,均存在氢离子与硝酸根离子。再从量的角度分析 Cu 与稀硝酸反应的离子方程式,學生很快就能发现硫酸的作用是补充氢离子,Cu 和硝酸反应的实质是 Cu 和氢离子与硝酸根共同作用的结果。这个探究过程从宏观和微观相结合的视角分析与解决了实际突发问题,提升学生“宏观辨识与微观探析”的素养。
二、教学过程分析
环节一
创设情境:介绍硝酸的工业用途,播放双辽市那木乡发生浓硝酸泄露事件。展示刚取出的浓硝酸样品,打开瓶塞,请学生闻气味后归纳其物理性质后再展示一瓶久置的浓硝酸样品。
〖思考 1〗视频中久置浓硝酸中为什么会出现黄色气体?
在此环节中,学生大致能根据实物归纳出硝酸的物理性质。而黄色的气体学生则猜测是硝酸分解产生的。
教师演示:将少量浓硝酸置于试管中加热,无色浓硝酸变黄色。
〖思考 2〗分解产物是什么?你能设计实验来证明你的猜想吗?
学生刚学习过氮的氧化物,故他们可以轻易设计出实验方案。向久置的浓硝酸试剂瓶中加入少量的水后得到无色溶液即可证明硝酸的分解产物是 NO2 。
〖思考 3〗已知硝酸分解的产物是 NO2,你能利用氧化还原有关知识补充分解方程式吗?
设计意图:引导学生从宏观色彩变化中,将守恒思想与微观粒子联系起来,并利用氧化还原理论得出宏观微观的桥梁—— 硝酸分解的反应式。在这过程中,学生认识到化学变化的本质是有新物质生成,并伴有能量变化,硝酸受热分解产生了二氧化氮。
〖思考 4〗影片中的消防员如何处理泄露的硝酸?为什么?
学生很容易从酸的通性得出消防员使用碱石灰处理泄露的硝酸。
探究 1:能否设计实验证明硝酸具有酸的通性?
学生小组汇报酸的通性可以通过硝酸与碱,金属氧化物,某些盐,酸碱指示剂反应等实验验证,并开始进行小组实验。
设计意图:创设问题情境,在激发学生兴趣的同时提升他们的提取信息的能力。从消防员使用碱石灰处理现场,引导学生学习新物质可以从物质的分类角度归纳其通性,并用其简单的性质锻炼学生完成简单实验设计的能力,也渗透了绿色化学的思想。
环节二
创设问题情境:在小组报告中,一些小组报告将紫色石蕊试液滴入含有浓硝酸的试管中,振荡,发现溶液颜色先变红后变淡这“意外”结果。
教师演示:将石蕊试验溶液放入含有浓硝酸的试管中,稍后稍稍加热试管。
设计意图:让学生在胸有成竹的验证试验中得到“出乎意外”的结果,并立即建立基于真实情景的实验探究活动,以激发学生的学习热情。
〖思考 1〗在浓硝酸中滴入几滴石蕊混合后出现褪色现象,从量的角度分析,是谁过量?是谁少量?这一结果可能是由谁造成的?
〖思考 2〗如何设计实验证明你的猜想?
设计意图:引导学生从量的角度分析得出褪色的主要原因来自石蕊,学生受到启发后很容易设计出:(1)向褪色的溶液补充适量硝酸,无明显变化;(2)将过量的石蕊滴入褪色溶液中,溶液呈红色。得出结论,浓硝酸能和石蕊反应使其褪色。
〖思考 3〗联系已学知识,硝酸的漂白原理与什么类似?请设计一个实验验证。
设计意图:学生根据教师引导很容易从漂白的三大类:吸附漂白、化合漂白、强氧化漂白中对比出可能与二氧化硫或次氯酸漂白原理类似。故能设计出加热无色溶液观察,红色是否恢复即可得出结论。该环节巧妙利用了学生的最近发展区,激发学生的求知欲且使得实验探究更具有针对性和目的性,也为后续重点硝酸的强氧化性的学习做了一个铺垫。
环节三
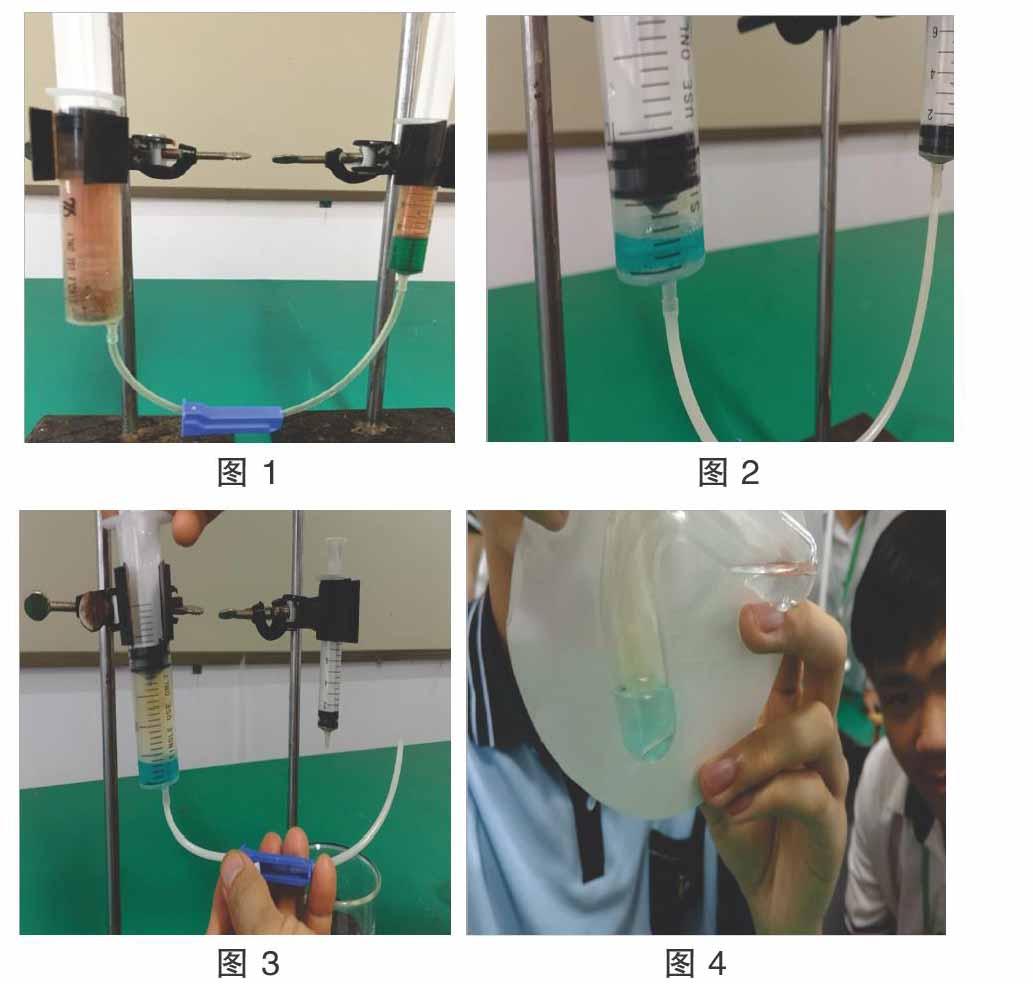
教师演示 1:改进实验装置,使用注射器和输液管形成一套密闭的实验装置,如图 1 所示。铜片放置于大管中,少量浓硝酸放置于小管中,轻推输液管开关,将浓硝酸推至大管,观察实验现象。在实验结束时,剩余的气体和溶液被排放到含有氢氧化钠的烧杯中。
〖思考 1〗根據实验现象,铜和浓硝酸反应的产物是什么?你能否根据氧化还原相关规律,结合实验现象写出反应方程式?
教师演示 2:另取一套装置,如图 2 所示。将浓硝酸改成稀硝酸。重复上述操作后,推动输液管开关以保持密闭环境,观察实验现象。在学生观察到蓝色溶液上方出现有无色气体存在后,将液体输送管轻轻从小管中取出,并将大管支架的活塞拉起来,让空气进入,如图 3。实验结束后,残余气体和溶液排放到含有氢氧化钠的烧杯中。
〖思考 2〗稀硝酸与 Cu 反应的产物是否仍然是氢气?请根据实验现象,写出铜与稀硝酸反应的方程式。
〖思考 3〗你认为这个实验的设计有哪些优点?
〖思考 4〗将少量稀硫酸注入该装置剩余的 Cu 和稀硝酸中,能否发生反应?
设计意图:在同一套装置上进行实验,在 Cu 片过剩装置中,通过移动注射管添加新的稀硫酸,使其与剩余溶液和 Cu 混合。学生能从“意料之中”的不反应,到“意料之外”的加入稀硫酸后竟然产生了 Cu 与稀硝酸相同的实验现象,激发学生探究 Cu 与稀硝酸反应的本质的欲望。将剩余的废液注入盛有氢氧化钠的烧杯中,向学生渗透绿色化学的思想。
〖思考 5〗请写出 Cu 与稀硝酸反应中的主要离子和实验中的离子方程式,并根据实验现象,推测稀硫酸的作用以及硝酸具有强氧化性的本质原因是什么?
设计意图:利用相同的实验现象,引导学生从溶液中存在的离子以及离子反应方程式的角度来看待问题,学生很容易想到反应的原因是氢离子与硝酸根。在等量的铜与稀硝酸的反应中,硝酸提供的氢离子不足以将铜反应完全,故稀硫酸加入后过量的氢离子与剩余的硝酸根可以继续与铜片反应产生同一现象。
〖思考 6〗你能设计实验来验证上述猜想吗?请分组设计探究硝酸氧化性的实验。
本班学生探究结果展示:
利用 Y 型管,铜片与稀硫酸在左边管,酸钾硝在右边管,并用橡胶塞塞紧管口。此时无现象,再向左倾斜 Y 型管将硝酸钾溶液与铜片、稀硫酸混合。此时得到的现象和铜片与稀硫酸反应一致,如图 4 所示(见上页)。说明铜与硝酸的反应是氢离子与硝酸根共同作用的结果。
设计意图:沿着“发现问题—提出假设—实验探究”这一流程,引导学生从微观离子角度思考问题,渗透微粒观的同时激发学生的主观能动性,突破本节课的重点与难点,升华离子反应的有关内容。
课后探究:
从金属活动顺序表来看,硝酸与 Cu、Al 反应谁更剧烈?请到实验室完成 Al、Cu 与浓、稀硝酸反应的实验。然后查阅相关资料,在下一节以小组的形式汇报本组的探究结果。
三、教学反思
(一)巧妙设计问题情境
让每一次的探究都发生在学生自己“意外”的实验中,并在教师帮助下,建立正确的认识方式和角度。通过自己的努力完成对“意外”现象的解密,能让整节课在“发现问题—提出假设—实验探究—得出结论”流程中将本节课知识串联成线。
(二)巧妙改进实验
在硝酸和铜的实验中,不用教科书的开放实验,而是用注射器形成了非污染的实验环境。注射器的使用可以大大减少氧气的存在,让 NO 能稳定存在,上拉活塞将空气注入后可以明显看到无色变为红色。这使得原本模糊不清的现象更清晰,帮助学生更接近反应的本质。注射器的输注管可以提供类止水夹的功能,并且容易形成闭合的系统。反应结束后,将剩余的气体和溶液注入强钠试剂中除去,不污染环境,让这个本来很多教师敬而远之的实验变得更安全、更有操控性、更符合绿色化学的要求。
【参考文献】
[1]王 磊.基于学生核心素养的化学学科能力研究[M].北京:北京师范大学出版社,2018
[2]梁东旺,杨 欢.基于化学学科核心素养的《硫和氮的氧化物》第一课时教学设计[J].中学化学教学参考,2018(4)
[3]庄德刚.基于学科观念构建的元素化合物“硝酸的性质”教学设计[J].中学化学教学参考,2015(9)
[4]王 晶.高中化学教材的研究和编制——人教版高中化学必修模块教材分析[J].中学化学教学参考,2009(Z1)
(责编 卢建龙)

