连续性肾脏替代治疗急性肾损伤对肾功能和氧化应激水平的影响
雷清凤,艾俊英
(长江大学第一临床医学院 荆州市第一人民医院肾内科,湖北 荆州 434000)
急性肾损伤(Acute kidney Injury,AKI)是临床常见的急性肾脏病变,常继发于多脏器功能衰竭、急性胰腺炎、慢性肾脏病等原发疾病。AKI患者的肾小球滤过率持续性或突然性下降,导致体内大量的毒性代谢产物不能排出,并诱发酸碱失衡、水电解质紊乱等,进而导致多系统并发症[1]。AKI的危害极大,如不及时救治可导致患者死亡。单纯的药物治疗用药复杂、治疗周期长、治疗难度大,不利于病情的控制[2]。
CRRT是临床常用的肾脏替代疗法,可清除循环中中小分子物质,纠正水、电解质紊乱和酸碱失衡,同时对血流动力学指标的影响很小,有助于维持较稳定的有体循环灌注和内环境,对患者的肾功能起到一定的保护作用,同时还可避免间歇性血液透析时血浆渗透压骤降导致的急性肺水肿、低血压等不良事件[3]。本研究探讨了连续性肾脏替代治疗AKI对患者肾功能和氧化应急因子的影响情况,现将结果报道如下。
1 资料与方法
1.1 一般资料
选取我院2013年2月至2018年2月收治的AKI患者180例,根据血液滤过方式不同分为对照组和观察组。对照组90例,其中男49例,女41例,年龄30~75岁,平均(53.66±12.52)岁;原发疾病:多脏器功能衰竭21例,急性胰腺炎42例,慢性肾脏病(CKD)15例,其他12例。观察组90例,其中男51例,女39例,年龄30~75岁,平均(54.10±12.82)岁;原发疾病:多脏器功能衰竭23例,急性胰腺炎44例,CKD14例,其他9例。两组AKI患者一般资料比较,具有均衡性(P>0.05)。纳入标准:①符合KDIGO诊断AKI标准,符合《内科学》[4]中AKI的诊断标准。②均接受肾脏替代疗法。③急性生理学和慢性健康状况评分(APACHEⅡ)≥12分。④3个月内未服用激素及免疫抑制剂者。排除标准:①合并房间隔或室间隔缺损。②严重的的肺动脉高压、心脏瓣膜反流。③精神疾病者。
1.2 方法
对照组患者采用间歇性血液透析,采用Seldinger技术穿刺股静脉建立血管通路后置入单针双腔导管。采用贝朗Dialog血透机血液透析,血流量200~350mL/min,透析液流量500mL/min,采用低分子肝素抗凝,剂量2500~5000U。3~5h/次,3次/周,有出血倾向者采用无肝素透析。
观察组患者采用连续性静脉血液滤过,每周3次,每次8h,采用Seldinger技术穿刺股静脉建立血管通路后置入单针双腔导管。采用贝朗Diapact CRRT机血液滤过。血流量150~200mL/min,置换液采用后稀释法输入,保持置换液流速1900~2800mL/h,根据患者容量负荷及具体病情确定超滤量及治疗时间,一般超滤量150~250mL/h。采用低分子肝素抗凝,首剂量2500U,之后每小时增加500U维持,有出血倾向者采用无肝素或枸橼酸钠抗凝。
1.3 检测方法
分别于治疗前、治疗7d后抽取患者空腹静脉血,采用日本日立株式会社7600型全自动生化分析仪检测血肌酐(Scr)、血尿素氮(BUN)、血钾(K+)。另取一份血标本,3000r/min低速离心10min,取上清液检测肿瘤坏死因子(TNF-α)、白细胞介素-8(IL-8)、丙二醛(MOD)、谷胱甘肽过氧化物酶(GSH-Px)水平。检测方法为双抗体夹心酶联免疫吸附法,检测仪器为美国伯腾ELX800多功能酶标仪,试剂盒购自南京建成生物工程研究所,严格按照试剂盒说明书操作。 APACHEⅡ评分:括年龄、急性生理健康、慢性健康等维度,分数越高,预后越差。
1.4 统计学分析
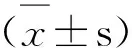
2 结果
2.1 两组患者治疗前后MAP、HR、PaO2水平比较
治疗前,两组患者MAP、HR、PaO2水平比较,差异无统计学意义(P>0.05)。治疗后,观察组患者MAP、HR、PaO2水平与对照组比较,差异无统计学意义(P>0.05)。见表1。

表1 两组患者治疗前后MAP、HR、PaO2水平比较
2.2 两组患者治疗前后肾功能变化情况
治疗前,两组患者肾功能指标水平比较,差异无统计学意义(P>0.05)。治疗后,观察组患者血Scr、BUN、K+水平低于对照组,差异有统计学意义(P<0.05)。见表2。
2.3 两组患者治疗前后TNF-α、IL-8、MOD、GSH-Px变化情况
治疗前,两组患者TNF-α、IL-8、MOD、GSH-Px水平比较,差异无统计学意义(P>0.05)。治疗后,观察组患者TNF-α、IL-8、MOD水平低于对照组,GSH-Px水平高于对照组,差异有统计学意义(P<0.05)。见表3。

表2 两组患者治疗前后肾功能变化情况
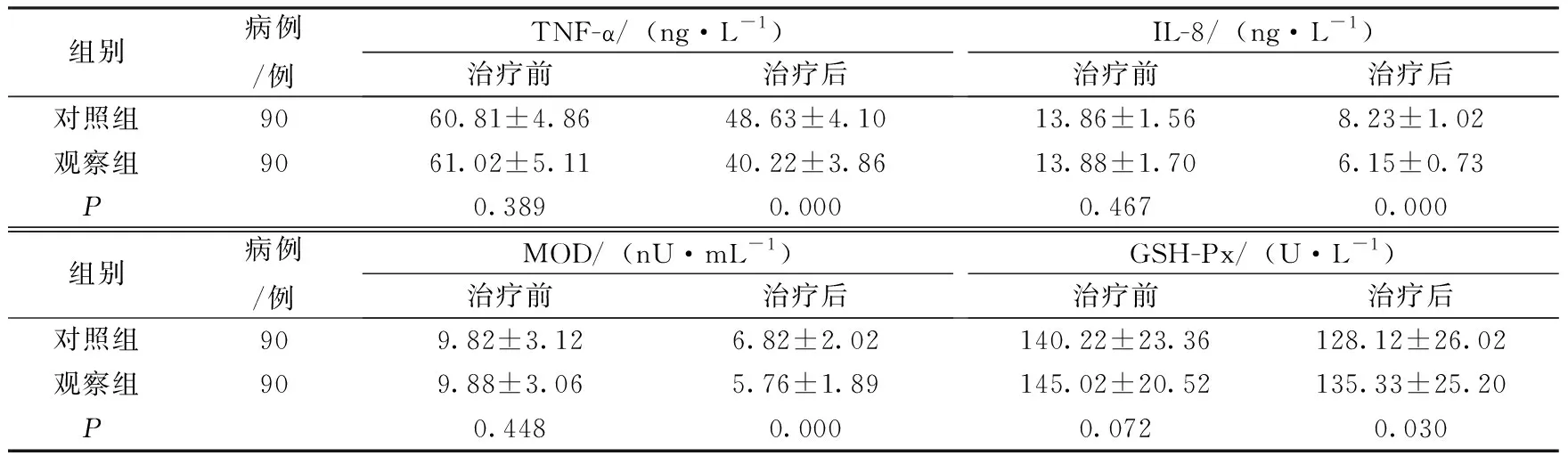
表3 两组患者治疗前后TNF-α、IL-8、MOD、GSH-Px水平变化情况
2.4 两组患者治疗前后APACHEⅡ评分比较
表4 两组患者治疗前后APACHEⅡ评分比较
治疗前,两组患者APACHEⅡ评分比较,差异无统计学意义(P>0.05)。治疗后,观察组患者APACHEⅡ评分低于对照组,差异有统计学意义(P<0.05)。见表4。
3 讨论
AKI是严重创伤、多脏器功能衰竭、急性胰腺炎、CKD等疾病的常见并发症之一,其发生机制比较复杂,可能与上述疾病引起的相对缺血、缺氧状态易导致肾小管坏死、肾小球滤过率下降,进而促进肾功能衰竭进程。疾病治疗时如使用升压药物,可导致周围动脉收缩、肾脏灌注不足而导致肾皮质缺血缺氧性损伤[5,6]。AKI发生后肾脏的排泄功能下降,体内大量的毒性代谢产物不能排出,并诱发酸碱失衡、水电解质紊乱等,进而导致多系统并发症[7]。
血液透析治疗是AKI常用的肾脏替代疗法,可清除循环中小分子物质,有助于体内毒性代谢产物的排出,并纠正机体酸碱失衡、水电解质紊乱状态[8],。有研究发现AKI患者多伴有水负荷过大、高内毒素水平,间歇性血液透析法需要快速消除溶质和水,引起血流动力失衡,进而引发低血压、心率失常等不良反应,甚至加重多器官功能障碍[9]。此外间歇性血液透析可清除肾上腺素、去甲肾上腺素等小分子物质,继而引起血压变化,不利于肾功能的恢复[10]。本研究中虽单次血液透析后Scr、BUN、K+低于单次CRRT治疗者,但采用IHD治疗者治疗1周后Scr、BUN等肾功能指标和K+水平高于采用CRRT治疗者,与上述研究相符[9,10]。
CRRT治疗模拟肾脏清除溶质和水的过程,脱水反应持续、缓慢,可维持治疗过程中血流动力学的稳定,避免因血浆渗透压突然下降所致的低血压、急性肺水肿等不良反应[11]。有研究认为[2],采用CRRT治疗AKI对患者的MAP、HR等血流动力学指标水平影响更小。但本研究中两组MAP、HR、PaO2水平差异无统计学意义。这与已有的临床研究结论并不一致,有待于进一步研究探讨。
AKI的发生与炎性损伤、氧化应激损伤密切相关[12]。TNF-α是炎症反应的起始因子,可引起IL-8等促炎介质大量释放,引起或加重炎症反应。而炎症因子的释放失控可导致炎症级联反应,进一步损伤其他器官和组织[13]。本研究中采用连续性肾脏替代治疗者治疗后TNF-α、IL-8水平低于采用间断血液透析治疗者。这一结果提示,连续性肾脏替代治疗AKI可更好地减轻机体炎症反应程度。这是由于连续性血液滤过具有强大的滤过功能,可迅速清除炎症介质。
MOD是机体脂质过氧化反应的副产物,是反映机体氧化应激损伤的敏感指标[14]。GSH-Px是天然的抗氧化物质,可对抗MOD,保护组织、细胞免受过氧化损伤[15]。本研究中采用CRRT治疗者治疗后MOD水平低于采用间断血液透析治疗者,GSH-Px水平高于采用间断血液透析治疗者。这一结果提示,连续性肾脏替代治疗AKI可更好地减轻机体的氧化应激反应程度,避免氧化应激反应对肾脏造成的损伤。
本研究还发现,采用CRRT治疗者治疗后的APACHEⅡ评分低于采用间断血液透析治疗者。这一结果提示,连续性肾脏替代治疗AKI可更好地改善患者的健康状况和病情转归。综上所述,CRRT治疗AKI可平稳患者生命体征,改善肾功能并减轻氧化应激反应程度。

