术前超声及钼靶BI-RADS分类对早期乳腺癌的诊断价值
席晓萍,闫 玮,张怡靓,丁 雪,徐 闻,李文红,王松涛
乳腺癌是女性最常见的恶性肿瘤,严重危害身心健康和生活质量。随着影像学技术的发展和体检的普及,近年来,乳腺结节的发现率不断上升,乳腺癌的发病率也逐年上升。WHO提出对于癌症的三级预防[1]:一级为病因学预防,二级为早发现、早诊断、早治疗,三级为临床预防或康复预防。目前对于乳腺癌的发病原因并不明确,一级预防受限,因此二级预防中早期诊断尤为关键,尽早发现并及时治疗对预后有着十分重要的意义。本研究回顾性分析我院近两年的早期乳腺癌患者,比较术前超声、钼靶BI-RADS分类对早期乳腺癌的诊断价值。
1 资料与方法
1.1 一般资料 回顾性分析2015-08至2017-08在我院病理确诊为早期乳腺癌(TNM分期为Ⅰ、Ⅱ期)患者的临床资料,入选标准为术前同时进行超声和钼靶X线检查。共43例(44个病灶),年龄30~79岁,平均(51.9±10.1)岁。44个病灶最大径平均值为(1.78±0.76)cm(0.6~4.0 cm),其中浸润性导管癌32个,黏液癌5个,导管内癌3个,其他类型髓样癌、浸润性小叶癌、大汗腺分化癌、小管状癌各1个。
1.2 检查方法 (1)超声:采用飞利浦iu22彩色超声诊断仪,探头频率为5~10 Hz,患者平卧位,扫查方法为以乳头为中心,顺时针方向放射状扇形扫查;(2)钼靶检查:采用GE钼靶机,型号为Alpha ST,对患者乳房的轴位和斜位进行拍片,必要时增加病灶局部进行重点摄片。
1.3 观察指标及读片 超声观察指标包括肿瘤大小、位置、形态、边缘、钙化及腋下有无肿大淋巴结。钼靶指标包括病灶边缘有无毛刺状改变,及其周围有无皮肤增厚、沙砾样钙化影、粗大血管影。超声和钼靶检查结果分别由两名工作5年以上的超声科和放射科医师完成,诊断意见不一致时讨论后决定。参考乳腺影像报告和数据系统(breast imaging reporting and data system, BI-RADS)分类诊断:0级,无法完成评估,需结合其他检查再次评估;1级,无可疑病灶;2级,良性病灶;3级,病灶良性可能性大,恶性风险<2%,建议3~6个月短期随访;4级,病灶恶性风险2%~95%,其中4a级为恶性风险2%~10%,4b级为10%~50%,4c级为50%~95%,建议活检;5级,病灶恶性风险>95%,建议手术;6级,已病理证实为恶性。本研究设定以BI-RADS分类≤3判为良性,=4a为可疑恶性,≥4b判为恶性。回顾性分析超声、钼靶及两者联合对各种病理类型早期乳腺癌的诊断价值。

2 结 果
2.1 超声和钼靶BI-RADS分类 病理诊断为早期乳腺癌的病灶术前超声BI-RADS分类判为可疑恶性及恶性的比例为93.2%(41/44),明显高于钼靶75%(33/44),差异有统计学意义(P<0.05),两者联合为95.5%(42/44)。其中对于黏液腺癌,超声判读为可疑恶性及恶性的比例明显高于钼靶,而浸润性导管癌、导管内癌及其他类型乳腺癌超声与钼靶BI-RADS分类差异无统计学意义(表1)。

表1 早期乳腺癌不同病理类型对应的术前超声、钼靶及两者联合的BI-RADS分类
2.2 漏诊病例 超声与钼靶联合,BI-RADS分类仍判为良性的病灶2个,分别为髓样癌和导管内癌,其中髓样癌最大径为1.4 cm,位于右乳(图2),导管内癌最大径为1.2 cm,位于右乳(图1)。
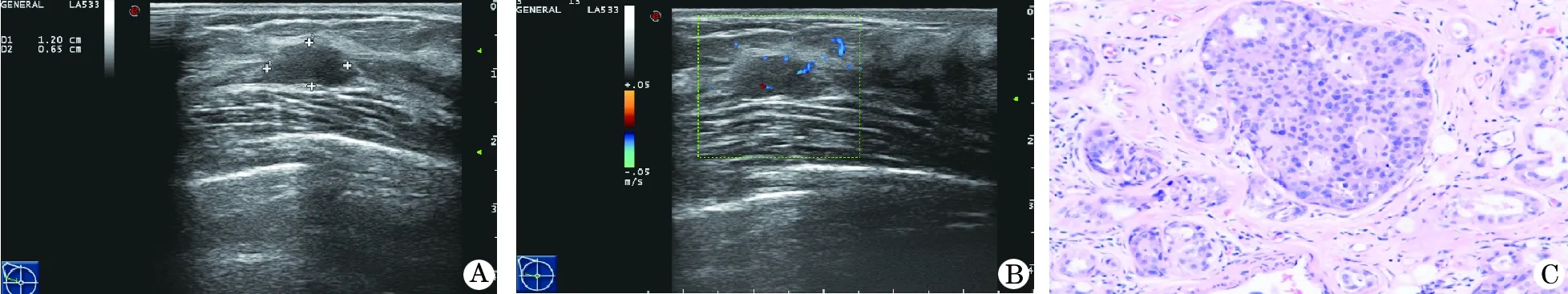
图1 乳腺导管内早期癌(41岁)超声与病理图
A.二维超声所示右乳外上象限低回声结节,大小约1.20 cm×0.65 cm,边界清,形态规则;B.彩色多普勒显示病灶内部少许条形血流,Ⅰ级;C.病理提示导管内癌

图2 乳腺早期髓样癌(49岁)
A.二维超声所示右乳外下象限低回声结节,大小约1.44 cm×0.98 cm,边界清,形态规则; B.彩色多普勒显示病灶无明显血流,0级;C.乳腺钼靶显示右乳下象限边界清晰的稍高密度病灶,边界清晰,周围腺体结构未破坏;D.病理提示髓样癌
3 讨 论
乳腺癌是全球第二大恶性肿瘤,占女性恶性肿瘤病死率的13.7%;中国女性每年的发病率为(10~60)/10万,总数约16.9万[2],严重危害女性的生命健康。因此,对于乳腺癌的早期发现、早期诊断至关重要,如何从筛查出来的大量乳腺结节中发现并诊断早期乳腺癌是现阶段面临的挑战。目前常用的影像学方法有很多种,包括MRI、超声、钼靶、CT等,但临床应用最多是钼靶和超声及其对应的BI-RADS分类系统,因为这两者较之MRI等其他方法更经济方便。
钼靶目前仍是国际上公认的早期乳腺癌的有效诊断方法[3]。乳腺癌钼靶的典型表现为腺体内肿块影、形态不规则、边缘毛刺、有微小钙化等[4],但钼靶的诊断敏感性与乳腺腺体密度成负相关[5];中国女性大部分属于高密度型腺体。高频超声有很好的分辨率,可清晰地显示乳腺断层的结构,能早期发现腺体内局部结构和形态的异常,且不受腺体密度的影响,现已被广泛应用于乳腺癌早期筛查和临床诊断,典型乳腺癌的超声表现为病灶形态不规则、纵横比>1、边缘毛刺或者蟹足样、内部可见微小或簇状钙化灶,彩色多普勒血流显示病灶内部丰富粗大血流[6]。因此,本研究希望通过比较术前超声、钼靶BI-RADS分类,探索两者在早期乳腺癌中的诊断价值,以提高对早期乳腺癌的诊断敏感性。
本研究发现,对于早期乳腺癌患者,术前超声BI-RADS分类判为可疑恶性的比例为93.2%,明显高于钼靶75%(P<0.05)。分析其原因:(1)本研究包含了多种病理类型的乳腺癌,尤其是黏液腺癌因其特殊的病理类型,钼靶缺乏特异性,容易被误认为良性病变。有研究表明,对于黏液腺癌的诊断敏感性钼靶明显低于超声[7],本研究结果与其相符。(2)与背景乳腺腺体类型有关,钼靶BI-RADS分类归为良性的4个浸润性导管癌的背景乳腺结构均为致密型,而致密型乳腺由于腺体重叠会影响X线成像[8, 9]。
超声和钼靶两者联合诊断可疑恶性及恶性的比例为95.5%,与术前超声BI-RADS分类诊断比例类似,说明超声对本组早期乳腺癌病例已有较高的能力诊断可疑恶性及恶性,区别为超声误诊为假体的一例浸润性导管癌。超声误诊为假体的原因:一方面可能是该病灶紧邻假体,回声与假体相近;另一方面血流信号并不明显,但钼靶诊断为4b类,后进行穿刺证实为浸润性导管癌。术前对此病灶补充进行了超声弹性成像,发现此病灶的硬度明显高于正常腺体组织,这也提示病灶为恶性。因此,对于假体置入后的乳腺,超声发现乳腺腺体内有类似假体回声的结节时,作出假体诊断时需谨慎,建议联合钼靶或一些超声新技术如弹性成像再次评估。
超声和钼靶BI-RADS分类诊断结合后仍有两例被误诊为良性,其中一例为髓样癌,另一例为导管内癌。乳腺髓样癌占所有乳腺癌的5%左右,是一种特殊类型的乳腺癌,由于其超声表现与纤维腺瘤极为相似,均可表现为形态规则、边界清楚、内部回声均匀,所以容易误诊;另有研究显示,髓样癌的彩色多普勒血流信号以Ⅱ~Ⅲ级多见,肿块大小对血流程度的影响最大,随着病灶增大,血流信号也更丰富[10, 11]。此例髓样癌病灶的最大径为1.4 cm,其对应得血流分类为0~1级,为诊断增加了难度,更易误诊为纤维腺瘤;再者,检查医师对于此种少见的特殊类型的乳腺癌缺少经验,导致术前超声BI-RADS分类归为3类。另外,典型乳腺髓样癌钼靶表现为腺体实质密度相等或略高,没有钙化且毛刺少见[12],因此也不易鉴别。然而,在我们回顾性分析该例患者资料时,发现该患者既往手术史中有一项为乳腺髓样癌术后,这提示影像医师在对疾病进行诊断时,了解患者的临床资料非常重要。对于另一例导管内癌,既往大量研究提示,超声和钼靶对导管内癌诊断的准确率均较低[13, 14],如本例所示,乳腺病灶为实性无钙化的病例,超声无法将其与乳腺增生、纤维腺瘤、腺病等良性病灶鉴别,而钼靶未能发现微小钙化,也无法与良性病灶鉴别,因此误诊。
对于早期乳腺癌尤其是黏液腺癌,术前超声BI-RADS分类判为可疑恶性及恶性的比例较钼靶更高;术前超声和钼靶判为可疑恶性及恶性的比例与乳腺癌病理类型密切相关;而对于特殊类型的早期乳腺癌及导管内癌超声和钼靶结合仍有可能漏诊。

