心脏外科Ⅰ类切口预防用抗菌药物路径式专项管理效果研究
石秀锦,秦 英,方振威,郑青敏,刘治军,王海燕,魏娟娟,徐晓宇,林 阳(首都医科大学附属北京安贞医院药事部,北京 100029)
外科手术预防使用抗菌药物一直是医院管理中的一个难题,卫生部相继制定了一系列相关文件旨在促进临床合理使用抗菌药物。心脏手术由于具有特殊性,如体外循环降低机体抵抗力,手术时间通常较长,瓣膜、血管等异物植入,术后都会留置中心动/静脉插管、胸/心腔引流管、呼吸道插管、泌尿道插管等,因此与其他清洁手术相比手术部位感染发生率较高[1]。而一旦发生感染,即便是浅表伤口感染,也会延长患者住院时间,增加其经济负担。更为严重的胸骨感染和纵膈感染等,则会显著增加死亡率,降低长期存活率[2-3]。由于心脏手术的高风险和临床医生的顾虑等多种因素,我院心外科Ⅰ类切口手术预防用抗菌药物存在使用品种级别高、疗程长、单次使用剂量大等诸多问题。2017年12月我院药事部联合其他部门进行了心脏外科Ⅰ类切口手术预防用抗菌药物路径式专项管理,实施了全程环节质量控制,以规范我院心脏外科手术预防性抗菌药物的使用,保证预防性抗菌药物使用的有效性、安全性和经济性。由于心脏移植手术、全腹主动脉替换和孙氏手术的感染风险高,以上三种手术不被纳入此次管理范围。此外,感染性心内膜炎由于术前即存在感染,也不纳入此次路径式管理。本文对围手术期预防用抗菌药物管理后成效进行了回顾、统计和分析,旨在探索路径式管理在抗菌药物管理中的应用成效,为医院加强围手术期预防性抗菌药物管理提供参考。
1 资料与方法
1.1 资料来源
住院患者抗菌药物使用情况分析的资料来源于医院HIS系统中提取的我院心脏外科七个病房路径式管理前(2016年12月、2017年11月)和路径式管理后(2017年12月)住院患者抗菌药物数据,包括抗菌药物名称、剂型、规格、用量、金额等数据。术后感染率的比较,选取七个病房中某病房2016年12月1日-2017年1月15日期间进行手术的所有患者作为路径式管理前组,2017年12月1日- 2018年1月15日期间进行手术的所有患者作为路径式管理后组,排除接受心脏移植术、全腹主动脉替换术、孙氏手术的患者和术前即存在感染的患者。
1.2 路径式管理措施
路径式管理措施包括:药事部联合医务部、感染科、院感办、心脏外科共同制定本院《心脏外科Ⅰ类切口预防用抗菌药物专项管理办法》和《心脏外科Ⅰ类切口手术预防用抗菌药物管理规范实施细则》,主要规范预防用药品种、时机、术中追加和疗程,并成立抗菌药物使用合理性评判专家组,针对心外科手术抗菌药物使用涉及的每一个环节,包括麻醉科、ICU和心外科室均制定抗菌药物使用的点评标准;路径式管理正式实施前,上述几个部门联合对各心脏外科医护人员针对心外科手术抗菌药物使用涉及的每一个环节进行抗菌药物合理使用及以上院内规章制度的培训,同时将审核评价标准(见表1)与临床医师进行沟通确认;路径式管理实施期间,临床药师每日下临床实时审核各心脏外科所有抗菌药物医嘱,每位临床药师负责一个心外科室;临床药师发现的不合理医嘱,当日由专人进行汇总并提交专家组讨论,经专家组讨论确定为不合理的医嘱进行公示及处罚。
1.3 住院患者抗菌药物使用情况的分析
提取路径式管理前和管理后抗菌药物的使用数据,并分别计算各个时间段内抗菌药物使用金额、抗菌药物使用率、抗菌药物用药频度(defined daily doses,DDDs)和抗菌药物使用强度(antimicrobial use density,AUD)。DDDs=药品消耗的总量/相应的限定日剂量(defined daily dose,DDD)。AUD=(DDDs/同期收治患者总人天数)×100。

表1 Ⅰ类切口清洁手术预防用抗菌药物合理性评价标准Tab 1 Evaluation criteria for rationality of prophylactic antibiotics for typeⅠ incision operation
1.4 术后切口感染判断标准及术后感染率的比较
依据卫生部医政司制定的诊断标准,凡切口局部红、肿、热、痛,筋膜组织以上有脓性渗出物,或拆线后局部有脓液渗出,无论有无细菌学证据,均属切口感染[4-5]。在感染与否无法界定时按感染对待。本研究采用回顾性的方法,分别调查路径式管理前后患者一般情况(性别、年龄、诊断等)、手术情况(手术名称、手术时间、是否体外循环、体外循环时间、出血量等)、术后感染情况(感染部位、病原菌等)及预后。使用SPSS 19.0软件进行统计学分析,计数资料采用χ2检验,P < 0.05为差异具有统计学意义。
2 结果
2.1 路径式管理前后住院患者抗菌药物使用强度的变化
路径式管理前2016年12月和2017年11月的抗菌药物使用强度分别为85.62和80.14,路径式管理后2017年12月的抗菌药物使用强度为56.85,与2016年12月相比同比下降33.60%(28.77/85.62),与2017年11月相比环比下降29.06%(23.29/80.14),详见表2。
2.2 路径式管理前后住院患者抗菌药物用药频度的变化
路径式管理前2016年12月和2017年11月的抗菌药物用药频度分别为10 680和9721,路径式管理后2017年12月的用药频度为6355,与2016年12月相比同比下降40.49%(4325/10 680),与2017年11月相比环比下降34.62%(3366/9721),详见表2。
2.3 路径式管理前后住院患者抗菌药物使用金额的变化
路径式管理前2016年12月和2017年11月的抗菌药物使用金额分别为281.30万元和201.22万元,路径式管理后2017年12月的使用金额减少为95.58万元,与2016年12月相比同比下降66.02%(185.72/281.30),与2017年11月相比环比下降52.49%(105.64/201.22),详见表2。

表2 管理前后抗菌药物使用强度、用药频度及使用金额的变化情况Tab 2 Effects of the path special management on AUD, DDDs and consumption fee of antimicrobials
2.4 路径式管理前后心外科住院患者常用抗菌药物品种的变化
路径式管理前(2016年12月)DDDs排名前10位的抗菌药物见表3,除注射用头孢呋辛钠的DDDs升高,其他9种药品的DDDs均有所下降,其中注射用头孢噻肟舒巴坦、注射用头孢米诺、注射用头孢哌酮舒巴坦钠、注射用头孢噻利、注射用磺苄西林钠,到2017年12月用药频度大幅下降,降幅分别为80.0%、96.0%、36.0%、92.0%、99.8%。路径式管理后(2017年12月),注射用头孢呋辛钠作为主要的手术预防用药,用药频度由2016年12月的921升高到3725,升高304%,增加4倍,排在第1位。

表3 路径式管理前用药频度排名前十位抗菌药物Tab 3 The top 10 antimicrobial agents in DDDs before the path special management
2.5 路径式管理前后术后感染率的比较
2016年12月1日- 2017年1月15日期间选取7个病房中某病房进行手术的患者共137例,排除接受心脏移植的患者3例和因感染性心内膜炎进行手术的患者1例,路径式管理前组共纳入患者133例。2017年12月1日- 2018年1月15日期间该病房进行手术的患者共148例,排除接受心脏移植的患者4例和因感染性心内膜炎进行手术的患者6例,路径式管理后组共纳入患者138例。
路径式管理前组133例患者中,6例患者术后发生感染,其中3例患者发生多部位感染,感染例数为10例,感染率为7.52%。路径式管理后组138例患者中,5例患者术后发生感染,其中2例患者发生多部位感染,感染例数为7例,感染率为5.07%。具体到感染部位,路径式管理前后两组发生肺部感染的例数分别为4例和3例,感染率分别为3.01%和2.17%;发生伤口感染的例数均为2例,感染率分别为1.50%和1.45%;发生血流感染的例数均为2例,感染率分别为1.50%和1.45%。此外,路径式管理前组发生感染性心内膜炎和胸骨感染1例,感染率为0.75%,路径式管理后组无感染性心内膜炎和胸骨感染发生。路径式管理前后两组总的感染率及各部位的感染率均无统计学差异(P > 0.05)。
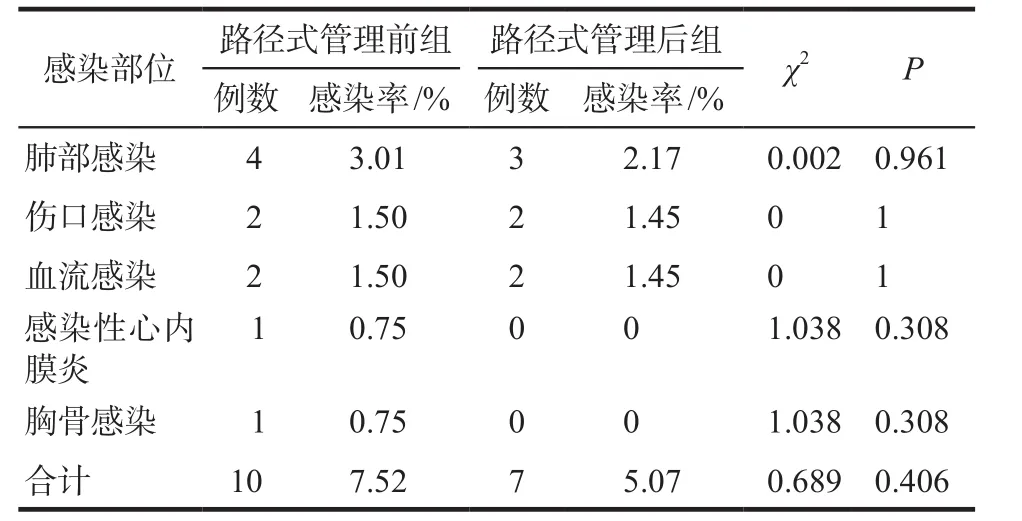
表4 路径式管理前后术后感染情况Tab 4 The postoperative infection rates before and after the path special management
3 讨论
本研究对我院多部门联合出台的心脏外科Ⅰ类切口手术预防用抗菌药物路径式管理前后心脏外科病房的住院患者抗菌药物使用强度、使用金额、用药频度、常用抗菌药物品种和术后感染率的变化进行比较,结果显示,通过心脏外科Ⅰ类切口手术预防用抗菌药物路径式管理一系列行政干预和药学干预措施实施后,预防用抗菌药物的合理性得到了显著提高,抗菌药物选择品种趋于合理,住院患者抗菌药物使用强度、使用金额和用药频度均大幅下降,表明抗菌药物的消耗量显著降低,这主要是源于路径式管理后预防用药疗程的缩短,其次不必要的联合用药和不合理的用法用量的改善对于抗菌药物消耗量的降低也有所帮助。
3.1 预防用抗菌药物品种选择
路径式管理前后我院心脏外科病房住院患者常用抗菌药物品种发生了较大变化。心脏外科手术部位感染的主要致病菌是革兰阳性菌,包括金黄色葡萄球菌和凝固酶阴性葡萄球菌,预防用药首选第一、二代头孢菌素[6]。对β-内酰胺类抗生素过敏的患者,可选用万古霉素或克林霉素。对于已知耐甲氧西林金黄色葡萄球菌定植患者,应使用万古霉素。统计数据显示,管理前用药频度排名前三位的抗菌药物分别是注射用头孢噻肟舒巴坦、注射用头孢米诺钠和注射用头孢哌酮钠舒巴坦钠,均为广谱抗菌药物,均对革兰阳性球菌活性比第一、二代头孢菌素类药物弱,广泛用于手术预防用药可能会导致耐药菌株的产生,其中注射用头孢米诺钠为头霉素类药物,对厌氧菌和革兰阴性杆菌有较强活性,以上均不宜用于心脏手术部位感染的预防。排名靠前的四代头孢药物头孢噻利亦为广谱抗菌药物,以及磺苄西林作为对铜绿假单胞菌有活性的青霉素类药物,主要用于怀疑有铜绿假单胞菌感染时,用于心脏手术预防用药也是不合理的。路径式管理后,以上五种药物的用药频度分别降低80.0%、96.0%、36.0%、92.0%、99.8%。第二代头孢菌素注射用头孢呋辛钠是路径式管理后预防用药最主要的品种,其用药频度与去年同期相比增加4倍,为主要的手术预防用药,预防用药品种趋于合理。
3.2 预防用抗菌药物疗程
心脏外科手术预防用抗菌药物疗程,是一个具有较大争议的话题,感染率的降低需要与抗菌药物带来的潜在风险如耐药菌株的产生和继发感染等进行权衡。各指南的推荐意见也有一定差异(从术前单剂量到术后48 h)。我国的《抗菌药物临床应用指导原则(2015年版)》规定,清洁手术的预防用药时间不超过24 h,心脏手术可视情况延长至48 h[7]。然而,由于心脏外科医师对术后并发感染的担心,包括我国在内的许多国家心脏外科预防用药疗程均偏长[8],有专家认为,心脏外科手术后,抗菌药物必须进入手术操作所留下的缝线和人工植入物与其密切结合的纤维组织中,方能起到预防感染的作用,而这些纤维组织在术后数日内才能形成,因此术后抗菌药物要应用约1周[9-10]。一项关于澳大利亚心脏外科手术预防性抗菌药物使用情况的调查显示,仅有10%左右医院在预防用药疗程方面符合《澳大利亚抗生素治疗指南》[11]。Kendall等[12]调查了英国36个成人心脏外科中心感染控制方法,结果显示17%中心预防用药疗程超过48 h,通常心脏瓣膜手术用药持续时间较长。国外学者Paul等[13]的研究表明,延长给药时间并未使深部切口感染的发生率明显降低。国内的研究显示,规范化的短程用药方案,在预防手术感染部位上与长期用药方案无显著差异[14]。在此次管理实施过程中,心脏外科病房对部分感染风险较低的患者做到了术后24 h停药,除非患者的症状、体征或者辅助检查提示感染性改变,或部分感染风险较高的瓣膜手术患者用药时间超过72 h。通过管理,心外科医生反映许多观念已改变,之前预防用药疗程结束后不敢停药,担心患者感染,但发现规范停药后,患者更安全。
3.3 术后感染率
本研究结果显示,路径式管理后,一方面抗菌药物的使用量显著下降,另一方面,术后感染率较管理前并未增加。诸多研究表明,预防性抗菌药物的使用可以显著降低心脏外科手术部位感染的发生率。预防的有效性受到多种因素的影响。首先是预防用药品种的选择,头孢菌素类药物是目前研究最多证据最为充分的心脏外科手术预防用药品种,第一代头孢菌素(头孢唑啉)、第二代头孢菌素(头孢孟多和头孢呋辛)以及第三代头孢菌素(头孢噻肟)在减少心脏外科手术部位感染方面疗效相当[15]。其次,确保整个手术期间具有足够的抗菌药物血清和组织浓度非常重要。这就需要在皮肤黏膜切开前30 ~ 60 min内或麻醉开始时给药,在输注完毕后开始手术,研究显示过早或过晚给予预防用药均会降低预防的有效性,增加感染的风险[16-17]。此外,如果手术时间超3 h或超过所用药物半衰期2倍以上,或成人出血量超过1500 mL,术中应补充一个剂量,必要时可追加第三剂。通过路径式管理,麻醉科医生对预防用药起始时间,需要追加药物的时间点高度关注,患者安全有了整体提升。本次管理对于预防用药的品种、剂量、给药时机、追加情况均进行了规范,从而保证了预防的有效性。
3.4 规范应用抗菌药物可显著减轻患者的经济负担
国内外的研究[13-14]均证明,短程单药抗菌药物预防心血管外科术后感染的效果与长程的抗菌药物应用相比并无差异,本研究也印证了相似的观点。另外,本研究还证实,选用价格相对低廉的第一、二代头孢菌素预防术后感染的效果,不劣于价格较为昂贵的抗菌药物。且短程用药和选用价格低廉的药物可使患者的抗菌药物费用明显减少,同时减轻患者的经济负担,本研究抗菌药物的使用金额大幅降低,节约了有限的医药资源,从长远来看,其社会经济学价值也是显而易见的。
综上所述,我院的心脏外科Ⅰ类切口手术预防用抗菌药物路径式管理规范了围手术期抗菌药物的使用,降低了抗菌药物的消耗量,管理前后患者感染率无明显差异。初步证实,规范、合理地预防用抗菌药物,可有效预防心血管外科手术术后感染、降低抗菌药物治疗费用。今后应进一步加大合理使用抗菌药物宣教力度,提升临床药师药学服务水平,彻底改变医师过度依赖抗菌药物的观念,提高医师合理用药意识,加大职能部门干预力度,建立督导长效机制,将抗菌药物的合理使用作为一项常规管理工作,促使抗菌药物的使用更趋于安全、合理、有效。

