4476例大株红景天注射液的安全性评价
张新茹,孙秀波,谢莉娜,付秀娟 (吉林大学第二医院药学部,吉林 长春 130041)
大株红景天注射液是由大株红景天提取物制成的中药制剂,具有改善急性心肌缺血和心肌梗死、减轻心肌缺血再灌注损伤、抑制血小板聚集等作用,临床用于活血化瘀、通脉止痛,主治心血瘀阻之胸痹心痛症(冠心病心绞痛)[1]。大株红景天注射液被广泛用于冠心病、不稳定型心绞痛、脑梗死、肺心病等的治疗,临床也存在一些应用不规范的情况[2-3]。关于大株红景天注射液不良反应及安全性评价虽然有些许报道[4-5],但对其不良反应的发生率、性质、临床表现、影响因素等缺乏全面的研究,为了全面认识大株红景天注射液上市后的安全性,本文采用非干预前瞻对照性医院集中监测的方法,选取本院大株红景天注射液使用最为集中的心血管内科,对其临床使用情况及安全性进行观察,旨为临床用药提供参考。
1 资料与方法
1.1 研究资料
选取2013年11月- 2016年8月在我院心血管内科使用通化玉圣制药有限公司生产的大株红景天注射液的全部住院患者(精神异常者除外)为评价对象,观察记录患者的用药情况和不良反应发生情况。
1.2 方法
1.2.1 前期工作 首先制定监测研究方案,并经过我院药事管理与药物治疗学委员会、医院伦理委员会论证同意,然后对参研人员进行统一培训,包括:大株红景天注射液的适应证、用法用量、安全性评价方案、《大株红景天注射液上市后安全性评价筛选卡》和《监测表》(病例组及对照组)的填写、药品不良反应(adverse drug reaction,ADR)/药品不良事件(adverse drug event,ADE)的识别和处理。
1.2.2 开放式对照研究 (1)观察组:参研人员每天深入研究科室内对每例用药患者进行观察监测,并填写《大株红景天注射液上市后安全性评价筛选卡》,保证无遗漏、无重复。(2)病例组:发现ADR/ADE立即上报,并纳入病例组,填写《大株红景天注射液上市后安全性评价监测表》,由药学、临床专家组成的不良反应评价小组进行ADR/ADE的关联性评价。(3)对照组:选择与病例组同期入住心血管内科,原患疾病与病例组相同或相似,未使用大株红景天注射液的患者。
1.2.3 ADR/ADE观察方法 从开始用药(即第1滴药液进入人体)立即密切观察30 min,观察有无ADR/ADE发生,30 min以后采取医护人员定期检查的方法或由患者主动汇报的方法观察。患者出院后仍接受患者主动汇报,但此时应注意鉴别是否为用药原因引起的ADR/ADE,并加以记录。由药学、临床专家组成的不良反应评价小组依照《药品不良反应报告和监测管理办法》进行ADR/ADE关联性评价[6]。
1.3 统计学处理
应用EpiData 3.1软件建立数据库,录入筛选表和监测表中记录的事项,双人核对,应用SPSS 20.0软件进行数据处理和分析。计量资料用()表示,大株红景天注射液相关不良事件与患者年龄、过敏史、用法用量间的比较采用χ2检验,病例组和对照组的对照研究采用t检验,P < 0.05表明差异有统计学意义。
2 结果
2.1 患者基本情况及ADR/ADE发生情况
纳入观察的患者共计4476例,其中男性2329例(52.03%),女性2147例(47.97%),年龄17 ~ 97岁,平均(60.32 ± 11.34)岁,≥50岁患者占83.91%。39例患者用药后出现ADR/ADE,依照《药品不良反应报告和监测管理办法》[6]进行关联性评价可知,很可能8例,可能29例,可能无关2例。因此大株红景天注射液相关ADR/ADE为37例,发生率为0.83%。37例患者中,男性15例,女性22例;年龄35 ~ 83岁,平均(59.4 ± 11.0)岁。
对大株红景天注射液所致ADR/ADE与患者年龄进行相关性分析可知,不同年龄段患者ADR/ADE发生率差异无统计学意义(χ2= 2.81,P = 0.73),除外70 ~ 79岁年龄段,其他各年龄段女性ADR/ADE的发生率明显高于男性(χ2= 0.79,P = 0.02)。在皮疹、寒战、面部肿胀等可视临床表现方面,男性与女性不良事件的发生率基本相似(χ2= 0.00,P = 1.00);而在头晕、心前区不适、心悸、恶心等主观描述性临床表现方面,女性高于男性(χ2= 2.92,P = 0.09),可能与女性患者神经比较敏感有关,详见表1。
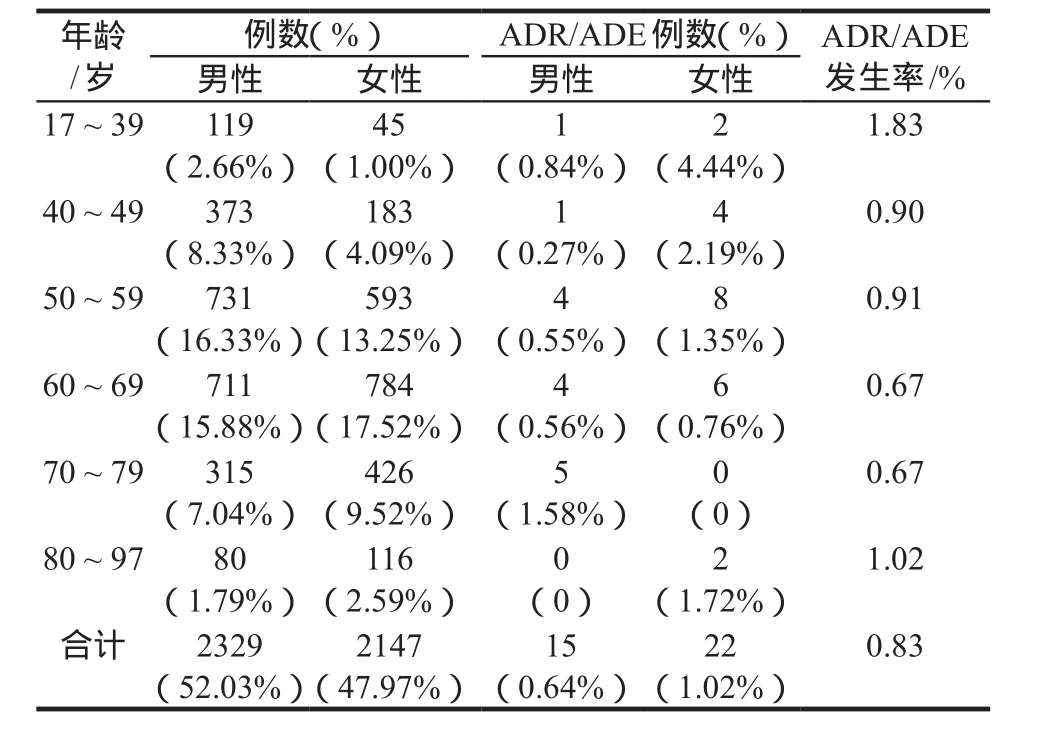
表1 4476例患者年龄分布及ADR/ADE发生情况Tab 1 Age distribution and ADR/ADE incidence of 4476 cases
2.2 患者过敏史与ADR/ADE的关系
4476例患者中37例有过敏性疾病史或药物食物过敏史,37例用药后发生ADR/ADE的患者中5例有过敏性疾病史或药物食物过敏史(其中过敏性疾病史1例、药物或食物过敏史3例,二者兼有者1例),对大株红景天注射液所致ADR/ADE与患者过敏史进行相关性分析,结果显示:既往有过敏史者ADR/ADE发生率高于无过敏史者,差异有统计学意义(P = 0.00),详见表2。
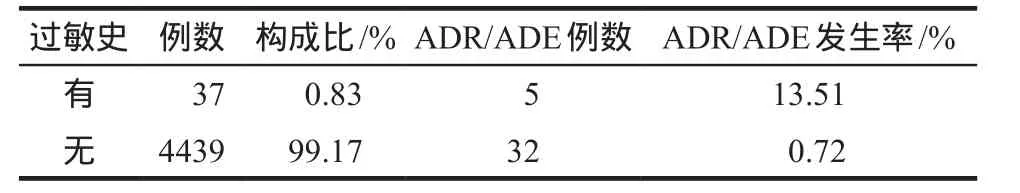
表2 大株红景天注射液相关ADR/ADE发生率与患者过敏史的关系分析Tab 2 Analysis of the relationship about the sofren injection related to ADR/ADE and the patient's allergic history
2.3 药品用法用量与ADR/ADE的关系
4476例患者均采用说明书推荐用量(10 mL,qd,ivgtt),无超剂量给药情况;大株红景天注射液说明书推荐溶媒为5%葡萄糖注射液,观察病例较多采用5%葡萄糖注射液和0.9%氯化钠注射液作为溶媒。
我院大株红景天注射液在临床实际使用中存在不符合说明书推荐的现象,大多数患者选择说明书未推荐的0.9%氯化钠注射液作为溶媒,且溶媒剂量偏小,对溶媒选择与ADR/ADE的关系进行分析,结果表明,使用0.9%氯化钠注射液作为溶媒者ADR/ADE发生率为0.80%,反而低于使用说明书推荐的5%葡萄糖注射液者(1.39%),但差异无统计学意义(χ2=0.30,P = 0.58),详见表3。
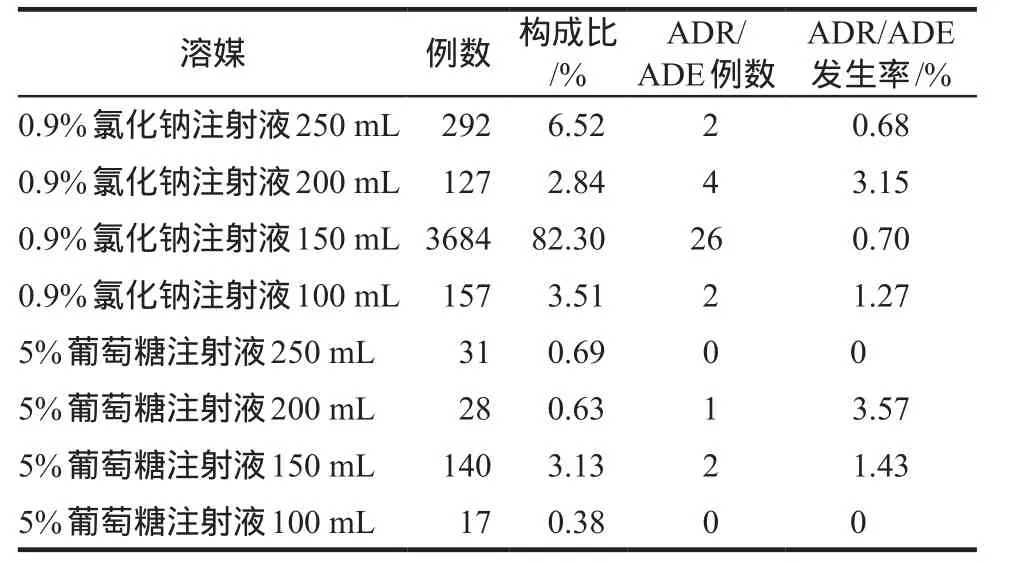
表3 溶媒选择与ADR/ADE发生率的关系Tab 3 The relationship between solvent and incidence of ADR/ADE
2.4 联合用药与ADR/ADE的关系
4476例患者中有4475例联合用药1 ~ 31种,平均(9.5 ± 4.2)种,其中联合用药1 ~ 5种者685例(15.31%);联合用药6 ~ 10种者2243例(50.12%),所占比例最大;≥11种者1547例(34.57%)。与大株红景天注射液联合使用的药物主要有阿司匹林肠溶片(3820例)、他汀类(3845例)、硫酸氢氯吡格雷(2636例)、硝酸酯类(2633例)、β-受体阻滞剂(2563例)、环磷腺苷类(2516例)、血管紧张素转化酶抑制剂/血管紧张素Ⅱ受体拮抗剂(1675例)、质子泵抑制剂(1574例)、曲美他嗪(1501例)、肝素类(1456例)、利尿剂(1254例)、钙通道阻滞剂(1104例)和复合辅酶(1068例)等。对大株红景天注射液相关ADR/ADE与患者联合用药个数进行相关性分析,结果显示随着联合用药种类的增多,大株红景天注射液相关ADR/ADE发生率有增加趋势,但差异无统计学意义(χ2=0.616,P = 0.735)。具体情况见表4。
2.5 ADR/ADE主要临床表现
37例患者共发生ADR/ADE 60例次,其中心血管系统损害17例次(心悸9例次、心前区不适6例次、前胸及后背疼痛1例次、胸闷1例次);消化系统损害17例次(恶心9例次;呕吐6例次;腹痛、腹胀各1例次);皮肤及其附件损害11例次(皮疹、瘙痒各4例次;面部红肿、面部潮红、面部及眼睑水肿各1例次);神经系统损害11例次(头晕8例次、头痛2例次、头胀1例次),眼部损害2例次(飞蚊症1例次;眼睛发胀1例次);全身性损害2例次(寒战大汗1例次;周身不适1例次)。37例患者ADR/ADE发生在用药第1天者19例、第2天者3例、第3天及第4天者各4例、第5 ~ 7天者共7例;无严重ADR/ADE的发生。30例患者在停药后症状好转;3例患者停药同时经对症处理后好转(1例表现为前胸、后背疼痛,停药并给予罂粟碱肌内注射,10 min后缓解;1例为全身皮疹伴瘙痒,停药并给予口服依巴斯汀、静脉滴注5%葡萄糖+维生素C +葡萄糖酸钙,2 d后皮疹消失;1例为恶心、呕吐,停药后给予甲氧氯普胺后缓解);3例皮疹伴瘙痒者,医生考虑症状较轻,权衡利弊未予停药,经口服西替利嗪、氯雷他定及外用曲咪新乳膏后症状消失;1例心前区不适、恶心症状也较轻,未予停药,未出现同一批次注射液导致大量ADR/ADE发生的情况。

表4 大株红景天注射液相关ADR/ADE发生率与患者联合用药种数的关系分析Tab 4 Relationship analysis of sofren injection related to ADR/ADE with combined drug numbers
2.6 病例组与对照组的对照分析
本文采取开放式对照研究的方法,即选择与病例组同期(± 7 d)入住心血管内科,原患疾病与病例组相同或相似,未使用大株红景天注射液者作为对照组,并对其基本情况、生命体征、实验室检查结果进行对照分析,详见表5 ~ 7。
2.6.1 病例组和对照组的一般情况 37例发生ADR/ADE患者的年龄平均(58.46 ± 11.60)岁,男性15例(40.54%),女性22例(59.46%);148例对照患者年龄平均(59.91 ± 10.74)岁,男性65例(43.92%),女性83例(56.08%)。37例病例组和148例对照组患者的年龄、性别比例、身高、体质量等一般资料差异均无统计学意义(P > 0.05),病例对照匹配情况良好,详见表5。
2.6.2 病例组和对照组的生命体征情况 病例组心率平均(75.70 ± 9.15)次·min-1,高于对照组平均(71.97 ± 8.53)次·min-1,差异具有统计学意义(t =2.34,P = 0.02),这与大株红景天所致ADR/ADE的临床表现(60例次ADR/ADE中包含17例次心血管系统损害,其中9例次表现为心悸)相一致,详见表6。

表5 病例组和对照组的一般情况Tab 5 The basic information in case and control groups
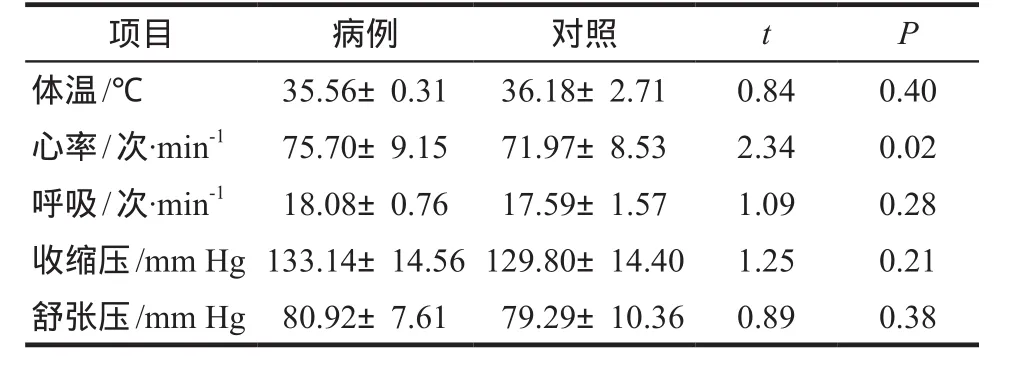
表6 病例组和对照组的生命体征情况Tab 6 The vital signs in case and control groups
2.6.3 病例组和对照组的实验室检查结果 病例组与对照组相比,红细胞计数、白细胞计数、中性粒细胞百分比及血小板计数等血常规指标、凝血常规指标、肝肾功能及血离子等实验室检查指标均无明显差异,详见表7。
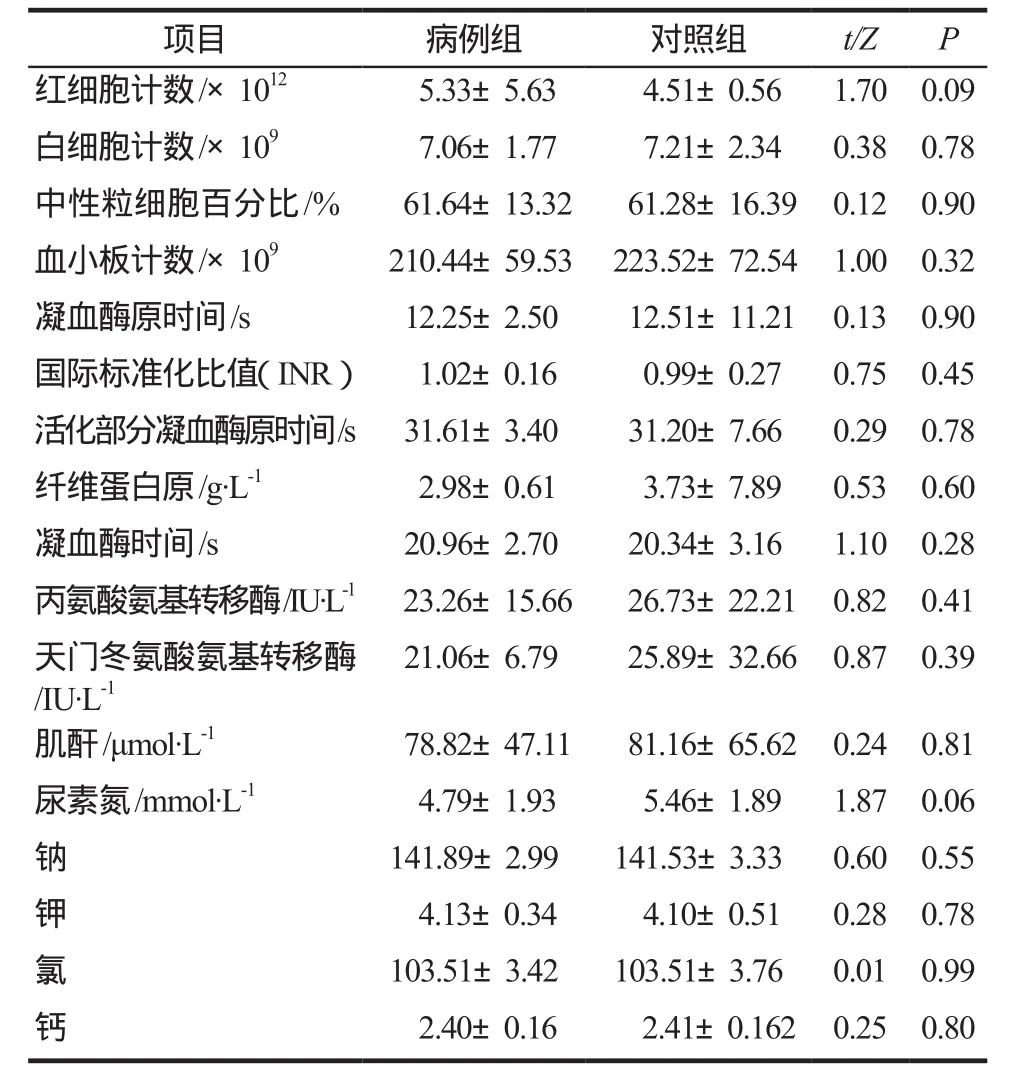
表7 病例组和对照组的实验室检查结果Tab 7 Results of laboratory examination in case and control groups
3 讨论
大株红景天注射液是由大株红景天经微波协助提取分离、精制、膜过滤制成的中药注射液,含有红景天苷、酪醇、红景天芬、红景天任、红景天素、多糖等,成分较为复杂。为系统评价其在临床的实际应用情况和不良事件发生情况,本研究采用非干预前瞻对照性医院集中监测的研究方法,对我院心血管内科4476例处方使用大株红景天注射液的患者进行了观察,对大株红景天注射液相关ADR/ADE情况进行统计分析,并将发生ADR/ADE的病例与同期(± 7 d)入住心血管内科、原患疾病相同或相似、未使用大株红景天注射液者进行对照研究。
研究结果显示,使用大株红景天注射液的4476例患者性别比例接近1∶1,年龄主要集中在50岁以上(83.91%),与心血管疾病的高发年龄相符;不同年龄段之间ADR/ADE的发生率无明显差异,表明该药所致不良事件的发生不受年龄因素影响。但在不同性别间,女性ADR/ADE的发生率明显高于男性(χ2=0.79, P = 0.02)。对具体临床表现进行分析发现,皮疹、寒战、面部肿胀等可视性临床表现的病例,男性与女性ADR/ADE的发生率基本相似(χ2= 0.00,P =1.00),而头晕、心前区不适、心悸、恶心等主观描述性临床表现,女性高于男性(χ2= 2.92,P = 0.09),考虑可能与女性患者神经比较敏感有关,但具体原因还需进一步研究。
对大株红景天注射液相关ADR/ADE与患者过敏史进行相关性分析,结果表明既往有过敏史者ADR/ADE发生率高于无过敏史者,提示有过敏性疾病史、药物及食物过敏史或过敏体质的患者应避免使用该药。研究还发现使用说明书推荐的5%葡萄糖注射液作为溶媒者ADR/ADE发生率为1.39%,反而高于说明书未推荐的选用0.9%氯化钠注射液作为溶媒者(0.8%),差异虽然无统计学意义(χ2= 0.303,P =0.582),仍值得密切关注。周芬等[7]曾对大株红景天注射液与不同溶媒配伍的不溶性微粒考察发现0.9%氯化钠注射液中不溶性微粒数量小于5%葡萄糖注射液,二者之间是否存在因果联系,仍需进一步研究。心血管内科患者常合并糖尿病,使得葡萄糖注射液在临床的使用很受限制,若能够证实0.9%氯化钠注射液作为大株红景天注射液的溶媒,其安全性优于5%葡萄糖注射液,或者与其相当,将会为大株红景天注射液的临床使用提供巨大便利。当然,本研究也存在一定的局限性,使用5%葡萄糖注射液作为溶媒者明显少于使用0.9%氯化钠注射液者,所以数据难免存在偏差,还需要进一步的研究来证实。
4476例患者中,由大株红景天注射液所致ADR/ADE者37例,发生率为0.83%,属偶见范畴[8],其中以心血管系统损害和消化系统损害多见,其次为皮肤及其附件损害和神经系统损害,眼部损害和全身性损害少见。37例患者均为一般ADR/ADE,无严重ADR/ADE发生,停药或对症处理后症状均好转或消失,未出现同一批次注射液导致大量ADR/ADE发生,另外用药第1天时ADR/ADE发生率为51.4%,因此建议在用药初期密切监测患者的反应。
病例组与对照组的对照研究结果显示,病例组患者的心率明显高于对照组(t = 2.34,P = 0.02),在60例次ADR/ADE中有9例次表现为心悸。因此,应警惕大株红景天注射液引起心率加快,建议心率较快的患者应慎重使用大株红景天注射液。实验室检查方面,病例组和对照组在红细胞计数、白细胞计数、中性粒细胞百分比及血小板计数等血常规指标、凝血常规指标、肝肾功能及血离子等实验室检查指标方面均无明显差异(P > 0.05),表明大株红景天注射液相关的ADR/ADE未累及造血、凝血、肝肾功能及离子水平。
综上所述,大株红景天注射液的安全性较好,但在临床应用中,需要对女性患者给予更多关注,应警惕大株红景天注射液引起的心率加快,对于心率较快的患者应慎重使用该药。本研究结果提示,大株红景天注射液溶媒的选择与药品说明书存在矛盾,还需要进一步的研究加以证实。

