妊娠合并先天性心脏病相关肺动脉高压患者围产期结局及影响因素分析
郑玉霞 孙秀云
辽宁省抚顺矿务局总医院(113008)
妊娠合并先天性心脏病(CHD)影响母婴安全[1]。随着外科手术的进步,CHD女性获得妊娠机会增加,使妊娠合并CHD的发生率逐渐增高[2]。肺动脉高压(PAH)在妊娠合并CHD患者中发生率为10%[3],可致孕产妇心功能衰竭、死亡,并威胁胎儿生命安全[4],是妊娠禁忌[5]。妊娠合并CHD相关PAH孕妇面临巨大的风险并严重影响围产期结局。为探讨影响妊娠合并CHD相关PAH预后的相关因素,本文回顾性分析了相关临床资料。
1 资料与方法
1.1 研究对象
①纳入标准:诊断结合病史、体格检查、心电图、心脏彩色多普勒超声检查,并由心外科会诊后确诊CHD[6];PAH诊断为静息状态下超声心动图通过三尖瓣反流压差间接测得肺动脉收缩压(sPAP)≥36mm Hg[7];单胎妊娠;临床资料完整。②排除标准:药物所致PAH,家族遗传性PAH;先天性左心疾病;先天性肺部器质性病变;门脉高压;合并其他妊娠合并症;感染;临床资料缺失;随访失访。本研究获得本院伦理会批准。
1.2 诊断标准
①PAH分类:轻度36~49 mm Hg,中度50~79 mm Hg,重度≥80 mm Hg原发性或继发性肺动脉高压[1,6,8]。②心功能分级,按照纽约心脏病协会(NYHA)心功能分级标准:Ⅰ级,患者从事日常活动不引起气喘、心悸、疲劳或心绞痛;Ⅱ级,体力活动轻微限制,休息时无明显症状,从事一般体力活动引起心绞痛、心悸及气喘;Ⅲ级,体力活动明显受到制约,休息时即可出现轻微症状,活动即出现气喘、心绞痛及心悸症状;Ⅳ级,临床症状明显,在从事体力活动后气喘、心悸、心绞痛症状明显加重[9]。
1.3 研究指标
①临床资料:收集入组患者基础临床资料,包括年龄、孕周、CHD类型、心脏手术史、孕期及产后心功能分级、PAH分级、围产期结局、围生儿结局。②实验室指标:收集分娩前血红蛋白(Hb)、血小板计数(PLT)、氧分压(PaO2),根据收集肺动脉收缩压(Pp)循环收缩压(Ps)计算Pp/Ps值。
1.4 随 访
收集所有研究对象至2018年1月份,随访采用电话和走访形式,随访内容为母婴生存结局、NYHA心功能分级等。
1.5 统计学分析
采用SPSS22.0进行数据分析,计量资料采用t检验,数据用均数±标准差(¯x±s)表示,采用F检验,等级资料采用Kruskal-Wallis H检验;百分比(%)表示计数资料,采用χ2检验;建立lgistic多因素回归分析模型,分析引起围产期不良结局的危险因素。P<0.05为差异具有统计学意义。
2 结果
2.1 孕产妇基线资料
共收集到本院2013年1月—2018年1月收治的合并CHD相关PAH孕产妇临床资料76例。年龄(29.7±6.1)岁,孕(30.3±8.9)周;初产妇39例,经产妇37例;接受围产保健42例,未接受围产保健34例。PAH轻度13.2%(10/76),中度38.2%(29/76),重度48.7%(37/76);妊娠期NYHA心功能分级Ⅱ级以上54.0%(41/76),孕产妇心衰率6.6%(5/76);医源性胎儿丢失率30.3%(23/76),早产率21.1%(16/76),足月分娩42.1%(32/76);极低出生体重儿占新生儿(含死亡)21.1%(15/71),新生儿窒息发生率11.3%(8/71),新生儿死亡率5.6%(4/71)。
2.2 不同PAH孕妇的临床指标比较
依据PAH程度和NYHA心功能分级将76例孕产妇临床资料进行分类统计发现,孕周、妊娠期NYHA心功能分级、心脏手术史、分娩前PaO2、PLT、Pp/Ps、Hb指标在PAH不同程度组间均存在差异(P<0.05);重度PAH组的平均孕周最短、妊娠期NYHA心功能分级Ⅱ级以上占比最多、心脏手术史比例最少、分娩前PaO2、PLT指数最低、分娩前Pp/Ps、Hb指示最高,孕产妇心衰率、医源性胎儿丢失率、早产率、极低出生体重儿比例、新生儿窒息率、新生儿死亡率均最高,新生儿出生体重低于其他组。见表1。
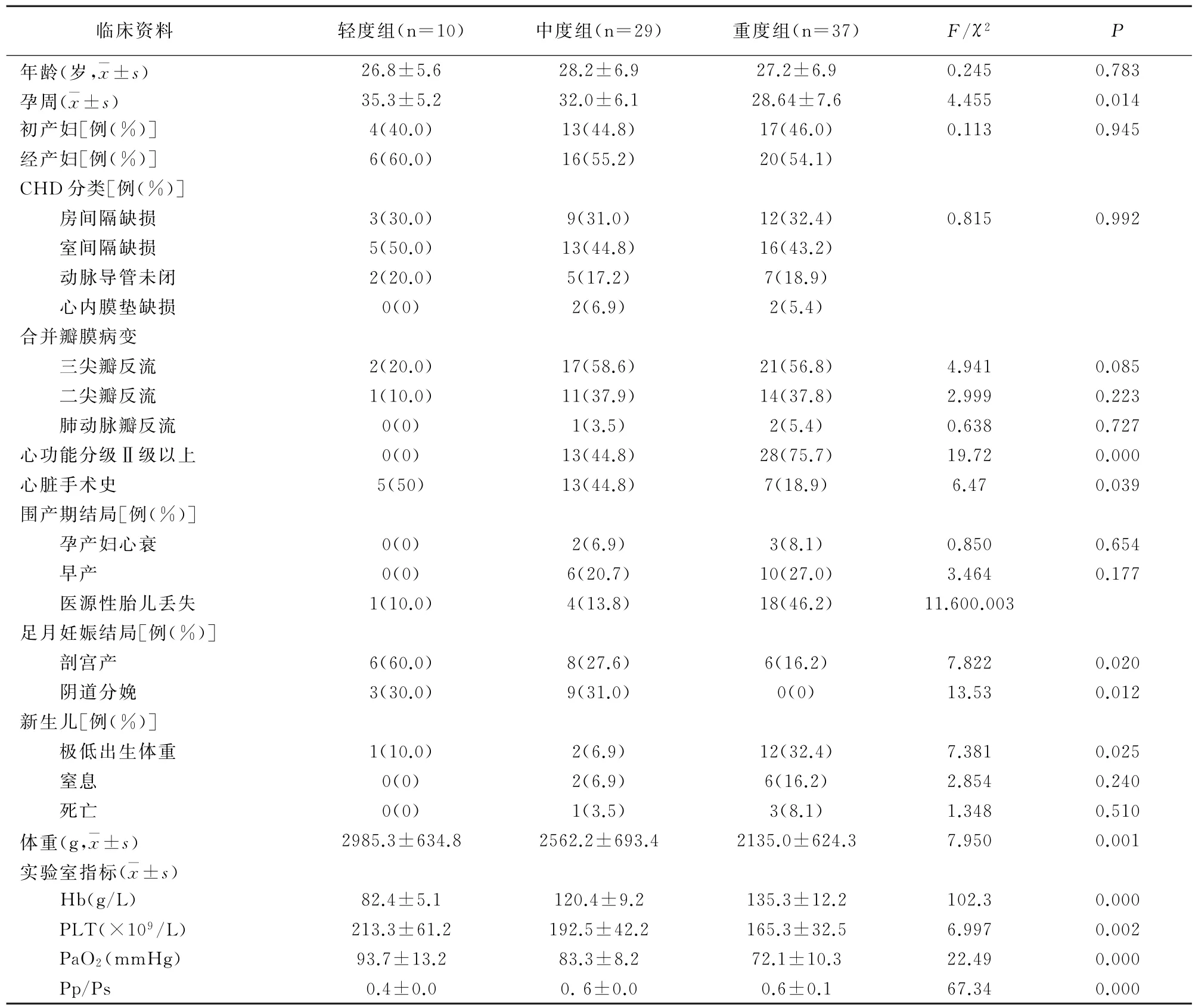
表1 不同PAH组临床孕产情况比较
2.3 随访新生儿生存结局情况
排除9例胎儿或新生儿院内死亡,76例产妇和67例新生儿分别获得随访51例(67.11%)、48例(71.6%),孕产妇和新生儿均存活。6例新生儿存在先天性心脏畸形,其中1例伴消化道畸形。随访51例产妇中,34例孕期心功能恶化者中有11例分娩后出现心功能下降,余23例恢复至孕前水平;17例孕期无心功能恶化者中有9例产后出现心功能恶化。妊娠期心功能恶化率与产后心功能恶化率未存在相关性(χ2=2.015,P=0.156)。孕期PAH 不同程度者产后心功能情况见表2。
2.4 妊娠CHD相关PAH不良妊娠结局的多因素分析
将NYHA心功能分级、肺动脉收缩压、心脏手术史、分娩前PaO2、PLT、Pp/Ps、Hb指标纳入logistic回归分析模型,采用Backward法逐一剔除无关因素。最终肺动脉收缩压、PaO2、NYHA分级是不良妊娠结局的独立危险因素。见表3。
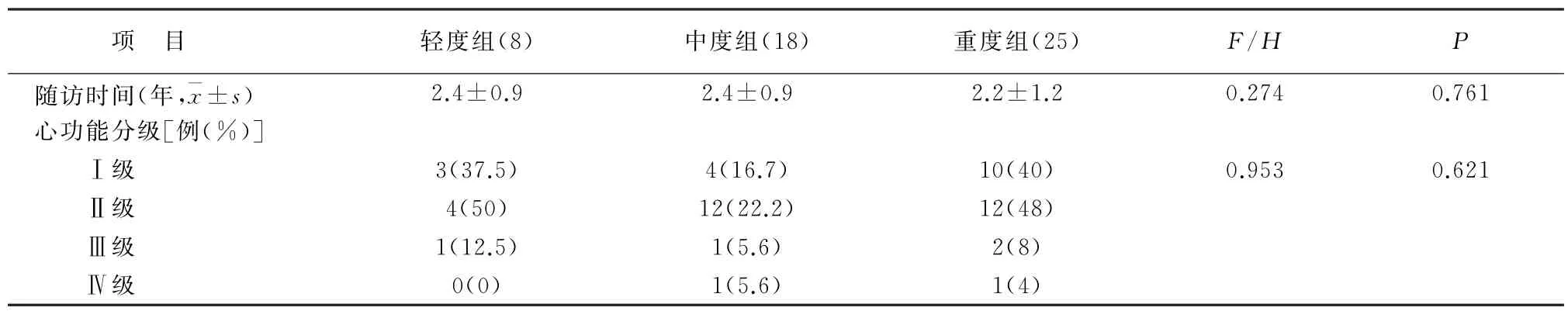
表2 孕期不同PAH组产后心功能分级情况比较
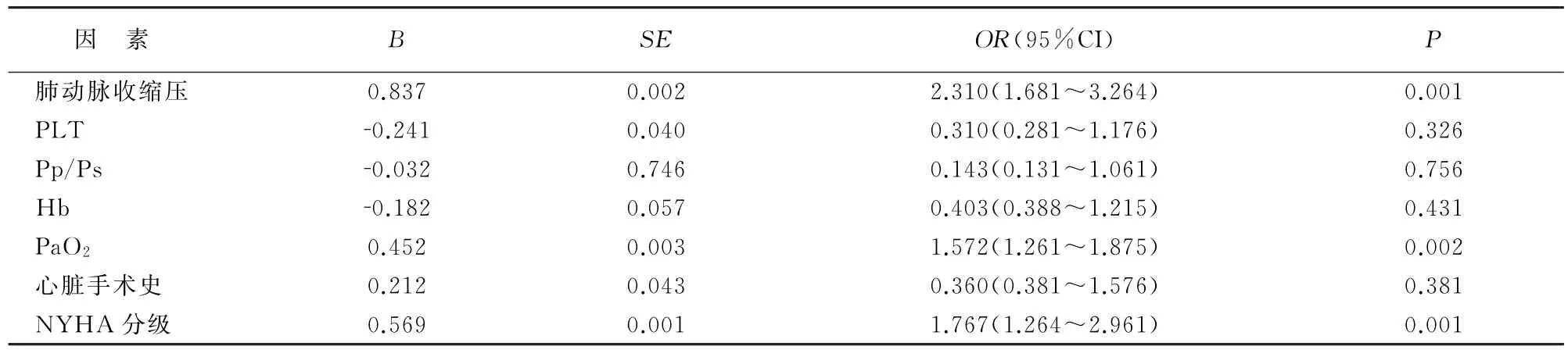
表3 妊娠CHD相关PAH不良妊娠的多因素分析
3 讨论
PAH临床特征以肺小动脉的血管痉挛、内膜增生和重构为主,妊娠晚期可引起一系列心功能衰竭症状,严重时可导致孕产妇死亡[10]。妊娠期合并CHD相关PAH病死率国外报道[10-11]达6.7%~23%,国内为3.4%~14.0%[12-14],严重影响了母婴健康。
本研究分析显示,PAH与妊娠周期、妊娠期NYHA心功能分级、心脏手术史,以及分娩前PaO2、PLT、Pp/Ps、Hb指标密切相关。这与妊娠期PAH的发生机制有关,证实随着妊娠周期的增加,母体血容量增加,肺动脉收缩压增大,导致PAH逐渐加重。妊娠期 NYHA心功能分级、PaO2、PLT、Pp/Ps、Hb是评估孕期PAH的主要指标[14]。范颖[15]对比分析了12例死于妊娠合并CHD相关PAH患者和86例存活的临床资料,结果显示死亡组PaO2低于存活组,且死亡组患者均为心功能分级Ⅲ级以上。本组研究显示死亡患者均为PAH中、重度患者,心功能分级均在Ⅱ级以上。刘永平[9]报道,妊娠合并CHD相关PAH患者中PAH重度患者PaO2、PLT均显著降低,Pp/Ps值显著增高,本文资料也证实了这一结果。
本研究经多因素分析显示,肺动脉收缩压增高是妊娠合并CHD相关PAH患者不良妊娠结局的主要原因,且每增加1个变量就会增加2.310倍的不良结局风险。提示PAH程度与妊娠合并CHD相关PAH患者不良妊娠结局的重要关系。单因素分析中,PAH重度组孕妇的心衰率、医源性胎儿丢失率、早产率、极低出生体重儿比例、新生儿窒息率、新生儿死亡率均最高。欧啟添[6]在其研究中同样认为重度PAH患者是妊娠期不良事件的危险因素。提醒临床应加强对重度PAH孕产妇的治疗和护理,纠正低氧血症,增加心输出量,预防PAH危象,改善氧供,改善患者的预后。
本研究随访产后心功能和PAH评估显示,在孕期出现心功能恶化孕产妇中67.7%的人心功能恢复至孕前水平,而孕期无心功能恶化者52.9%在产后出现心功能恶化,但统计分析未见其有相关性。分析认为:产妇产褥期后总体心功能得到改善,与产后雌孕激素恢复,体循环血量减少等生理性改善有关。
综上,妊娠合并CHD相关PAH对母婴均有较高的风险,PAH程度越重,风险越大。对CHD患者应及时手术纠正,而合并PAH者不建议妊娠,尤其是重度PAH患者。发现妊娠应及时终止;对于坚持继续妊娠者,需在多学科协作密切监护下适时终止妊娠,以减少死亡发生。

