微创经椎间孔腰椎椎体间融合术与传统开放手术的疗效和对多裂肌损伤的对比研究
苏锴 栾继耀 梅伟 张忠民
作者单位:450000 郑州市骨科医院脊柱外科 ( 苏锴、梅伟 );450000 郑州,河南中医药大学 ( 栾继耀 );510630 广州,南方医科大学第三附属医院脊柱外科 ( 张忠民 )
2003 年,Foley 和 Smith 报道了微创经椎间孔腰椎椎体间融合术 ( minimally invasive transforaminal lumbar interbody fusion,MIS-TLIF ),它利用管道牵开系统通过肌间隙入路而达到手术目的[1]。但其在保留腰椎后方附件结构的同时,可能会造成减压的不充分,并且在融合率、并发症发生率以及对椎旁肌的影响等方面尚存有争议[2-6]。与传统开放后路腰椎椎体间融合术 ( posterior lumbar interbody fusion,PLIF ) 相比,微创 TLIF 是否达到了更好的疗效及真正“微创”的目的?近年来,这一问题逐渐引起人们的反思。回顾分析 2014 年 1~12 月,我院收治的110 例患者的临床资料,就此两种术式的临床疗效和对多裂肌的损伤进行对比研究。报告如下。
资料与方法
一、纳入与排除标准
1. 纳入标准:( 1 ) 单节段的腰椎退变性疾病:巨大型腰椎间盘突出症并不稳、腰椎管狭窄症并不稳、腰椎滑脱症;( 2 ) 存在机械性下腰痛和 ( 或 ) 下肢放射痛、麻木、间歇性跛行,保守治疗 6 个月以上无效。
2. 排除标准:( 1 ) 合并脊柱其它疾病 ( 包括结核、肿瘤、感染、后凸或侧凸畸形 );( 2 ) 既往脊柱手术史;( 3 ) 末次随访时已取出内固定物。
二、一般资料
本组共纳入 110 例,开放组 60 例,其中男26 例,女 34 例;年龄 26~77 岁,平均 56 岁;巨大型腰椎间盘突出症合并不稳 16 例,腰椎管狭窄症合并不稳 29 例,腰椎滑脱症 15 例;L4~538 例,L5~S121 例。微创组 50 例,其中男 16 例,女 34 例;年龄 36~87 岁,平均 61 岁;巨大型腰椎间盘突出症合并不稳 14 例,腰椎管狭窄症合并不稳 17 例,腰椎滑脱症 19 例;L4~536 例,L5~S114 例。
三、手术方法
微创组:全麻后,患者取俯卧位。做旁正中切口,长约 3.5~5.0 cm。切开皮肤、皮下组织,切开腰背筋膜,钝性分离多裂肌与最长肌肌间隙,安装Quadrant 系统 ( 美国枢法模公司 ),暴露该侧关节突关节,切除上、下关节突、上位椎体部分椎板,进行减压。处理椎间隙,在椎间隙前方约 1 / 3 和 cage中填塞自体骨 ( 切除的小关节和椎板 ) 和异体骨 ( 上海大鹏公司 ) 的混合骨粒,将 cage 植入椎间隙,植入椎弓根螺钉。取出工作通道,根据症状决定对侧是否行减压,同前法植入对侧螺钉。选择合适长度的钛棒,预弯并连接上、下椎弓根螺钉。术毕放置引流管,逐层缝合,关闭切口。
开放组:麻醉方法及体位同微创组。做后正中切口,长约 5.0~8.0 cm。沿棘突骨膜下剥离椎旁肌,植入双侧椎弓根螺钉,行全椎板切除。选择合适长度钛棒,预弯并连接,予以临时固定。处理椎间隙,在椎间隙前方约 1 / 3 和 cage 中填塞之前切除的自体骨粒,将 cage 植入椎间隙,再次取出之前固定的钛棒,调整长度并加压锁紧。
两组手术均由同一治疗组的医生完成,均使用威高椎弓根螺钉 ( 山东威高公司 ) 和 LDR cage ( 法国LDR 公司 ),均徒手植入钉棒,未使用经皮椎弓根螺钉系统。
四、术后处理
两组术后均预防性使用抗生素 24 h 以及对症治疗。微创组第 2 天拔除引流管,开放组待引流量<50 ml / 天后拔除引流管,拔管后均指导患者行腰背肌功能锻炼,并复查腰椎正侧位 X 线片,明确内固定物位置满意后带腰围或胸腰支具下床活动。
五、观察指标
1. 疗效评价:记录两组手术时间、术中出血量、术后引流量、住院时间、住院费用、并发症发生率、融合率。采用术前与末次随访的疼痛视觉模拟评分 ( visual analogue scale,VAS )、Oswestry 功能障碍指数 ( oswestry disability index,ODI ) 评分、日本骨科协会 ( Japanese orthopaedic association scores,JOA ) 评分评估临床疗效。采用 Mirza 影像学腰椎退变程度评分[7],评估两组退变是否有差异。根据末次随访腰椎正侧位 X 线片,必要时联合腰椎 CT 三维重建,评估内固定物是否有松动、移位。采用Bridwell 标准[8]评价植骨融合情况:I 级,骨块融合重塑完全,骨小梁存在;II 级,骨块完整,骨块重塑不完全,无透亮区;III 级,骨块完整,上方或下方透亮区;IV 级,骨块塌陷、吸收。
2. 多裂肌损伤:共 22 例行 L4~5手术的患者 ( 开放组 12 例;微创组 10 例 ) 在 MRI ( 1.5 T,Philips,荷兰 ) 上进行多裂肌的测量。在矢状位图像上平行病变椎间盘平面将其平分为 3 份 ( 切片厚度 4 mm,层间距 1 mm ),将 T2加权像中间的轴位像纳入研究。末次随访时再次行腰椎 MRI 检查,为了减少融合节段螺钉和钛棒的干扰,取上方的轴位像纳入研究。
图像的存储、传输和测量均采用南方 PACS 系统( 广州南方宜信信息科技有限公司 )。在轴位像上多裂肌周围画闭合曲线得出其横截面积 ( cross-sectional area,CSA ),取同一水平左右两侧 CSA 之和作对比。在同一水平测量多裂肌萎缩分级,将多裂肌萎缩分为 0 ( 正常 )、1 ( 轻度 )、2 ( 中度 )、3 ( 重度 ) 四级。轻度萎缩 ( 1 级 ) 指<10% 的多裂肌被脂肪和纤维组织所取代;中度萎缩 ( 2 级 ) 指 10%~50% 的多裂肌被脂肪和纤维组织所取代;重度萎缩 ( 3 级 ) 指>50% 的多裂肌被脂肪和纤维组织所取代[9]。
所有影像学数据的测量均由未知分组情况的影像科医师和骨科医师,至少间隔 1 周,分别测量3 次取其平均值得出。
六、统计学处理
采用 SPSS 21.0 软件进行统计学分析。计量资料以±s表示,组内比较采用配对样本t检验;组间比较采用两独立样本t检验。计数资料以率或例数表示,组内比较采用两相关样本非参数检验;组间比较采用χ2或两独立样本非参数检验。P<0.05 为差异有统计学意义。
结 果
一、临床疗效
两组患者均随访 20 个月,两组术前一般资料以及各项观察指标之间的差异均无统计学意义 (P>0.05 ),具有可比性。
微创组并发症发生率为 22.00% ( 11 / 50 ),高于开放组的 11.67% ( 7 / 60 ),差异无统计学意义 (χ2=2.128,P=0.145 )。微创组中 29 例行单侧减压,21 例行双侧减压,微创组术中出血量、术后引流量均明显低于开放组,差异有统计学意义 (P<0.01 )。两组手术时间、住院时间及住院费用的差异无统计学意义 (P>0.05 ) ( 表1 )。
两组末次随访的 VAS、ODI 评分均明显低于术前,JOA 评分明显高于术前,差异有统计学意义 (P<0.001 ) ( 表2 )。开放组 ΔVAS ( VAS术前-VAS末次随访) 为 ( 4.49±1.61 ) 分、ΔODI ( ODI术前-ODI末次随访) 为 ( 40.44±20.52 ) %、JOA 改善率[ ( JOA末次随访-JOA术前) / ( 29-JOA术前)×100% ]为 ( 59.73±24.74 ) %,微创组 ΔVAS 为 ( 3.89±2.01 ) 分、ΔODI 为 ( 37.81±23.02 ) %、JOA 改善率为 ( 51.92±36.42 ) %,两组相比差异无统计学意义(P>0.05 )。对于非腰椎间盘突出症,开放组 ΔVAS为 ( 4.32±1.38 ) 分,明显高于微创组的 ( 3.53±1.88 ) 分,差异有统计学意义 (t=2.281,P=0.025 )。其中微创组 15.8% ( 3 / 19 ) 的腰椎滑脱症患者末次随访时仍残存间歇性跛行。末次随访时植骨融合情况:开放组,I 级 49 例,II 级 6 例,III 级3 例,IV 级 2 例;微创组,I 级 42 例,II 级 4 例,III 级 3 例,IV 级 1 例,差异无统计学意义 (Z=-0.315,P=0.753 )。
表1 两组手术相关情况比较 ( ± s )Tab.1 Comparison of surgery-related conditions between the 2 groups (± s )
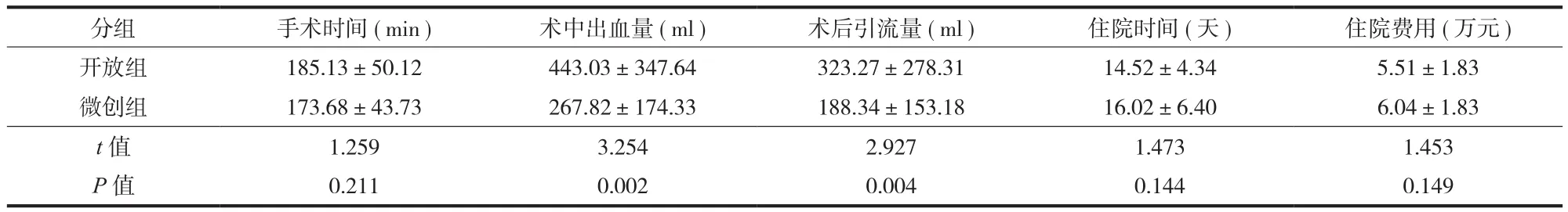
表1 两组手术相关情况比较 ( ± s )Tab.1 Comparison of surgery-related conditions between the 2 groups (± s )
开放组 185.13±50.12 443.03±347.64 323.27±278.31 14.52±4.34 5.51±1.83微创组 173.68±43.73 267.82±174.33 188.34±153.18 16.02±6.40 6.04±1.83 t 值 1.259 3.254 2.927 1.473 1.453 P 值 0.211 0.002 0.004 0.144 0.149
表2 两组评分及多裂肌 CSA 比较 (± s )Tab.2 Comparison of evaluation scores and multifidus CSA between the 2 groups (± s )
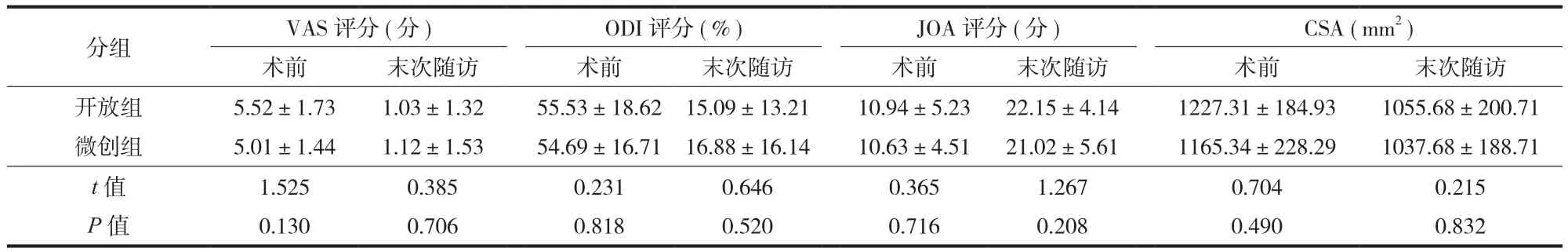
表2 两组评分及多裂肌 CSA 比较 (± s )Tab.2 Comparison of evaluation scores and multifidus CSA between the 2 groups (± s )
注:同组同指标末次随访与术前相比,P<0.001Notice: Comparing the same indicators in the same group preoperatively and at the last follow-up, P < 0.001
开放组 5.52±1.73 1.03±1.32 55.53±18.62 15.09±13.21 10.94±5.23 22.15±4.14 1227.31±184.93 1055.68±200.71微创组 5.01±1.44 1.12±1.53 54.69±16.71 16.88±16.14 10.63±4.51 21.02±5.61 1165.34±228.29 1037.68±188.71 t 值 1.525 0.385 0.231 0.646 0.365 1.267 0.704 0.215 P 值 0.130 0.706 0.818 0.520 0.716 0.208 0.490 0.832
二、多裂肌损伤
随访时间 11~26 个月,平均 17 个月。两组术前多裂肌 CSA 及萎缩分级的差异均无统计学意义(P>0.05 )。两组末次随访 CSA 及萎缩分级均明显低于术前,差异有统计学意义 (P<0.05 ) ( 表2、3 )。开放组 ΔCSA ( CSA术前-CSA末次随访) 为 ( 171.63±93.51 ) mm2,微创组为 ( 127.66±71.43 ) mm2,差异无统计学意义 (t=1.218,P=0.238 )。两组末次随访多裂肌萎缩分级的差异无统计学意义 (P>0.05 )( 表3 )。典型病例见图1、2。
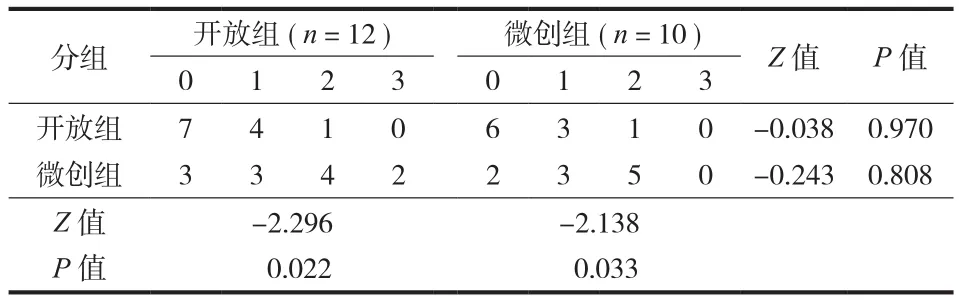
表3 两组多裂肌萎缩分级比较 ( 例 )Tab.3 Comparison of multifidus atrophy grading between the 2 groups ( case )
讨 论
近些年来,微创脊柱外科手术因其具有术中出血少、恢复快、住院时间短等优点,而逐渐受到人们的关注,但同时它具有透视时间长、医疗设备昂贵的缺点[10-11],而这些可能会危害术者的健康和增加患者的花费。经胸腔、腹腔或关节腔的微创手术,均存在潜在的腔隙这一共同特点。然而后路的微创脊柱手术缺少这种类似“钥匙孔”样的解剖学结构,所以其有效性和安全性受到了质疑。微创的脊柱手术缺少三维空间的解剖学暴露,可能会导致定位困难,而术中一旦发生不可预测的并发症,因其操作空间的狭小,处理将变得相对困难[12];同时它还具有技术依赖性高及学习曲线长的缺点[13-14]。
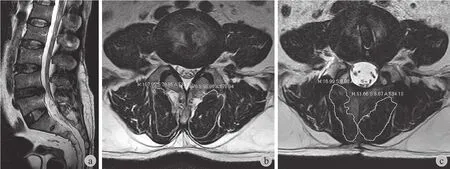
图1 开放组,患者,男,47 岁,腰椎管狭窄症合并不稳 ( L4~5 ),行开放 PLIF a:术前矢状位 MRI 示 L4~5 水平椎管狭窄,椎间盘退变;b:术前 L4~5 水平轴位像示多裂肌 CSA 1215.44 mm2,萎缩分级 0 级;c:术后 21 个月 L4~5水平轴位像示多裂肌 CSA 1012.52 mm2,萎缩分级 1 级Fig.1 PLIF group, male,47 years old, spinal stenosis with instability ( L4-5 ) a:Preoperative sagittal MRI showed L4-5 level spinal stenosis, disc degeneration; b: Preoperative mulitifidus CSA 1215.4 mm2 in the axial position L4-5 level, atrophy grading 0; c: 21 months after surgery, mulitifidus CSA 1012.5 mm2 in the axial position L4-5 level, atrophy grading 1
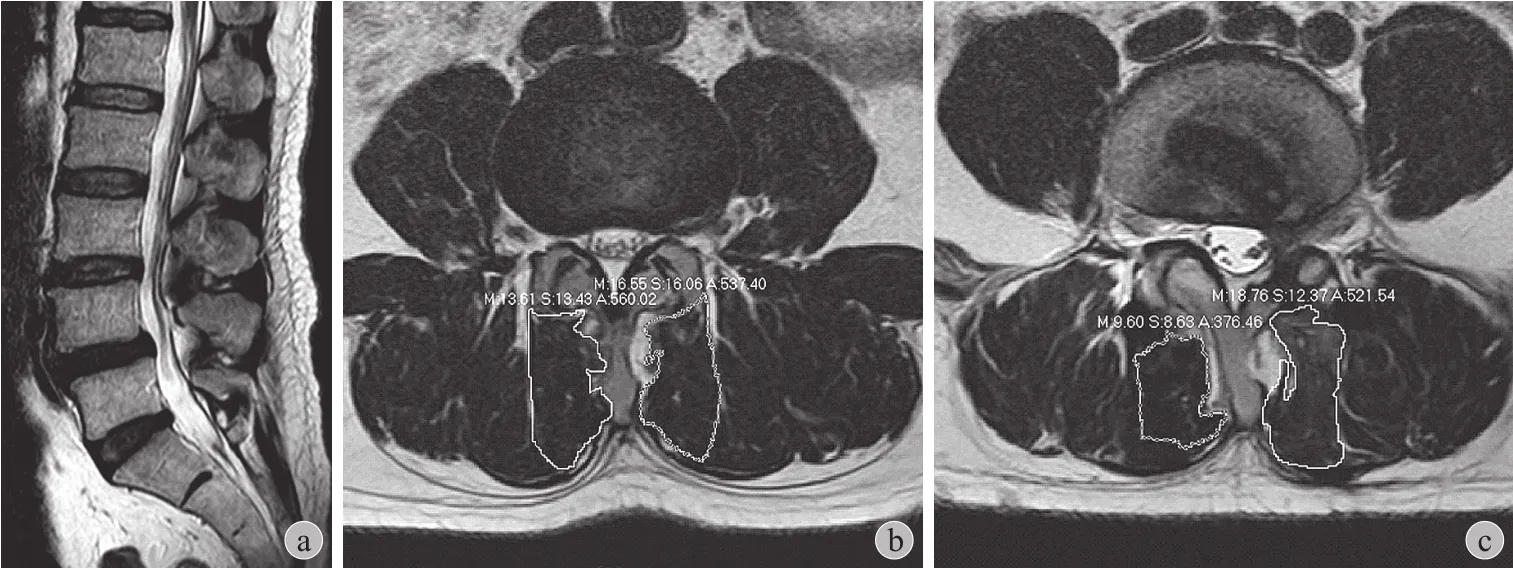
图2 微创组,患者,男,48岁,峡部裂型腰椎滑脱症 ( L4 I° ),行微创 TLIF a:术前矢状位 MRI 示 L4 向前滑脱,椎管狭窄;b:术前 L4~5 水平轴位像多裂肌CSA 1097.42 mm2,萎缩分级0 级;c:术后 23 个月 L4~5水平轴位像示多裂肌 CSA 898.00 mm2,萎缩分级 1 级Fig.2 TLIF group, male, 48 years old, isthmus spondylolisthesis ( L4 I° ) a: Preoperative sagittal MRI showed L4 forward spondylolisthesis, spinal stenosis; b: Preoperative mulitifidus CSA 1097.4 mm2 in the axial position L4-5 level,atrophy grading 0; c: 21 months after surgery, mulitifidus CSA 898.0 mm2 in the axial position L4-5 level, atrophy grading 1
微创 TLIF 的临床疗效并没有明显优于开放手术。Villavicencio 等[3]分析研究了 76 例微创 TLIF和 63 例开放 TLIF 病例,发现开放组具有较高的VAS 改变 ( 5.2 分和 4.1 分 ) 和患者满意度 ( 72.1% 和64.5% ),但两组的差异无统计学意义 (P>0.05 )。Schizas 等[15]总结了 18 例微创 TLIF 和 18 例开放TLIF 病例,发现微创与开放手术在术后疼痛、镇痛药使用、VAS 评分和 ODI 评分方面的差异均无统计学意义 (P>0.05 )。本研究发现对于非腰椎间盘突出症,开放组的 ΔVAS 明显高于微创组 (P=0.025 )。其中微创组有 15.79% ( 3 / 19 ) 腰椎滑脱症患者末次随访时仍残存间歇性跛行,这也许是因为微创 TLIF 在保留脊柱后方附件结构的同时,可能会造成减压的不充分。Dasenbrock 等[16]认为无论采用何种手术方式,减压充分才能有效地治疗患者不适症状。
同时微创手术并发症的发生率较高[3,17-19],这可能与其陡峭的学习曲线有关[17]。另外微创手术的小切口可能会造成减压的不充分,另外在撑开器抵达椎板时,为了给植钉和减压做准备,需要在其表面用电刀烧毁部分附着于关节突和椎板上的多裂肌,这样就使得其手术切口形成了一个底大口小的“火山口”样结构,同时其撑开器持续的撑压,会对皮肤和椎旁肌造成损伤,容易引起椎旁肌的缺血性改变及皮缘的缺血性坏死。开放手术中对于解剖结构的充分暴露,可能更有助于减少并发症的发生率[20]。
在后路腰椎手术中,多裂肌是最容易损伤的椎旁肌,因为它仅由腰神经后支的内侧支支配,且分支间无交通支[21]。术后多裂肌会发生去神经改变和水肿,进而萎缩[22-23]。血清中肌酸激酶 ( creatine kinase,CK ) 浓度的升高可以反映肌肉损伤的严重程度。Arts 等[6]测量了 216 例术前和术后 1 天的CK 浓度的改变,发现两组之间的差异无统计学意义 (P=0.74 )。Adogwa 等[24]发现微创 TLIF 组术后1 天的 CK 峰值为 ( 739±1 002 ) U / L,高于开放组的 ( 387±242 ) U / L,因此微创 TLIF 可能对肌肉的创伤更大。术后多裂肌的损伤,远期随访表现在多裂肌 CSA 的减少和脂肪浸润的增加。笔者发现两组末次随访的 CSA 及萎缩分级均较术前明显减少 (P<0.05 ),说明不管微创 TLIF 还是开放 PLIF 都会明显损伤多裂肌。但是两组多裂肌 ΔCSA 及末次随访萎缩分级的差异均无统计学意义 (P>0.05 ),因此微创TLIF 与开放 PLIF 相比并没有明显减少对多裂肌的损伤。
Kawaguchi 等[25]认为术中牵拉力的大小以及手术时间均会影响腰椎术后椎旁肌的损伤程度,牵拉 1 h 放松 5 min,可以明显减少对椎旁肌的损伤。Gejo 等[26]发现,腰椎术后椎旁肌的损伤程度受牵拉时间的影响,牵拉时间>2 h,椎旁肌内的毛细血管内的血流量会显著减少,可引起肌肉的缺血性变化。微创脊柱手术的小切口和术区,加上其较长的持续牵拉时间,虽然可以减少术中出血量,但会引起毛细血管内皮细胞的功能障碍,反而会对椎旁肌造成更大的创伤[25]。另外,微创 TLIF 不切除棘突,其撑开器将多裂肌向棘突挤压,使其处在套管与棘突之间,承受一个挤压力和反挤压力。并且,撑开器入路并没有真正地达到肌间隙入路,而可能只是钝性地分开多裂肌纤维,仅保留了多裂肌在椎板和棘突上的小部分附着点。因此,经多裂肌肌间隙入路的微创脊柱手术可能并未真正地减少对多裂肌的损伤。
本研究表明,微创 TLIF 能明显减少术中出血量及术后引流量,但其临床疗效和对多裂肌的损伤并没有明显优于开放 PLIF。对于非腰椎间盘突出症,开放 PLIF 的 ΔVAS 更高,说明其临床疗效可能更好。本研究随访时间较短,两组手术由不同的术者完成,且减压范围不同,可能造成一定的误差;样本量有限,仍需要大样本的随机对照研究。

