聚乙二醇化重组人粒细胞刺激因子对骨肉瘤化疗患者行预防性中性粒细胞治疗的多中心临床研究
黄真 鱼锋 王涛 张清 郝林 杨沛 胡宇贤 牛晓辉
作者单位:100035 北京积水潭医院骨肿瘤科 ( 黄真、鱼锋、王涛、张清、郝林、牛晓辉 );101200 北京,平谷岳协医院骨肿瘤科 ( 杨沛 );100038 北京水利医院骨肿瘤科 ( 胡宇贤 )
中性粒细胞 ( neutrophilicgranulocyte,ANC ) 减少是大多数化疗中最常见、也是最严重的一种并发症。ANC 减少的程度、持续时间与感染甚至死亡风险直接相关,严重影响了化疗药物的剂量强度( relative dose intensity ) 与周期[1],致使临床上不得不降低药物剂量、延迟治疗时间或更改方案,最终难以达到预期的疗效,因此,预防或治疗 ANC 减少症是保证足剂量化疗或剂量密集化疗顺利进行的根本。此外,ANC 减少也可增加患者感染的危险性,当 ANC<1500 / mm3时,感染危险性增加;当ANC<500 / mm3时,严重感染危险性明显增加;当ANC<100 / mm3时,10%~20% 甚至可能更多的患者会发生菌血症,严重威胁着患者,尤其可危及有假体等内植物的患者的肢体安全。此外,研究显示约 25%~40% 接受常规化疗的患者会出现中性粒细胞减少性发热 ( febrile neutropaenia,FN ),对于临床工作来说,FN 更易出现复杂感染、延长住院时间、甚至引发死亡[2];而骨肉瘤化疗药物均为大剂量,骨髓抑制发生率更高些,III+IV 度骨髓抑制的发生率可达 25.93%~63.6%,ANC 减少发生率更高达 81.48%~90.18%,粒细胞减少性发热率也约为11.11% ( 6 / 54 )[3-12]。因此,在骨肉瘤化疗中,如何治疗与预防粒细胞减少尤其受到临床关注。
重组人粒细胞集落刺激因子 ( rhG-CSF ) 已广泛应用于临床,然而它半衰期短,一个化疗周期中需要连续多日给药,患者痛苦增加、依从性欠佳。而新型的长效 rhG-CSF,即聚乙二醇化重组人粒细胞集落刺激因子 ( PEG-rhG-CSF ),药动学与药效学上都具有不同于常规 rhG-CSF 的特点 ( 图1 ),在一个化疗周期中一次给药的升白细胞作用可维持数天与rhG-CSF 多次给药的效果相仿。因此,为评价 PEG-rhG-CSF 在接受化疗的骨肉瘤患者中预防 ANC 减少的有效性和安全性,笔者设计了一项多中心、非随机、对照临床研究。
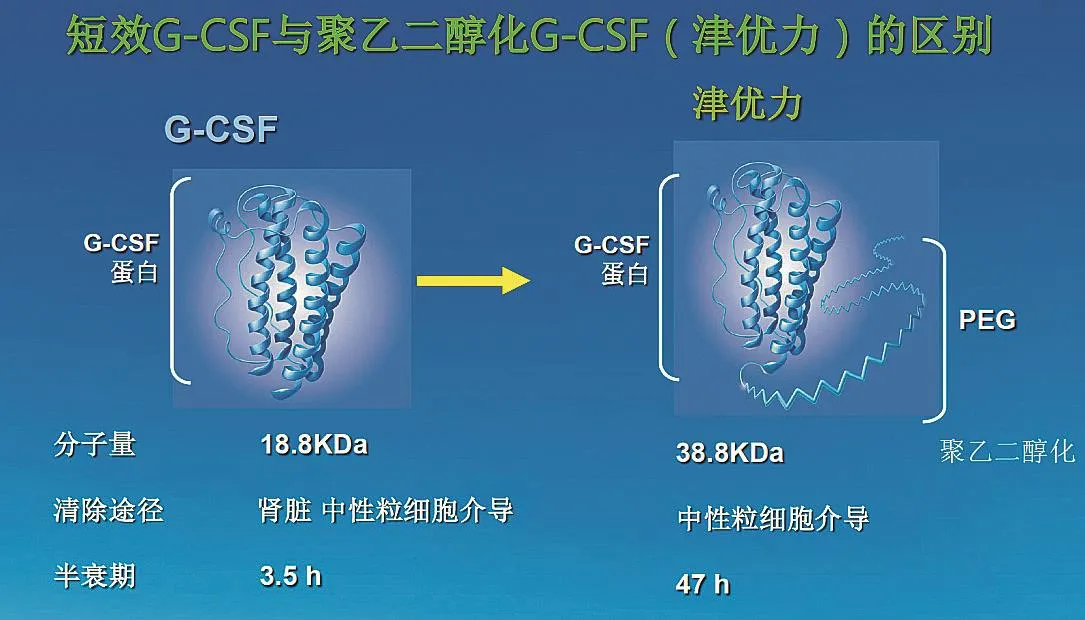
图1 短效 G-CSF 与聚乙二醇化 G-CSF 的区别Fig.1 Differences between short-effect G-CSF and polyethylene Glycol G-CSF
资料与方法
一、纳入与排除标准
1. 纳入标准:( 1 ) 经组织病理学确诊的需要化疗的骨肉瘤者;( 2 ) 年龄 ≥ 18 岁者;( 3 ) 体力状况( KPS ) 评分 ≥ 70 分者;( 4 ) 预计生存期 3 个月以上者;( 5 ) 无明显血液系统疾病征象,入组前 ANC ≥1.5×109/ L,血小板计数 ≥ 80×109/ L,Hb ≥ 80 g /L,WBC ≥ 4.0×109/ L,且无出血倾向者;( 6 ) 签署知情同意书的患者或法定代理人者。
2. 排除标准:( 1 ) 心电图检查明显异常者;( 2 )肝功能检查总胆红素 ( TBIL )、谷丙转氨酶 ( ALT )、谷草转氨酶 ( AST ) 均>2.5 倍正常值上限者;若由于肝转移所致,上述指标>5 倍正常值上限者;( 3 )肾功能检查:血清肌酐 ( Cr )>1.5 倍正常值上限者;( 4 ) 对本品或其它基因工程大肠杆菌来源的生物制品过敏者;( 5 ) 患有精神或神经系统疾患,不能配合者。
本研究选自 2014 年 7 月至 2015 年 1 月,于北京积水潭医院、北京水利医院、平谷岳协医院 3 家医院骨肿瘤科中就诊的骨肉瘤化疗患者。根据纳入与排除标准,本研究共纳入 67 例。
二、研究方案
1. 非随机分成试验组和对照组两组:( 1 ) 试验组 ( PEG-rhG -CSF 组 ):在每个化疗周期,最后一个化疗药物使用结束后 24 h 皮下注射 PEG-rhG-CSF ( 生产厂家:石药集团的津优力 ),体重 ≥45 kg 者给予 6 mg / 次,<45 kg 者给予 3 mg / 次,每个化疗周期使用一次,然后密切监测血常规;( 2 ) 对照组:不预防性使用任何 rhG-CSF,密切监测血常规,当化验提示出现 ANC 减少时 (<4×109/ L,正常值:4~10×109/ L ) 开始应用 rhG-CSF( 生产厂家:齐鲁制药的瑞白 ),每日 1 次,每次200 μg,直至白细胞 ( WBC ) ≥ 4.0×109/ L。
2. 化疗方案选择 CSCO 肉瘤专家委员会共识推荐[13]的 MTX-IFO-ADR-DDP 多药联合方案 ( 图2 )。
三、数据收集与试验流程
1. 数据采集包括主要的临床、病理数据。有效性分析的数据包括,每个化疗周期的化疗前后血常规 ( 化疗后每 3 天监测 1 次,如发生 III-IV 度 ANC则每日监测 1 次血常规 ),化疗前肝肾功能、电解质、胸 X 线片、心电图,并观察各种化疗期间及用药后的药物不良反应。
2. 流程图 ( 表1 )
四、评价指标
1. 有效性分析:( 1 ) III 度 ( ANC<1×109/ L ) 及IV 度 ( ANC<0.5×109/ L ) ANC 减少的发生率和持续时间;( 2 ) 粒细胞缺乏性发热的发生率;( 3 ) 短效重组人粒细胞刺激因子 ( rhG-CSF ) 的使用天数、使用剂量。
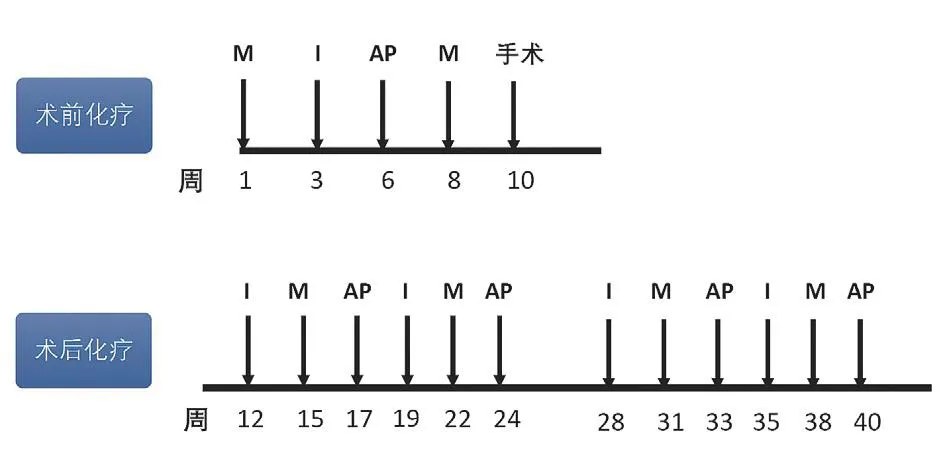
图2 骨肉瘤化疗给药方案计划Fig.2 Chemotherapy plan for ostesarcoma
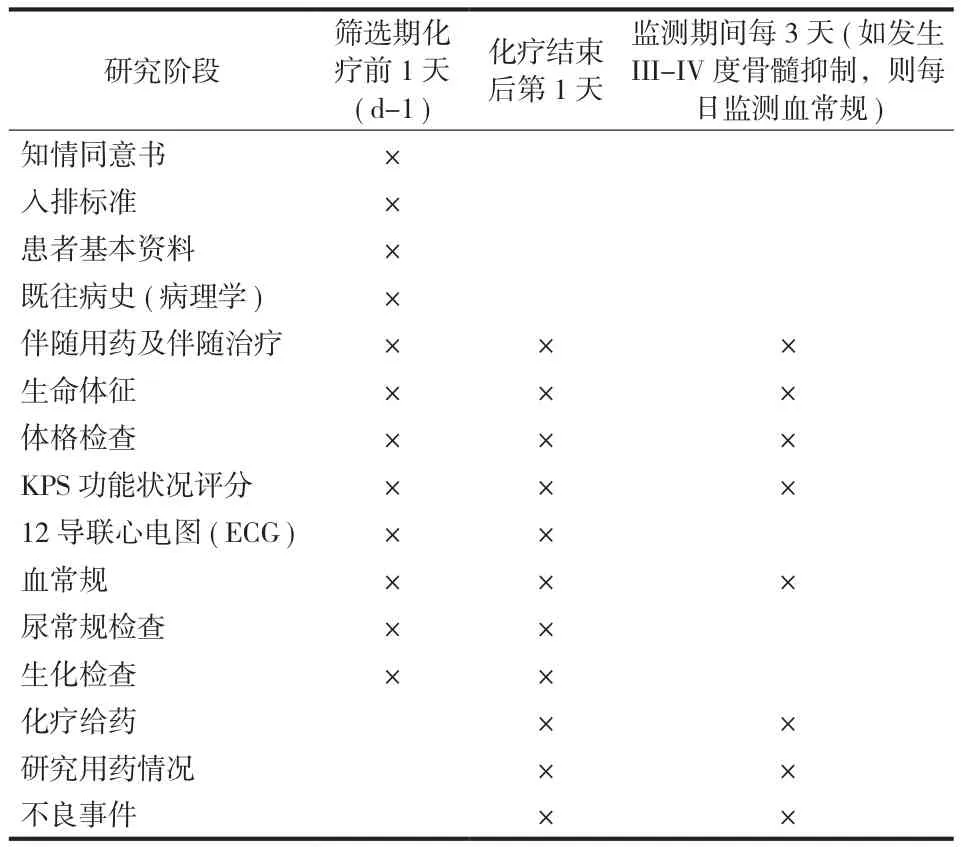
表1 流程图Tab.1 Flow chart
2. 安全性:不良反应发生率。
五、统计学处理
数据统计分析采用 SPSS 18.0 软件。包括独立样本t检验,χ2检验,Fisher 精确检验,P<0.05 表示差异有统计学意义。
结 果
一、一般情况
两组患者基本资料匹配,在性别、年龄、身高、体重、化疗方案上差异无统计学意义 (P值分别为 0.2456、0.0093、0.9708、0.2728、0.6808 )。
二、有效性分析
1. ( 3°~4° ) ANC 减少发生率及持续时间:试验组、对照组分别为 33.33% 和 65.71% (P=0.0114 )( 表1 )。将不同方案间进行亚组分析提示 IFO 化疗的患者两组 ( 3°~4° ) ANC 发生率分别为 53.33% 和68.75% (P=0.776 );DDP+ADR 化疗的患者两组( 3°~4° ) ANC 发生率分别为 16.67% 和 63.64% (P=0.1312 );大剂量 MTX 化疗的患者两组 ( 3°~4° )ANC 发生率分别为 0.00% 和 62.5% (P=0.0310 )。整体上试验组显著降低了 ( 3°~4° ) ANC 减少的总发生率,尤其以大剂量 MTX 化疗方案时预防效果最为显著 ( 表2、3,图3 )。
试验组较对照组 ( 3°~4° ) ANC 减少持续时间短 ( 3 天vs.4 天 ),但二者差异无统计学意义 (P=0.6800 )。亚组分析显示,三种不同化疗方案 ( 3°~4° ) ANC 减少持续时间显示,差异均无统计学意义(P=0.776、0.2606、0.3656 )。
2. FN 的发生率:本研究中,对照组 1 例发生 FN ( 1 / 35,2.86% ),试验组无 FN 发生 ( 0 / 7,0% ),两组比较,差异无统计学意义 (P=1.000 )。
3. 短效 G-CSF 的使用:试验组短效 G-CSF 的中位使用天数为 3 ( 2~5 ) 天,对照组短效 G-CSF 的中位使用天数为 9 ( 4~16 ) 天,试验组比对照组应用短效 G-CSF 的天数总体要短。
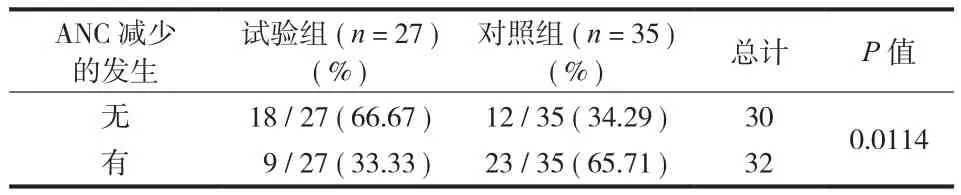
表2 ( 3°~4° ) ANC 减少的发生率比较Tab.2 Comparison of the incidence of 3° - 4° ANC
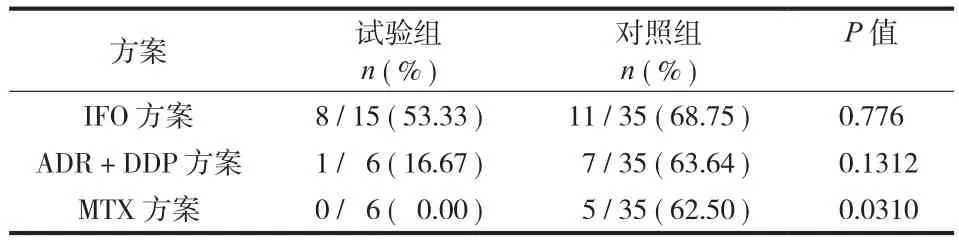
表3 不同方案间 ( 3°~4° ) ANC 减少的发生率比较Tab.3 Comparison of the incidence of 3° - 4° ANC in different regimens
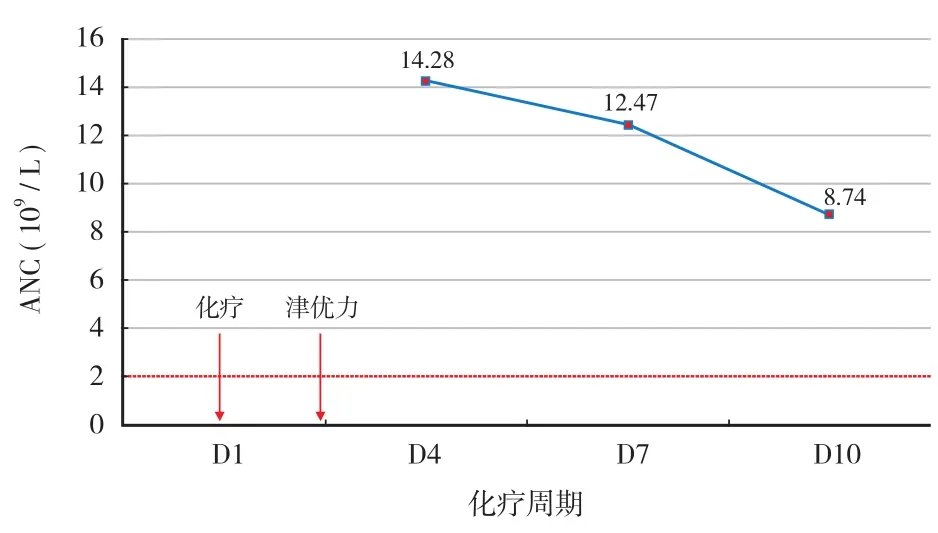
图3 MTX 方案化疗患者使用 PEG-GCSF 期间患者 ANC 变化趋势Fig.3 Granulocyte change in patients with MTX chemotherapy when using PEG-GCSF
三、安全性分析
本临床观察中,试验组未出现有记录的骨关节痛等不良反应发生,对照组记录有 1 例出现中度骨关节痛,未观察到其它不良反应,使用非甾体类抗炎药后患者症状缓解。
讨 论
骨与软组织肉瘤患者的大剂量化疗中,最常见的不良反应为骨髓抑制,其中以粒细胞减少最为多见。指南指出,对于接受高 FN 风险化疗方案的患者,无论治疗目的是治愈、延长生存时间或是改善疾病相关症状,均建议其预防性使用 G-CSF ( CSCO证据级别为 1A )[14]。对于接受中度 FN 风险化疗方案的患者,须评估患者自身风险因素 FN 发生风险的因素中,若患者满足任意一条引起风险系数增加的因素时,建议预防性使用 G-CSF。骨肉瘤化疗均为中重度 FN 化疗风险,临床上基本每个患者在不同阶段都需要使用 G-CSF,尤其对预防升白上,既往应用为每日注射短效生白药物,久而久之,患者的依从性和耐受性均减弱。此外,保证剂量强度可提高骨肉瘤化疗效果,Bramwell 等[15]将 98 例骨肉瘤随机分为两组,两组间剂量强度下降了 44.4%,且给药亦相对延迟,结果发现 5 年生存率分别是 64% 和51%;无独有偶,Uchida 等[16]通过对 67 例骨肉瘤5 年随访发现药物剂量强度对骨肉瘤预后的影响比加入新药的影响要大。因此,预防使用升白药物保证骨肉瘤大剂量化疗顺利进行,意义重大。
PEG-rhG-CSF 与 rhG-CSF 疗效相当,且应用方便,已有文献报道在接受 TAC 或 TA 方案化疗的乳腺癌及接受多西他赛联合卡铂的非小细胞肺癌患者中,预防性使用 PEG-rhG-CSF 100 μg / kg 组、PEG-rhG-CSF 6 mg 和 rhG-CSF 5 μg / kg 组的 3°~4°ANC 减少症的发生率和持续时间、FN 及不良反应发生率的差异均无统计学意义 (P=0.935 )[17]。PEG-rhG-CSF 在其它肿瘤中早已开始应用,然在骨肉瘤化疗中应用情况尚无报道,在此种环境中,本临床观察到预防性使用 PEG-rhG-CSF 在骨肉瘤化疗中安全可耐受,其可显著降低 3°~4° ANC 减少的发生率,在缩短 3°~4° ANC 减少的持续时间、预防性使用 PEG-rhG-CSF 可降低 FN 的发生率,保证化疗安全进行方面有一定优势,从而可作为 PEG-rhG-CSF在骨肉瘤应用情况的有益补充。另一方面,在临床实践中由于患者依从性差、医师意愿或非工作时间用药不便等原因,rhG-CSF 的规范使用往往难以实现,聚乙二醇化 G-CSF 是在短效 G-CSF 蛋白 N 末端定点交联 20 Kda 的聚乙二醇形成,结构变化之后,药物的分子量增大、清除途径改变、肾脏清除降低,半衰期由 3.5 h 到 47 h,因此 PEG-rhG-CSF每个化疗周期只需要使用一次,相比较短效只需1 日注射,注射后如仍出现较严重骨髓抑制时补充短效 G-CSF 的时间也较短,临床使用更容易为患者接受,有一定的临床推广价值。
本研究的局限性:样本量小,因条件所限无法进行随机分组,同时化疗方案为多药序贯联合化疗。另外,PEG-rhG-CSF 用的是标准剂量 ( 6 mg>45 kg 者,3 mg<45 kg 者 ),这些因素均有可能使得部分研究结论无法得出差异有统计学意义,但从中可看出 PEG-rhG-CSF 在骨肉瘤化疗中具有一定的优势,值得更进一步深入研究确认 PEG-rhG-CSF 最佳有效剂量和最优化给药时间及儿童患者中应用价值等。

