树脂DX吸附ADN的热力学和动力学研究
潘永飞,汪 伟,汪营磊,闫峥峰,赵宝东,姬月萍
(西安近代化学研究所,陕西 西安 710065)
引 言
二硝酰胺铵(ADN)是一种新型高能氧化剂,具有能量特性高、特征信号低和绿色环保等优点,被认为是下一代推进剂的候选氧化剂之一,广泛应用于高能、无烟、低特征信号的固体火箭推进剂[1-4]。但ADN的吸潮性阻碍其实际应用。研究表明[5-6],若ADN的纯度大于99.5%,吸潮性显著降低。因此,建立一种分离纯化ADN的方法十分关键。
目前,ADN主要采用混酸法合成,但该法合成过程会产生大量副产物硝酸铵和硫酸铵。因此,必须建立一种经济高效的分离纯化手段[7-8]。国外关于ADN的分离方法研究,大多申请了专利保护或未公开报道,而国内分离纯化ADN最普遍的方法是活性炭吸附法,该方法虽然可以从ADN溶液中分离出ADN,但分离效率低,且分离产生废水量大。本项目组通过前期研究发现[9],采用活性炭吸附法,每生产1kg的ADN,需要2~3个工作日,且会产生500kg的工业废水。因此,本研究选择了一种选择性好、吸附体积大、吸附速度快、易于解吸附、物理化学性能稳定的树脂DX作吸附剂,研究其对ADN的吸附性能及ADN在树脂DX上的吸附热力学和动力学,以期为优化ADN分离纯化工艺提供理论和实验依据。
1 实 验
1.1 试剂与仪器
树脂DX,工业品,沧州宝恩吸附材料科技有限公司; ADN,纯度≥98%,西安近代化学研究所;硝酸铵(AN),分析纯,斯百全化学(上海)有限公司;硫酸铵(AS),分析纯,广州卡芬生物科技有限公司。
LC-10A 高效液相色谱仪,日本岛津公司;UV-1800型紫外可见分光光度计,上海仪电科学仪器股份有限公司;AY-120精密电子天平,日本岛津公司。
1.2 样品溶液制备
准确称取50.0mg ADN标准品,精确至0.0001g,用2.0mL 蒸馏水溶解,并定容至5.0mL 容量瓶中,冷冻保存。分别取0.5、1.0mL上述标准溶液至1.0、10.0mL容量瓶中,用蒸馏水定容,混匀后配制成质量浓度为5000、1000、10000mg/L的系列标准溶液;分别取1000mg/L的标准溶液10、50、100、500μL至1.0mL的容量瓶中,用蒸馏水定容。混匀后配置成质量浓度为10、50、100、500mg/L的系列标准溶液。
准确称取50.0mg AN标准品,精确至 0.0001g,用2.0mL 蒸馏水溶解,并定容至 5.0mL 容量瓶中,冷冻保存。分别取100、500、800μL上述标准溶液至1.0mL容量瓶中,用蒸馏水定容至1mL,混匀后配制成质量浓度为1000、5000、8000、10000mg/L的系列标准溶液;再准确量取1000mg/L的ADN标准溶液100μL,用蒸馏水定容至1.0mL容量瓶中,制成100mg/mL标准溶液。
1.3 实验方法
利用反向高效液相色谱法测定ADN母液中ADN与AN的含量。对以上标准品溶液分别取0.5mL,进行高效液相色谱(HPLC)分析,进样1μL。以峰面积Y对质量浓度C(在标准曲线方程中对应为X)进行线性回归,分析获得标准曲线。
ADN标准曲线:Y=84.17997+1.75319X,R2=0.99984
AN标准曲线:Y=129.51554+0.46575X,R2=0.99941。
1.4 吸附热力学测定
(1)取100mL烧杯5个,分别加入ADN原液、稀释2倍、5倍、10倍ADN原液20mL,分别记为ADN原、ADN/2、ADN/5、ADN/10,原液质量浓度为30.15532×103mg/L;取DX树脂5mL(1.3g),加入已备好的ADN母液中,在恒定温度28、40、50℃下分别充分搅拌10min,随后静置使其充分吸附,并开始计时。
(2)在充分吸附10、20、30、60、90、120min后,分别取烧杯中ADN母液进行HPLC分析,利用标准曲线法计算其中ADN的质量浓度,重复3次求平均值。温度T下树脂平衡吸附量qe按公式(1)计算:
(1)
式中:qe为平衡吸附量,mg/g;c0为吸附前溶液的质量浓度,mg/mL;ce为吸附平衡时溶液的质量浓度,mg/mL;VL为溶液的体积,mL;m为树脂质量,g。
1.5 吸附动力学测定
准确称取5mL DX树脂置于100mL烧杯中,加入稀释10倍的10mL ADN母液,质量浓度为3015.53mg/L,室温下充分搅拌10min。随后静置使其充分吸附,并开始计时。在充分吸附10、20、30、60、90、120min后,分别取烧杯中ADN母液进行HPLC分析,检测ADN质量浓度的变化,计算吸附量,重复3次求平均值。t时刻树脂上ADN的吸附量(qt)按公式(2)计算:
(2)
式中:qt为t时刻的吸附量,mg/g;c0为吸附前溶液的质量浓度,mg/mL;ct为t时刻溶液的质量浓度,mg/mL;VL为溶液的体积,mL;m为树脂质量,g。
2 结果与讨论
2.1 ADN母液主要化学成分含量分析
用大肚移液管准确量取1.0mL的ADN母液,用蒸馏水定容至10.0mL的容量瓶中,将ADN母液稀释10倍,取0.5mL,进样1μL,进行HPLC分析,得到ADN与AN的峰面积,利用标准曲线计算ADN母液中ADN和AN的质量浓度,分别为30.15532×103和275.03907×103mg/L。
取1mL ADN母液烘干,计算固体含量,平行测定4组,得到ADN母液的固体质量浓度为368.20000×103mg/L。根据母液中的固体、ADN及AN的质量浓度,得到硫酸铵AS的质量浓度约为63.00561×103mg/L。
2.2 吸附热力学研究
2.2.1 吸附等温线
分别在温度28、40、50℃下测定DX树脂在不同质量浓度ADN溶液中的吸附量,得到吸附等温线,结果见图1。
由图1可知,随着样品溶液质量浓度的增加,吸附量也在增加,在28~50℃范围内吸附量随着温度的升高而降低。
2.2.2 吸附等温方程
当吸附剂在液相中进行吸附时,实质上是溶剂与被吸附组分对吸附剂的竞争,当溶剂的吸附作用可以忽略时,则吸附体系可以按单组分吸附来处理。Langmuir和Freundlich吸附等温线模型是吸
附分离研究中最常用的2种吸附等温线模型[10-12]。其中,Langmuir模型是基于吸附剂的表面只能发生单分子层吸附的假设提出的,其液相吸附表达式为:
(3)
由式(3)变换为:
(4)
式中:qm为饱和吸附量,mg/g;qe为平衡吸附量,mg/g;KL为Langmuir等温方程常数;ce为吸附平衡时溶液的质量浓度,mg/mL。
而Freundlich模型描述的也是单分子层吸附,但这种模型考虑了实际固体表面的非均一性,以及吸附剂表面覆盖程度的不同对吸附热的影响,提供了一种单组分吸附平衡的经验描述:
qe=KFc1/n
(5)
由式(5)变换为:
lgqe=lgKF+(1/n)lgce
(6)
式中:qe为平衡吸附量,mg/g;KF,n为Freundlich等温方程常数;ce为吸附平衡时溶液的质量浓度,mg/mL。
分别采用Langmuir、Freundlich吸附等温线模型拟合树脂DX对ADN的吸附过程,得到的方程参数见表1,吸附数据拟合结果见图2。
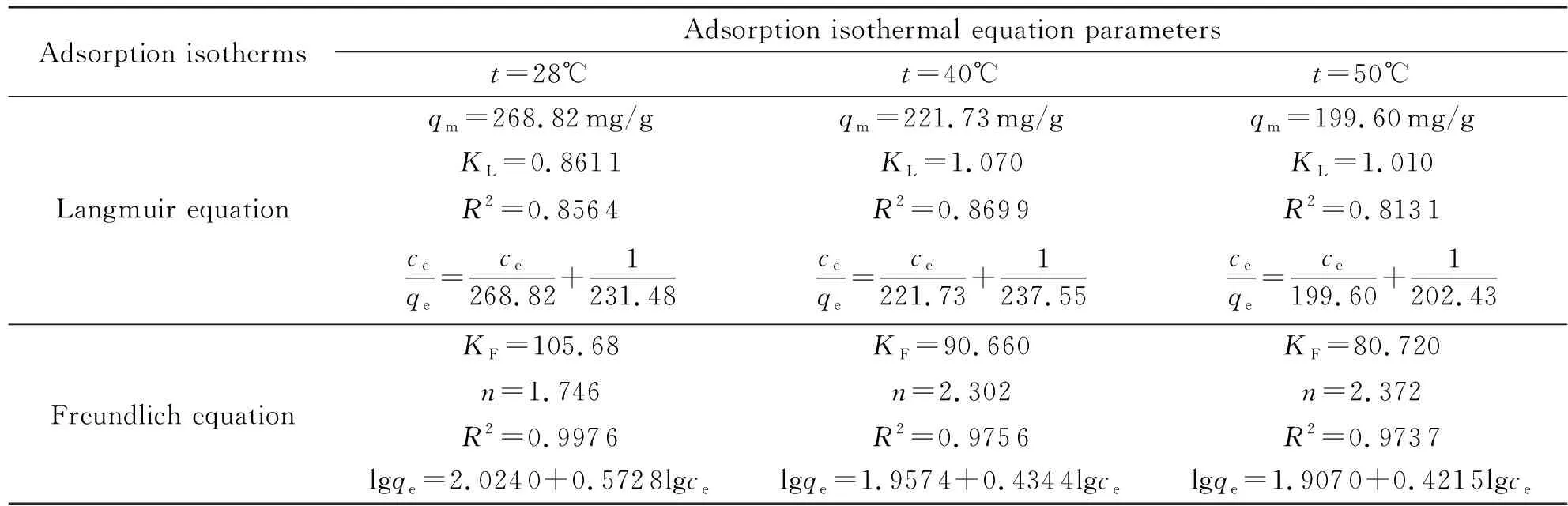
表1 不同温度下的吸附等温方程参数
由表1和图2可知,Freundlich方程比Langmuir方程能更好地描述DX树脂在溶液中对ADN的吸附过程,Langmuir模型一般适用于单分子层吸附,而Freundlich模型可适用于不均匀表面的多分子层吸附。吸附剂DX是多孔吸附材料,ADN不仅会吸附在树脂表面,还可能进入材料内部空隙,从而形成多分子层吸附。所以,Freundlich方程更适用于本吸附系统。平衡吸附系数KF表示吸附量的相对大小,该数值随温度升高而降低,结合图2(b)可知,28℃对该吸附过程更为有利。Freundlich方程中的n值是吸附剂表面非理想性的指标。一般情况下,n>1为优惠吸附,吸附较易发生;n=1为线性吸附;n<1为非优惠吸附,吸附几乎无法发生。本实验中,各条件下的吸附n值都是大于1的,即为优惠吸附,说明DX是ADN的良好吸附剂。用 Freundlich方程拟合得到的等温吸附曲线见图3。由图3可知,树脂DX对ADN有很好的吸附效果,表现为随溶液中ADN含量的升高,吸附量不断升高。
2.2.3 吸附热力学参数
树脂DX吸附ADN的过程中,吸附焓变与吸附量有密切关系,当吸附量固定在一个定值时,所推导出的焓变称为等量吸附焓变。吸附过程的吸附焓变ΔH、熵变ΔS和自由能变ΔG可按下述公式计算[13-15]:
(7)
ΔS=(ΔH-ΔG)/T
(8)
(9)
式中:ce为吸附平衡时溶液的质量浓度,mg/mL;K0为Claperyron-Clausius常数。
根据公式(7),以lnce对1/T作图,见图4。根据直线斜率求得ΔH的值,然后分别由公式(8)和(9)计算得ΔS和ΔG的值,计算结果见表2。
从表2可知,在28~50℃范围内,ADN在DX上的吸附吉布斯自由能ΔG始终为负值,而吸附熵变ΔS均为正值,这表明吸附过程可自发进行。不同吸附量下的吸附焓变ΔH均大于零,这表明ADN在DX上的吸附为吸热过程。低温有利于反应进行,说明整个吸附过程不是一个完全的物理吸附,而是在物理吸附的同时伴有化学吸附过程。ADN是离子化合物,同时DX表面有一定的离子,所以,发生化学吸附是DX树脂表面与ADN分子共同作用的结果。
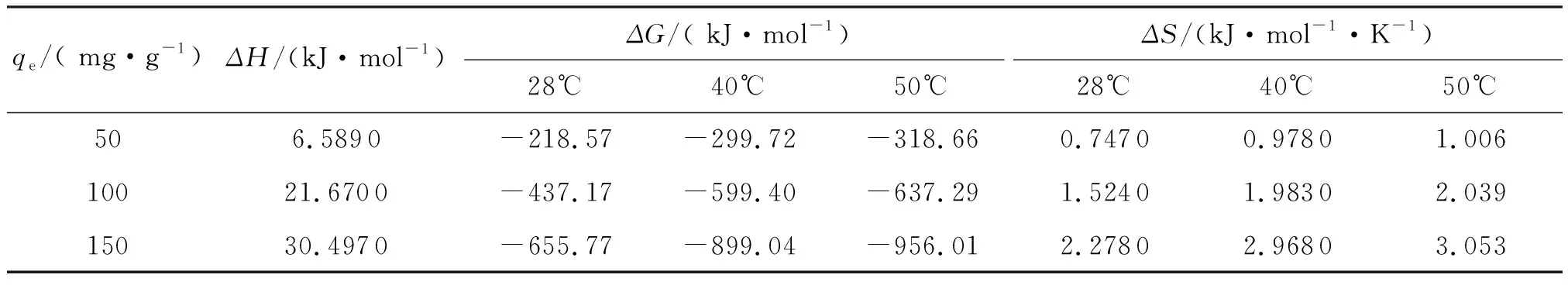
表2 ADN在DX上吸附过程的热力学参数
2.3 吸附动力学研究
为了分析不同温度下的吸附速率情况,分别利用拟一级和拟二级动力学模型分析树脂DX对ADN的吸附过程[16]。
拟一级动力学方程为:
(10)
拟二级动力学方程为:
(11)
式中:qt为t时刻的吸附量,mg/g;qe为平衡吸附量,mg/g;k为吸附速率常数。
根据计算结果,拟二级动力学方程能更好地描述DX树脂对ADN的吸附动力学行为 (R2>0.99),其中k=4.39×10-2min-1,qe=23.425mg/g,代入式(11)得到拟二级吸附动力学方程如下:
(12)
吸附量随时间的变化以及拟合结果见图5。
由图5可知,拟二级吸附动力学模型能较好地描述DX对ADN的吸附过程。在树脂吸附前期,吸附速率相对较大,随着吸附的进行,吸附速率逐渐降低,吸附过程可以分为3个阶段[17]:第一阶段,0~30min,吸附量迅速增大,说明树脂上有大量的吸附位点;第二阶段,30~60min,吸附量增长变缓并逐渐接近平衡;第三阶段,60~120min,吸附已达到平衡。此后,溶液中的ADN浓度和吸附量基本不变。树脂上大量的吸附位点使得前30min DX迅速从溶液中吸附ADN,当大部分的位点被ADN分子占据后,分子间的排斥力使ADN难于被吸附,需要较长的时间才达到吸附平衡。
3 结 论
(1)通过DX树脂对ADN的吸附过程进行研究,获得了相关的热力学和动力学数据,为优化ADN分离纯化工艺提供了理论和实验依据。
(2)DX树脂吸附ADN的热力学研究表明,用Freundlich方程能较好地描述DX树脂在溶液中对ADN的吸附过程,属单分子层吸附。通过Freundlich方程拟合可知,DX树脂是ADN的良好吸附剂。此吸附过程ΔG<0,ΔS>0,吸附过程可自发进行,吸附过程ΔH>0,表明是一个吸热过程。
(3)DX树脂吸附ADN的动力学研究表明,DX树脂对ADN的吸附属于快速平衡型,通过吸附动力学曲线可知,前30min大量ADN被吸附在树脂DX上,60min后,吸附趋于平衡,拟二级动力学方程可以较好地描述DX树脂对ADN的吸附过程。
(4)采用树脂吸附工艺操作简便,吸附效率高,且可重复利用,节约了成本,在ADN分离纯化方面具有广阔的应用前景。

