净水污泥柠檬酸钠改性焙烧制备陶粒吸附剂及其对废水中氨氮吸附性能的研究
罗书舟,王东田,2*
(1.苏州科技大学环境科学与工程学院,江苏 苏州 215009;2.苏州科技大学化学生物与材料工程学院,江苏 苏州 215009)
以铁盐和铝盐为混凝剂去除原水中的胶体杂质是水净化的主要预处理工艺,这些胶体杂质不断聚集沉淀下来则形成了净水污泥。净水污泥作为给水厂的废弃物,少部分用于农田堆肥、建筑利用,还有大量的净水污泥采用陆上填埋、海洋弃投等方式处理,会对环境造成污染。
氨氮进入水体后会引起藻类异常繁殖,导致水质下降,并对鱼类及水生物种产生毒性。吸附法具有低能耗、高效等特点,是去除水中氨氮的有效方法之一,但由于吸附材料的吸附性能及成本等原因,限制了其在实际工程中的应用,因此需要开发更为高效、廉价的吸附剂。
净水污泥含有丰富的土壤颗粒、铁铝氧化物等物质,其表面粗糙、多微孔,还含有大量的铁(Fe)、铝(Al)、硅(Si)的活性位点,因此对废水中污染物有较好的吸附效果,如对重金属、磷(P)、甲基蓝等的吸附。将净水污泥通过高温焙烧等工艺制备成污泥灰吸附剂用于去除废水中污染物已有大量的研究。如李荣等将净水污泥与粉末活性炭通过复合-焙烧等工艺制备成吸附剂,其对水中氨氮的吸附量可达1.02 mg/g;刘啟迪等研究了煅烧净水污泥制备除磷材料的可行性,结果表明与未煅烧的净水污泥相比,煅烧后的净水污泥对废水中P的吸附量增加了48.2%。
由于净水污泥表面的吸附位点有限,其对废水中污染物的吸附效果不够理想,许多研究者对净水污泥进行了改性处理以提高其吸附性能。如杜明展等将煤矸石经盐酸处理后,发现其内部形成了大量孔隙,且比表面积增大,对稀土废水中氨氮的吸附能力增强;林丰等研究了氢氧化钾改性埃洛石对养猪废水中氨氮的去除效果,结果表明其对养猪废水中氨氮的吸附量可达14.75 mg/g,较改性前提高了5.1倍;林海等研究了经浓度为0.05 mol/L的柠檬酸钠改性后的沸石对废水中氨氮的吸附性能,结果表明改性后的沸石对废水中氨氮的去除率可达98.14%,比原沸石提高了44.42%。
基于上述研究,本试验以净水污泥为原料,选用盐酸、氢氧化钾、柠檬酸钠作为改性剂,通过研磨—改性—造粒—焙烧等工艺制备改性净水污泥陶粒吸附剂,测定其对水中氨氮的吸附量,得到最优的改性净水污泥陶粒吸附剂,探讨其对废水中氨氮吸附效果的影响因素,并对试验数据进行吸附等温线和吸附动力学模型拟合研究,以期为净水污泥在氨氮废水处理方面的应用提供技术支持。
1 材料与方法
1.1 净水污泥改性试验
取某自来水厂脱水污泥放入烘箱中于100℃下干燥24 h,经粉碎后过200目筛,得到净水污泥粉末。将净水污泥粉末投入不同浓度的酸(盐酸)、碱(氢氧化钾)、盐(柠檬酸钠)改性剂溶液中搅拌(净水污泥质量/改性剂溶液体积=50 g/L),在振荡器中于25℃和120 r/min转速下振荡24 h后过滤并用蒸馏水冲洗多次,放入造粒机制成直径约为5 mm的圆柱形颗粒,经烘箱干燥5 h后,在马弗炉中于500℃下焙烧5 h,制备得到改性净水污泥陶粒吸附剂(以下简称改性陶粒吸附剂)。以氨氮吸附量为衡量指标,筛选出上述最佳改性陶粒吸附剂和最佳改性陶粒吸附剂浓度。此外,在相同的条件下制备原净水污泥陶粒吸附剂(以下简称原泥陶粒吸附剂),用于对比试验。
1.2 吸附剂的表征方法
采用能量色散X射线光谱仪(EDX)测定吸附剂的元素组成及其含量;采用X射线衍射(XRD)仪(D-8,德国Brucker)测试分析吸附剂的晶型;采用赛默飞IS50型原位傅里叶红外光谱(FT-IR)仪测试分析吸附剂的官能团;采用Quanta FEG 250扫描电子显微镜(SEM)测试分析吸附剂的表面形貌;采用比表面积及孔径分析仪(BET)测试分析吸附剂的比表面积和总孔容。
1.3 氨氮水样的配制及测定方法
采用氯化铵配制模拟氨氮废水,水中氨氮含量采用纳氏试剂分光光度法检测。吸附剂对水中氨氮的平衡吸附量和去除率由以下公式计算:

(1)
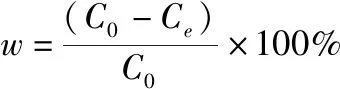
(2)
式中:q
为吸附剂对溶液中氨氮的平衡吸附量(mg/g);m
为吸附剂用量(g);w
为吸附剂对溶液中氨氮的去除率(%);C
为溶液中氨氮的初始浓度(mg/L);C
为吸附平衡时溶液中氨氮的浓度(mg/L);V
为溶液的体积(L)。1.4 吸附试验
1.4.1 吸附剂对氨氮吸附效果的对比试验
分别称取1.0 g不同改性条件下制备的改性陶粒吸附剂和原泥陶粒吸附剂,投入50 mL浓度为50 mg/L的氨氮溶液中,在振荡器中于25℃和120 r/min转速下吸附24 h后,测量溶液中氨氮的浓度。
1.4.2 吸附剂对氨氮吸附效果的影响因素分析试验
(1) 溶液初始pH值对氨氮吸附效果的影响。将氨氮溶液初始pH值分别调节为1、3、5、7、9、11,分别称取1.0 g原泥陶粒吸附剂和改性陶粒吸附剂投入50 mL浓度为50 mg/L的不同初始pH值氨氮溶液中,在振荡器中于25℃和120 r/min转速下吸附24 h后,测量溶液中氨氮的浓度。
(2) 吸附时间对氨氮吸附效果的影响。分别称取1.0 g原泥陶粒吸附剂和改性陶粒吸附剂投入50 mL浓度为50 mg/L的氨氮溶液中,将溶液调至最佳pH值,在振荡器中于25℃和120 r/min转速下吸附时间分别为0.5 h、1 h、2 h、3 h、4 h、5 h、6 h、7 h、8 h时取样,测量溶液中氨氮的浓度。
(3) 吸附剂投加量对氨氮吸附效果的影响。分别称取不同质量(0.5 g、1 g、2 g、3 g)的原泥陶粒吸附剂和改性陶粒吸附剂投入50 mL浓度为50 mg/L的氨氮溶液中,将溶液调至最佳pH值,在最佳吸附时间下进行振荡吸附后,测量溶液中氨氮的浓度。
(4) 氨氮初始浓度对氨氮吸附效果的影响。分别称取1.0 g原泥陶粒吸附剂和改性陶粒吸附剂投入50 mL不同初始浓度的氨氮溶液中,将溶液调至最佳pH值,在最佳吸附时间下进行振荡吸附后,测量溶液中氨氮的浓度。
1.5 吸附等温线与吸附动力学拟合
1.5.1 吸附等温线拟合
吸附等温线是指在一定温度下,当吸附达到平衡时,溶液中离子浓度与吸附剂对该离子的吸附量之间的关系。按照第1.4节(4)中步骤进行吸附试验,并采用Langmuir模型和Freundlich模型对试验数据进行了吸附等温线拟合。其中,Langmuir模型一般用来描述发生在均匀吸附剂表面上的单分子定位吸附;Freundlich模型一般用来描述在非均匀吸附剂表面上的多分子层吸附。Langmuir模型和Freundlich模型的计算公式如下:

(3)
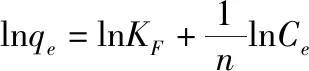
(4)
式中:q
为单分子层饱和吸附量(mg/g);K
为Langmuir模型平衡常数(L/mg);n
为与吸附能力有关的常数;K
为Freundlich模型平衡常数[(mg/g)·(L/mg)1]。1.5.2 吸附动力学拟合
吸附动力学模型主要表达了吸附材料对污染物的吸附量随时间的变化情况。按照第1.4节(2)中步骤进行吸附试验,并采用准一级动力学模型和准二级动力学模型对试验数据进行了吸附动力学拟合,分析吸附剂对氨氮的吸附过程,并计算吸附速率。其中,准一级动力学模型是假定吸附质从溶液转移至吸附剂表面的过程受扩散步骤的控制;准二级动力学模型是在假定吸附速率受化学吸附机理控制的基础上,吸附剂与吸附质之间电子对的公用或转移。准一级动力学模型和准二级动力学模型的计算公式如下:
ln(q
-q
)=lnq
-k
t
(5)

(6)
式中:k
为准一级动力学常数(min);t
为吸附时间(min);k
为准二级动力学常数[g/(mg·min)];q
为t
时刻的氨氮吸附量(mg/g)。1.6 氨氮解吸和重复利用试验
称取1.0 g改性陶粒吸附剂投入50 mL浓度为50 mg/L的氨氮溶液中,恒温吸附24 h后过滤并用蒸馏水冲洗多次;再将吸附饱和的改性陶粒吸附剂分别用50 mL不同浓度(0.01~1.5 mol/L)的NaOH、NaCl、HCl进行解吸,振荡脱附24 h后过滤,离心分离,测量溶液中氨氮浓度,并利用下式计算其解吸率:

(7)
式中:q
为饱和改性陶粒吸附剂对溶液中氨氮的释放量(mg/g);n
为改性陶粒吸附剂对溶液中氨氮的解吸率(%)。将解吸后的改性陶粒吸附剂投入50 mL浓度为50 mg/L的氨氮溶液中,多次重复以上吸附解吸步骤,并按公式(2)计算其对氨氮的去除率。
2 结果与讨论
2.1 净水污泥最佳改性条件的确定
分别采用盐酸、氢氧化钾和柠檬酸钠改性剂对净水污泥进行改性,得到3种改性净水污泥陶粒吸附剂简称改性陶粒吸附剂,得到添加不同改性剂的净水污泥对溶液中氨氮的吸附效果,见图1。
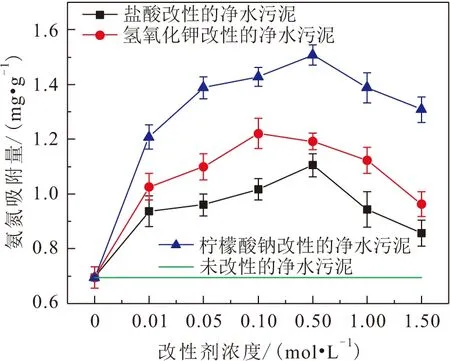
图1 添加不同改性剂的净水污泥对溶液中氨氮的吸附效果Fig.1 Adsorption effect of different modifiers on ammonia nitrogen in solution
由图1可见,3种改性剂均能提高净水污泥对溶液中氨氮的吸附性能,其中0.5 mol/L的柠檬酸钠对净水污泥的改性效果最佳,对水溶液中氨氮的吸附量可达1.508 mg/g,因此选用0.5 mol/L的柠檬酸钠对净水污泥进行改性。
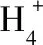
为了进一步提高柠檬酸钠改性净水污泥对溶液中氨氮的吸附性能,将净水污泥置于0.5 mol/L的柠檬酸钠溶液中搅拌后,对其进行水浴加热,考察水浴温度和水浴时间对溶液中氨氮吸附效果的影响,经此工序后制得的改性陶粒吸附剂对溶液中氨氮的吸附效果,见图2。
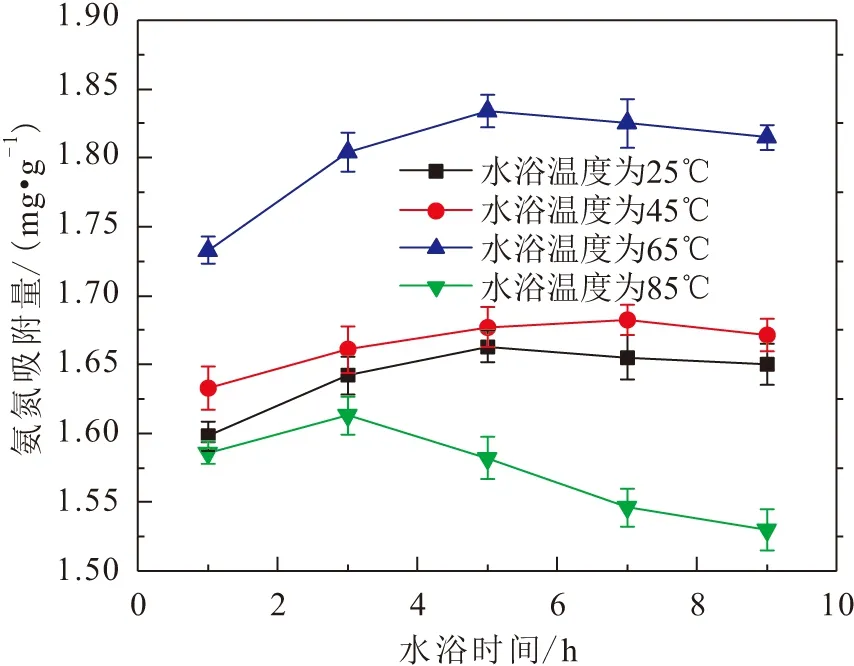
图2 水浴温度和水浴时间对改性陶粒吸附剂对溶液中氨氮吸附效果的影响Fig.2 Effect of water bath temperature and bath time on the adsorption effect of ammonia nitrogen by modified ceramsite adsorbent
由图2可见,在45℃、65℃和85℃的水浴温度下,对改性过程进行水浴加热,均能提高改性陶粒吸附剂对溶液中氨氮的吸附性能,其中在65℃下加热5 h时其对溶液中氨氮的吸附量达到最大,为1.838 mg/g。这是由于随着水浴温度的提高,离子的热运动加快,单位时间内Na接触净水污泥表面的次数增多,有利于离子交换过程的进行,但水浴温度过高时,会降低Na在净水污泥表面的吸附强度,导致离子交换容量减小。因此,净水污泥的最佳改性条件为:采用0.5 mol/L的柠檬酸钠搅拌混合,并在水浴温度为65℃下浸泡5 h。
2.2 吸附剂的表征结果分析
2.2.1 吸附剂EDX和SEM分析
本文采用能量色散X射线光谱(EDX)仪对原泥陶粒吸附剂和改性陶粒吸附剂的元素组成及其含量进行测试分析,其测试结果见表1。
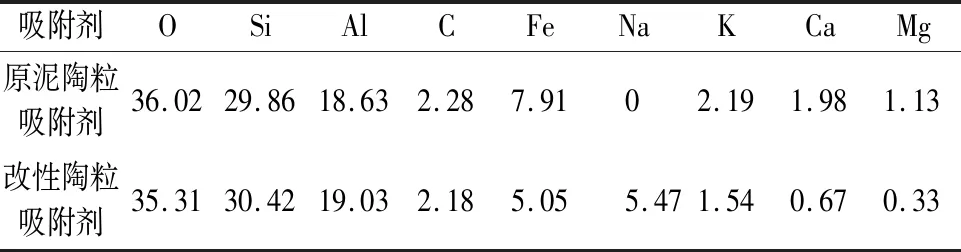
表1 原泥陶粒吸附剂和改性陶粒吸附剂的元素组成及其含量(wt%)Table 1 Element composition of raw sludge ceramsite adsorbent and modified ceramsite adsorbent (wt%)
由表1可知,原泥陶粒吸附剂和改性陶粒吸附剂两种吸附剂的主要元素组成均为O、Si、Al,而净水污泥经柠檬酸钠改性后,其Na元素含量由0%增加至5.47%,说明溶液中的Na已通过置换作用进入净水污泥中。这是由于Na的半径较小,根据体积效应,使得改性陶粒吸附剂的空间位阻减小,内扩散速度加快,离子交换容量增大。
本文采用扫描电子显微镜(SEM)对原泥陶粒吸附剂和改性陶粒吸附剂的表面形貌进行测试分析,其测试结果见图3。

图3 原泥陶粒吸附剂和改性陶粒吸附剂的SEM图Fig.3 SEM images of raw sludge ceramsite adsorbent and modified ceramsite adsorbent
由图3可见,与原泥陶粒吸附剂的表层结构相比,改性陶粒吸附剂表面片层数量变多、变薄且更加疏松。这是由于柠檬酸钠在500℃高温焙烧时分解后产生了CO等气体物质,当气体物质由内向外逸出时产生的冲击力不断作用于吸附剂表面,使其表层结构发生了变化。
2.2.2 吸附剂BET分析
本文采用比表面积及孔径分析(BET)仪对原泥陶粒吸附剂和改性陶粒吸附剂的比表面积及孔容进行测试分析,其测试结果见表2。

表2 原泥陶粒吸附剂和改性陶粒吸附剂的比表面积、孔容和平均孔径Table 2 Specific surface area,pore volume and average pore size of raw sludge ceramsite adsorbent and modified ceramsite adsorbent
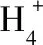
2.2.3 吸附剂XRD分析
本文采用X射线衍射(XRD)仪对原泥陶粒吸附剂和改性陶粒吸附剂的晶型进行测试分析,其测试结果见图4。

图4 原泥陶粒吸附剂和改性陶粒吸附剂的XRD图Fig.4 XRD patterns of raw sludge ceramsite adsorbent and modified ceramsite adsorbent
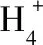
2.2.4 吸附剂FT-IR分析
本文采用傅里叶红外光谱(FT-IR)仪对原泥陶粒吸附剂和改性陶粒吸附剂的官能团进行测试分析,其测试结果见图5。
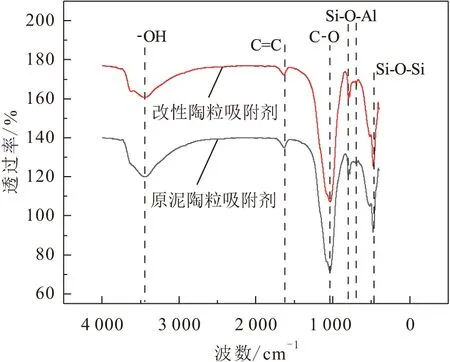
图5 原泥陶粒吸附剂和改性陶粒吸附剂的FT-IR图Fig.5 FTIR spectra of raw sludge ceramsite adsorbent and modified ceramsite adsorbent
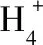
2.3 吸附剂对氨氮吸附效果的影响因素分析
2.3.1 溶液初始pH值对氨氮吸附效果的影响
溶液初始pH值对原泥陶粒吸附剂和改性陶粒吸附剂两种吸附剂吸附氨氮效果的影响,见图6。
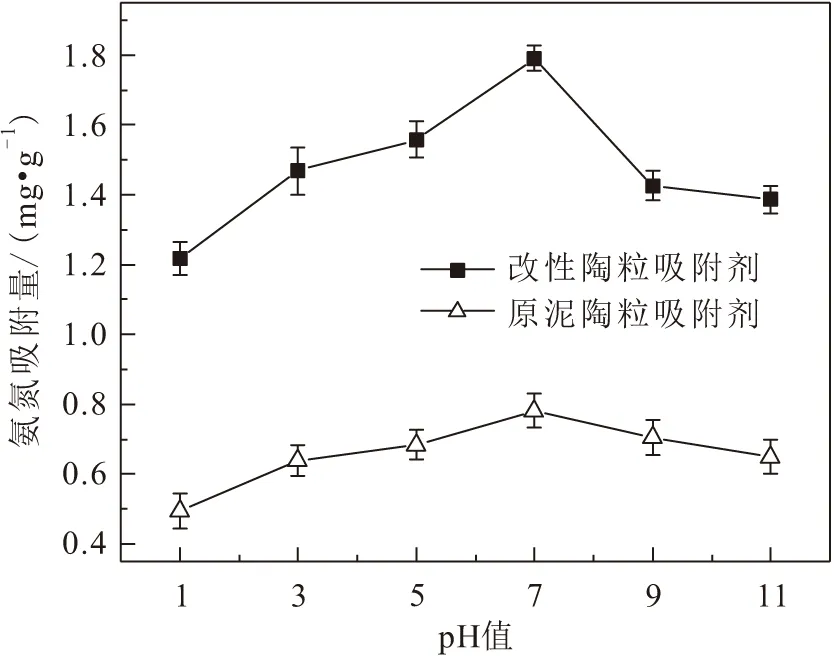
图6 溶液初始pH值对两种吸附剂吸附氨氮效果的影响Fig.6 Effect of initial pH of solution on the adsorption of ammonia nitrogen by the two adsorbents
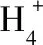
2.3.2 吸附时间对氨氮吸附效果的影响
吸附时间对原泥陶粒吸附剂和改性陶粒吸附剂两种吸附剂吸附氨氮效果的影响,见图7。
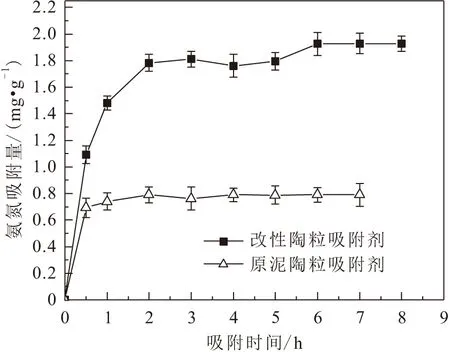
图7 吸附时间对两种吸附剂吸附氨氮效果的影响Fig.7 Effect of time on the adsorption of ammonia nitrogen by the two adsorbents
由图7可见,在前1 h内,改性陶粒吸附剂对溶液中氨氮的吸附量急剧上升,从0 mg/g增加至1.481 mg/g;在4~6 h内,改性陶粒吸附剂对溶液中氨氮的吸附量仍在上升,但吸附速率较前1 h明显放缓,并在6 h时达到吸附饱和。这是由于在吸附前期,吸附剂表面未被利用的吸附位点的数目较多,且吸附剂表面液膜与溶液之间存在一定的浓度差,加快了氨氮的扩散速度,使得溶液中氨氮被快速吸附。
2.3.3 吸附剂投加量对氨氮吸附效果的影响
吸附剂投加量对原泥陶粒吸附剂和改性陶粒吸附剂两种吸附剂吸附氨氮效果的影响,见图8。
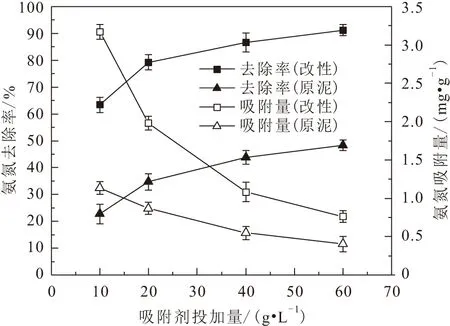
图8 吸附剂投加量对两种吸附剂吸附氨氮效果的影响Fig.8 Effect of the dosage of adsorbents on the adsorption of ammonia nitrogen by the two adsorbents
由图8可见,当改性陶粒吸附剂的投加量由10 g/L增加至60 g/L时,其对溶液中氨氮的平衡吸附量从3.17 mg/g降至0.76 mg/g,而吸附率则从63.40%増至91.20%。
这是由于吸附剂的投加量决定了吸附位点的数目,当其投加量增加时,吸附剂表面的吸附位点未被完全利用,使得单位吸附位点的吸附量变低,对氨氮的吸附效率增加。当改性陶粒吸附剂的投加量由0 g/L增加至20 g/L时,对氨氮的去除率增加了77.52%;而当改性陶粒吸附剂的投加量由20 g/L增加至60 g/L时,对氨氮的去除率仅增加了13.68%。因此,综合考虑经济成本因素,选取改性陶粒吸附剂的投加量为20 g/L。
2.3.4 氨氮初始浓度对氨氮吸附效果的影响
氨氮初始浓度对原泥陶粒吸附剂和改性陶粒吸附剂两种吸附剂吸附氨氮效果的影响,见图9。

图9 氨氮初始浓度对两种吸附剂吸附氨氮效果的影响Fig.9 Effect of initial concentration of ammonia nitrogen on the adsorption of ammonia nitrogen by the two adsorbents
由图9可见,当氨氮初始浓度为0~150 mg/L时,随着氨氮初始浓度的升高,两种吸附剂对氨氮的平衡吸附量增加;当氨氮初始浓度增加至150 mg/L时,两种吸附剂对氨氮的吸附量趋于平衡,此时两种吸附剂对溶液中氨氮的吸附量分别为3.115 mg/g、1.702 mg/g。这是由于当氨氮初始浓度较低时,吸附剂表面存在未被利用的吸附位点,使得其对氨氮的吸附量显著增加;而当氨氮初始浓度较高时,吸附剂表面已无可进行吸附的位点,继续增加氨氮浓度则其对氨氮的吸附量不再增加。
2.4 吸附等温线拟合
原泥陶粒吸附剂和改性陶粒吸附剂两种吸附剂对氨氮吸附过程的吸附等温线拟合结果,见图10和图11。将试验数据与拟合结果按公式(3)和(4)计算,所得吸附等温线的拟合参数见表3。

图10 两种吸附剂对氨氮吸附过程的Langmuir模型拟合结果Fig.10 Langmuir model fitting of ammonia nitrogen adsorption process by the two adsorbents

图11 两种吸附剂对氨氮吸附过程的Freundlich模型拟合结果Fig.11 Freundlich model fitting of ammonia nitrogen adsorption process by the two adsorbents
由表3可知,Langmuir模型的R
值大于Freundlish模型,表明Langmuir模型的拟合效果更佳,说明发生在吸附剂表面的吸附过程为单分子层吸附。吸附模型的性质可以用分离因子R
进行分析,其计算公式为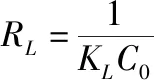
(8)
当0<R
<1时判定为有利吸附。由表3可知,两种吸附剂的R
值均在0~1之间,说明氨氮在两种吸附剂上的吸附为有利吸附。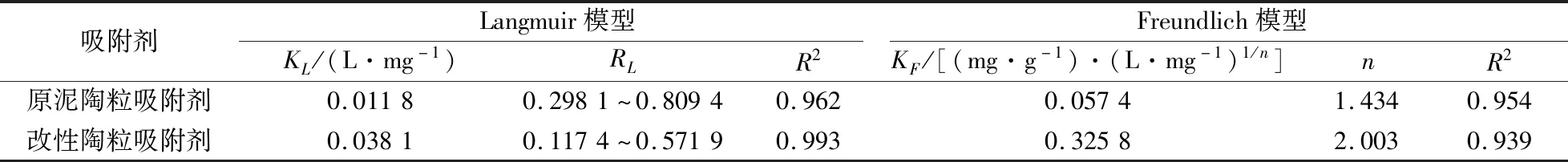
表3 吸附等温线的拟合参数Table 3 Fitting parameters of the adsorption isotherm model
2.5 吸附动力学拟合
原泥陶粒吸附剂和改性陶粒吸附剂两种吸附剂对氨氮吸附过程的吸附动力学模型拟合结果,见图12。将试验数据与拟合结果按公式(5)和(6)计算,所得吸附动力学模型的拟合参数见表4。
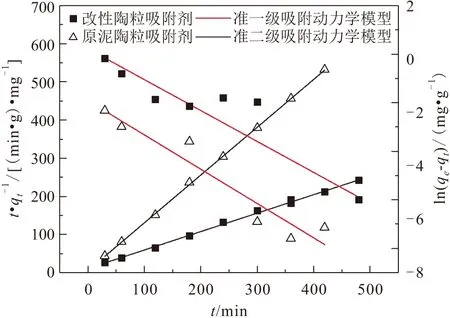
图12 两种吸附剂对氨氮吸附动力学过程的准一级动力学模型和准二级动力学模型拟合结果Fig.12 Pseudo-first order kinetics model and Pseudo- second order kinetics model fitting of ammonia nitrogen adsorption process by two adsorbents
由表4可知,准二级动力学模型的R
值大于准一级动力学模型,表明准二级动力学模型的拟合效果更佳,而且改性陶粒吸附剂和原泥陶粒吸附剂两种的吸附剂对溶液中氨氮的理论吸附值q
,thero(2.06 mg/g、0.81 mg/g)与实际吸附值q
,exp(1.938 mg/g、0.785 mg/g)也更为吻合,说明该吸附过程为在吸附剂表面进行的化学吸附。吸附剂的初始吸附速率h
可由下式计算: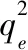
(9)
由表4可知,改性陶粒吸附剂的h
值大于原泥陶粒吸附剂,说明相比于原泥陶粒吸附剂,改性陶粒吸附剂对氨氮的初始吸附速率更快。
表4 吸附动力学模型的拟合参数Table 4 Fitting parameters of the adsorption kinetics model
2.6 氨氮解吸和重复再生结果分析
2.6.1 不同再生液对饱和改性陶粒吸附的氨氮解吸效果对比
按照第1.6节中步骤,采用NaOH、NaCl、HCl 3种再生液对吸附饱和的改性陶粒吸附剂进行解吸试验,其对氨氮的解吸效果见图13。
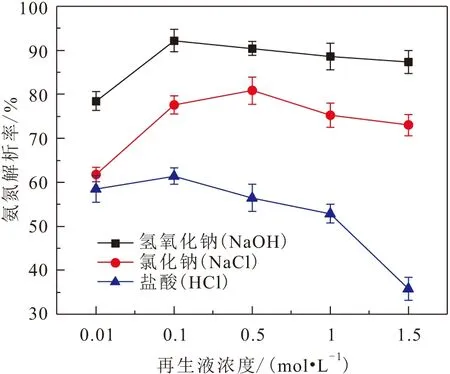
图13 不同再生液对饱和改性陶粒吸附剂的氨氮解吸效果对比Fig.13 Comparison of different regenerated fluids on ammonia nitrogen desorption by saturated modified ceramsite adsorbents

2.6.2 重复再生效果分析
本文采用NaOH溶液对吸附饱和的改性陶粒吸附剂进行5次重复再生试验,其对氨氮的解吸效果见表5。
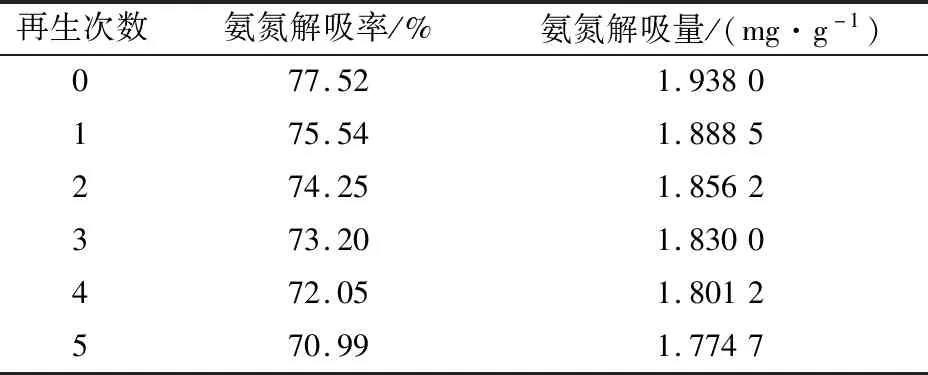
表5 饱和改性陶粒吸附剂的重复再生效果比较Table 5 Comparison of repeated regeneration effect of saturated modified ceramsite adsorbents
由表5可知,NaOH溶液对吸附饱和的改性陶粒吸附剂有较好的重复再生效果,经过5次解吸再生后,改性陶粒吸附剂对氨氮的解吸率和解吸量分别为70.99%和1.7747 mg/g,其再生和解吸能力保持良好。
2.7 改性陶粒吸附剂与商用吸附剂的比较
对于吸附法来说,选择一种高效、价格低廉的吸附剂对降低处理成本有着重要的现实意义。从吸附性能和经济性两方面,将改性陶粒吸附剂与目前商用氨氮吸附剂进行了对比,详见表6。
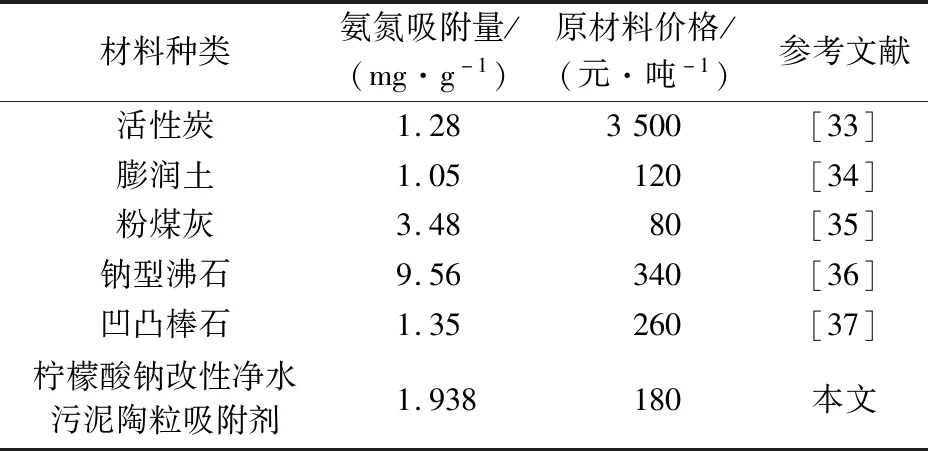
表6 不同氨氮吸附剂的对比Table 6 Comparison of different ammonia nitrogen adsorbents
由表6可知,改性陶粒吸附剂对氨氮的吸附效果优于大部分氨氮吸附剂,其对氨氮的吸附量仅低于钠型沸石和粉煤灰,而且在原材料成本上也具有一定的优势,而制成陶粒更易于回收再利用,可以达到以废治废的目的,说明柠檬酸钠改性净水污泥陶粒吸附剂具有很强的应用潜力。
3 结 论
(1) 净水污泥的最佳改性条件为:采用0.5 mol/L的柠檬酸钠搅拌混合,并在水浴温度为65℃下浸泡5 h。与原泥陶粒吸附剂相比,改性陶粒吸附剂的表面片层数量变多且更加疏松,离子交换容量、孔径和比表面积增大,提高了对氨氮的吸附性能。
(2) 改性陶粒吸附剂对氨氮的吸附效果与原泥陶粒吸附剂相比有显著提高,当溶液最佳pH值为7、饱和吸附时间为6 h、吸附剂经济投加量为20 g/L、氨氮初始浓度为50 mg/L时,改性陶粒吸附剂对氨氮的最大吸附量为1.938 mg/g,为原泥陶粒吸附剂的2.46倍。
(3) 改性陶粒吸附剂和原泥陶粒吸附剂对氨氮的吸附过程均符合Langmuir模型和准二级动力学模型。分离因子R
计算结果表明,氨氮在两种吸附剂上的吸附均为有利吸附,且改性陶粒吸附剂对氨氮的初始吸附速率高于原泥陶粒吸附剂。(4) 改性陶粒吸附剂的最佳再生液为0.1 mol/L的NaOH溶液,对氨氮的解吸率可达92.22%。吸附饱和的改性陶粒吸附剂经过5次解吸和回用后,对氨氮的解吸率仅下降了6.53%,其再生和解吸能力保持良好。

