和辉胶囊的毒理学安全性评价
肖云峰,李文妍,马睿婷,乔俊缠
(1.内蒙古医科大学新药安全评价研究中心,内蒙古呼和浩特 010110)(2.内蒙古自治区人民医院药学处,内蒙古呼和浩特 010017)(3.内蒙古医科大学附属医院,内蒙古呼和浩特 010000)(4.内蒙古医科大学药学院,内蒙古呼和浩特 010110)
近年来,我国动脉粥样硬化引起的心脑血管疾病发生率显著升高,而其最重要的诱发因素为高脂血症[1]。高脂血症,是指脂肪代谢或运转异常使血浆中一种或多种脂质浓度超出正常范围的而诱发的一系列疾病[2],即为古籍中常述之为“膏”的病症表现。《黄帝内经灵枢集注》记载:中焦之气,蒸津液化,其精微溢于外则皮肉膏肥,余于内则清育丰满[3]。研究发现,高血脂症会导致机体氧自由基增加,抗氧化能力下降,脂质过氧化作用增强[4];临床主要表现为血管硬化、血浆或血清浑浊、血管某部位形成斑块等。目前,临床常使用他汀类药物治疗高血脂症,但需长期服用,副作用较多。因此,研究具有辅助调节血脂功能的保健食品日益受到关注。
和辉胶囊以丹参、荜茇和沙棘为主要原料,是一种具有辅助降脂功能的保健食品。丹参祛瘀止痛、活血通经、清心除烦。《本经》记载:丹参主心腹邪气,寒热积聚;破癥除瘕,止烦满,益气;临床主要用于冠心病以及血栓闭塞性脉管炎等疾病的治疗[5,6]。荜茇温中散寒,下气止痛。《本草纲目》记载:荜茇辛热,入阳明经散浮热;临床用于脘腹冷痛、呕吐、泄泻以及冠心病等疾病的治疗[7,8]。沙棘能消食化滞,活血散瘀。《四部医典》记载:沙棘健脾养胃、破瘀治血;临床用于消化不良、食积腹痛以及跌扑瘀肿等疾病的治疗[9~11]。组方后发现,和辉胶囊不仅能够改善血脂异常、脂肪肝和各种肥胖相关的症状,而且对血脂异常所引发的高血压、糖尿病具有良好的调节作用。本文就和辉胶囊的食用安全问题,进行毒理学研究,报告如下。
1 材料与方法
1.1 受试物
和辉胶囊,内容物为黄棕色颗粒和粉末(内蒙古谨康医药科技有限公司,批号 20101014),基本组方为丹参、荜茇和沙棘等药食同源的物品;粒重0.32 g,人体推荐用量为3次/d,3粒/次,常温保存。
1.2 实验动物及饲养环境
SD大鼠,清洁级,由第四军医大学实验动物中心提供,实验动物生产许可证编号:SCXK(军)2007-007。
昆明种小鼠,清洁级,由第四军医大学实验动物中心提供,实验动物生产许可证编号:SCXK(军)2007-007。全部实验均于陕西省中医医院/陕西省疾病预防控制中心开展,实验动物使用许可证编号:SYXK(陕)2007-004。
1.3 主要仪器与试剂
全自动生化分析仪,型号OLYMPUS AU400;全自动血细胞计数仪,型号 HEMAVET950FS;电子天平,型号YB1201/0.1 g;电子天平,型号DT200A/0.01 g;电子天平,型号BS323S320/0.001 g;生物显微镜,型号OLYMPUS41。
1.4 主要试剂
复方环磷酰胺片,天津金世制药有限公司;阿的平,Sigma公司;注射用盐酸柔红霉素,浙江海正药业股份有限公司;叠氮化钠,Sigma公司;2-氨基芴,Sigma公司;丝裂霉素C,Sigma公司;1,8-二羟基蒽醌,Sigma公司。
1.5 试验方法
1.5.1 大鼠急性经口毒性试验[12]
选取SD大鼠20只,雌、雄各半,体重180~220 g,于试验前隔夜禁食12 h。将受试物按最大耐受剂量设计为15.0 g/kg·bw,试验时称取样品50.0 g加蒸馏水至100 mL制成混悬液备用,以1.0 mL/100 g·bw的灌胃剂量,给予大鼠灌胃三次(间隔4 h)。观察其饮食情况、活动情况、中毒症状及死亡现象等,连续14 d。按急性毒性剂量分级标准评价受试物的急性毒性强弱。
1.5.2 遗传毒性试验[13~15]
1.5.2.1 小鼠骨髓细胞微核试验
选取昆明种小鼠50只,雌、雄各半,体重25~30 g,采用数字随机法分为5组,每组10只。将受试物设3个剂量组,分别为10.0 g/kg·bw、5.0 g/kg·bw、2.5 g/kg·bw,同时设阴性对照组(蒸馏水)和阳性对照组(环磷酰胺40 mg/kg·bw)。将受试物10.0 g、5.0 g、2.5 g各加蒸馏水至20 mL分别配成50.0%、25.0%、12.5%的混悬液。以0.2 mL/10 g·bw的灌胃剂量,给予小鼠灌胃两次(间隔24 h)。第二次灌胃6 h后,颈椎脱臼处死小鼠,取其股骨骨髓用小牛血清稀释涂片,甲醇固定,Giemsa染色。在光学显微镜下,每只小鼠计数1000个嗜多染红细胞(PCE),观察含有微核的嗜多染红细胞数,微核率以千分率表示;同时计数200个嗜多染红细胞,计算嗜多染红细胞与成熟红细胞的比值(PCE/NCE)。采用卡方检验统计处理结果,若试验组的微核率比阴性对照组高,并有明显的剂量-反应关系和统计学意义,则为阳性结果。
1.5.2.2 小鼠精子畸形试验
选取昆明种小鼠50只,雄性,体重25~35 g,数字随机法分为5组,每组10只。将受试物设3个剂量组,分别为 10.0 g/kg·bw、5.0 g/kg·bw、2.5 g/kg·bw,同时设阴性对照组(蒸馏水)和阳性对照组(环磷酰胺40 mg/kg·bw)。将受试物10.0 g、5.0 g、2.5 g各加蒸馏水至20 mL分别配成50.0%、25.0%、12.5%的混悬液。每天以0.2 mL/10 g·bw的灌胃剂量,给予小鼠灌胃一次,连续5 d。于首次给受试物后的第35 d,颈椎脱臼处死小鼠,取其双侧附睾的精子于生理盐水稀释液涂片,甲醇固定,伊红染色。在光学显微镜下,每只小鼠计数完整精子1000个,计算精子畸形率。采用Wilcoson秩和检验统计处理结果,若试验组的精子畸形率比阴性对照组增高,并有明显的剂量-反应关系和统计学意义,则为阳性结果。
1.5.2.3 Ames试验
将受试物设计 5000 μg/皿、1000 μg/皿、200 μg/皿、40 μg/皿、8 μg/皿五个剂量组。称取受试物1.0 g加蒸馏水至20 mL配成5%浓度的混悬液(高剂量),高压灭菌(0.103 MPa,20 min)后使用,依次加无菌水5倍稀释为其它各剂量的混悬液备用。另设自然回变对照组、阴性对照组(蒸馏水)和阳性对照组(环磷酰胺)。用Ames试验标准菌株TA97、TA98、TA100和TA102,在加与不加肝S-9混合液的条件下,分别对受试物做平板掺入法Ames试验。各菌株每剂量做三个平行皿,每皿加菌加样各0.1 mL,整个试验重复二次,培养48 h后,记录各皿回变菌落数。若受试物的回变菌落数是自然回变菌落数的二倍以上且有剂量-反应关系者,则为诱变试验阳性。
1.5.3 大鼠30 d喂养试验[16,17]
选取SD大鼠80只,雌、雄各半,体重51.0~77.3 g,数字随机法分为4组,每组20只。受试物设3个剂量组,分别为 4.80 g/kg·bw(相当于人体推荐用量的 100 倍)、2.40 g/kg·bw 和 1.20 g/kg·bw,另设一个阴性对照组(蒸馏水)。将受试物48 g、24 g和12 g各加蒸馏水至100 mL分别配成48%、24%和12%的混悬液备用,各组均以1.0 mL/100 g·bw灌胃剂量(阴性对照组灌胃等容量蒸馏水)每天给予小鼠灌胃一次,连续30 d。小鼠自由进食和饮水,每天观察并记录动物的一般表现(包括外表、体形、行动、呼吸、被毛、鼻、口腔、眼、耳、生殖器、尿、粪便及其它异常),每周称体重及进食量,最后计算食物利用率。试验结束时,摘眼球取血,用全自动生化分析仪测定血清生化指标(血红蛋白、红细胞计数、白细胞计数和白细胞分类计数等)。然后将试验动物脱颈椎处死,进行大体解剖,取肝、肾、脾、睾丸等脏器称重,观察有无异常,并将阴性对照组和高剂量组动物的肝、肾、脾、胃肠、睾丸(卵巢)固定,进行组织病理学检查。
1.5.4 统计学方法[18]
试验数据应用SPSS统计软件进行单因素方差分析。在统计分析时,先对数据进行方差齐性检验,若方差齐,采用单因素方差分析进行总体比较,发现差异再用Dunnett检验进行多个剂量组与对照组均数间的两两比较。若方差不齐则对数据进行适当的变量转换,满足方差齐性检验后,用转换后的数据进行统计;若转换后的数据仍未达到方差齐要求,改用秩和检验进行统计分析。
2 实验结果
2.1 大鼠急性毒性试验
以受试物最大剂量 15.0 g/kg·bw 给予大鼠灌胃后,大鼠饮食活动正常,生长良好,未见体重受到影响,未发现大鼠有明显中毒表现及死亡现象。试验结束解剖大鼠,大体观察:肝、肾、脾、胃、肠、心、肺等主要脏器均未见明显异常改变。根据《保健食品检验与评价技术规范》(2003年版)中急性毒性分级标准,保健食品和辉胶囊急性毒性属无毒级。结果表明,相当于人体推荐用量312.5倍剂量的和辉胶囊对雌、雄大鼠体重及脏器均无影响,属无毒级保健食品,结果见表1。

表1 和辉胶囊对急性毒性试验大鼠体重的影响Table 1 The effect of Hehui capsules on the body weight of rats in acute toxicity test
2.2 遗传毒性试验
2.2.1 小鼠骨髓细胞微核试验
与阴性对照组相比,雌、雄小鼠阳性对照组微核率均明显升高,具有极显著性差异(p<0.01);受试物各剂量组微核率与阴性对照组,无显著性差异(p>0.05)。结果表明,和辉胶囊在试验剂量 2.5 g/kg·bw~10.0 g/kg·bw 范围内,小鼠骨髓细胞微核试验结果为阴性。初步认为和辉胶囊无明显致小鼠骨髓细胞染色体完整性受损及染色体分离作用。
2.2.2 小鼠精子畸形试验
与阴性对照组比较,阳性对照组小鼠畸形率明显高于阴性对照组,有极显著性差异(p<0.01);受试物各剂量组小鼠精子畸形率与阴性对照组比较,均无显著性差异(p>0.05)。结果表明,和辉胶囊在试验剂量2.5 g/kg·bw~10.0 g/kg·bw 范围内,对小鼠精子无明显毒性,初步认为无明显致小鼠精子畸形作用。结果见表3。

表2 和辉胶囊对小鼠骨髓细胞微核试验的影响Table 2 The effect of Hehui capsules on the bone marrow cells of mice in micronucleus test

表3 和辉胶囊对小鼠精子畸形试验的影响Table 3 The effect of Hehui capsules on the mouse sperm abnormality test
2.2.3 Ames试验
与自然回变菌落数相比,受试物各剂量组及阴性对照组各菌株回变菌落数均未超过自然回变菌落数的二倍,而阳性对照组菌落数达到自然回变菌落数的二倍以上。结果表明,和辉胶囊在试验剂量8 μg/皿~5000 μg/皿范围内,Ames试验结果为阴性。未发现和辉胶囊存在诱变作用。结果见表4。
表4 和辉胶囊对Ames试验的影响Table 4 The effect of Hehui capsules on the Ames test(±s)

表4 和辉胶囊对Ames试验的影响Table 4 The effect of Hehui capsules on the Ames test(±s)
菌株组别 TA97 TA98 TA100 TA102 S-9(-) S-9(+) S-9(-) S-9(+) S-9(-) S-9(+) S-9(-) S-9(+)阴性对照 144±7 146±14 37±2 37±3 168±12 167±11 269±15 278±9阳性对照 2721±233 1808±192 2956±144 5808±194 2857±212 2951±298 2169±284 969±62自然回变 148±22 147±8 38±7 35±2 173±19 161±12 275±23 278±28 5000 μg 皿 151±12 158±21 33±3 30±2 156±6 167±14 276±24 280±22 1000 μg 皿 150±8 160±10 39±2 38±2 186±6 170±9 273±21 270±11 200 μg/皿 138±10 153±9 34±4 33±1 180±16 172±3 281±9 277±14 40 μg/皿 151±5 140±22 37±7 33±6 174±24 172±22 287±8 282±4 8 μg/皿 142±15 145±14 39±5 38±8 184±4 171±8 266±9 274±4阿的平10 μg/皿10 μg/皿 柔毛霉素6.0 μg/皿2AF 2AF 10 μg/皿NaN3 1.5 μg/皿2AF 10 μg/皿丝裂霉素C 0.5 μg/皿1,8-二羟基蒽醌50.0 μg/皿
2.3 30 d喂养试验
与阴性对照组比较,受试物各剂量组雌、雄鼠各期体重均无显著性差异(p>0.05);受试物各剂量组雌、雄大鼠各周进食量、食物利用率及总食物利用率均无显著性差异(p>0.05)。结果表明,和辉胶囊长期食用不会影响大鼠体重、进食,观察期内未发现大鼠出现明显毒作用表现。
2.3.1 对大鼠体重的影响
与阴性对照组相比,受试物各剂量组大鼠给药期间体重均无显著性差异(p>0.05)。结果表明,和辉胶囊对大鼠给药期间体重增长无影响。结果见表5。
表5 和辉胶囊对大鼠体重的影响Table 5 The effect of Hehui capsules on the body weight of rats(±s)
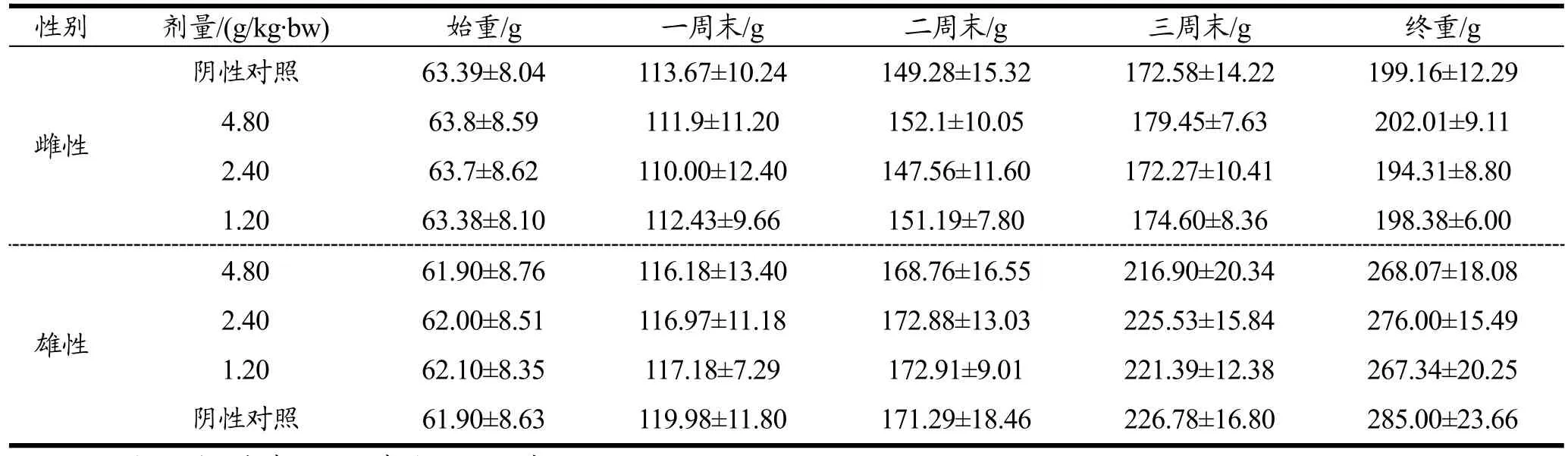
表5 和辉胶囊对大鼠体重的影响Table 5 The effect of Hehui capsules on the body weight of rats(±s)
性别 剂量/(g/kg∙bw) 始重/g 一周末/g 二周末/g 三周末/g 终重/g阴性对照 63.39±8.04 113.67±10.24 149.28±15.32 172.58±14.22 199.16±12.29雌性雄性4.80 63.8±8.59 111.9±11.20 152.1±10.05 179.45±7.63 202.01±9.11 2.40 63.7±8.62 110.00±12.40 147.56±11.60 172.27±10.41 194.31±8.80 1.20 63.38±8.10 112.43±9.66 151.19±7.80 174.60±8.36 198.38±6.00 4.80 61.90±8.76 116.18±13.40 168.76±16.55 216.90±20.34 268.07±18.08 2.40 62.00±8.51 116.97±11.18 172.88±13.03 225.53±15.84 276.00±15.49 1.20 62.10±8.35 117.18±7.29 172.91±9.01 221.39±12.38 267.34±20.25阴性对照 61.90±8.63 119.98±11.80 171.29±18.46 226.78±16.80 285.00±23.66
2.3.2 对大鼠进食量和食物利用率的影响
2.3.2.1 对大鼠各周进食量的影响
与阴性对照组相比,受试物各剂量组大鼠给药期间各周进食量均无显著性差异(p>0.05)。结果表明,和辉胶囊对大鼠各周进食无影响。结果见表6。
2.3.2.2 对大鼠食物利用率的影响
与阴性对照组相比,受试物各剂量组大鼠给药期间食物利用率均无显著性差异(p>0.05)。结果表明,和辉胶囊对大鼠给药期间食物利用率无影响。结果见表7。
2.3.2.3 对大鼠总食物利用率的影响
与阴性对照组相比,受试物各剂量组大鼠给药期间总食物利用率均无显著性差异(p>0.05)。结果表明,和辉胶囊对大鼠给药期间总食物利用率无影响。
表6 和辉胶囊对大鼠各周进食量的影响Table 6 The effect of Hehui capsules on the food intake of rats each week(±s,n=10)

表6 和辉胶囊对大鼠各周进食量的影响Table 6 The effect of Hehui capsules on the food intake of rats each week(±s,n=10)
性别 剂量/(g/kg∙bw) 第一周/g 第二周/g 第三周/g 第四周/g阴性对照 95.17±7.69 101.08±11.09 101.68±8.64 149.04±10.52雌性雄性4.80 94.84±6.35 106.26±10.43 109.56±8.79 149.39±16.18 2.40 91.13±3.85 101.14±9.74 97.34±8.48 144.24±12.48 1.20 94.12±6.56 102.07±6.87 106.84±8.85 143.21±16.89阴性对照 105.01±9.12 119.81±14.27 142.99±11.42 204.18±14.17 4.80 98.76±6.49 120.82±11.69 135.97±16.83 198.43±14.03 2.40 98.64±5.04 124.72±4.79 135.42±7.45 194.10±16.19 1.20 100.54±4.00 120.78±13.22 133.88±15.77 193.91±24.52
表7 和辉胶囊对大鼠各周食物利用率的影响Table 7 The effect of Hehui capsules on the weekly food utilization of rats(±s,n=10)

表7 和辉胶囊对大鼠各周食物利用率的影响Table 7 The effect of Hehui capsules on the weekly food utilization of rats(±s,n=10)
性别 剂量/(g/kg∙bw) 第一周/% 第二周/% 第三周/% 第四周/%阴性对照 52.84±1.69 34.91±6.03 23.03±4.27 17.67±3.50雌性雄性4.80 50.60±2.54 38.23±5.43 24.56±5.29 14.98±2.25 2.40 50.60±3.19 37.07±3.19 25.40±6.02 15.17±2.12 1.20 52.15±2.30 38.14±5.47 21.69±3.99 16.39±2.96阴性对照 55.37±2.55 42.38±6.70 38.84±4.82 28.33±5.91 4.80 54.92±4.46 43.56±2.41 35.57±2.66 25.82±3.69 2.40 55.74±4.02 44.82±2.36 38.86±3.59 25.78±6.65 1.20 54.76±3.30 46.48±5.01 36.42±4.97 23.41±3.21
表8 和辉胶囊对大鼠总食物利用率的影响Table 8 The effect Hehui capsules on the total food utilization of rats(±s,n=10)

表8 和辉胶囊对大鼠总食物利用率的影响Table 8 The effect Hehui capsules on the total food utilization of rats(±s,n=10)
性别 剂量/(g/kg·bw) 体重总增重/g 总进食量/g 总食物利用率/%阴性对照 135.77±10.10 446.97±24.66 30.38±1.55雌性雄性4.80 138.12±12.45 460.05±18.32 30.00±2.04 2.40 130.52±7.35 433.85±15.18 30.10±1.75 1.20 135.00±7.74 446.24±19.30 30.28±1.88阴性对照 223.10±26.09 571.99±34.86 38.96±3.32 4.80 206.17±12.11 553.98±37.69 37.27±1.75 2.40 214.00±12.72 552.88±17.36 38.72±2.21 1.20 205.24±18.97 549.11±41.42 37.39±2.31
2.3.3 对大鼠血常规的影响
与阴性对照组相比,受试物各剂量组大鼠血常规各指标均无显著性差异(p>0.05)。结果表明,和辉胶囊对大鼠血液中红细胞、白细胞和血红蛋白的数量变化及形态分布无影响。结果见表9。
表9 和辉胶囊对大鼠血常规的影响Table 9 The effect of Hehui capsules on the blood routine of rats(±s,n=10)
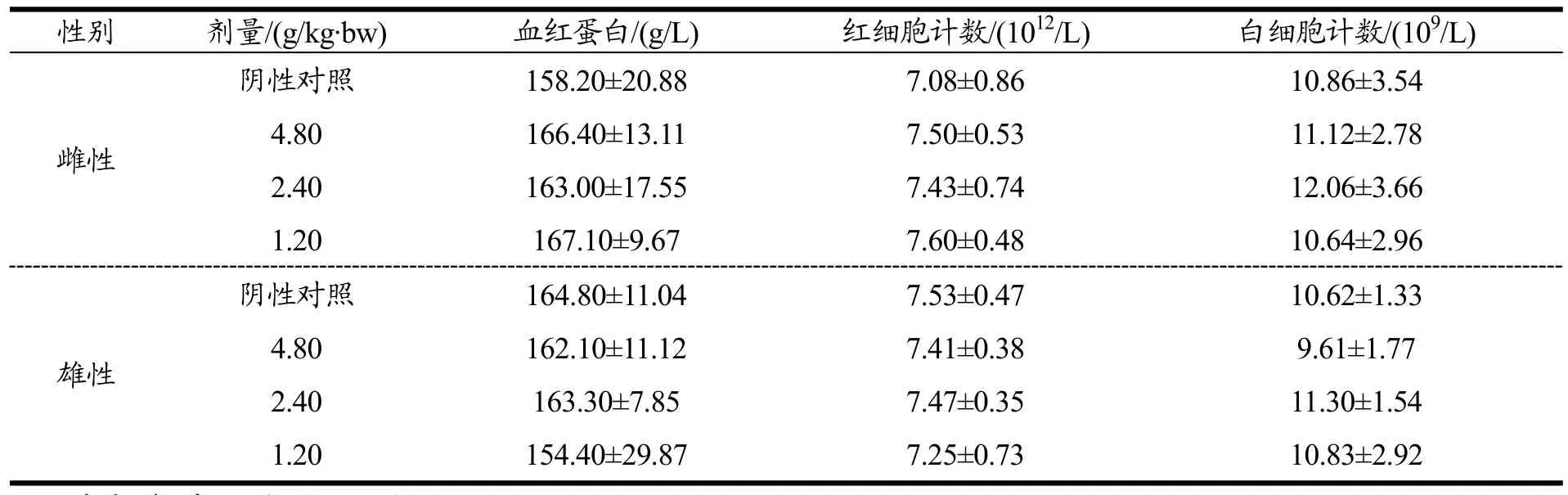
表9 和辉胶囊对大鼠血常规的影响Table 9 The effect of Hehui capsules on the blood routine of rats(±s,n=10)
性别 剂量/(g/kg∙bw) 血红蛋白/(g/L) 红细胞计数/(1012/L) 白细胞计数/(109/L)阴性对照 158.20±20.88 7.08±0.86 10.86±3.54雌性雄性4.80 166.40±13.11 7.50±0.53 11.12±2.78 2.40 163.00±17.55 7.43±0.74 12.06±3.66 1.20 167.10±9.67 7.60±0.48 10.64±2.96阴性对照 164.80±11.04 7.53±0.47 10.62±1.33 4.80 162.10±11.12 7.41±0.38 9.61±1.77 2.40 163.30±7.85 7.47±0.35 11.30±1.54 1.20 154.40±29.87 7.25±0.73 10.83±2.92
2.3.4 对大鼠生化指标的影响
与阴性对照组比较,雄鼠受试物各剂量组肌酐均有显著性差异(p<0.05),受试物高剂量组总胆固醇有极显著性差异(p<0.01);其余受试物各剂量组各项生化指标均无显著性差异(p>0.05)。结果表明,雄性雄鼠受试物各剂量组肌酐和高剂量组总胆固醇均低于阴性对照组,但均在本实验室正常参考值范围内,故无生物学意义。结果见表10。
表10 和辉胶囊对大鼠生化指标的影响Table 10 The effect of Hehui capsules on the biochemical indicators of rats(1)(±s,n=10)

表10 和辉胶囊对大鼠生化指标的影响Table 10 The effect of Hehui capsules on the biochemical indicators of rats(1)(±s,n=10)
性别 剂量/(g/kg∙bw) 谷丙转氨酶/(U/L) 谷草转氨酶/(U/L) 白蛋白/(g/L) 总蛋白/(g/L) 白/球阴性对照 30.15±5.46 195.40±37.62 34.40±2.42 71.32±4.11 0.94±0.08雌性4.80 33.11±8.50 167.80±12.52 34.50±1.40 71.02±3.15 0.94±0.07 2.40 31.50±12.50 176.70±39.74 34.59±2.39 71.70±4.94 0.95±0.05 1.20 34.03±7.72 184.80±21.09 34.82±1.14 71.75±2.66 0.96±0.05雄性阴性对照 33.91±5.80 198.60±23.66 33.00±1.27 66.61±1.12 1.00±0.07 4.80 34.18±7.67 206.50±17.92 31.93±1.21 64.38±1.62 0.97±0.05 2.40 39.87±8.82 222.80±28.40 31.42±2.09 64.97±2.82 0.93±0.10 1.20 42.39±10.47 204.90±20.20 31.99±2.18 64.90±2.85 0.97±0.08性别 剂量/(g/kg∙bw) 尿素氮/(mmol/L) 肌酐/(μmol/L) 血糖/(mmol/L) 总胆固醇/(mmol/L)甘油三酯/(mmol/L)雌性 阴性对照 6.61±0.72 50.54±2.50 3.44±0.63 2.06±0.35 1.22±0.34 4.80 6.71±1.06 51.84±4.50 3.63±0.63 1.82±0.27 1.44±0.34

注:与阴性对照组比较,*p<0.05,**p<0.01。
2.3.5 病理学大体解剖观察检查
各组大鼠肝脏、肾脏、胃和脾脏的大体检查结果均正常,病理组织学检查也未见明显的病理改变。2.3.5.1 对大鼠脏器重量的影响
与阴性对照组相比,受试物各剂量组大鼠脏器重量均无显著性差异(p>0.05)。结果表明,和辉胶囊对大鼠脏器重量无影响。结果见表11。
表11 和辉胶囊对大鼠脏器重量的影响Table 11 The effect of Hehui capsules on the organ weight of rats(±s,n=10)
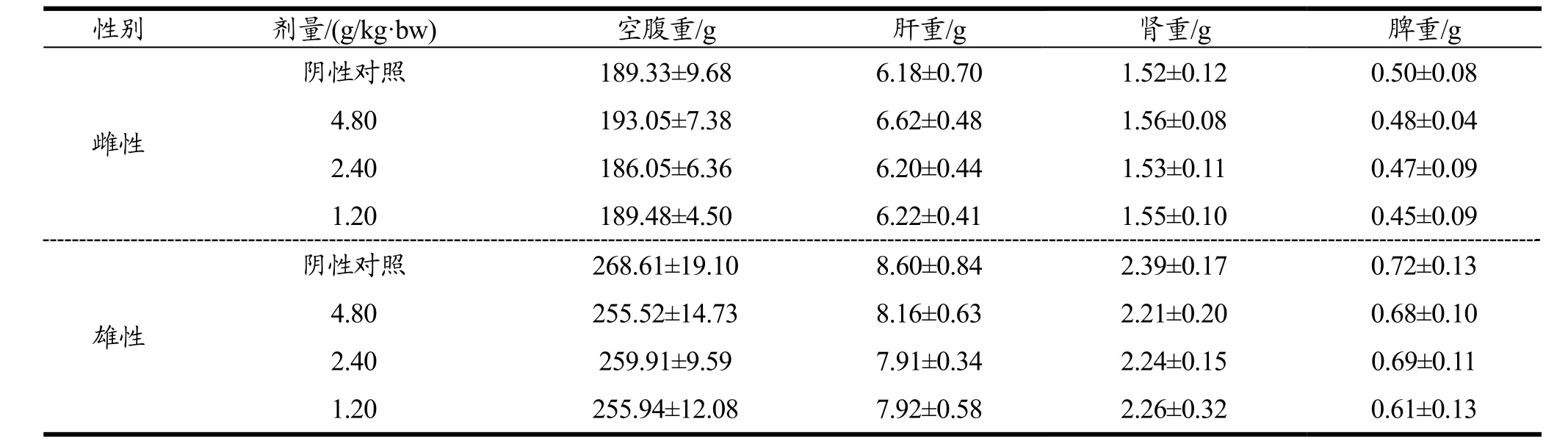
表11 和辉胶囊对大鼠脏器重量的影响Table 11 The effect of Hehui capsules on the organ weight of rats(±s,n=10)
性别 剂量/(g/kg·bw) 空腹重/g 肝重/g阴性对照 189.33±9.68 6.18±0.70雌性4.80 193.05±7.38 6.62±0.48 2.40 186.05±6.36 6.20±0.44 1.20 189.48±4.50 6.22±0.41雄性阴性对照 268.61±19.10 8.60±0.84 4.80 255.52±14.73 8.16±0.63 2.40 259.91±9.59 7.91±0.34 1.20 255.94±12.08 7.92±0.58肾重/g 脾重/g 1.52±0.12 0.50±0.08 1.56±0.08 0.48±0.04 1.53±0.11 0.47±0.09 1.55±0.10 0.45±0.09 2.39±0.17 0.72±0.13 2.21±0.20 0.68±0.10 2.24±0.15 0.69±0.11 2.26±0.32 0.61±0.13
2.3.5.2 对大鼠脏器系数的影响
与阴性对照组相比,受试物各剂量组大鼠脏器系数均无显著性差异(p>0.05)。结果表明,和辉胶囊对大鼠脏器系数无影响。结果见表12。
表12 和辉胶囊对大鼠脏器系数的影响(±s,n=10)Table 12 The effect for rats of organ coefficient by Hehui capsules (±s, n=10)
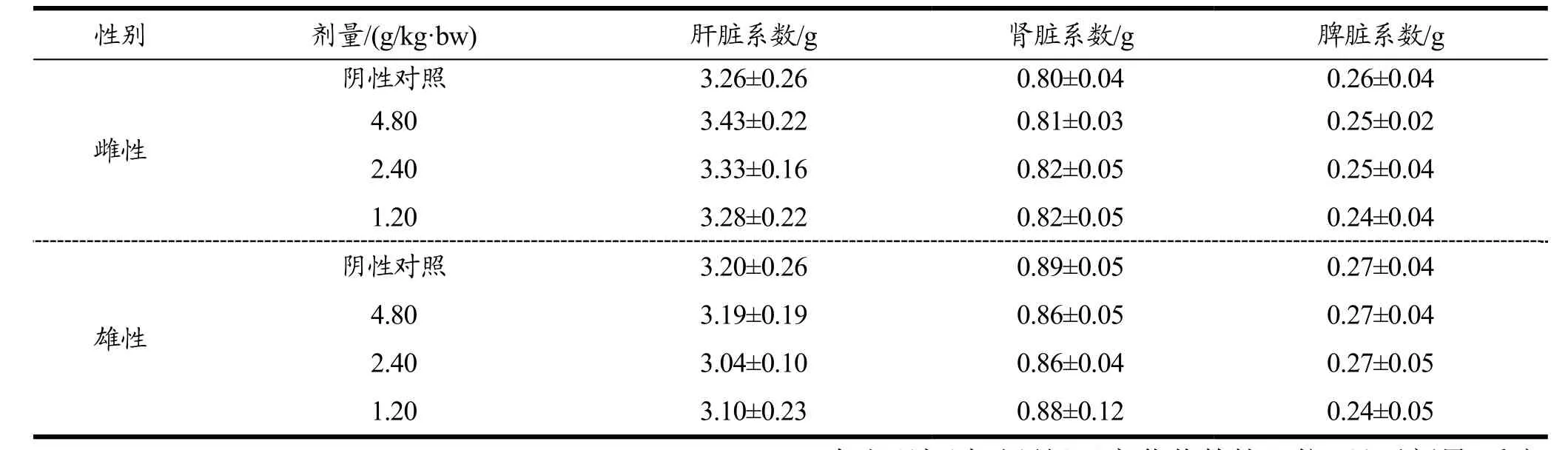
表12 和辉胶囊对大鼠脏器系数的影响(±s,n=10)Table 12 The effect for rats of organ coefficient by Hehui capsules (±s, n=10)
性别 剂量/(g/kg·bw) 肝脏系数/g阴性对照 3.26±0.26雌性4.80 3.43±0.22 2.40 3.33±0.16 1.20 3.28±0.22雄性阴性对照 3.20±0.26 4.80 3.19±0.19 2.40 3.04±0.10 1.20 3.10±0.23肾脏系数/g 脾脏系数/g 0.80±0.04 0.26±0.04 0.81±0.03 0.25±0.02 0.82±0.05 0.25±0.04 0.82±0.05 0.24±0.04 0.89±0.05 0.27±0.04 0.86±0.05 0.27±0.04 0.86±0.04 0.27±0.05 0.88±0.12 0.24±0.05
3 结论
为科学地评价和辉胶囊作为保健食品的安全性,本次试验中,对其进行了大鼠急性经口毒性试验、3项遗传毒性试验和大鼠30 d喂养试验。大鼠急性经口毒性试验结果显示和辉胶囊对雌、雄大鼠急性经口最大耐受剂量(MTD)均大于15.0 g/kg·bw,急性经口毒性属无毒级。Ames试验采用标准的掺入法,实验结果显示和辉胶囊受试样品各剂量组的回变菌落数均未出现超过对照组回变菌落数的2倍,且无剂量-反应关系,Ames试验结果为阴性,表明和辉胶囊无致突变作用。小鼠骨髓微核试验和小鼠精子畸变试验的结果皆为阴性,表明和辉胶囊对哺乳动物体细胞和生殖细胞无致染色体畸变和基因突变的作用。上述3项遗传毒性试验采用不同试验方法对和辉胶囊进行了遗传毒性检测,结果均为阴性,表明该样品无遗传毒性。大鼠30 d喂养试验中,在1.20、2.40和4.80 g/kg·bw剂量下(相当于人体推荐量的25、50和100倍),连服1个月,大鼠一般生理体征、行为、大小便和皮毛等均无异常,各脏器未见明显的功能损害,体重和食物利用率指标正常,血液学和血液生化学指标均无统计学差异,组织病理学检查结果未见特异性病理改变。以上试验表明在本试验条件下口服和辉胶囊无明显毒副作用。

