2型糖尿病微血管病变患者血浆内脂素水平变化及意义
刘真真,刘金波,刘传谦,赖宏,柳宪翠,陶军(济宁市第一人民医院,山东济宁7000;山东大学齐鲁医院;济阳县人民医院;平阴孝直中心卫生院)
糖尿病微血管病变是糖尿病常见的特异性并发症,与糖尿病病程、血糖控制水平、遗传等因素密切相关。糖尿病肾病(DN)和糖尿病视网膜病变(DR)是最常见的糖尿病微血管病变的表现形式。随着2型糖尿病(T2DM)发病率的不断上升,DN、DR的危害也日益加重,已经成为导致T2DM患者致残、致死的重要原因。研究表明,在无症状的T2DM患者中,微血管病变的发生率为32.55%[1]。T2DM微血管病变的早期检出并无特异性的指标。内脂素是一种与肥胖和糖尿病有关的脂肪细胞因子[2],其水平与机体的糖脂代谢有关,但其具体作用机制尚不十分明确。本研究通过检测发生T2DM微血管病变患者的血浆内脂素水平,探讨T2DM微血管病变患者血浆内脂素水平的变化及意义,为T2DM微血管病变的早期检出提供依据。
1 资料与方法
1.1 临床资料 收集2013年10月~2014年5月在山东大学齐鲁医院住院的T2DM患者108例,男55例、女53例,年龄(59.5±17.5)岁。均符合1999年WHO制定的T2DM诊断标准。排除T1DM、继发性糖尿病、合并感染性疾病者、原发性肾病综合征、合并严重全身性疾病(如心血管系统、呼吸系统、消化系统、神经系统等)者、恶性肿瘤患者。DN诊断标准:T2DM患者血糖控制平稳后,连续两次24 h尿微量白蛋白平均值≥30 mg/24 h,并排除原发性肾脏疾病、肾结石、泌尿系感染者。DR诊断标准:扩瞳后行眼底检查并行眼底荧光造影,发现视网膜有渗出、微血管瘤、出血及新生血管病变者。以诊断为DN、DR中任何一项者为存在T2DM微血管病变。将T2DM患者分为有微血管病变者55例、无微血管病变者53例。收集患者腰围(WC)、腰臀比(WHR)、BMI、空腹血糖(FBG)、空腹胰岛素(FINS)、空腹C肽(FCP)、糖化血红蛋白(HbA1c)、TG、TC、LDL-C、同型半胱氨酸(Hcy)水平及胰岛素抵抗指数(HOMA-IR)等资料。见表1。
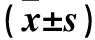
表1 有无T2DM微血病变患者一般资料及生化指标情况
1.2 血浆内脂素水平测定 研究对象均禁食空腹8 h以上,肘正中静脉采血,用酶联免疫吸附试验(ELISA)测定血浆内脂素水平。
2 结果
2.1 有无T2DM微血管病变患者血浆内脂素水平比较 有T2DM微血管病变、无T2DM微血管病变患者的血浆内脂素水平分别为(72.92±38.97)、(38.89±6.93)μg/L,有T2DM微血管病变患者的血浆内脂素水平高于无微血管病变患者(P<0.01)。
2.2 内脂素与各项临床指标相关性 将WC、WHR、BMI、FBG、FINS、FCP、HbA1c、TG、TC、LDL-C、Hcy、HOMA-IR分别与内脂素进行简单相关分析,血浆内脂素水平与WC(r=0.625)、BMI(r=0.573)、FBG(r=0.553)、HOMA-IR(r=0.578)均呈正相关(P均<0.05)。以血浆内脂素水平为因变量,以WC、WHR、BMI、FBG、FINS、FCP、HbA1c、TG、TC、LDL-C、Hcy、HOMA-IR为自变量进行多重线性回归分析,WC(b=0.422,SE=0.149,t=2.830,P=0.015)、HOMA-IR(b=1.509,SE=0.602,t=2.508,P=0.028)是血浆内脂素水平的影响因素。
2.3 内脂素与糖尿病微血管病变的关系 非条件Logistic回归结果示,病程、HbAlc、内脂素进入回归方程,Y=-9.608+病程(年)×0.231+ HbA1c×0.125+内脂素×0.169,病程、HbA1c、内脂素水平是糖尿病微血管病变的影响因素。见表2。
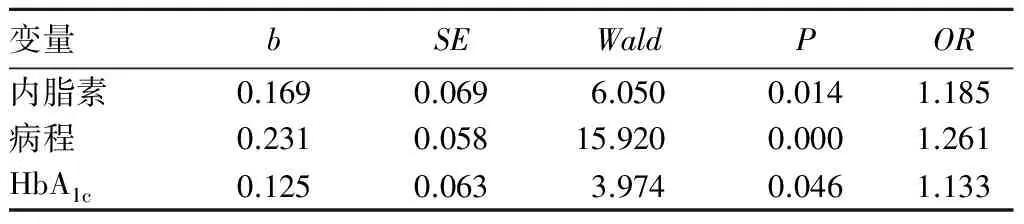
表2 T2DM微血管病变患者的影响因素
3 讨论
糖尿病微血管病变的发生与多种因素相关。研究证实,糖尿病微血管病变的发生与病程、血糖控制水平、HbA1c、年龄有着密切的关系[3]。近年来,内脂素与糖尿病微血管病变的关系也成为研究热点。内脂素是从人体内脏脂肪组织中分离出来一种新的脂肪因子,具有调节糖脂代谢、参与免疫反应等多种生物学作用。Fukuhara等[4]研究发现,血浆内脂素水平与内脏脂肪量有相关性。Mu等[5]研究发现,内脂素水平与WHR、BMI呈正相关。Berndt等[4,6]研究发现,血浆内脂素水平与 BMI、体脂率显著相关,而与WC、WHR无相关性。尽管以上研究结果对于内脂素与WHR、BMI的关系尚存在争议,但均提示血浆内脂素水平与肥胖密切相关。本研究发现,血浆内脂素水平与WC、BMI均呈正相关,WC是血浆内脂素水平的影响因素,表明血浆内脂素水平与内脏脂肪有关。
近年来,内脂素与T2DM及胰岛素抵抗的多项研究结果并不一致。多项研究发现,T2DM患者血浆内脂素水平高于健康对照人群[7,8]。有研究表明,高内脂素是T2DM的独立相关因素[8]。国内也有研究[5,9,10]发现,T2DM患者血浆内脂素水平低于健康人群。熊海亮等[11]研究发现,初诊T2DM患者的外周血内脂素水平与HOMA-IR呈显著正相关。Moschen等[12]研究报道,在人单核细胞中内脂素含量剂量依赖性地上调IL-1β、IL-1Ra、IL-6、IL-10和 TNF-α等炎症因子的水平,而上述炎症因子又会分别以不同的途径单独或协同作用诱导IR[13]。本研究发现,有T2DM微血管病变患者的血浆内脂素水平高于无微血管病变患者,提示随着糖尿病病情的进展,外周血内脂素水平呈现逐渐递增的趋势;HOMA-IR是在T2DM患者血浆内脂素水平的影响因素,表明血浆内脂素水平与胰岛素抵抗有关。
尿微量蛋白在早期糖尿病肾病患者是一个重要的预测因素。研究表明,外周血内脂素水平在DN早期就已经开始明显升高,并且随着尿蛋白排泄率的升高而增加[14]。刘树娇等[15]研究发现,外周血内脂素水平与炎症标志物有密切相关,提示慢性炎症反应可能是内脂素参与DN发生的途径之一。陈永生[16]发现,DR患者视网膜受损程度与外周血内脂素水平呈正相关。陶弢等[17]研究发现,内脂素有抗凋亡、促进细胞增殖等类似生长因子的作用,能够促进视网膜毛细血管内皮细胞的增殖,参与DR的发生。本研究通过回归分析证实,糖尿病病程、HbA1c、内脂素是T2DM微血管病变的危险因素,提示随着血浆内脂素水平的升高,糖尿病微血管病变的发生率越来越高,表明内脂素在糖尿病微血管病变的发生发展过程中起到了重要的作用。
综上所述,T2DM微血管病变患者血浆内脂素水平升高,血浆内脂素在T2DM微血管病变过程中发挥重要作用,是导致T2DM患者发生微血管病变的危险因素。进一步深入研究内脂素在T2DM微血管病变发生发展中的参与机制,可为糖尿病微血管并发症风险的评估和预测提供一个新的途径。
:
[1] Gupta A, Singh T. Occurrence of complications in newly diagnosed type 2 diabetes patients: a hospital based study[J]. J Indian Med Assoc, 2013,111(4):245-247.
[2] 陈饶饶.血清内脂素与2型糖尿病及脂代谢的相关性研究[J].世界最新医学信息文摘,2017,4(17):90-92.
[3] Chandni R, Ramamoorthy KP. Lipoprotein(a) in type 2 diabetic and its relationship to diabetic microvascular complications[J]. World J Diabetes, 2012,3(5):105-109.
[4] Fukuhara A, Matsuda M, Nishizawa M, et al. Visfatin:a protein secreted by visceral fat that mimics the effects of insulin[J]. Science, 2005,307(5708):426-430.
[5] Mu J, Feng B, Ye Z, et al. Visfatin is related to lipid dysregulation,endothelialdysfuction and atherosclerosis in patients with chronic kidney disease[J]. J Nephrol, 2011,24(2):177-184.
[6] Berndt J, Klting N, Kralisch S, et al. Plasma visfatin concentrations and fat depot-specific mRNA expression in humans[J]. Diabetes, 2005,54(10):2911-2916.
[7] Uslu S, Kebapci N, Kara M, et al. Relationship between adipocytokines and cardiovascular risk factors in patients with type 2 diabetes mellitus[J]. Exp Ther Med, 2012,4(1):113-120.
[8] Chen MP, Chung FM, Chang DM, et al. Elevated plasma level of visfatin/pre-B-Cell colonyenhancing factor in patients with type 2 diabetes mellitus[J].J Clin Endocrinol Metab, 2006,91(1):295-299.
[9] 兰平,尹爱萍,申斐,等.2型糖尿病肾病患者血清内脂素水平的变化[J].西安交通大学学报(医学版),2012,33(6):736-738.
[10] 张丽丽,张晓乾,郭志新,等.内脂素与2型糖尿病及其大血管病变的关系[J].中国医药与临床,2012,12(6):727-729.
[11] 熊海亮,田凤石,雒瑢,等.初发2型糖尿病合并高血压患者血清内脂素、网膜素和TNF-α水平的变化[J].天津医药,2013,41(5):408-411.
[12] Moschen AR, Koser A, Enrich B, et al. Visfatin, an adipocytokine with proinflammatory and immunomodulating properties[J]. J Immunol, 2007,178(3): 1748-1758.
[13] 李影,闫鹏,董平栓.胰岛素抵抗的分子学机制[J].医学综述,2014,20(17):3122-3124.
[14] 李健,王怀国,刘泽玮,等.2型糖尿病肾病患者血清visfatin、apelin的变化及其临床意义[J/OL].中华临床医师杂志:电子版,2014,8(17):3107-3112.
[15] 刘树娇,唐灵,陈春莲,等.2型糖尿病肾病患者内脂素、同型半胱氨酸和高敏C-反应蛋白变化及临床意义[J].河北医药,2014,36(8):1125-1127.
[16] 陈永生.2型糖尿病视网膜病变与visfatin和SAA的相关性研究[J].国际眼科杂志,2012,12(1):39-42.
[17] 陶弢,刘伟.内脂素研究进展[J].中华内分泌代谢杂志,2007,23(1):92-94.

