左炔诺孕酮宫内缓释系统治疗子宫肌腺症的患者行超促排卵的结局分析
梁 舟,尹明茹,马 猛,朱 静,匡延平
(上海交通大学医学院附属第九人民医院 辅助生殖科,上海200011)
子宫腺肌症的特点是子宫内膜腺体和基质位于子宫内膜深处,引起局部或弥漫性增厚和子宫壁增大,可导致育龄妇女的生殖功能损害[1-3]。它是月经过多和痛经的重要原因。子宫腺肌病临床上与不孕有关,一系列的发病假说解释了这一相关性。左炔诺孕酮释放宫内节育系统(LNG-IUS)自1990年以来已在欧洲得到使用,后用于治疗子宫腺肌症。 LNG-IUS每天释放20微克左炔诺孕酮进入子宫腔,有效期5年[4-6]。 据报道,LNG-IUS通过控制症状,使子宫腺肌病妇女受益[6-10]。左炔诺孕酮在宫腔局部的浓度是血浆浓度的数百倍,利用这一特性,我们在曼月乐治疗子宫肌腺症的同时,进行超促排卵,探索是否得到有发育潜能的胚胎。为了阻断促排卵周期中的提前出现的或隐匿性的黄体生成素峰(LH serge),孕激素主导的卵巢刺激(PPOS)和冷冻胚胎移植已经成为我们中心的主要刺激方案[11,12]。自2015以来,一些诊断为子宫肌腺症的患者在我们的中心接受了PPOS+LNG-IUS治疗。在本文中,我们研究了LNG-IUS对卵母细胞回收或胚胎发育是否有负面影响。
1 材料与方法
1.1 临床资料
这项回顾性研究是在上海交通大学医学院第九人民医院辅助生殖科进行的。本研究经第九人民医院伦理评审委员会批准。所有患者均经阴道超声检查(TVS)诊断。对子宫腺肌病的超声诊断的主要标准是不对称的肌层增厚的外观,不规则的囊性区内的子宫肌层和线性条纹辐射[13]。在2015年1月至2017年12月期间,回顾性分析在我中心就诊的通过PPOS+LNG-IUS方案治疗的子宫肌腺症155个OPU周期,对照组仅PPOS治疗的267周期。纳入标准:①年龄<42岁;②采用促性腺激素(gonadtropin,Gn)联合安宫黄体(medroxyprogesterone acetate,MPA)的高孕激素超促排卵方案;③ 近3个月未口服或注射促排卵药物和未使用激素类药物。排除标准:①严重的内外科系统性疾病不适宜接受促排卵治疗及不能耐受妊娠患者;②有高泌乳素血症及产生高雄激素的其他内分泌疾病,如卵巢和肾上腺肿瘤等。
1.2 方法
1.2.1超促排卵 从月经周期的第3-5天开始口服安宫黄体酮(Medroxyprogesterone Acetate Tablets,MPA,浙江仙琚制药)10 mg/d,同时肌注尿促性素(Human Menopausal Gonadotropophin,HMG,上海丽珠)150 IU/d或225 IU/d,在促排卵治疗7-8天后,阴道超声检查卵泡的发育情况,并进行性激素水平的测定,根据卵泡的发育情况及血清中的激素水平,调整HMG及MPA的用量,每隔2-4天行阴道B超检测继续监测卵泡的发育情况及进行性激素水平的测定,当有1个以上卵泡的直径达到20 mm或者3个以上的卵泡直径达到18 mm以上时,注射短效促性腺激素释放激素激动剂(Gonadotropin Releasing Hormone agonist,GnRH-a,达必佳,德国辉凌)或者联合使用达必佳和绒促性素(Human Chorionic Gonadotrophin,HCG)或者单独注射HCG来诱发排卵,在诱发排卵34-36小时后在阴道超声引导下行取卵术。
1.2.2放置曼月乐环和随访 在研究组患者开始控制性超排卵(COH)前,放置LNG-IUS(拜耳先灵医药、柏林、德国)。LNG-IUS是一种 T 型塑料支架(纵臂内载有左炔诺孕酮 激素)的宫内节育器,在宫腔局部发生作用 ,促孕激素水平居较高水平 ,使子宫内膜腺体出现变薄萎缩情况,内膜上皮原有活性呈丧失显示 ,内膜血管出现退行性变化。
1.2.3体外受精及胚胎观察 取卵后根据精子情况或既往受精情况采用常规IVF/ICSI授精。 取卵后18 h观察受精情况,72 h观察胚胎卵裂情况。 根据胚胎原核评分、 发育速度及形态学参数等进行胚胎质量评分,将胚胎分为4级,Ⅰ级:卵裂球大小均匀,胞质均质透明,无碎片;Ⅱ级:卵裂球均匀,有碎片<20%;Ⅲ级:卵裂球大小不均等,碎片较多(20%-50%);Ⅳ级:卵裂球不均等,碎片>50%。取卵周期优质胚胎以玻璃化方法进行冷冻保存,剩余胚胎继续培养至囊胚后冷冻保存。

2 结果
2.1 基本资料
研究组和对照组年龄、不孕年限、体重指数、基础FSH水平、基础LH水平等差异无统计学意义(P>0.05),详见表1。
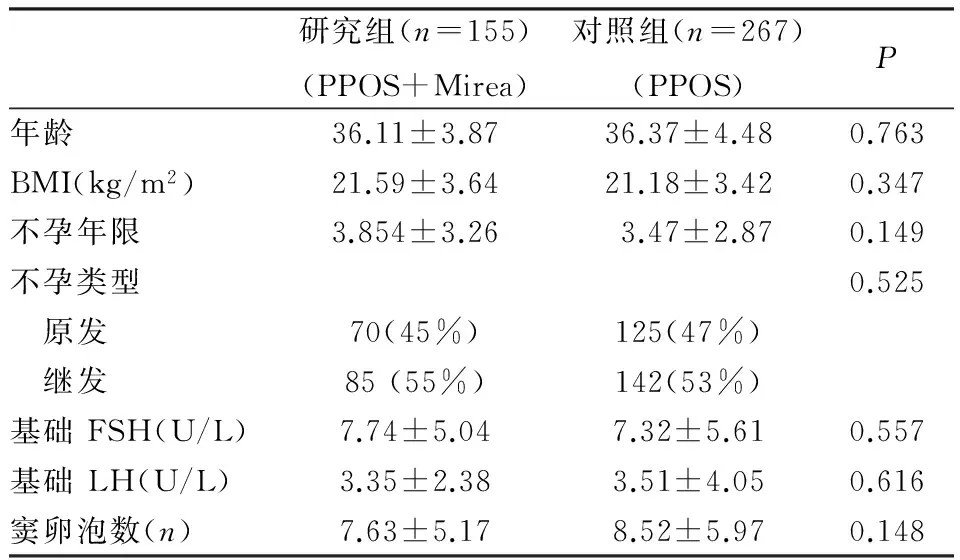
表1 基本资料
2.2 促排卵结局
Gn用药剂量、 Gn 用药天数、治疗结束时直径>14 mm 的卵泡数、 获卵数、成熟卵数、 正常受精卵数、优质胚胎数、有效胚胎总数等组间比较均无统计学差异(P>0.05),详见表2。
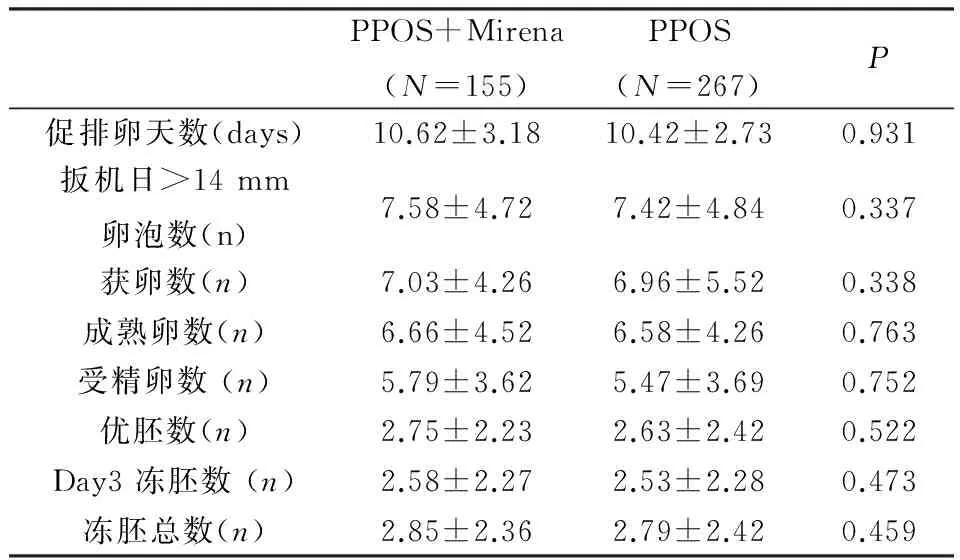
表2 促排卵治疗的结局
3 讨论
左炔诺孕酮宫内缓释系统(LNG-IUS,曼月乐)是一种高效的避孕方法,近年来的研究强调了它的非避孕效果,特别是在治疗子宫腺肌病方面,它与痛经和月经过多有关[13,14]。与口服孕酮相比,由于曼月乐中的LNG直接释放到子宫腔内,血浆LNG水平较低,因此,据报道,LNG-IUS的系统副作用较小。与口服孕酮相比,LNG-IUS在子宫内膜中的LNG浓度提高了近100倍[5],这使得LNG-IUS对子宫内膜具有深远的形态学和功能效应影响。在局部LNG暴露仅4周后,可观察到子宫内膜基质细胞的广泛蜕膜化和腺体和表面上皮的萎缩[15]。
目前常用的几种不同的避孕药具均释放左炔诺孕酮LNG,其中口服避孕药的LNG血浆浓度为1.5至2 ng/ml,皮下埋植避孕药的LNG血浆浓度为0.35 ng/ml[16,17],紧急避孕药的 LNG血浆浓度高达14.6 ng/ml[18],而曼月乐的LNG血浆浓度仅为0.1-0.2 ng/ml[19]。LNG的血浆浓度同时受到BMI(体质指数)的影响,从药代动力学角度看,LNG和其他脂溶性激素一样,分布于脂肪组织[19,20],所以在相同的药物剂量下,体重大的患者,其LNG血浆浓度相对较低。
左炔诺孕酮在宫腔局部的浓度是血浆浓度的数百倍,Nilsson等[21]研究表明,放置曼月乐环组与口服避孕药组相比,LNG的浓度梯度如下:在子宫内膜的浓度(药物质量/组织质量)分别为808±511 ng/g及3.5 ng/g,若表达为蛋白质匀浆中的比例,则为6937±3126 pg/g及44 pg/g。在子宫肌层的浓度分别为2.43±1.86 ng/g 及1.42±0.46 ng/g,若表达为蛋白质匀浆中的比例,则为34±23 pg/g及15±25 pg/g。在输卵管的浓度分别为1.8 ng/g及1.7 ng/g;在血浆的浓度分别为0.2±0.1 ng/ml及0.56±0.2 ng/ml。
我们的治疗策略是利用曼月乐环释放的LNG-IUS的浓度阶梯差极大,在LNG-IUS持续对子宫内膜及肌层局部强烈作用的同时,而卵巢局部的LNG-IUS浓度相对很低,而进行超促排卵和取卵的治疗。对于LNG-IUS组患者,Gn用药剂量、 Gn 用药天数、治疗结束时直径>14 mm 的卵泡数、 获卵数、成熟卵数、 正常受精卵数、优质胚胎数、有效胚胎总数等组间比较均无统计学差异(P>0.05)。我们的统计结果表明,LNG-IUS的使用对回收的卵母细胞和胚胎的发育没有影响,与对照组相比可以获得相同的胚胎结局。这表明利用左炔诺孕酮宫内缓释系统释放的LNG的浓度阶梯差极大的特性,在LNG持续治疗子宫肌腺症的同时,进行超促排卵和取卵的治疗,对促排卵结果无明显影响,可以得到有发育潜能的胚胎。
参考文献:
[1]Maheshwari A,Gurunath S,Fatima F,et al.Adenomyosis and subfertility:a systematic review of prevalence,diagnosis,treatment and fertility outcomes[J].Hum Reprod Update,2012,18(4):374.
[2]Tremellen K,Russell P.Adenomyosis is a potential cause of recurrent implantation failure during IVF treatment[J].Aust N Z J Obstet Gynaecol,2011,51(3):280.
[3]Salim R,Riris S,Saab W,et al.Adenomyosis reduces pregnancy rates in infertile women undergoing IVF[J].Reprod Biomed Online,2012,25(3):273.
[4]Cho S,Nam A,Kim H,et al.Clinical effects of the levonorgestrel-releasing intrauterine device in patients with adenomyosis[J].Am J Obstet Gynecol,2008,198(4):373.
[5]Nilsson CG,Haukkamaa M,Vierola H,et al.Tissue concentrations of levonorgestrel in women using a levonorgestrel-releasing IUD[J].Clin Endocrinol (Oxf),1982,17(6):529.
[6]Peng FS,Wu MY,Yang JH,et al.Insertion of the Mirena intrauterine system for treatment of adenomyosis-associated menorrhagia:a novel method[J].Taiwan J Obstet Gynecol,2010,49(2):160.
[7]Fong YF,Singh K.Medical treatment of a grossly enlarged adenomyotic uterus with the levonorgestrel-releasing intrauterine system[J].Contraception,1999,60(3):173.
[8]Bragheto AM,Caserta N,Bahamondes L,et al.Effectiveness of the levonorgestrel-releasing intrauterine system in the treatment of adenomyosis diagnosed and monitored by magnetic resonance imaging[J].Contraception,2007,76(3):195.
[9]Fedele L,Bianchi S,Raffaelli R,et al.Treatment of adenomyosis-associated menorrhagia with a levonorgestrel-releasing intrauterine device[J].Fertil Steril,1997,68(3):426.
[10]Champaneria R,Abedin P,Daniels J,et al.Ultrasound scan and magnetic resonance imaging for the diagnosis of adenomyosis:systematic review comparing test accuracy[J].Acta Obstet Gynecol Scand,2010,89(11):1374.
[11]Kuang Y,Chen Q,Fu Y,et al.Medroxyprogesterone acetate is an effective oral alternative for preventing premature luteinizing hormone surges in women undergoing controlled ovarian hyperstimulation for in vitro fertilization[J].Fertil Steril,2015,104(1):62.
[12]Massin N.New stimulation regimens:endogenous and exogenous progesterone use to block the LH surge during ovarian stimulation for IVF[J].Hum Reprod Update,2017,23(2):211.
[13]Nilsson CG,Luukkainen T,Diaz J,et al.Intrauterine contraception with levonorgestrel:a comparative randomised clinical performance study[J].Lancet,1981,1(8220 Pt 1):577.
[14]Varma R,Sinha D,Gupta JK.Non-contraceptive uses of levonorgestrel-releasing hormone system (LNG-IUS)-a systematic enquiry and overview[J].Eur J Obstet Gynecol Reprod Biol,2006,1(125):19.
[15]Orbo A,Vereide A,Arnes M,et al.Levonorgestrel-impregnated intrauterine device as treatment for endometrial hyperplasia:a national multicentre randomised trial[J].BJOG,2014,121(4):477.
[16]Orme ML,Back DJ,Breckenridge AM.Clinical pharmacokinetics of oral contraceptive steroids[J].Clin Pharmacokinet,1983,8(2):95.
[17]Sivin I,Lähteenmäki P,Ranta S,et al.Levonorgestrel concentrations during use of levonorgestrel rod (LNG ROD) implants[J].Contraception,1997,55(2): 81.
[18]Kives S,Hahn PM,White E,et al.Bioavailability of the Yuzpe and levonorgestrel regimens of emergency contraception:vaginal vs.oral administration[J].Contraception,2005,71(3):197.
[19]Seeber B,Ziehr SC,Gschlieβer A,et al.Quantitative levonorgestrel plasma level measurements in patients with regular and prolonged use of the levonorgestrel-releasing intrauterine system[J].Contraception,2012,86(4):345.
[20]JP G.The textbook of pharmaceutical medicine[M].6th ed.Oxford:Wiley-Blackwell,2009.
[21]Nilsson CG,Haukkamaa M,Vierola H,et al.Tissue concentrations of levonorgestrel in women using a levonorgestrel-releasing IUD[J].Clin Endocrinol (Oxf),1982,17(6):529.
——既能避孕又能治病的环

