一种HBV DNA定量检测试剂的准确性分析
孔祥沙,杨瑞锋,季颖,朱凌,张海莹,王震宇,魏来
[北京大学人民医院(北京大学肝病研究所),北京 100044]
HBV DNA是反映乙型肝炎病毒(hepatitis B virus,HBV)复制比较直接和可靠的指标[1]。定量检测血清或血浆中HBV DNA可作为急性或慢性HBV感染的诊断以及初始治疗方案制定的依据,其动态变化又可作为抗病毒疗效监测以及抗药性是否形成的重要指标[2]。同国际主流试剂相比,国产试剂在检测的敏感性和精密性上尚有较大差距[3]。罗氏公司生产的“Cobas AmpliPrep/Cobas TaqMan HBV Test”(Cobas Taqman HBV V2.0)检测系统采用全自动化操作,由于具有较高的敏感性、精确性、可重复性和较宽的检测范围而获得美国FDA批准[2,4-5]。而careHBV PCR Assay是临床应用较广泛的一种国产HBV DNA定量检测试剂,其第3代试剂产品(careHBV PCR Assay V3.0)相对之前产品改进了纯化技术,增加了检测用量,提高了敏感性和线性范围。本文以罗氏公司的Cobas Taqman HBV V2.0为参比试剂,评价careHBV PCR Assay V3.0试剂检测的准确性。
1 资料与方法
1.1 标本来源
收集2015年1~11月北京大学人民医院收治的HBV感染者的血清标本93份。所有患者均符合慢性乙型肝炎防治指南(2010)标准[6]:既往有乙型肝炎病史或HBsAg阳性超过6个月,现HBsAg和(或)HBV DNA仍为阳性者,可诊断为慢性HBV感染。该部分患者血清HBV DNA经Cobas Taqman HBV V2.0检测均为阳性,并且涵盖了HBV DNA载量的高、中、低值。同期收集健康体检者血清标本30份。所有标本-20℃冷冻保存。
1.2 主要试剂及仪器
主要试剂:第3代HBV DNA WHO国际标准品(购自英国国家生物制品检定所,编号:10/264,浓度赋值8.5×105IU/ml),稀释用阴性血清为HBsAg、抗-HCV、抗-HIV均为阴性的人AB型血清(天津川贝公司),careHBV PCR Assay V3.0试剂盒(深圳凯杰公司,检测上下限为 30×108~ 1.1×108IU/ml),Cobas TaqMan HBV V2.0试剂盒(德国罗氏诊断公司,检测上下限为20×108~ 1.7×108IU/ml),巢式 PCR 所用的 dNTP、Taq DNA Polymerase、PCR buffer和引物(美国赛默飞世尔公司)。主要仪器:LightCycler 480Ⅱ荧光定量PCR仪(德国罗氏诊断公司),Cobas AmploPrep/Cobas TaqMan 96型自动提取及扩增仪器(德国罗氏诊断公司),巢式PCR使用Mastercycler PCR仪扩增,Bio-Rad电泳仪以及凝胶成像仪鉴定PCR产物。
1.3 WHO标准品检测
用不含核糖核酸酶的灭菌双蒸水将HBV DNA WHO国际标准品配制成6份不同梯度浓度的样本,分 别 为 8.5×105、8.5×104、8.5×103、8.5×102、85及42.5 IU/ml。用careHBV PCR Assay V3.0定量检测HBV DNA载量,每份样本重复检测3次,计算均值。
1.4 临床标本检测
用careHBV PCR Assay V3.0和Cobas Taqman HBV V2.0同时对收集的93份HBV感染者标本和30份健康者标本进行HBV DNA定量检测。对于超出试剂盒检测上限的标本,使用HBV阴性人血清将原始标本稀释后重复检测,用所得结果乘以稀释倍数进行校正。
1.5 HBV DNA基因型的测定
采用巢式PCR扩增漏检阳性标本中的HBV S区[7],巢式PCR外引物正向:5'-AGGACCCCTGCTCGT GTTAC-3',反向:5'-ACATACTTTCCAATCAATAG-3';内引物正向:5'-GATGTGTCTGCGGCGTTTTATCAT-3',反向 :5'-ACATATCCCATGAAGTTAAG-3'。两轮PCR 循环参数相同,94℃ 5 min;94℃ 30 s,56℃ 30 s,72℃ 45 s,共35个循环;72℃ 7 min。制备12 g/L琼脂糖凝胶电泳用于鉴定PCR产物。将符合标准的PCR产物送往北京诺赛公司测序,并与标准序列比对,从而判断其基因型。
1.6 统计学方法
所有数据采用SPSS 19.0软件分析,所有图形采用软件GrapPad Prism 5绘制。将HBV DNA载量换算成对数形式(Log10IU/ml)进行统计学分析,计量资料以均数±标准差(±s)表示。两组数据进行Pearson相关分析,比较采用配对t检验,P<0.05为差异有统计学意义。
2 结果
2.1 careHBV PCR Assay V3.0检测WHO国际标准品的结果
对用careHBV PCR Assay V3.0检测配制的6份不同梯度浓度WHO HBV DNA国际标准品的结果与标准品理论值进行相关性分析,两者存在线性相关(R2=0.993,P=0.000)。见图 1。
2.2 2种试剂HBV DNA检测结果的相关性分析
Cobas Taqman HBV V2.0检测HBV DNA结果阳性的93份标本中,careHBV PCR Assay V3.0检测68份阳性,25份阴性。将2种试剂检测结果均阳性的68份标本进行相关性分析,结果呈线性相关(R2=0.947,P=0.000)。见图 2。
2.3 2种试剂HBV DNA检测结果的一致性分析
将2种试剂HBV DNA检测结果均阳性的68份标本进行一致性分析。数据显示95%一致性界限以外有2份标本(3.22%);一致性界限范围内,Cobas Taqman HBV V2.0与careHBV PCR Assay V3.0 HBV DNA检测结果的对数均值分别为(5.09±2.14)Log10IU/ml和(4.63±2.32)Log10IU/ml,经配对t检验,2种试剂HBV DNA检测结果差异无统计学意义(t=1.204,P=0.231)。2种检测试剂对30份健康体检者标本的检测结果均为阴性。见图3。
2.4 漏检标本分析及基因型检测
careHBV PCR Assay V3.0检测阴性的25份标本中,其中11份标本Cobas Taqman HBV V2.0检测结果<30 IU/ml(careHBV PCR Assay V3.0检测下限);而其余14份标本则为漏检。漏检标本中13份Cobas Taqman HBV V2.0检测结果位于30~2 000 IU/ml间;1份>2 000 IU/ml。采用巢式PCR扩增漏检标本的HBV S区,直接测序法测定基因型,其中1份标本经Cobas Taqman HBV V2.0检测HBV DNA结果为(7.79×102IU/ml)为C型基因型,其测序结果见图4。其他漏检标本因标本量不足或病毒载量较低等原因未能成功检测其基因型。
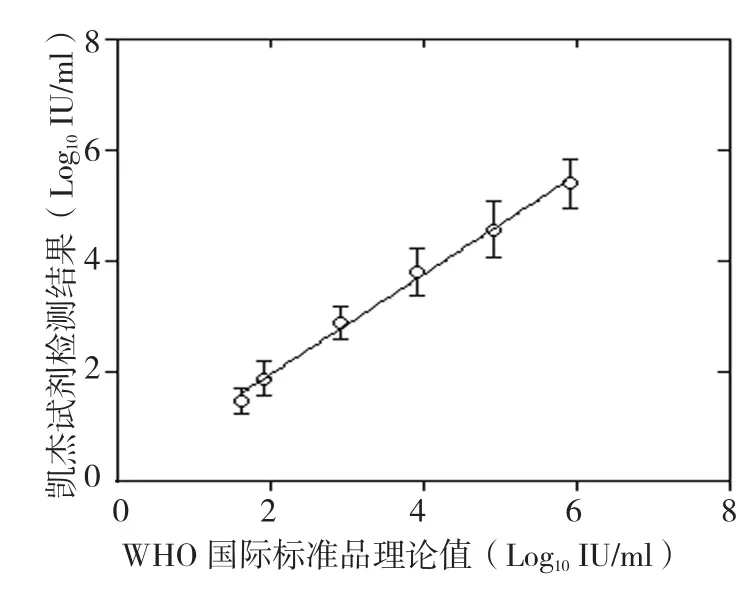
图1 WHO国际标准品结果
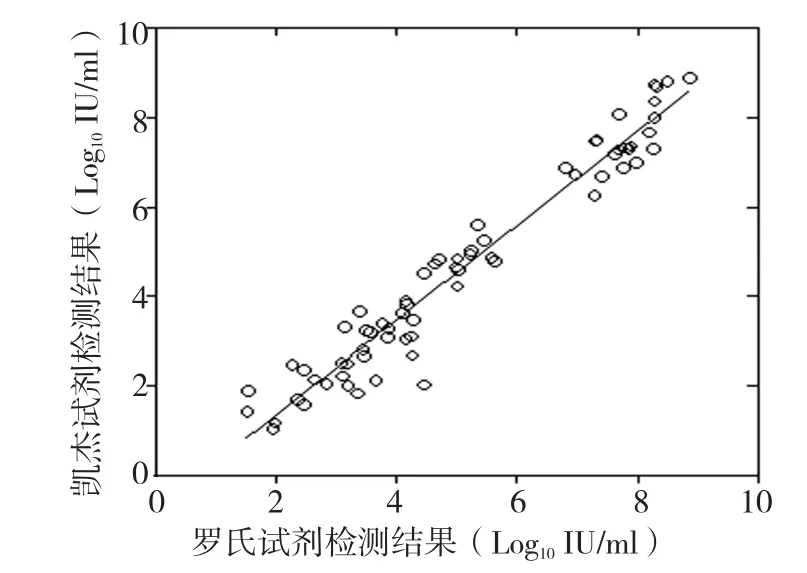
图2 2种试剂HBV DNA检测结果的相关性分析
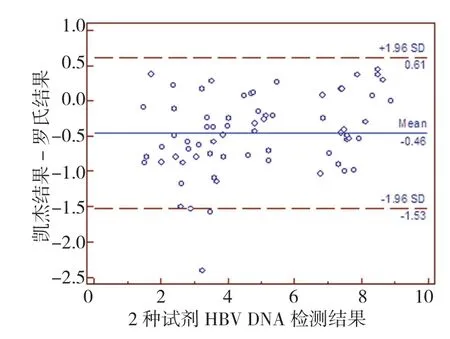
图3 2种试剂HBV DNA检测结果的一致性分析
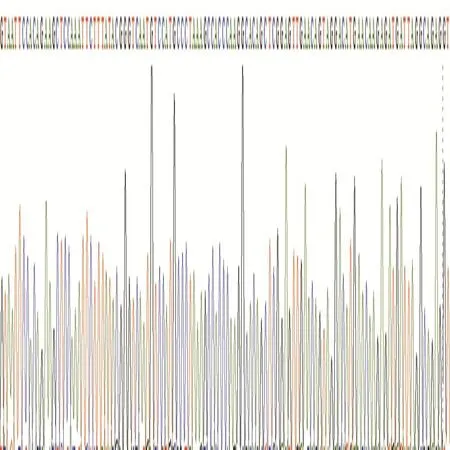
图4 漏检标本的测序结果
3 讨论
目前定量检测HBV DNA的方法很多,文献报道国产试剂与进口试剂有较好的相关性,比如凯杰试剂和美国Digene公司生产的Hybrid Capture-Ⅱ HBV DNA试剂[8]、国产实时荧光定量试剂和Cobas Taqman HBV V2.0[9]、以及 careHBV PCR Assay V2.0 和 Cobas Taqman HBV V1.0[10]等都有良好的相关性。本研究采用改良后的careHBV PCR Assay V3.0与Cobas Taqman HBV V2.0进行比较,结果显示careHBV PCR Assay V3.0与Cobas Taqman HBV V2.0具有良好的相关性。careHBV PCR Assay V3.0检测HBV DNA WHO国际标准品的实测值与理论值存在线性相关,且能检测到WHO国际标准品浓度为42.5 IU/mL的标本。但是,在分析2种试剂检测阳性标本的一致性时,尽管两组检测结果差异无统计学意义,但careHBV PCR Assay V3.0检测结果稍低于Cobas Taqman HBV V2.0检测结果均值,提示careHBV PCR Assay V3.0尽管具有较好的线性范围和较高的敏感性,但是其检测的准确性尚与Cobas Taqman HBV V2.0存在差距。
本研究检测结果发现,小于careHBV PCR Assay V3.0检测下限(30 IU/ml)的11份标本未检出。在低病毒载量(30~2 000 IU/ml)标本中,careHBV PCR Assay V3.0检测结果的漏检率,提示careHBV PCR Assay V3.0检测HBV DNA低病毒载量的敏感性比Cobas Taqman HBV V2.0低。表明用careHBV PCR Assay V3.0检测结果为阴性时,其实很多病例并非真正完全清除病毒,而是由于其检测系统分析敏感性不足,尚不能检出残留的HBV DNA,还需进一步提高敏感性。在careHBV PCR Assay V3.0试剂漏检的样本中有1份标本基因型为C型,由此可见careHBV PCR Assay V3.0对基因型为C型的HBV DNA检测可能存在漏检。当然,由于样本数量少,尚需进一步增加样本量验证。
国内研究[11]也证实了国产试剂与进口试剂存在差距,研究采用德国Qiagen公司的Anus HBV DNA荧光定量PCR试剂和国内生产的3种HBV DNA荧光定量PCR试剂,对HBV感染者的血清标本进行平行检测,并将结果按不同HBV DNA拷贝水平进行分组分析,研究发现不同试剂对高病毒载量标本的检测结果差异无统计学意义,而病毒载量低的标本则差异有统计学意义,且在低拷贝样本中,凯杰试剂与Anus试剂的检测结果相关性极差,且出现明显的漏检率。因此很多慢性乙型肝炎患者在抗病毒治疗过程中,以及低病毒载量的患者,国产试剂就不能很好地监测病毒载量的变化,也不能很好地指导治疗,以及判断停药的终点。
careHBV PCR Assay V3.0虽然通过改进纯化技术,加入磁珠,加入内标,增加标本用量,提高了检测的敏感性,增宽了检测线性范围,但是与实现全自动化检测与分析的Cobas Taqman HBV V2.0相比,仍有待进一步提高。
参 考 文 献:
[1]CIOTTI M, MARCUCCILLI F, GUENCI T, et al. Evaluation of the Abbott RealTime HBV DNA assav and comparison to the Cobas AmpliPrep/Cobas TaqMan 48 assay in monitoring patients with chronic cases of hepatitis B[J]. J Clin Microbiol, 2008, 46(4):1517-1519.
[2]CHEVALIEZ S, BOUVIER-ALIAS M, LAPERCHE S, et al.Performance of the Cobas AmpliPrep/Cobas TaqMan real-time PCR assay for hepatitis B virus DNA quantification[J]. J Clin Microbiol, 2008, 46(5): 1716-1723.
[3]杨瑞锋, 魏来. 乙型和丙型肝炎病毒核酸检测技术及进展[J].中华检验医学杂志, 2010, 33(5): 476-480.
[4]HOCHBERGER S, ALTHOF D, GALLEGOS DE SCHROTT R, et al. Fully automated quantitation of hepatitis B virus (HBV) DNA in human plasma by the COBAS AmpliPrep/COBAS TaqMan system[J]. J Clin Virol, 2006, 35(4): 373-380.
[5]ALLICE T, CERUTTI F, PITTALUGA F, et al. COBAS AmpIiPrep-COBAS TaqMan hepatitis B virus (HBV) test: a novel automated real-time PCR assay for quanti fi cation of HBV DNA in plasma[J].J Clin Microbiol, 2007, 45(3): 828-834.
[6]中华医学会肝病学分会, 中华医学会感染病学分会. 慢性乙肝肝炎防治指南(2010年版)[J]. 中华肝病杂志, 2011, 19(1):13-24.
[7]YANG R, CONG X, XU Z, et al. INNO-LiPA HBV genotyping is highly consistent with direct sequencing and sensitive in detecting B/C mixed genotype infection in Chinese chronic hepatitis B patients and asymptomatic HBV carriers[J]. Clin Chim Acta, 2010,411(23-24): 1951-1956.
[8]王豪, 陶其敏, 吴娟, 等. 两种乙型肝炎病毒DNA定量检测方法的比较与评价[J]. 中华检验医学杂志, 2002, 25(5): 318-320.
[9]SHI M, ZHANG Y, ZHU Y H, et al. Comparison of real-time polymerase chain reaction with the COBAS Amplicor test for quantitation of hepatitis B virus DNA in serum samples[J]. World J Gastroenterol, 2008, 14(3): 479-483.
[10]张海莹, 季颖, 朱凌, 等. 两种HBV DNA检测试剂的比较[J].中华检验医学杂志, 2011, 34(5): 459-464.
[11]李美忠, 王敏, 乐晓华, 等. 四种HBV DNA荧光定量PCR试剂比较及其结果分析[J]. 中华实验和临床感染病杂志, 2008,2(1): 7-12.

