“银树镀铜”微科技项目的设计与教学
凌一洲 陈静 陈鹏文 程鹏


摘要: 江苏省微科技课程基地开展的创新实践项目,具有小切口、低成本、易开发、有价值的特点,指向化学核心素养的培育,适合更普遍的中学生。在“银树镀铜”项目探究中,以“银树镀铜”现象为选题,多次提出假设并设计实验验证,确定了生成物的成分,解释了异常现象产生的原因,构建了反应的原电池模型,化解了认知冲突。
关键词: 核心素养; 微科技项目; 原电池; 银树镀铜; 实验探究
文章编号: 1005-6629(2018)11-0070-03中图分类号: G633.8文献标识码: B
2013年,江苏省南菁高级中学开始微科技课程的探索实践;2017年,学校被省教育厅命名为江苏省微科技课程基地。依托基地开展的微科技项目,是指在教师指导下,由学生完成的小切口、低成本、易开发、有价值的创新实践项目。
化学微科技项目主要以实验为选题,指向化学学科核心素养的培育。项目不照搬陈旧的选题,而是从现实中直接发现和提出;没有现成的实验方案,要根据探究目的自行设计并优化;无法提前预知结论,要学生提出可能的假设,在实验中收集证据、解释证据。笔者以“银树镀铜”实验项目为例,原汁原味地展示微科技项目层层深入的探究过程。
1 项目选题
以下是一个趣味实验: 在浸有硫酸銅溶液的滤纸上放一片锌片,可发生置换反应,生成向四周扩散的树枝状的铜单质(铜树)[1]。
笔者用类似的方法制作银树: 在浸有0.5mol/L硝酸银溶液的滤纸上放一片铜片,再在滤纸表面覆盖一层塑料膜(防止溶液蒸发)并避光保存。反应几分钟后,滤纸上生成银白色树枝状物质(银树),且银树周围溶液变蓝。
实验结束后,笔者将反应装置留下,过了两三天再来处理,却有了意外发现: 见图1,铜片上生长出的银树从银白色变成了红色(图1左图),在显微镜放大下更为明显(图1右图)。
这与笔者的预期不符,是个异常现象。笔者重做了实验,发现现象可以重复,而非偶然。虽然检索了文献,但未发现相关报道。出于好奇,笔者将其作为微科技项目的选题,做了如下探究。
2 项目探究一
2.1 探究目的
探究滤纸上生成的红色树枝状物质的成分。
2.2 探究过程
分析: 由颜色判断,树枝状物质表面是铜,但内部物质无法确定。
猜测: (1)树枝状物质可能是实心铜树;(2)树枝状物质可能是银树镀铜。
验证: 树枝状物质内部成分决定了整体形状,因此笔者分别在滤纸上制作了铜树和银树,然后在显微镜下观察形状,并与未知树枝状物质对比。
结果: 未知树枝状物质的形状与银树一致。
2.3 探究结论
滤纸上生成的红色树枝状物质的成分是银树镀铜。
3 项目探究二
3.1 探究目的
探究银树上生成铜镀层的原因。
3.2 探究过程
分析: 按照常规的理解,铜与硝酸银反应只生成银和硝酸铜,生成的银单质表面不会再生成铜。这个异常现象可能是受杂质干扰造成的。
猜测: 铜片含有铁等(更活泼的金属)杂质,与硝酸铜反应生成铜单质。
验证: 剪下一小块铜片和铁片,用胶带粘连,放入硝酸银溶液中,观察现象。
结果: 铜片和铁片上同时生成银单质,且铁片上生成银单质的速率快。
3.3 探究结论
即使铜片含有铁等杂质,也应该是杂质先与硝酸银反应,不会形成银树镀铜的现象,故猜测不成立。探究目的没有达到。
4 项目探究三
4.1 探究目的
改变猜想,重新验证,继续探究银树上生成铜镀层的原因。
4.2 探究过程
分析: 原反应体系中存在铜、银、硝酸铜、硝酸银等物质,但不一定都参与了镀铜的反应。如果能排除多余条件的干扰,就更容易探究反应的本质。
猜测: 只有铜、银、硝酸铜(铜离子)才与镀铜反应有关。
验证: 剪下长条状的铜片,将其一半浸入硝酸银溶液中约5分钟,使铜片一半镀银。取出铜片后,先在蒸馏水中洗去硝酸银残留,再放入0.5mol/L硝酸铜溶液中,观察银镀层表面现象。
结果: 铜片镀银时,银镀层呈灰黑色。浸入硝酸铜(或硫酸铜)溶液后,银镀层表面没有红色物质生成。
4.3 探究结论
银镀层颜色发黑说明本身就比较粗糙,所以即使生成了铜镀层,其颜色也可能是黑色的。本次实验既无法验证猜测,也无法推翻猜测,探究的目的没有达到。
5 项目探究四
5.1 探究目的
重新设计方案,再次验证“项目探究三”中的猜想,继续探究银树上生成铜镀层的原因。
5.2 探究过程
分析: 将反应过程继续抽象,可以把银镀层直接换成表面光滑平整的银片。
验证: 剪下一小块铜片和银片,用胶带粘连,完全浸没在0.5mol/L硝酸铜溶液中,观察现象(由于常温下反应较慢,可以用电磁炉加热至约80℃)。
结果: 如果不加热,1小时后银片边缘会微微泛红,铜片表面失去光泽。如果加热,15min后银片表面就会变红。
5.3 探究结论
由于铜片、银片、硝酸铜(铜离子)两两之间都无法反应,所以镀铜的反应是三者共同作用的结果。铜片与银片相互接触时,可以与硝酸铜溶液反应,在银片上生成铜镀层(与原本的异常现象吻合)。
6 项目探究五
6.1 探究目的
构建铜片、银片、硝酸铜(铜离子)三者共同存在时发生反应的模型。
6.2 探究过程
分析: 反应经过“项目探究五”的简化,已经排除了其他多余条件。剩下的反应在形式上符合原电池的特征。
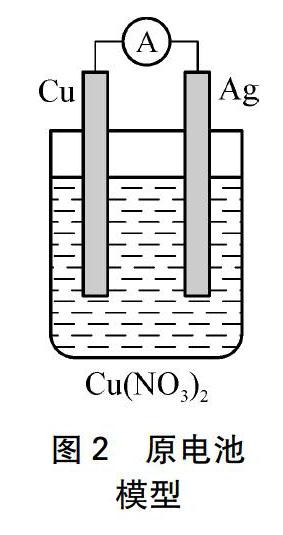
建模: 银树与铜片在硝酸铜环境中构成了如图2所示的原电池(-)Cu(s)|Cu(NO3)2(aq)|Ag(s)(+),铜片相当于负极,银树相当于正极,硝酸铜溶液相当于电解质。反应时,铜电极上的铜原子变为铜离子进入溶液,溶液中的铜离子再变为铜原子沉积在银电极表面。
解释: 负极上,铜单质表面的铜原子失去电子,变成铜离子进入溶液,发生电极反应:
正极上,溶液中的铜离子得到电子,变成铜原子附着在银片上,发生电极反应:
总反应是:
负极上,铜原子从铜片表面脱离时,发生了金属键的断裂;正极上,铜原子附着在银片表面时,铜原子插入金属银的晶格,形成新的金属键。由于旧的金属鍵键能小,新的金属键键能大,所以造成了2个电极的电势差,在热力学上表现为自发反应。当银片表面镀了一层铜后,反应即停止。
7 认知冲突的化解
7.1 化解与常规习题的冲突
绝大多数中学生一开始都认为这个反应不可能发生,甚至一些习题也认为同类反应(例如以铜片、锌片为电极,硫酸锌为电解质)不能构成原电池,理由是: 不能发生氧化还原反应,没有化学能转化为电能。
但实际上,这个实验发生了氧化还原反应,而且反应前后有化学键(金属键)能量的差异。造成认知冲突的关键在于,中学生通常把合金看作混合物,把铜原子从铜片转移到银片表面视为物理变化,没有考虑金属键的断裂与生成[2]。
7.2 化解与传统实验的冲突
传统的铜丝与硝酸银反应的实验现象只是铜丝表面变白,不会有银树镀铜的现象,与本实验的异常现象不符。推测可能有以下原因: 一是试管中的硝酸银通常来不及被反应完,而且生成的银树容易受到重力和人为扰动而被破坏,总之来不及等到铜镀层生成。二是因为试管中生成的银树表面相对粗糙,即使生成铜,也可能呈黑色,不便于观察。
8 结束语
通过对异常现象的不断探究,笔者最终解释了该现象。在此过程中,实验者加深了对电势差的理解: 产生电势差的原因是多样的,除了常规化学反应前后的能量差和温度差、浓度差,甚至铜原子存在于2片电极上的金属键键能差也能造成电势差。
化学微科技项目在目标定位上注重化学核心
素养的培育。如表1所示,在完成项目的过程中,多种核心素养得到了体现。
如今,许多中学生都参与了课外科研项目,各种高精尖(高级、精密、尖端)的化学项目在科技竞赛上屡见不鲜[4]。但笔者认为,高精尖项目只适合极少数的拔尖人才,各中学不应该盲目追求。对广大的中学生来说,小低易(小切口、低成本、易开发)的微科技项目同样具有研究价值和育人价值,值得推广应用。
参考文献:
[1]许燕红,杨吉祥,姚茜芸等.影响铜树生长因素的探究[J].化学教育, 2015, 36(23): 64~67.
[2]Bieron J.F. The “Golden Penny” Demonstration: An Explanation of the Old Experiment and the Rational Design of the New and Simpler Demonstration [J]. Journal of Chemical Education, 1995,72(5): 386~388.
[3]凌一洲,程鹏.有价值的异常现象“微科技”课题的教学实施[J].化学教学, 2018,(3): 34~37.
[4]中国科协青少年科技中心.第三十一届全国青少年科技创新大赛获奖作品集[M].北京: 科学普及出版社, 2016.

