(U)HPLC及LC/MS技术在枣果功能性成分分离分析中的应用
田 晶 ,李存满 ,李巧玲
(1.河北科技大学,河北省分析测试研究中心,河北石家庄 050018;2.河北科技大学生物科学与工程学院,河北石家庄 050018)
枣(Ziziphus jujubaMill.)为鼠李科枣属的药食同源植物,在我国具有悠久的种植历史,主产于河北、河南、山东、陕西等诸多地区[1]。《本草纲目》记载:枣味甘、性温,能补中益气、养血生津。枣中含有丰富的营养成分,不仅含有糖类,还含有三萜酸类、环核苷酸类、黄酮类、脂肪酸类、蛋白质、氨基酸类、维生素类等多种化学成分[2],具有抗癌、降血压、降低胆固醇、保肝护肝、预防骨质疏松、预防心血管疾病、预防胆结石等多种功能[3]。
(超)高效液相色谱 [Ultra high performance liquid chromatography,(U)HPLC]及液质联用(Liquid chromatography/mass spectrumLC/MS)技术在复杂体系如食品、中药材等的分离分析中应用越来越广泛,尤其是LC/MS技术,将色谱技术的高分离能力与质谱技术的高灵敏和结构解析能力有机结合起来,其强大的定性定量能力在复杂体系中的应用越来越受到关注。
目前,对于枣的物质基础的研究还很欠缺,从枣的复杂体系中提取并分离分析其功效成分引起更多科研人员的关注。(U)HPLC及LC/MS技术在枣复杂体系的分离分析过程中起着重要的作用,本文主要对该技术在分离分析枣的功效成分研究方面的应用进行简要的综述。
1 应用(U)HPLC及LC/MS技术来提取枣果中的三萜酸类
枣果中含有丰富的三萜酸类化合物,其中研究最多的是齐墩果酸、熊果酸和白桦脂酸。研究表明,齐墩果酸不仅对肝脏具有保护作用,而且具有抑制艾滋病病毒的作用[4,5]。熊果酸对恶性肿瘤细胞具有抑制作用,能抵抗诱癌、致癌物,并且具有较高的安全性[6]。白桦脂酸对脑瘤、神经外胚层瘤、白血病等恶性肿瘤细胞有抑制作用[7]。
目前,提取三萜酸类化合物的主要方法有热回流、冷浸、超声[8-10]等。也有些研究采用甲醇或乙醇等有机试剂通过超声的方法来提取三萜酸[10-13],提取过程中可以通过70~80℃加热的方式,也可以加入纤维素酶来提高提取率[14],然后用大孔树脂方法进行分离[15],该法是一种比较简便、有效富集三萜酸的方法。
分析枣中三萜酸的方法多采取HPLC法。对新疆若羌灰枣不同等级样品中齐墩果酸、熊果酸和白桦脂酸的含量进行分析,发现其含量与品质之间不存在明显相关性。由于三萜酸呈弱酸性,通过HPLC法测定齐墩果酸、熊果酸和白桦脂酸时,可用磷酸盐体系、磷酸、冰醋酸调整流动相的酸碱性,选择甲醇-水体系,梯度洗脱方式[10],但该方法受流动相影响较大,检测灵敏度相对较低。三萜酸类物质紫外吸收极弱,可以利用蒸发光散射检测器(ELSD)对其进行定量测定,得出的峰形对称,杂峰较少,且灵敏度高;但ELSD也有其缺点,容易因气体体积流量过低导致尖峰信号或噪音信号[11]。不同的色谱柱,对物质分离能力有一定的差别,苗利军等[12]用4种色谱柱分离枣中三萜酸,比较得出C18型色谱柱优于CN型,反相色谱优于正相色谱,250mm长的BDS C18色谱柱优于200mm长BDSC18色谱柱,即采用较长色谱柱有利于提高三萜类物质分离效果。
HPLC法进行含量测定存在基线不理想、仅仅通过保留时间来确定待测成分可能造成误判的风险等问题;而利用LC/MS分析技术,不受基线的影响,可以很好地排除其他物质干扰,大大提高对枣等复杂体系中待测成分的定性定量分析能力[13]。Guo等人[16]通过UHPLC-MS/MS法更加精确地定性分析出枣中含有多种三萜酸以及在不同时期三萜酸的含量不同,发现三萜酸作为枣的质量指标,在9月份收获最为合适。关于近几年 (U)HPLC及LC/MS技术分离枣中三萜类物质应用见表1(见下页)。
2 应用(U)HPLC及LC/MS技术提取枣果中的环核苷酸类
环核苷酸及其衍生物有10多种,其中有重要生物活性的主要为环磷酸腺苷(cAMP)和环磷酸鸟苷(cGMP)。刘世军报道,枣果中的cAMP和cGMP含量是所有已测动植物材料中最高的,鲜重分别为100~500nmol/g和30~40nmol/g[1]。cAMP和cGMP已被公认为两种具有反向调节作用的第二信使物质,共同参与多种生理生化过程的调节,并可用于基因转录,影响蛋白质合成,枣中cAMP是枣果中最重要的生物活性物质,不仅能调节细胞内的物质代谢,还能降血糖、抑制癌细胞生长等显著作用[17,18]。简便快速地对枣中天然cAMP和cGMP的提取及检测对进一步开发枣产品、推动医疗保健发展具有重要意义[19]。
目前多采用冷浸超声、热回流、索氏提取、有机溶剂提取等方法来提取环核苷酸类物质[20],其中大多以水为提取溶剂[21,22],这样较有机溶剂提取更具安全和环保性能。分离方法采用最多的是大孔吸咐树脂法,不同型号的大孔树脂其作用的机理不同,可以除去多种杂质,达到分离纯化的目的[18,23]。
传统检测环核苷酸方法有纸层析色谱、薄层色谱法、竞争蛋白法以及酶联免疫法等,这些方法存在检测时间长、灵敏度不高、重复性差、人为实验操作误差大等问题,而HPLC法较之更具有灵敏度高、准确度高及精确度好的特点。用HPLC法测定壶瓶枣中的cAMP含量高于大龙枣中cAMP的含量[24],蒋励博[25]采用UPLC法测得了枣中cAMP实际提取量,与理论值相差不大。除了用常见的反相色谱法测定不同枣品种中cAMP的含量外[21],还可以采用亲水作用液相色谱(HILIC)法测定枣中环核苷酸含量,HILIC具有良好的精密度、重现性和稳定性[26]。
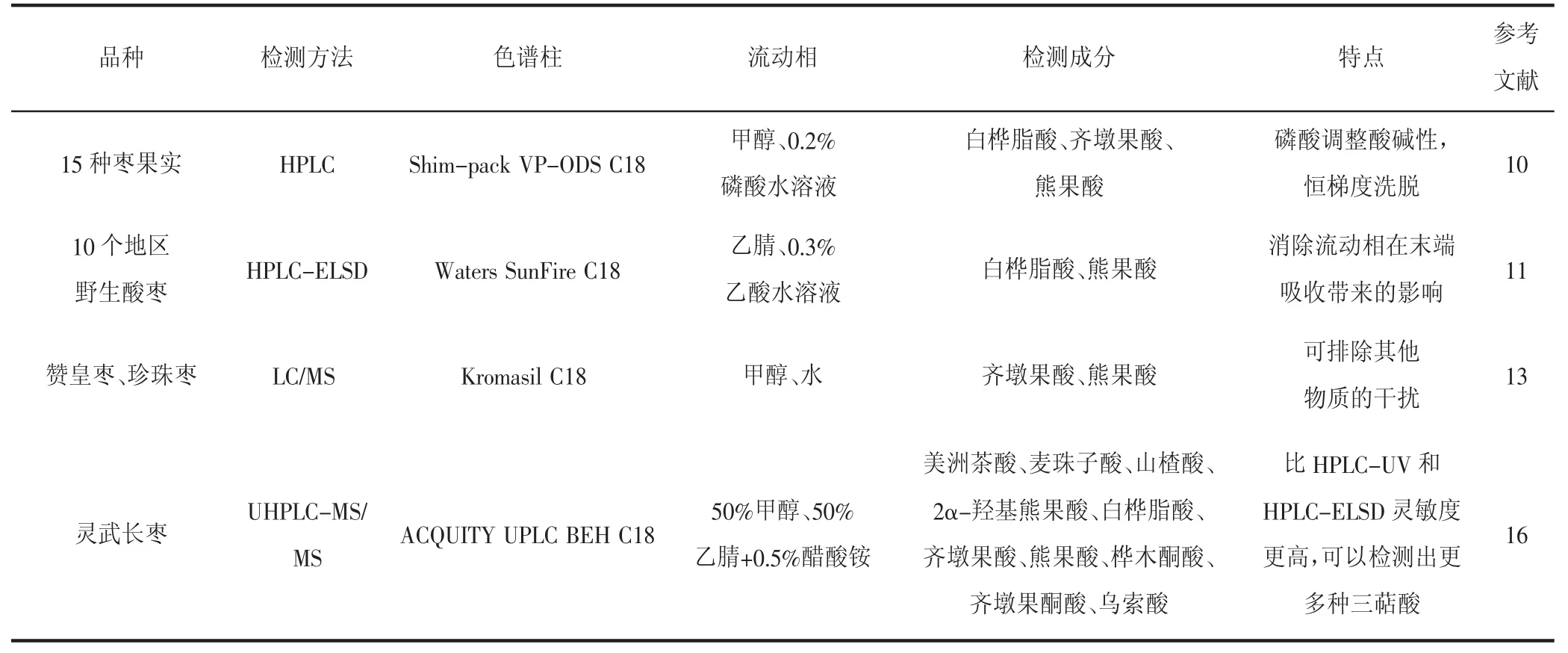
表1 (U)HPLC及LC/MS技术分离分析枣中三萜类物质应用Table 1 The application of(U)HPLC and LC/MS technology in separation of three terpenoids in jujube
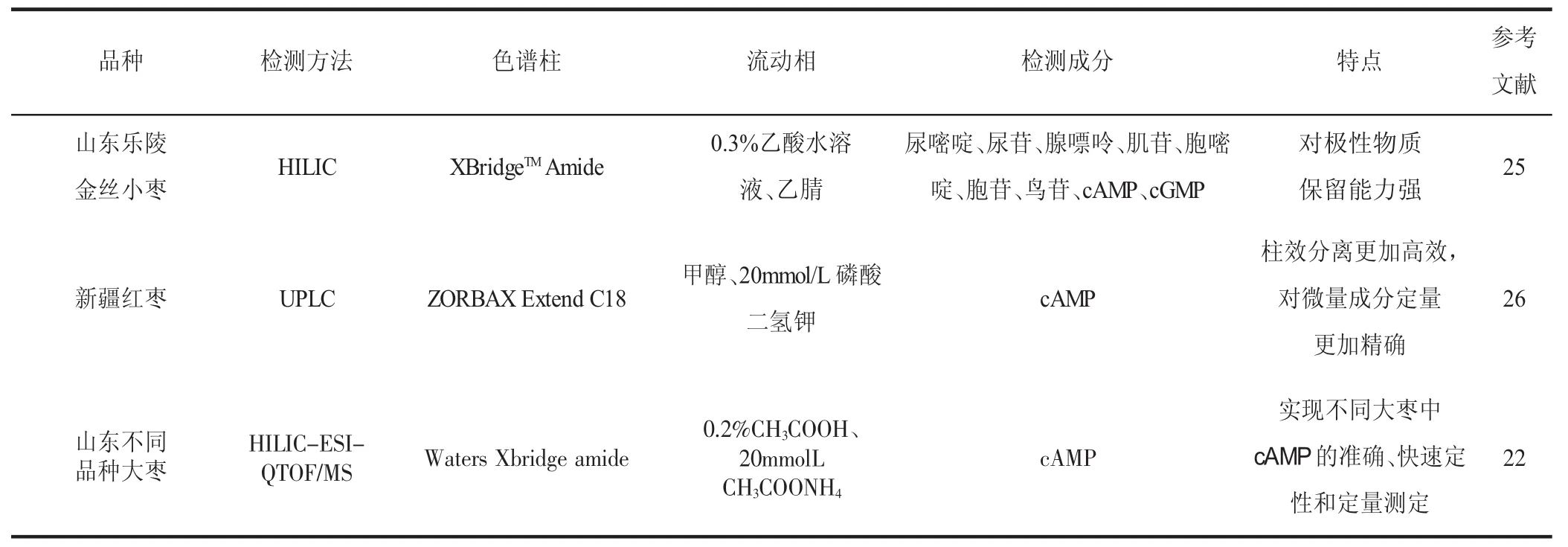
表2 (U)HPLC及LC/MS技术分离分析枣中核苷类物质应用Table 2 The application of(U)HPLC and LC/MS technology in separation of nucleosides in jujube
关于近几年 (U)HPLC及LC/MS技术分离枣中环核苷酸应用见表2。LC/MS技术用来分析枣果中的复杂成分是十分有利的,赵恒强等[22]建立了亲水作用液相色谱-电喷雾离子源-四极杆飞行时间质谱(HILIC-ESI-QTOF/MS)定性、定量分析枣中cAMP的方法,该方法具有很好的分离度、灵敏度,可以实现不同枣中cAMP的准确、快速定性和定量测定。Q-TOF-MS高分辨质谱可以推断出cAMP的分子式,对于化合物的结构解析是非常有利的。
3 应用(U)HPLC及LC/MS技术提取枣果中的黄酮类
黄酮类化合物是枣的主要化学成分之一,枣中总黄酮对油脂具有抗氧化作用,并且能清除羟自由基[27];同时,黄酮类化合物对血管有舒张作用,拮抗血小板活化因子[1]。随着人们对黄酮类化合物的深入研究,学者们还发现其具有抗炎、抗病毒、镇静镇痛以及调节免疫、抗肿瘤等重要作用[28]。
目前,大枣中黄酮提取方法有超声提取法、回流提取法等[29,30],还可以通过加入乙酸乙酯进行冰浴均质后再提取[31],考虑到绿色环保、安全技术方面,可以用环糊精作为提取剂提取黄酮类化合物[32],分离黄酮类多用双向纸层析、薄层层析及柱层析,还可运用QuEChERS法达到快速分离纯化的目的[33]。
国内外对黄酮化合物的提取分离研究很多,但对枣中黄酮的提取分离研究较少[34]。Zhao等[35]通过HPLC法同时测定了7种枣中根皮苷、儿茶素、没食子酸、绿原酸和咖啡酸,并测得这些酚类物质的含量与抗氧化能力呈正相关。李喜悦[36]利用HPLC法同时检测出14种不同枣叶中槲皮素-3-O-洋槐糖苷、芦丁、槲皮素-3-O-β-D-葡萄糖苷、山奈酚-3-O-芸香糖苷、槲皮素-3-O-α-L-阿拉伯糖-(1→2)-α-L-鼠李糖苷5种黄酮的含量。
袁亚娜[37]将不同时间出峰的液相馏分收集起来再分别进行质谱分析,推测出枣中存在双黄酮类化合物。师仁丽等[29]采用二极管阵列检测器(DAD)-HPLC和LC/MS技术对金丝小枣中黄酮类物质进行分析和鉴别,并测得金丝小枣中含有杨梅素、芦丁、槲皮素、异鼠李素4种黄酮类物质。LC/MS技术在黄酮类分析中的应用较枣中其它物质应用更为广泛。关于近几年(U)HPLC及LC/MS技术分离枣中黄酮类物质应用见表3。
4 应用(U)HPLC及LC/MS技术提取枣果中的糖类
枣多糖是枣中重要的生物活性物质,鲜枣的总糖含量大约为30%~40%,水溶性糖以D-葡萄糖为主。阿拉伯糖、核糖、甘露糖、半乳糖、鼠李糖和葡萄糖等共同组成大枣中的低聚糖[1]。多糖类被证明具有免疫调节、抗氧化、抗衰老、补血养血、抗肿瘤作用等功能,且其对进入细胞内病毒的繁殖也有一定的抑制作用[38,39]。
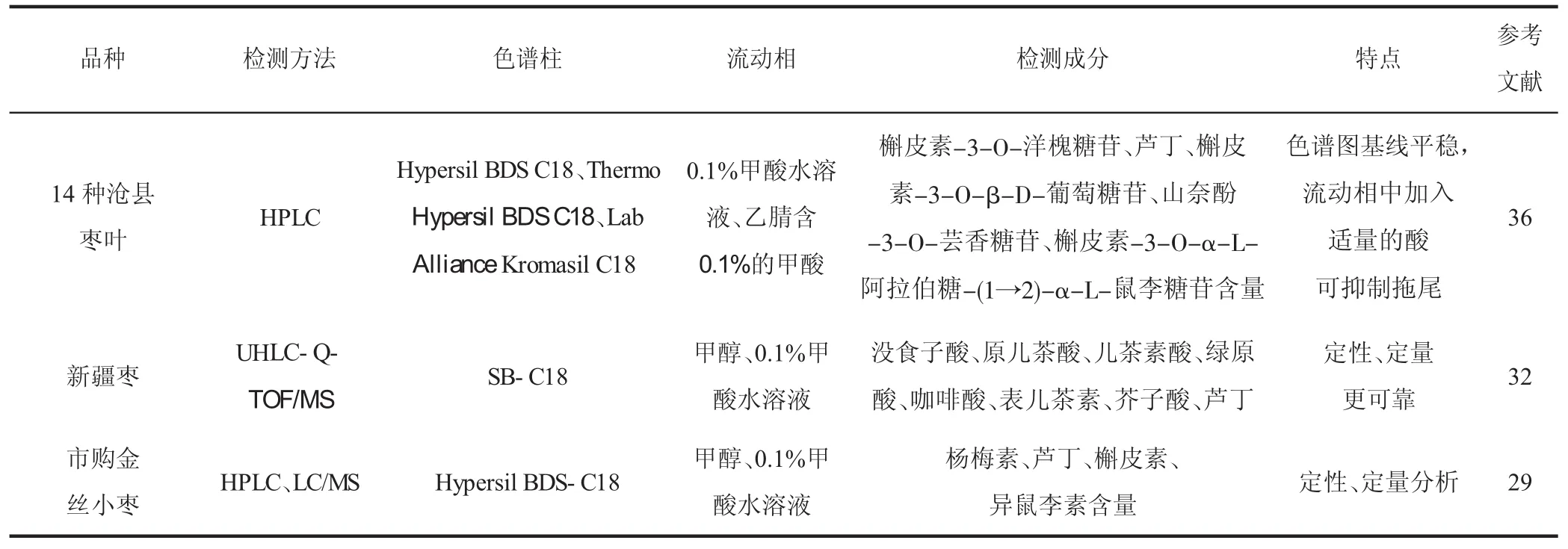
表3 (U)HPLC及LC/MS技术分离分析枣中黄酮类物质应用Table 3 The application of(U)HPLC and LC/MS technology in separation of flavonoids from jujube
多糖种类繁多,其提取方法也很多,如水提法、超声法以及微波法[40-42]等。超声波辅助提取法能够缩短提取时间及提取温度[39],水提法可以得粗多糖,多糖中无机盐主要采用层析法去除,活性炭、树脂进行脱色,凝胶色谱柱进一步分离纯化[43]。方法提取率不高,粗提物纯度较低,成分复杂。目前国内外测定多糖中单糖组分的色谱分离方法主要有气相色谱法(GC)、HPLC法和薄层色谱法(TLC)等[40],由于GC法[44]对食品中糖的测定需要衍生化反应且操作复杂,误差较大。而HPLC法[45]采用示差折光检测器不需要衍生化,操作简便,所以近年来得到了快速发展。据报道,可以同时采用GC/MS和HPLC来实现大枣功能性糖分的单糖组成及平均分子质量测定[40]。也可以用HPLC配备紫外检测器(UV)法测定糖类,但需要衍生化。王向红等人[46]利用柱前衍生HPLC-UV法检测出不同品种枣的水溶性多糖是由葡萄糖、鼠李糖、阿拉伯糖、半乳糖、半乳糖醛酸、甘露糖6种单糖组成的,且单糖组成比例存在很大差异[46]。不同产地鲜枣中糖的组分和含量不同,研究发现鲜枣中单糖的组成主要为蔗糖,并且糖分含量表现为蔗糖>果糖>葡糖糖>麦芽糖,由此可知产地对糖分含量有一定影响[45],此研究与之前的研究[47]相比,前处理阶段未用到固相萃取柱。目前,尚未见LC/MS技术在枣糖类分析检测中的报道。关于近几年HPLC技术分析枣中糖类物质应用见表4。

表4 HPLC技术分离分析枣中糖类物质应用Table 4 The application of HPLC technology in the separation of saccharides in jujube
5 其它物质的提取
枣中的有机酸不仅起到调解风味作用,还增加了其营养的功效[48]。提取有机酸的方法可以用水提取或者甲醇提取。HPLC法[49]测得枣果中6种有机酸含量由高到低依次为:苹果酸>柠檬酸>酒石酸>奎宁酸>草酸>富马酸,本方法较固相萃取、毛细管电泳等传统的有机酸测定方法灵敏度高,较GC/MS法方便快捷[50]。Bekir San等[51]利用HPLC法测得枣中含有儿茶素、咖啡酸、表儿茶酸、阿魏酸、芦丁、对羟基苯甲酸和绿原酸,其中酚类物质主要是儿茶素(含量为2.46~3.74mg/100g)和芦丁(含量是0.88~3.60mg/100g),同时利用GC/MS法检测出油酸、亚油酸、棕榈酸、棕榈油酸,得出棕榈酸是主要的饱和脂肪酸,不饱和脂肪酸含量为枣果总脂肪的68.54%~72.44%。枣在不同浸泡温度条件下糖精钠的含量不同[52],该检测对食品安全具有重要实际意义。
6 结论
(U)HPLC、LC/MS技术在枣等复杂体系的分离分析中的应用很普遍,并且随着新型的分离材料及功能材料的不断推出、(U)HPLC及LC/MS技术的不断提升,其应用会越来越广泛。枣中含有丰富的多糖、酚类、环核苷酸等营养物质被越来越多的发现,为进一步开发利用枣新产品奠定了基础。
[1] 刘世军,唐志书,崔春利,等.大枣化学成分的研究进展[J].云南中医学院学报,2015,(3):96-100.
[2] 王蓉珍,赵子青,林勤保,等.大枣功效成分检测的研究进展[J].食品工业科技,2012,33(4):423-426.
[3] 黄微,徐瑞晗,程妮,等.红枣生物活性成分的研究进展[J].食品研究与开发,2012,33(4):198-201.
[4] Santos R C,Garca GMD,Saenz RMT,et al.Antihistaminic and antieicosanoid effects of oleanolic and ursolic acid fraction from Helichrysumpicardii[J].Pharmazie,2007,62(6):459-462.
[5] Ync MC.Nonenzymatic antioxidative and antiglycative effects of oleanolic acid and ursolic acid[J].J Agric Food Chem,2007,55(17):7177-7181.
[6] 张明发,沈雅琴.熊果酸和齐墩果酸抗脑瘤作用的研究进展[J].药物评价研究,2016,(1):132-135.
[7] 徐军,王晋萍,钱辰旭,等.白桦脂酸的研究进展[J].生命科学,2011,(05):503-510.
[8] 苗利军.枣果中三萜酸等功能性成分分析[D].保定:河北农业大学,2006.
[9]栗巧云.白桦脂酸型三萜类化合物的提取分离工艺及测定方法研究[D].西安:西北大学,2009.
[10]高娅,杨洁,杨迎春,等.不同品种红枣中三萜酸及环核苷酸的测定[J].中成药,2012,34(10):1961-1965.
[11]孙延芳,梁宗锁,刘文婷,等.HPLC-ELSD法分析酸枣果中的白桦脂酸和熊果酸[J].中成药,2012,34(5):895-898.
[12]苗利军,刘晓光,刘孟军.4种液相色谱柱对枣果中三萜类物质的分离效果[J].江苏农业科学,2013,41(1):254-256.
[13]李成,何义,陈灿,等.HPLC/MS法测定枣中的齐墩果酸和熊果酸[J].食品研究与开发,2013,(15):75-77.
[14]许牡丹,邹继伟,史芳.超声波辅助酶法提取木枣环磷酸腺苷的工艺条件优化[J].食品科技,2013,07:220-224.
[15]朱西平,王茂广,孟少华,等.大孔树脂分离纯化芡实壳三萜类化合物[J].食品工业科技,2015,(1):288-291.
[16]GUO S,DUAN J N,QIAN D W,et al.Content variations of triterpenic acid,nucleoside,nucleobase,and sugar in jujube(Ziziphus jujuba)fruit during ripening[J].Food Chemistry,2015,167:468-474.
[17]Wang W,Zhang X L,Zheng J Q,et al.High glucose stimulates adipogenic and inhibits osteogenic differentiation in MG-63 cells through cAMP/protein kinase A/extra cellular signalregulated kinase pathway [J].Molecularand Cellular Biochemistry,2010,338(1/2):115-122.
[18]Subr A H,Walter U,Gambar Y S.Differential regulation of platelet inhibition by cGMP and cAMP dependent protein kinases[J].BMCPharmacologyand Toxicology,2013,14(1):69.
[19]杨芳媛,赵智慧,赵锦,等.枣中环磷酸腺苷的研究进展[J].塔里木大学学报,2016,03:119-122.
[20]赵堂,郝凤霞,杨敏丽.几种红枣中生物活性物质环磷酸腺苷的含量分析[J].湖北农业科学,2011,(23):4955-4957.
[21]张明娟,李薇,庞晓明.枣果中环磷酸腺苷(cAMP)的提取工艺及含量测定 [J].食品与发酵工业,2012,38(5):228-231.
[22]赵恒强,耿岩玲,苑金鹏,等.UAE-HILIC-DAD-ESI-QTOF/MS法测定大枣中的环磷酸腺苷[J].食品研究与开发,2013,18:46-50.
[23]王维有,曹晨晨,欧赟,等.大枣中环磷酸腺苷的提取及体外抗过敏活性研究 [J].食品工业科技,2013,11:49-52,282.
[24]KOU X H,CHEN Q,LI X H,et al.Quantitative assessment of bioactive compounds and the antioxidant activity of 15 jujube cultivars[J].Food Chemistry,2015,173:1037-1044.
[25]蒋劢博.红枣中环磷酸腺苷提取与纯化工艺研究[D].乌鲁木齐:新疆农业大学,2013.
[26]东莎莎,杨晓,王春燕,等.HILIC测定金丝小枣中核苷酸含量[J].中国果菜,2014,12:56-59.
[27]孙协军,李秀霞,冯彦博.冬枣黄酮抗氧化活性的研究[J].包装与食品机械,2015,33(2):12-16.
[28]Li J W,FAN L P,DING X L.Nutritional composition of five cultivars of Chinese jujube[J].Food chemistry,2007,103:454-460.
[29]师仁丽,翟龙飞,于文龙,等.利用DAD-HPLC和LC-MS法检测金丝小枣中黄酮类化合物 [J].食品科学,2016,37(16):123-127.
[30]李秀霞,孙协军,冯彦博,等.凌枣黄酮提取及自由基清除能力研究[J].食品工业科技,2013,34(12):234-237,242.
[31]GAO Q H,W P T,LIU J R,et al.Physico-chemical properties and antioxidant capacity of different jujube (Ziziphus jujuba Mill.)cultivars grown in loess plateau of China[J].Scientia Horticulturae,2011,130:67-72.
[32]ZHU Q Y,Zhang Q Y,CAO J,et al.Cyclodextrin-assisted liquid-solid extraction for determination of the composition of jujube fruit using ultrahigh performance liquid chromatography with electrochemical detection and quadrupole time-of-flight tandem mass spectrometry[J].Food Chemistry,2016,(213):485-493.
[33]张琼,周广芳,王中堂,等.枣类黄酮化合物的快速提取方法[J].塔里木大学学报,2016,03:37-40.
[34]潘少香,孟晓萌,郑晓冬,等.枣中黄酮类物质的研究进展[J].中国果菜,2013,12:33-37.
[35]Zhao H X,ZHANG H S,YANG S F.Phenolic compounds and its antioxidant activities in ethanolic extracts from seven cultivars of Chinese jujube[J].Food Science and Human Wellness,2014,(3):183-190.
[36]李喜悦,高哲,王荣芳,等.HPLC法同时测定枣叶中5种黄酮的含量[J].食品工业科技,2015,18:49-52,58.
[37]袁亚娜,张平平,何庆峰,等.冬枣黄酮的分析及体外抗氧化活性[J].食品科学,2013,17:70-73.
[38]张耀雷,黄立新,张彩虹,等.红枣多糖的研究进展[J].食品工业科技,2013,23:349-353.
[39]王雅,孙翠,陈丽琼,等.沙枣多糖的研究进展[J].中国食品工业,2015,(3):54-55.
[40]赵子青,原超,林勤保.大枣中4种功能性糖分的分离纯化及其单糖组成分析[J].食品科学,2012,(23):70-74.
[41]方元.大枣多糖的提取与产品开发 [D].乌鲁木齐:新疆农业大学,2014.
[42]高岐.微波提取广枣中多糖的应用研究[J].山东工业技术,2013,07:109,127.
[43]潘莹,许经伟.冬枣多糖的分离纯化及抗氧化活性研究[J].食品科学,2016,13:89-94.
[44]石浩,王仁才,庞立,等.糖枣多糖的单糖组成分析[J].食品科学,2015,(6):169-172.
[45]孙涛,赵子刚,刘圣红,等.高效液相色谱法测定鲜枣中糖的组成[J].分析仪器,2015,(1):38-41.
[46]王向红,吉爽爽,生庆海,等.柱前衍生高效液相色谱法检测8种枣水溶性多糖的单糖组成[J].中国食品学报,2014,(9):257-262.
[47]李云康,潘思轶.高效液相色谱法测定柑橘汁糖的组成[J].食品科学,2006,27(4):190-192.
[48]赵松,王颉,刘亚琼.不同发酵方法对枣醋主要有机酸含量的影响[J].中国食品学报,2014,(3):135-139.
[49]马倩倩,吴翠云,蒲小秋,等.高效液相色谱法同时测定枣果实中的有机酸和VC含量 [J].食品科学,2016,14:149-153.
[50]胡小露,刘卉,鲁宁,等.HPLC法同时测定蓝莓汁及其发酵酒中9种有机酸[J].食品科学,2012,33(16):229-232.
[51]Bekir San,Adnan Nurhan Yildirim.Phenolic,alpha-tocopher ol,beta-carotene and fatty acid composition of four promising jujube(Ziziphus jujubaMiller)selections[J].Journal of Food Composition and Analysis,2010,(23):706-710.
[52]顾建华,何倩倩,何鹏妍.高效液相色谱法测定冬枣中的糖精钠[J].中国卫生检验杂志,2016,26(11):1561-1565.

