2,6-二氯-4-三氟甲基苯胺合成工艺的改进
张增兴,张泉泉,李俊奇,赵红英
(1.浙江巍华新材料股份有限公司, 浙江 绍兴 312300;2.浙江巍华化工有限公司, 浙江 东阳 322109)
2,6-二氯-4-三氟甲基苯胺合成工艺的改进
张增兴1,张泉泉2,李俊奇2,赵红英2
(1.浙江巍华新材料股份有限公司, 浙江 绍兴 312300;2.浙江巍华化工有限公司, 浙江 东阳 322109)
研究了2,6-二氯-4-三氟甲基苯胺合成工艺中生成2,6-二氯-4-三氟甲基苯酚副反应的影响因素,通过工艺改进,减少了副产物的生成,并将反应收率从72.8%提高至88.6%。
对三氟甲基苯胺;2,6-二氯-4-三氟甲基苯胺;2,6-二氯-4-三氟甲基苯酚;工艺改进
2,6-二氯-4-三氟甲基苯胺,熔点:33℃~36℃,是重要的医药、农药和染料中间体[1-2]。目前已经工业化的合成工艺主要有:(1)3,4,5-三氯三氟甲苯直接高压氨解合成2,6-二氯-4-三氟甲基苯胺[3];(2)对氯三氟甲苯(或 3,4-二氯三氟甲苯)在180℃与二甲基甲酰胺在碱存在下进行氨解反应,然后在光照下通氯水解脱甲基后再通氯得到 2,6-二氯-4-三氟甲基苯胺[4];(3)对三氟甲基苯胺环氯化生成2,6-二氯-4-三氟甲基苯胺,其环氯化方法有在溶剂下直接通氯气氯化和双氧水/盐酸体系的氧化氯化[5-6]。我公司所采用的工艺是以对三氟甲基苯胺为原料,双氧水/盐酸体系的氧化氯化,该工艺有反应条件简单易控、多氯化物生成量少、氯原子利用率高等优点。该工艺具体过程为:先将对三氟甲基苯胺溶于10当量的稀盐酸(10%~18%)中,再缓慢加入2~4当量双氧水(50%),并控制反应温度在50℃~80℃,双氧水加完后保温2~3 h,冷却、静置分层,上层水相去浓缩后套用,下层有机相经水洗后简单蒸馏得2,6-二氯-4-三氟甲基苯胺产品。但在实际生产过程中有一较高的副反应发生,如控制不当副产物含量最高可达20%左右,严重影响了反应收率和产品的质量。我们对此副产物进行了提纯并进行了相关的定性分析,并确定其为2,6-二氯-4-三氟甲基苯酚,其分子结构如图1。

图1 2,6-二氯-4-三氟甲基苯酚结构式
该副反应相当于产品2,6-二氯-4-三氟甲基苯胺中氨基被羟基取代,该副反应在本合成工艺中都未见文献报道,所以笔者对此副反应进行了研究,以找出不同反应条件对该副反应的影响因素,进而可以在实际生产中采取相应措施来降低其发生。
1 实验部分
1.1 试剂与仪器
试剂:对三氟甲基苯胺 (本公司,纯度:99.5%);2,6-二氯-4-三氟甲基苯胺 (本公司,纯度:99.8%);盐酸(32%),双氧水(50%)为工业级。
仪器:岛津GC-14C高效气相色谱。
1.2 实验步骤
在常温常压下,将对三氟甲基苯胺70 g分批加入到1.0 L盐酸(15%)中,充分搅拌使其成盐。加热至50℃后开始滴加100 g双氧水,控制反应温度在70℃。双氧水加完后保温5 h,冷却分相,上层水相经蒸馏浓缩后可循环套用,下层有机相用200 mL水洗涤后简单蒸馏得2,6-二氯-4-三氟甲基苯胺粗品107 g,含量77.7%,其中副产物2,6-二氯-4-三氟甲基苯酚含量为20.1%。粗品经熔融结晶后得2,6-二氯-4-三氟甲基苯胺纯品(99.5%),总收率72.8%。反应式见图2。
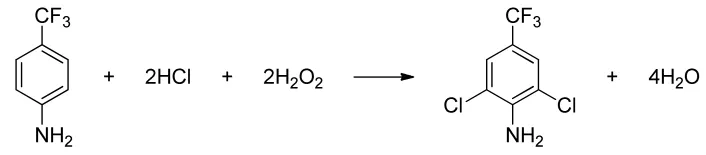
图2 氧化氯化反应
2 结果与讨论
为探索研究副反应发生的反应机理和影响因素,进行了以下实验:
2.1 探索双氧水是否参与副反应
实验步骤同上,将对三氟甲基苯胺溶于盐酸成盐后,不加双氧水,70℃搅拌5 h,GC检测无任何反应发生,固可推理出副反应需双氧水参与。
2.2 盐酸质量浓度对副反应的影响
因对三氟甲基苯胺氧化氯化反应中盐酸的适宜浓度为8%~18%,故研究了该浓度范围内不同盐酸浓度下反应得到的2,6-二氯-4-三氟甲基苯酚的含量,其它反应条件同实验步骤,实验结果见图3。
从图3中可看出在盐酸浓度为8%~18%范围内,不同的盐酸浓度下反应体系最后得到的2,6-二氯-4-三氟甲基苯酚的含量几乎无差别,故可推理出在8%~18%的盐酸浓度范围内,盐酸的浓度对该副反应无影响。
2.3 反应温度对副反应的影响
因对三氟甲基苯胺氧化氯化的适宜反应温度为50℃~80℃,故研究了该温度范围内不同反应温度下反应最后得到的2,6-二氯-4-三氟甲基苯酚的含量,其它反应条件同实验步骤,结果见图4。
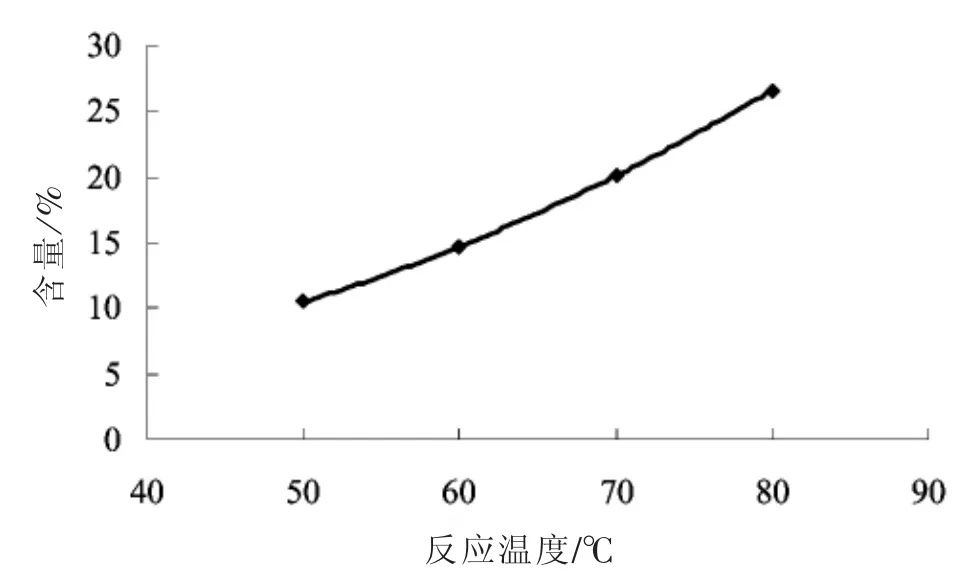
图4 反应温度对副反应的影响
从图4中可看出,反应体系最后得到的2,6-二氯-4-三氟甲基苯酚的含量随反应温度上升而增加,且反应温度越高,增加趋势越明显,故可推理出高温有利于副反应的进行。
2.4 反应时间对反应的影响
为保证原料能够被完全二氯化,现有工艺中双氧水加完后一般再保温(70℃)反应5 h以上,现将反应温度控制在50℃,其它反应条件同实验步骤,以双氧水滴加完毕后开始计时,研究反应体系中产物2,6-二氯-4-三氟甲基苯胺和副产物2,6-二氯-4-三氟甲基苯酚的含量随时间的变化,结果见表1。
从表1中可看出,副产物2,6-二氯-4-三氟甲基苯酚的含量随反应时间增加而不断增加,而产物2,6-二氯-4-三氟甲基苯胺含量先随时间增加而增加,当反应时间为3.5 h时,产物的含量达到最大,为91.3%,随后随反应时间增加而开始缓慢减小,推测是产物2,6-二氯-4-三氟甲基苯胺分子中氨基继续被羟基取代生成2,6-二氯-4-三氟甲基苯酚。因笔者在研究之前认为2,6-二氯-4-三氟甲基苯胺分子中氨基两边有两个较大的氯原子“包裹”保护,其性质应该稳定,不会再发生其它反应;副产物2,6-二氯-4-三氟甲基苯酚是原料对三氟甲基苯胺被水解成对三氟甲基苯酚后再被氯化后生成的。为验证2,6-二氯-4-三氟甲基苯胺在该实验条件下可继续被水解生成2,6-二氯-4-三氟甲基苯酚,进行了下面的实验。
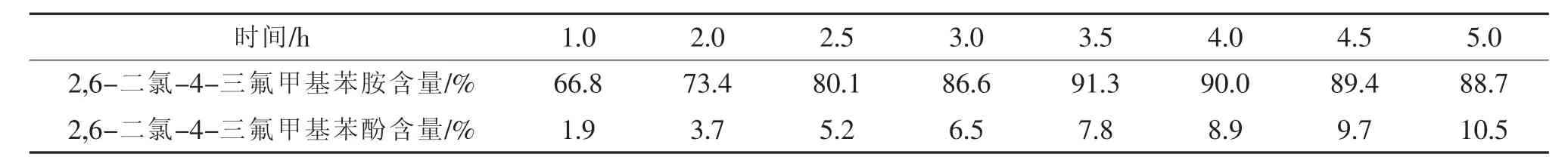
表1 反应时间对反应的影响
2.5 2,6-二氯-4-三氟甲基苯胺水解实验
将2,6-二氯-4-三氟甲基苯胺纯品 (99.8%)替代对三氟甲基苯胺进行实验,反应温度控制在50℃,其它反应条件同实验步骤,以双氧水滴加完毕后开始计时,研究反应体系中2,6-二氯-4-三氟甲基苯胺和2,6-二氯-4-三氟甲基苯酚的含量随时间的变化,结果见表2。

表2 2,6-二氯-4-三氟甲基苯胺水解实验
从表2数据可推测出:在该反应条件下,2,6-二氯-4-三氟甲基苯胺可转化生成 2,6-二氯-4-三氟甲基苯酚,2,6-二氯-4-三氟甲基苯胺分子中的氨基仍有反应活性,仍可被羟基取代。
综合以上实验数据分析,2,6-二氯-4-三氟甲基苯酚有两条生成路径:(1)对三氟甲基苯胺被水解成对三氟甲基苯酚后再被氯化后生成;(2)2,6-二氯-4-三氟甲基苯胺直接水解生成。所以为提高该反应收率和减少副产物2,6-二氯-4-三氟甲基苯酚产生,应做好反应中控,当目标产物含量达到最高时及时冷却停止反应。
2.6 反应后处理工艺的改进
因反应副产物2,6-二氯-4-三氟甲基苯酚为苯酚类物质,其可以和碱反应成盐而溶于水,可利用该性质对反应后的粗品进行处理,将2,6-二氯-4-三氟甲基苯酚从产物中除去,从而利于后面熔融结晶的提纯收率。具体实验操作同实验步骤,反应温度控制在50℃,反应时间为3.5 h,反应结束后下层有机相用200 mL氢氧化钠溶液(5%)洗涤,再经简单蒸馏得 2,6-二氯-4-三氟甲基苯胺粗品92.6 g,含量98.9%,粗品经熔融结晶后得2,6-二氯-4-三氟甲基苯胺纯品,工艺改进后的收率达88.6%。
2.7 反应机理推测
综合以上实验研究,提出图5反应机理如下:
该机理类似于苯胺类物质和氧化剂亚硝酸反应生成重氮盐,再高温水解生成苯酚类产物的反应机理,该反应机理中的氧化剂为双氧水,苯环上氨基先被其氧化成碱性弱易离去的羟胺基团,接着在酸性和加热条件下离去,并剩下苯正离子,苯正离子立刻和亲核的水分子反应生成酚。笔者在该反应结束后的水相中检测到了盐酸羟胺,可作为该机理的佐证。
3 结论
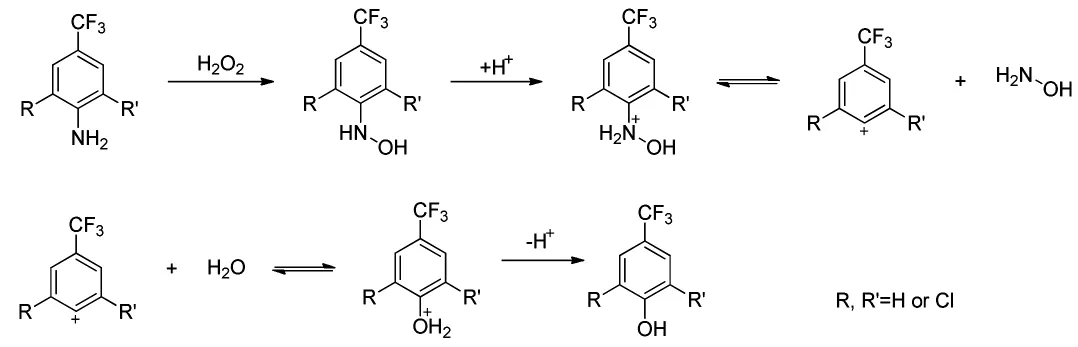
图5 反应机理
通过实验分析研究了氧化氯化生产2,6-二氯-4-三氟甲基苯胺工艺中生成2,6-二氯-4-三氟甲基苯酚的副反应,找出了影响该副反应的因素,提出了可能的反应机理。通过工艺改进,使该副反应得以控制,副产物含量从20%左右降低至7.8%,进而将反应收率从72.8%提高至88.6%。
[1] 刘宇.2,6-二氯-4-三氟甲基苯胺的合成[J].农药,2002,41(6):21.
[2] 刘长令.含氟农药的开发[J].有机氟工业,1997,(4):10-21.
[3] 李惠跃,陈静华,吴江伟,等.一种合成2,6-二氯-4-三氟甲基苯胺的方法:CN,101289400 A[P].2008-10-22.
[4] 吴天泉,胡艾希.2,6-二氯-4-三氟甲基苯胺的合成[J].湖南师范大学自然科学学报,2007,30(4):77-80.
[5] 严中杰,任旭康,杜晓华,等.2,6-二氯-4-三氟甲基苯胺的合成[J].农药,2008,47(3):174-175.
[6] 陶坤山,张建华,谢兵,等.2,6-二氯-4-三氟甲基苯胺的生产方法:CN,101143829 A[P].2008-03-19.
Improved Synthesis of 2,6-Dichloro-4-(trifluoromethyl)benzenamine
ZHANG Zeng-xing1,ZHANG Quan-quan2,LIJun-qi2,ZHAO Hong-ying2
(1.Zhejiang Weihua Advanced Materials Co.,Ltd.,Shaoxing,Zhejiang 312300,China;2.Zhejiang Weihua Chemical Co.,Ltd.,Dongyang ,Zhejiang 322109,China)
This paper studied the factors of side reaction which produced by-product 2,6-dichloro-4-(trifluoromethyl)phenol in 2,6-dichloro-4-(trifluoromethyl)benzenamine synthesis.Through the process improvement,the by-product was reduced and the yield was increased from 72.8%to 88.6%.
4-aminobenzotrifluoride; 2,6-dichloro-4-(trifluoromethyl)benzenamine; 2,6-dichloro-4-(trifluoromethyl)phenol; process improvement
1006-4184(2017)12-0004-04
2017-08-31
张增兴(1984-),男,工程师,主要从事含氟中间体开发及市场信息研究。E-mail:16484136@qq.com。

