CXCR1基因编码区SNPs与荷斯坦牛泌乳性能和繁殖性状关联分析
王梦琦,倪 炜,唐 程,郭佳禾,张慧敏,李明勋,毛永江
CXCR1基因编码区SNPs与荷斯坦牛泌乳性能和繁殖性状关联分析
王梦琦,倪 炜,唐 程,郭佳禾,张慧敏,李明勋,毛永江*
(扬州大学动物科学与技术学院,江苏 扬州 225009)
研究旨在探索CXCR1(Chemokine(C-X-C motif)receptor 1)基因编码区SNPs与荷斯坦牛泌乳性状及部分繁殖性状间关系。用飞行时间质谱法检测865头荷斯坦牛CXCR1基因编码区c.642 A>G、c.816 C>A、c.980 A>G和c.1068 G>A 4个SNPs位点,同时收集采样牛2010年12月至2012年7月繁殖指标和2010年至2014年奶牛生产性能测定(Dairy herd improvement,DHI)记录。采用多因素方差分析法分析CXCR1基因CDS区SNPs基因型与测定日产奶量、乳脂率、乳蛋白率等泌乳性状和产犊间隔、产后首配泌乳天数、配种次数和妊娠泌乳天数关系。结果表明,CXCR1-642 A>G和CXCR1-980 A>G对乳中体细胞评分(Somatic cell score,SCS)影响显著(p<0.05),c.642 A>G、c.816 C>A、c.980 A>G和c.1068 G>A对乳中乳脂率、蛋白率和总固体影响显著(p<0.05)。CXCR1-980 A>G 和CXCR1-1068 G>A位点AA型个体测定日产奶量显著高于AG和GG型(p<0.05),但CXCR1-980 A>G AA型乳蛋白率、SCS和总固体显著低于AG和GG型(p<0.05)。CXCR1-816 C>A位点对产犊间隔影响达显著水平(P=0.033),AC基因型个体产犊间隔显著低于AA型个体。而CXCR1-642 A>G、CXCR1-980 A>G和CXCR1-1068 G>A位点对产犊间隔、产后首配泌乳天数、配种次数以及妊娠泌乳天数均无显著性关联(P>0.05)。CXCR1-980 A>G和CXCR1-1068 G>A对荷斯坦牛产奶量和乳品质存在显著遗传效应,CXCR1 c.816 C>A位点对产犊间隔影响显著。CXCR1基因CDS区SNP可作为提高产奶量和乳品质、缩短产犊间隔候选分子标记之一。
荷斯坦牛;CXCR1基因;SNPs;泌乳性状;繁殖性状
奶牛泌乳性能由微效多基因控制,直接影响奶牛生产效益。近年荷斯坦牛泌乳性状相关研究中,马彦男等发现,GHR(Growth hormone receptor,生长激素受体)基因F279Y突变对305 d产奶量、乳脂率和乳蛋白率有显著影响[1]。张润锋等发现,IGFBP-3(Insulin-like growth factor-binding protein-3,胰岛素样生长因子结合蛋白3)BB型个体305 d产乳量显著高于AA和AB型,BB型个体乳蛋白率和体细胞评分显著低于AB型[2]。方远洋等通过IL8(Interleukin-8,白细胞介素8)基因3'UTR SNPs与中国荷斯坦牛泌乳性状关联分析发现,SNP显著影响荷斯坦牛305 d产奶量和乳脂率[3]。奶牛繁殖性状为奶牛经济效益限制因素之一。早期育种目标以提高产奶量为主,产奶量和繁殖力呈遗传负相关[4],妊娠泌乳天数、产犊间隔和配种次数等繁殖性状与奶牛产奶量和生产性能直接相关,影响奶牛生产成本和效益[5]。因此,奶牛繁殖性状为影响牛奶产量和质量关键因素之一[6]。由于众多因素限制,365 d产犊间隔理想模式难以实现。郭翔羽等学者对影响荷斯坦奶牛繁殖性状非遗传因素展开大量研究[7-10],为饲养管理提供参考。
目前已有遗传因素对奶牛繁殖性状影响相关报道。周妍研究发现Rad54L(Rad54 like,Rad样)和RRM1(Ribonucleotidereductasecatalyticsubunit M1,核糖核苷酸还原酶催化亚基M1)基因多态性对配种天数和空怀天数等性状影响显著[11]。李鹏等发现Leptin基因外显子2 E2FB区上102 bp处突变对荷斯坦牛的产犊间隔影响显著[12]。赵佳强等发现FoxO1(Forkhead box protein O1)基 因 不 同 基 因型对奶牛产犊间隔、空怀期以及初产日龄影响显著,但对产犊到发情、犊牛初生重、配种次数影响不显著[13]。
牛趋化因子受体1(Chemokinereceptor1,CXCR1)基因定位于2号染色体,具有丰富多态性。CXCR1可介导活化中性粒细胞,杀灭病原菌[14]。Bannerman等研究表明,CXCR1基因及其突变与奶牛乳房炎和子宫内膜炎等均存在显著相关[15-18]。周雷等通过中国荷斯坦奶牛CXCR1基因外显子2多态性分析,发现291 C>T、333 C>T、337 A>G 和365 C>T 4个突变位点,并且发现CCCTGGCC基因型组合个体具有低SCS和高产奶量优势[19]。本实验室前期对CXCR1基因多态性和泌乳性状关联开展相关研究,发现CXCR1基因5'侧翼区-1830位点和编码区783位点对荷斯坦牛305 d产奶量、乳脂和乳蛋白等影响显著[20]。另外奶牛临床乳房炎和子宫内膜炎均对其繁殖性能影响显著,但目前尚未见有关CXCR1基因与繁殖性状关联分析报道。因此,本文在检测大量荷斯坦牛CXCR1基因CDS区SNP基础上,收集其泌乳性能相关生产记录及妊娠泌乳天数、产犊间隔和配种次数等繁殖记录,对CXCR1基因编码区不同连锁群SNP与荷斯坦牛泌乳性状作进一步关联分析,分析其SNP与繁殖性状间关联性,以期为荷斯坦牛繁殖性能分子选择育种提供参考。
1 材料与方法
1.1 样品与数据采集
2011年8月和2012年7月于江苏省大丰市上海牛奶集团海丰奶牛场有限公司采集78个公牛家系905头荷斯坦牛血样,每头公牛后代数5~60。尾静脉采血10 mL,肝素钠抗凝,-20℃冷冻保存备用。试验奶牛饲养管理条件相同,均参加奶牛群体改良计划(Dairy Herd Improvement,DHI),每月一次DHI测定,日挤奶3次,饲喂3次,美国博美特48位转盘式挤奶。根据泌乳阶段制定日粮配方,全混合日粮(Total Mixed Ration,TMR)饲喂。收集采样牛2010~2014年DHI测定记录及相关系谱信息,主要包括牛号、父号、测定日期、测定日产奶量、乳脂率、乳蛋白率、乳糖、乳中干物质量、乳中尿素氮及体细胞数。收集采样牛2010年12月至2012年7月繁殖相关指标:产犊间隔、产后首配泌乳天数、配种次数和妊娠泌乳天数等。
1.2 DNA提取及SNP分型
奶牛血液基因组DNA提取采用常规酚氯仿法,TE溶解,取部分DNA样品稀释至100 ng·μL-1,-20℃保存备用。使用NanoUV-2000超微量紫外分光光度计测定DNA浓度和纯度。DNA检测完毕后,取一部分稀释至100 ng·μL-1,-20℃备用,剩余部分-80℃保存。由于DNA提取过程中部分样品损失,最后用于SNP分析样本为865头。
根据王梦琦等牛CXCR1基因多态性检测结果,直接挑选来自不同连锁群中c.642 A>G、c.816 C>A、c.980 A>G和c.1068 G>A四个位点,用飞行时间质谱法检测各SNP基因型[21]。该系统主要利用基质辅助激光解吸电离飞行时间质谱(matrixassisted laser desorption ionization time-of-flight mass spectrometry,MALDI-TOF MS)技术,检测过程主要包括PCR反应、SAP处理、延伸反应、产物纯化及检测等部分。检测结束后,用仪器自带分析软件分析TYPER对试验结果,获得基因分型数据。
1.3 统计分析
用遗传学软件Shesis作常规群体遗传学统计分析(包括基因频率、基因型频率、Hardy-Weinberg平衡检测等)。
利用多因素方差分析法分析CXCR1基因SNP对泌乳性能及乳中SCS影响,模型如下:
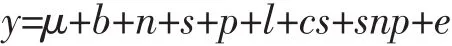
其中:y为测定日产奶量、乳脂率、乳蛋白率、乳糖、总固体、MUN及体细胞评分(SCS)性状观察值;μ为总体均值;b为种公牛效应;n为生产年度效应;s为生产季节效应;p为胎次效应(从第1胎到第3胎);l为泌乳阶段效应,分为三个阶段,即产犊后7~100 d、101~200 d和200~365 d;cs为泌乳牛各胎次产犊季节效应;snp为各基因SNP效应;e为残差效应。采用SPSS软件(Ver 16.0)中GLM(General Linear Model)分析, Duncan法对各基因SNP不同基因型泌乳性状作多重比较。根据当地气候特点,生产季节和产犊季节划分如下:3~5月为春季,6~8月为夏季,9~11月为秋季,12月~次年2月为冬季。
数据关联分析时,为保证结果可靠性,舍去不完整数据,限定DHI测定日记录:泌乳时间为产后第7~365天,测定日产奶量为5~60 kg,测定日乳脂率为2%~6%,测定日乳蛋白率为2%~5%,乳糖为3%~6%,总固体为9%~18%,MUN为1~25 g·100 mL-1,乳中体细胞数(×1000个·mL-1)为1~9 999。统计分析时,先将乳中体细胞数(SCC)转换为SCS,公式如下:SCS=log(SCC/100)2+3,四舍五入保留整数。关联分析时公牛数为75头,有效群体为865头,每个公牛后代数5~60,性状说明详见表1。
多因素方差分析模型分析CXCR1基因c.642 A>G、c.816 C>A、c.980 A>G和c.1068 G>A四个位点不同基因型对荷斯坦牛产犊间隔、产后首配泌乳天数、配种次数以及妊娠泌乳天数,模型如下:
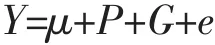
式中,Y为产犊间隔、产后首配泌乳天数、配种次数以及妊娠泌乳天数观察值,μ为群体均值,P为胎次效应值,G为基因型效应值,e为随机误差。
为提高数据代表性和整齐性,限定分析数据:正常产犊且健康牛,单胎。最终733头荷斯坦牛相关繁殖指标数据用于关联分析,其中1胎牛58头,2胎牛675头。
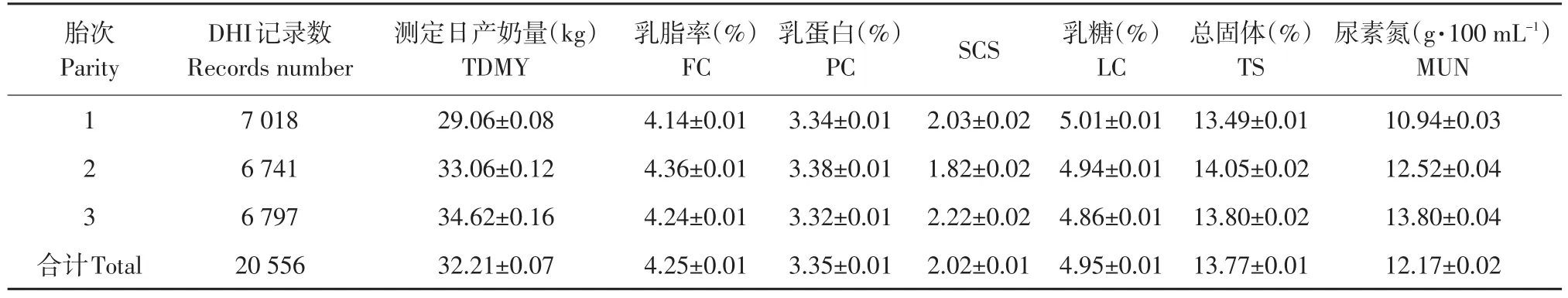
表1 泌乳性状及SCS描述性统计量Table 1 Descriptive statistics of the milking traits and SCS
2 结果与分析
2.1 基因(型)频率分布
利用飞行质谱法对865头奶牛群体CXCR1基因CDS区4个SNP位点分型,基因频率、基因型频率分布及Hardy-Weinberg平衡检验结果见表2。CXCR1-642、CXCR1-816、CXCR1-980和CXCR1-1068 4个SNP位点优势基因型分别为GG、CC、GG和GG型,频率分别为0.580、0.466、0.607和0.658,各位点优势等位基因分别为G、C、G和G,频率分别为0.758、0.688、0.784和0.811。CXCR1基因CDS区4个SNP位点均处于Hardy-Weinberg平衡状态。
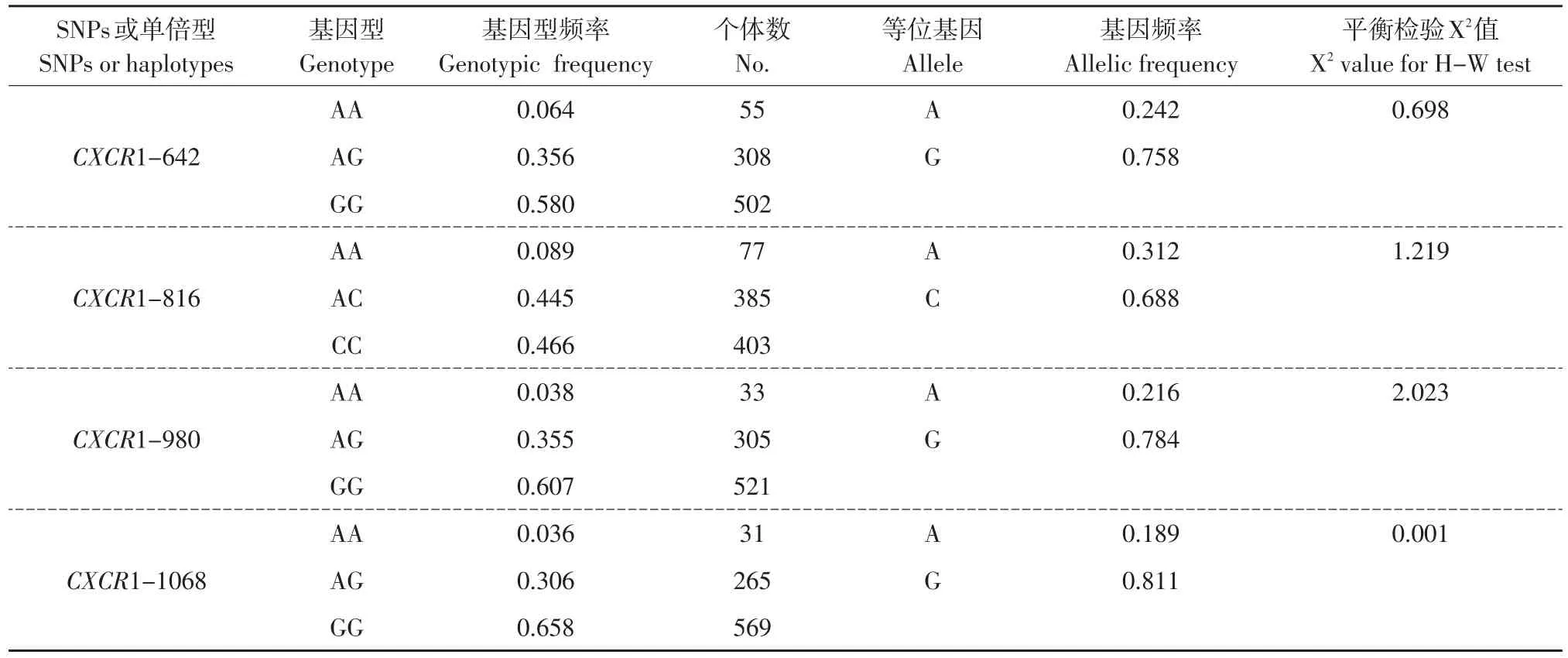
表2 CXCR1基因CDS区4个SNP位点等位基因、基因型频率及H-W平衡检验Table 2 Frequencies of genotypic,allelic,H-W test 4 SNP in the CDS of CXCR1 gene
2.2 CXCR1基因CDS区SNP与泌乳性能关联分析
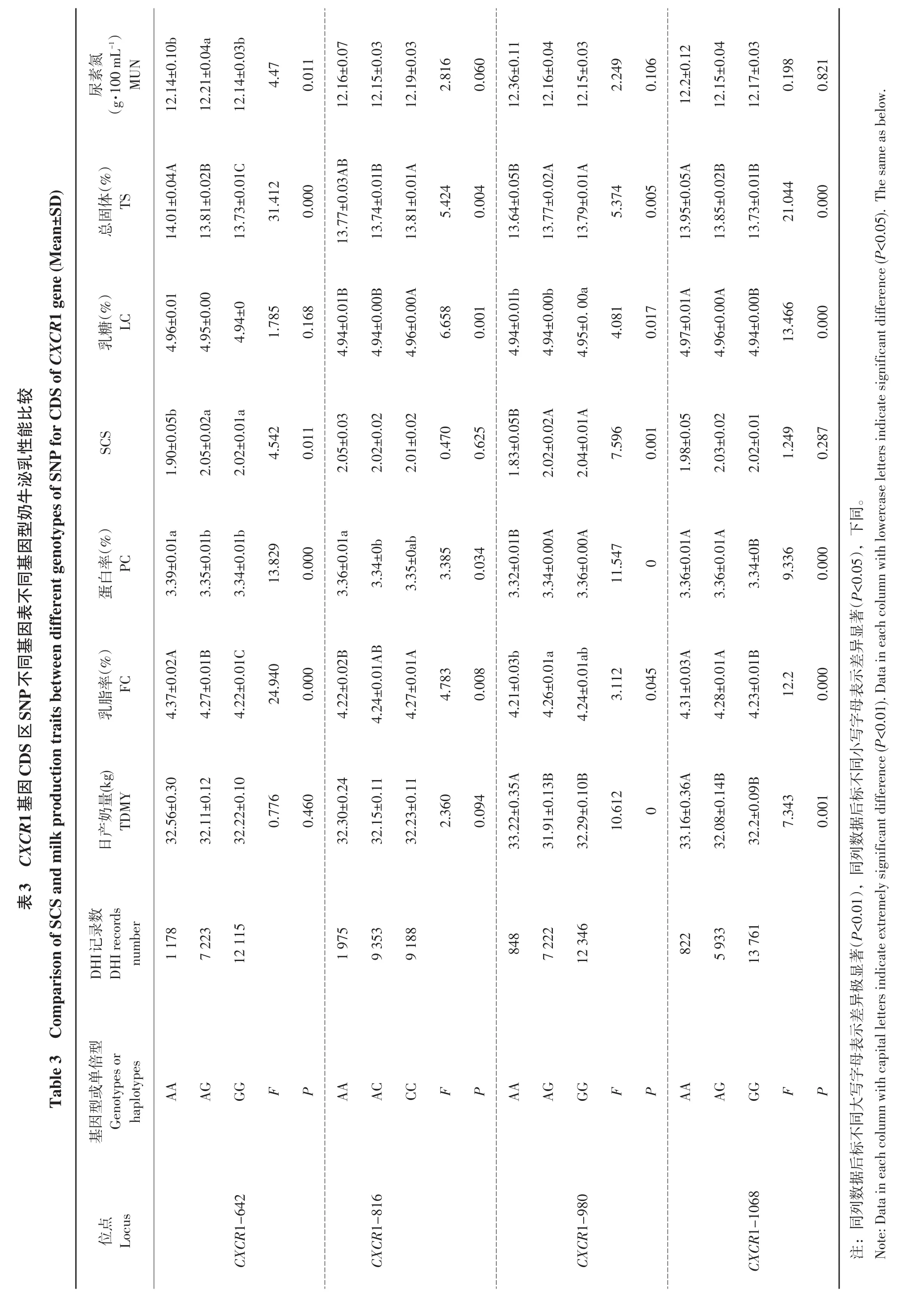
CXCR1基因CDS区SNP位点不同基因型泌乳性能平均数与标准差见表3。方差分析表明,CXCR1-642对乳脂率、蛋白率、总固体影响极显著(p<0.01),对SCS和乳中尿素氮含量影响显著(p<0.05),对日产奶量和乳糖无显著影响(P>0.05)。多重比较表明,AA型乳中乳脂率、蛋白率、总固体显著高于AG和GG型(p<0.05),GG型乳中乳脂率和总固体显著低于AA和AG型,AG型MUN含量显著高于AA和GG型(p<0.05)。
L1-)b 0a 4b 3 7 03 03 0 1 14 03 0 24 03 0氮mN 1.0 0.0 0.0711.0.0.06106.0.0.09460 1.0.0.08912素00U±4±1±4 4.40.±6±5±98.0.±6±6±52.1.±2±5±71.8.尿1M1.2.21.0 1.2 1.2 1.220 3.2 1.2 1.220.2 1.2 1.200注:同列数据后标不同大写字母表示差异极显著(p<0.01),同列数据后标不同小写字母表示差异显著(p<0.05),下同。·g(2 112 1 111111111)A4B2C1B AB1A1B5A2A1A5B2B1表3 CXCR1 基因CDS 区SNP不同基因表不同基因型奶牛泌乳性能比较%(0.0 0.0 0.0 210 0 30.0.0 0.0 4 24 0 0.0 0.0 0.0 4 75 0 0.0 0.0 0.0 440 0体T±1±1±3 4.1 0.0±±4±14.0.±4±7±93.0.±5±5±3 0.1 0.固0.8.3 7.3 30 77.7.3 8.50 6.3 7.7.509.8.3 7.3 20总41113 1131131313111)1000B 1B 0A0b 1b 0a 0 A1A0B 0%(C .0±.0±0±4 587 861 0.0 0.0 0.0 856 100 0.0 0.0 0.0 180 710 0.0 0.0 0.0 664.000糖L6959 9.4.1.0±4±4±6.6.0±4±4±5.4.0±7±6±43 1.0乳.4.4 9.4 9.4 9.4 9.4 9.4 9.4 9.4 9.4 9.4 b 5a 2a 1 302020B 5A 2A 1 502010 S 0.0 0.0 0.02411.0.0.00752 0.0 0.0 0.06910.0.0.09478 C S ±0±5±2 5.4 0.0±5±2±1 4.0 6.0±3±2±4 5.7 0.0±8±3±2 2.1 2.0 9.0.2 0.2 0.2 0.2 0.28.0.0.9.1 0.2 0.2 1 122)%(a10.b10.b10.9 200 a10.b 0 ba05843 B10.A00.A00.74 A10.A10.B 06300率CP 0±0±0±8.30.0±±4±53.0.0±0±0±5.100±0±±43.0.白93.53.43.10 63.3.3 3.330 23.43.63.1 63.63.3.3 90蛋333333333 Table 3 Comparison of SS ad milk poductio tits btw diffeet geotyes f NP fr CDS CXR1 gene (Mean±SD))%A 2B11B2B AA 1 b3a1baA 3A 1B1(0.0.0.04000.10.0.38800.0.10.21540.0.0.2.00Note: Data in each column with capital letters indicate extremely significant difference(p<0.01). Data in each column with lowercase letters indicate significant difference (p<0.05). The same as below.率CF 0±0±0±9.40.0±0±0±7.0.0±0±0±1.0.0±0±0±210.脂73.72.22.20 22.4 2 72.40 12.62.4230 13.82.32.0乳4444.4444.4444)gk020411ABBABB(Y 3.0 1.0 1.0 60 2.0 1.0 1.0 04 53.31.01.2 63.41.9031量M±6±1±27 76 4±0±5±36 39 00±0±0±16.00±0±.04 30 0奶DT 5.1.2..0.03.1.2..2.02219920 16180±2..7.0产2 32 32 3 2 32 32 3.3.13.23.3.23 23日3 3数sdrr录oceeb8732515735888226423316记I rIm u1 2 1 2 9 3 148 2 3 2 28 9 7 3 HHn1711997151 DD型ros倍see p单pyytoAGGFPACCFPAGGFPAGGFP或tonlpAAGAACAAGAAG型eah因G基2 4 6 1 0 8 86 su 6-8-9-01点位coL 1RCXC 1RCXC 1RCXC -1RCXC
CXCR1-816对乳脂率、蛋白率、乳糖和总固体影响达极显著水平(p<0.01),对蛋白率影响达显著水平(p<0.05),对日产奶量、SCS、MUN无显著影响(P>0.05)。多重比较表明,CC型个体乳脂率、和乳糖显著高于AA型(p<0.05),总固体含量显著高于AC型(p<0.05),AC型乳蛋白率显著低于AA型(p<0.05)。
CXCR1-980对日产奶量、乳蛋白率、SCS和总固体影响达极显著水平(p<0.01),对乳脂率和乳糖影响达显著水平(p<0.05),对MUN无显著影响(P>0.05)。多重比较表明,AA型个体日产奶量显著高于AG和GG型(p<0.05),但乳蛋白率、SCS和总固体显著低于AG和GG型(p<0.05),AG型乳脂率和显著高于AA型(P>0.05),GG型个体乳糖含量显著高于AA和AG型(p<0.05)。
CXCR1-1068位点对日产奶量、乳脂率、蛋白率、乳糖和总固体影响达极显著水平(p<0.01),对MUN无显著影响(P>0.05)。多重比较表明,AA型个体日产奶量、总固体显著高于AG和GG型(p<0.05),GG型个体乳脂率、乳蛋白率和乳糖显著低于AA和AG型(p<0.05),AA型个体显著高于GG型(p<0.05)。
2.3 CXCR1基因CDS区SNP与繁殖性能关联分析
CXCR1基因编码区多态性对荷斯坦牛产犊间隔、产后首配泌乳天数、配种次数以及妊娠泌乳天数影响如表4所示。其中,CXCR1-816位点对产犊间隔影响达显著水平(p<0.05),AC基因型个体产犊间隔(383.52±2.56 d)显著低于AA基因型个体(397.24±6.31 d)。CXCR1-816位点对产后首配泌乳天数、配种次数以及妊娠泌乳天数无显著性影响。CXCR1-642、CXCR1-980和CXCR1-1068对产犊间隔、首配泌乳天数、配种次数以及怀孕泌乳天数影响均未达显著水平(P>0.05)。
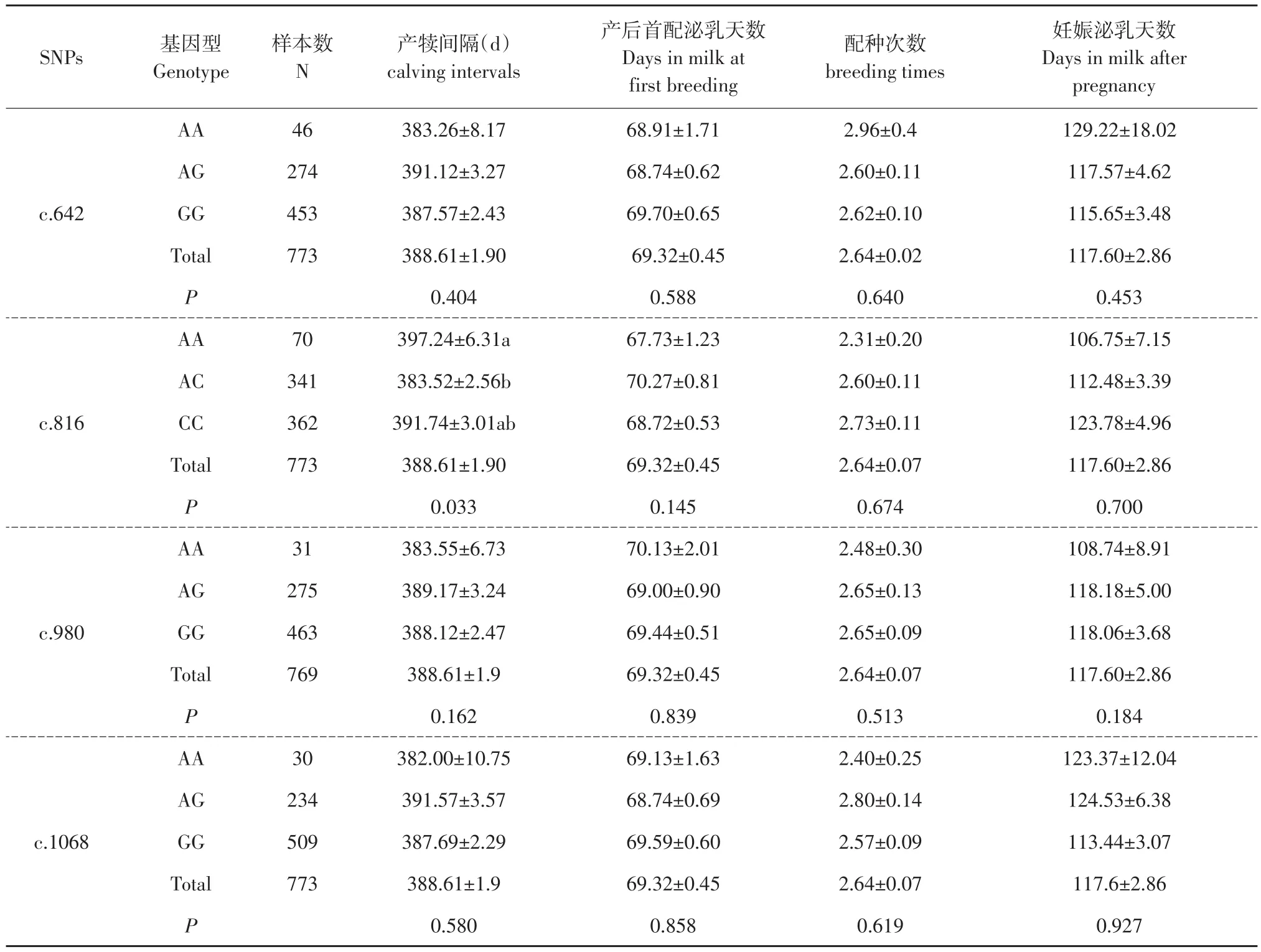
表4 CXCR1基因CDS区SNP位点不同基因型部分繁殖性能比较Table 4 Comparison of partial reproductive performance between different genotypes in SNP locus of CXCR1 gene CDS region(Mean±SD)
3 讨论与结论
3.1 CXCR1基因CDS区SNPs对泌乳性能影响
CXCR1在诱导中性粒细胞趋化物、IL8及生长相关基因等趋化物引起炎症反应中发挥重要作用。CXCR1基因呈高度多态性[22]。官久强等分析470头中国荷斯坦牛CXCR1基因编码区多态性,在CXCR1基因编码区共发现6个SNPs,其中位点735(C>G)、816(C>A)、819(A>G)与SCS、产奶量关联达极显著水平(p<0.01)[23]。Leyva-Baca等研究330头加拿大荷斯坦公牛发现-1768(T>A)位点对SCS影响达极显著水平(p<0.01)[24]。Goertz等对739头德国荷斯坦奶牛研究表明,CXCR1基因735(G>C)、-1768(T>A)位点对SCS影响不显著(P>0.05)[25]。本试验侧重于CXCR1基因CDS区位点SNP与泌乳性能关联分析。结果表明,CXCR1-642 A>G和CXCR1-980 A>G对乳中SCS影响显著,c.642 A>G、c.816 C>A、c.980 A>G和c.1068 G>A对乳中乳脂率、蛋白率和总固体影响显著。CXCR1-980 A>G和CXCR1-1068 G>A位点AA型个体日产奶量显著高于AG和GG型。Pighetti等对CXCR1基因全长的多态性分析表明,该基因呈高度多态,但各SNP间连锁程度较高[22]。其中980A>G属于第2连锁群,与 CDS 区 995A>G、 5'端 -481 C>T、 -465 A>T、-182 C>T及3'端97 A>G共6个SNP位点完全连锁,且980 A>G和995 A>G均属于非同义突变,AA变化分别为K327R和H332R。另外,与980A>G连锁5'端-481 C>T、-465 A>T、-182 C>T由于SNP突变导致转录因子结合位点突变,或基因3'端SNP突变导致与之结合miRNA活性发生变化,改变基因和蛋白表达量,影响对乳房炎易感性。CXCR1基因4个SNP位点对乳脂率、乳蛋白率和总固体含量影响同理。
3.2 CXCR1基因CDS区SNPs对繁殖性能影响
奶牛繁殖是奶牛生产和延续泌乳前提,其性状为复杂遗传和环境因素综合作用结果,遗传力较低,不同品种、资料来源、分析方法等对遗传参数估计影响较大。其中,环境因素与牧场饲养管理相关,可通过科学方法改善。遗传因素只能通过选择育种改善,分子育种是有效手段之一,特别是对低遗传力性状[13]。本试验通过分析CXCR1基因SNPs不同基因型对产犊间隔、产后首配泌乳天数、配种次数和妊娠泌乳天数影响,评估CXCR1基因对荷斯坦牛部分繁殖性状效应,结果表明,CXCR1-816位点对产犊间隔影响显著。
奶牛产犊间隔由奶牛空怀期和奶牛妊娠期共同决定。妊娠期变化范围较小,空怀期为决定产犊间隔主因。叶东东等研究发现,不同胎次荷斯坦牛产犊间隔差异极显著[27]。为排除胎次等其他非遗传因素影响,本试验选取牧场1~2胎荷斯坦牛分析CXCR1基因多态性对部分繁殖性能影响,其中产犊间隔仅针对2胎牛(1胎牛只无记录)。本研究中,CXCR1-816位点AC基因型个体产犊间隔为383.52±2.56 d,显著低于AA基因型个体(397.24±6.31 d)。CXCR1基因在机体免疫中发挥重要作用,CXCR1基因与临床乳房炎、子宫内膜炎以及难产等常见疾病等显著相关,疾病发生导致荷斯坦牛产犊间隔加长[18,27]。官永强研究发现,CXCR1-816 AC和CC基因型个体牛奶体细胞评分(Somatic cell score,SCS)显著低于AA基因型个体,说明AC基因型较AA基因型个体对临床乳房炎抗性较好,不易患病[28]。临床乳房炎不仅显著影响产奶量,且生产中临床乳房炎荷斯坦牛治疗期间无法配种,延长产犊间隔。本研究发现AC型个体产犊间隔显著低于AA型个体,与上述研究及原因分析相符。CXCR1-642、CXCR1-980和CXCR1-1068对产犊间隔、首配泌乳天数、配种次数以及怀孕泌乳天数无显著性影响。CXCR1-816位点对产犊间隔影响显著,AC基因型个体产犊间隔显著低于AA基因型个体。CXCR1基因CDS区部分SNPs可为提高产奶量和乳品质、缩短产犊间隔分子标记辅助选择育种提供参考。
[1] 马彦男,贺鹏迦,朱静,等.GHR基因F279Y位点突变对中国荷斯坦牛泌乳性状的影响[J].中国应用生理学杂志,2013,29(5):400-404.
[2] 张润锋,陈宏,雷初朝,等.IGFBP-3基因PCR-RFLP多态性与中国荷斯坦牛泌乳性状的相关分析[J].中国畜牧杂志,2006,42(3):9-11.
[3] 方远洋,宋雪梅,姜俊芳,等.IL8基因3'UTR SNPs与中国荷斯坦牛泌乳性状的关联分析[J].浙江农业学报,2015,27(3):338-342.
[4] Hoekstraa J,Vander Lugh A W,Vander W J,et al.Genetic and phenotypic parameters for milk production and fertility traits in upgraded dairy cattle[J].Livestock Production Science,1994,40(3):225-232.
[5] 梁春年,阎萍,郭宪,等.牛繁殖性状候选基因的研究进展[J].中国畜牧兽医,201 l,38(8):103-106.
[6] 于孟虎.荷斯坦牛体尺体重与繁殖性状的相关分析[J].中国奶牛,2002(4):30-31.
[7] 郭翔羽,郭刚,李锡智,等.北京地区荷斯坦青年牛繁殖性状影响因素分析[J].中国奶牛,2011(24):1-6.
[8] 廖想想,陈丹,张美荣,等.产犊季节和胎次对荷斯坦牛部分繁殖指标的影响[J].中国奶牛,2013(11):20-23.
[9] 李艳华,王海浪,朱玉林,等.高产荷斯坦牛繁殖障碍的诱因分析及应对策略[J].中国奶牛,2014(15):18-22.
[10] 汪聪勇,苏银池,陈江凌,等.荷斯坦牛的繁殖性状及影响因素分析[J].家畜生态学报,2015,36(10):45-48.
[11] 周妍.荷斯坦奶牛繁殖性状相关的分子标记筛选与鉴定[D].武汉:华中农业大学,2013.
[12] 李鹏,何举,赵国丽,等.荷斯坦牛Leptin基因外显子2多态性与繁殖力性状的相关性研究[J].中国奶牛,2011(6):4-7.
[13] 赵佳强,周妍,于倩楠,等.中国荷斯坦奶牛FoxO1基因多态性及与繁殖性状关系研究[J].东北农业大学学报,2013,44(6):54-57.
[14] Paape M,Menrzad J,Zhao X,et al.Defense of the bovine mammary gland by polymorpho-nuclear neutrophil leukocytes[J].Journal of Mammary Gland Biology and Neoplasia,2002,7(2):109-121.
[15] Bannerman D D,Paae M J,Lee J W,et al.Escherichia coli and Staphylococcus aureus elicit differential innate immune responses following intramammary infection[J].Clinical&Diagnostic Laboratory Immunology,2004,11(3):463-472.
[16] Leyva-baca I,Schenkel F,Sharma B S,et al.Identification of single nucleotide polymorphisms in the bovine CCL2,IL8,CCR2 and IL8RA genes and their association with health and production in Canadian Holsteins[J].Animal Genetics,2007,38(3):198-202.
[17] Youngerman S M,Saxton A M,Pighetti G M.Novel single nucleotide polymorphism and haplotypes within the bovine CXCR2 gene[J].Immunogenetics,2004,56(5):355-359.
[18] Galvão K N,Pighetti G M,Chenog S H,et al.Association between interleukin-8 receptor-α(CXCR1)polymorphism and disease incidence,production,reproduction,and survival in Holstein cows[J].Journal of Dairy Science,2011,94(4):2083-2091.
[19] 周雷,王洪梅,王长法,等.中国荷斯坦牛CXCR1基因第二外显子新SNPs与乳腺炎的关联分析[J].畜牧兽医学报,2011,42(8):1063-1070.
[20] 张美荣,廖想想,陈丹,等.澳系进口荷斯坦奶牛CXCR1基因遗传多态性与泌乳性状及体细胞评分的关联性分析[J].中国兽医学报,2014,34(1):159-164.
[21] 王梦琦,倪炜,张慧敏,等.中国荷斯坦牛CXCR1基因编码区SNP突变对临床乳房炎和生产寿命的影响[J].中国农业科学,2017,50(12):2359-2370.
[22] Pighetti G M,Kojima C J,Wojakiewicz L,et al.The bovine CXCR1 gene is highly polymorphic[J].Veterinary Immunology and Immunopathology,2011,145(1/2):464-470.
[23] 官久强,王洪梅,王长法,等.中国荷斯坦牛CXCR1基因编码区的遗传多态性[J].西北农林科技大学学报:自然科学版,2009,37(6):47-52.
[24] Leyva-Baca I,Schenkel F,Martin J,et al.Polymorphisms in the 5'upstream regin of the CXCR1 chemokine receptor gene,and their association with somatic cell score in Holstein cattle in Canada[J].Journal of Dairy Science,2008,91(1):407-417.
[25] Goertz I,Baes C,Weimann C,et al.Association between single nucleotide polymorphisms in the CXCR1 gene and somatic cell score in Holstein dairy cattle[J].Journal of Dairy Science,2009,92(8):4018-22.
[26] 叶东东,张孔杰,毛波涛,等.影响新疆地区荷斯坦牛产犊间隔的因素分析[J].新疆农业科学,2010,47(8):1643-1646.
[27] 毛永江,陈仁金,陈莹,等.利用多因子降维法研究CXCR1和IL-8基因交互作用与中国荷斯坦牛乳房炎的关系[J].中国农业科学,2011,44(9):1908-1915.
[28] 官永强.奶牛CXCR1及CXCR2基因多态性与乳腺炎相关性研究[D].成都:四川农业大学,2009.
Association analysis between polymorphism ofCXCR1 gene coding region and milk production and partial reproductive traits in Holsteincattle/
WANG Mengqi,NI Wei,TANG Cheng,GUO Jiahe,ZHANG Huimin,LI Mingxun,MAO Yongjiang
(School ofAnimal Science andTechnology,Yangzhou University,Yangzhou 225009,China)
The purpose of this study was to explore the association between the single nucleotide polymorphisms(SNPs)in the coding region ofCXCR1(Chemokine(C-X-C motif)receptor 1)gene andmilk production traits and partial reproductive traits of Holstein cattle.4 SNPs in theCXCR1 gene coding region(c.642,A>G,c.816C>A,c.980A>G and c.1068G>A)were detected by time-of-flight mass spectrometry.The recordings about calving intervals,days in milk at first breeding for every parity,breeding times and days in milk after pregnancy of 865 cattle was were collected in a large dairy farm from Dec.2010 to July 2012.The DHI recordings were collected from 2010 to 2014.The association among the SNPs and milk production traits,calving intervals,days in milk after first breeding,breeding times and days in milk after pregnancy was analyzed by Multivariate analysis of variance.The results showed thatCXCR1-642 A>G andCXCR1-980 A>G had significant effects on SCS in milk(p<0.05),c.642 A>G,c.816 C>A,c.980 A>G and c.1068 G>A had significant effects on fat percentage,milk protein percentage and total solids in milk(p<0.05).For CXCR1-980 A>G orCXCR1-1068 G>A,the daily milk yield of the individual with AA genotype was significantly higher than that of AG and GG(p<0.05),but milk protein percentage,total solids and SCS was significantly lower than that of AG and GG forCXCR1-980 A>G(p<0.05).CXCR1-816 C>A had significant effects on calving intervals(P=0.033),the calving intervals of individuals with AC genotype are significantly shorter than that with AA genotype.CXCR1-642 A>G,CXCR1-980 A>Ga andCXCR1-1068 G>A had no effect on calving intervals,days in milk after first breeding,breeding times and days in milk after pregnancy(P>0.05).CXCR1-980 A>G or CXCR1-1068 G>A had significant genetic effect.CXCR1 c.816C>A had significant effect on calving interval.The SNPs in coding region ofCXCR1 gene could provide reference for selective breeding about improving the milk yield and quality and shortening calving interval in Chinese Holstein.
Holstein;CXCR1 gene;SNPs;milk production;reproductive trait
S823.8+9
A
1005-9369(2017)11-0035-08
时间2017-12-7 12:34:21 [URL]http://kns.cnki.net/kcms/detail/23.1391.S.20171207.1234.008.html
王梦琦,倪炜,唐程,等.CXCR1基因编码区SNPs与荷斯坦牛泌乳性能和繁殖性状关联分析[J].东北农业大学学报,2017,48(11):35-42.
Wang Mengqi,Ni Wei,Tang Cheng,et al.Association analysis between polymorphism ofCXCR1 gene coding region and milk production and partial reproductive traits in Holstein cattle[J].Journal of Northeast Agricultural University,2017,48(11):35-42.(in Chinese with English abstract)
2017-09-08
国家自然科学基金项目(31372286);江苏省农业自主创新基金(CX(17)1005)
王梦琦(1993-),女,硕士研究生,研究方向为奶牛遗传育种。E-mail:770406499@qq.com
*通讯作者:毛永江,教授,博士,硕士生导师,研究方向为牛遗传育种。E-mail:cattle@yzu.edu.cn

