超声内镜对胃十二指肠胰腺神经内分泌瘤定位优势的Meta分析
刘一平 罗海峰 崔士猛 王忠裕
·论 著·(临床实践)
超声内镜对胃十二指肠胰腺神经内分泌瘤定位优势的Meta分析
刘一平 罗海峰 崔士猛 王忠裕
目的系统评价超声内镜(EUS)对胃十二指肠胰腺神经内分泌瘤(gastroentero-pancreatic neuroendocrine tumors,GEP-NETs)的定位优势。方法通过检索Medline、PubMed、Embase、Science Citation Index、中国知网、万方、维普等相关数据库,按照纳入、排除标准,筛选符合标准的文献,用StataSE12.0进行Meta分析。选择行包括EUS的一种以上影像学检查,之后经术后病理或经超声内镜引导下细针穿刺病理(EUS-FNA)证实为GEP-NETs的病人。比较EUS与CT等其他影像学检查在GEP-NETs整体检出率、病灶<2 cm时GEP-NETs检出率、有功能性神经内分泌瘤上检出率上是否存在优势。结果共纳入10篇文献,543例病人,578个病灶。EUS较CT在GEP-NETs的整体检出率上存在优势(OR=4.61,95%CI:2.98,7.13,P=0.000);EUS较CT在小于2 cm的GEP-NETs的检出率上存在明显优势(OR=12.66,95%CI:6.06,26.44,P=0.000);EUS较CT在有功能的神经内分泌瘤的检出率上存在明显优势(OR=5.74,95%CI:2.97,11.09,P=0.000)。结论通过应用精细血流、高清精细放大及弹性成像等功能,EUS对于GEP-NETs,尤其是<2 cm的GEP-NETs或有功能的神经内分泌瘤的定位较以CT为代表的其他传统影像学方法更有优势。
超声内镜; 计算机断层扫描; 胃十二指肠胰腺神经内分泌瘤; Meta分析
神经内分泌瘤(neuroendocrine tumors,NETs)为罕见肿瘤,发病率约2/100 000[1],通常将发生在胃、十二指肠、胰腺的NETs统称为胃十二指肠胰腺神经内分泌肿瘤(gastroentero-pancreatic neuroendocrine tumors,GEP-NETs)。随着现代影像学检查技术的进步,GEP-NETs的检出率逐渐提高。有术后病理证据的报道显示,长径小于1 cm的NETs检出率为0.8%~10%[2]。虽然有些研究建议小的、无症状的GEP-NETs可以随诊[3],但外科手术切除仍然是目前唯一有希望治愈GEP-NETs的治疗手段[4]。准确的定位对获得好的手术效果至关重要。最新的指南将CT和MRI作为疑似GEP-NETs病例的首选检查方法[5-10]。两者对NETs的检出率为40%~80%[4-5]。生长抑素受体显像技术对表达该受体的GEP-NETs有高达90%的检出率[11],但受制于如良性胰岛素瘤这些不表达该受体病例的限制,总的检出率只有60%[12]。正电子发射计算机断层显像(positron emission tomography,PET) -CT有出色的分辨率,并可以定量分析肿瘤对示踪剂的摄取,然而受开展条件的限制较大。超声内镜(EUS)对GEP-NETs有很高的敏感性[13],从而实现检出多发病灶并准确定位的目的。许多报道都证实了在其他影像学检查阴性的病例中,EUS发现了GEP-NETs病灶。然而,对GEP-NETs应用EUS较其他检查手段在检出率上的优势缺乏定量分析。我们设计Meta分析的目的就是研究在GEP-NETs定位上EUS较CT等其他检查手段的优势情况。
资料与方法
一、资料来源与检索
按照PRISMA声明以及Cochrane系统评价手册系统检索发表日期位于近20年(1997~2017年),Medline(Ovid SP)、PubMed、Embase、Science Citation Index、Cochrane Central Register of Controlled Trials等外文数据库以及中国知网、万方、维普、中国生物医学文献等中文数据库。英文检索词:endoscopic ultrasound,EUS,ultrasound, endosonography,gastroentero-pancreatic neuroendocrine tumors,pancreatic mass等, 中文检索词:超声内镜,胃肠胰神经内分泌瘤,胰腺神经内分泌瘤,胰腺肿物等。采用自由词与主题词相结合的检索策略,根据题目及摘要进行初步检索。语种限制为中文和英文,人群及种族不限。
二、文献入组标准
1.纳入标准 ①行包括EUS的一种以上影像学检查;②经术后病理或经内镜超声引导下细针穿刺病理(EUS-FNA)证实为GEP-NETs的病人;③多次发表的研究结果,取最近一次数据。
2.排除标准 ①研究范围超出GEP-NETs包含其他疾病干扰统计数据;②缺少EUS与其他影像学检查对比;③数据类型不符合或不完整。
三、文献筛选和数据提取
文献筛选和数据提取均由2名研究人员独立提取,如果出现2名研究人员提取数据不一致,则由第3位研究人员重新提取,再与前2名研究人员提取的数据进行核对比较。从每篇文献中提取如下数据:第一作者、发表年份、分组、样本量、平均年龄、年龄范围、性别比例,EUS、CT、超声(US)、MRI对病灶的整体检出率、对<2 cm病灶的检出率、对功能性神经内分泌瘤(FTs)的检出率。文献筛选流程见图1。
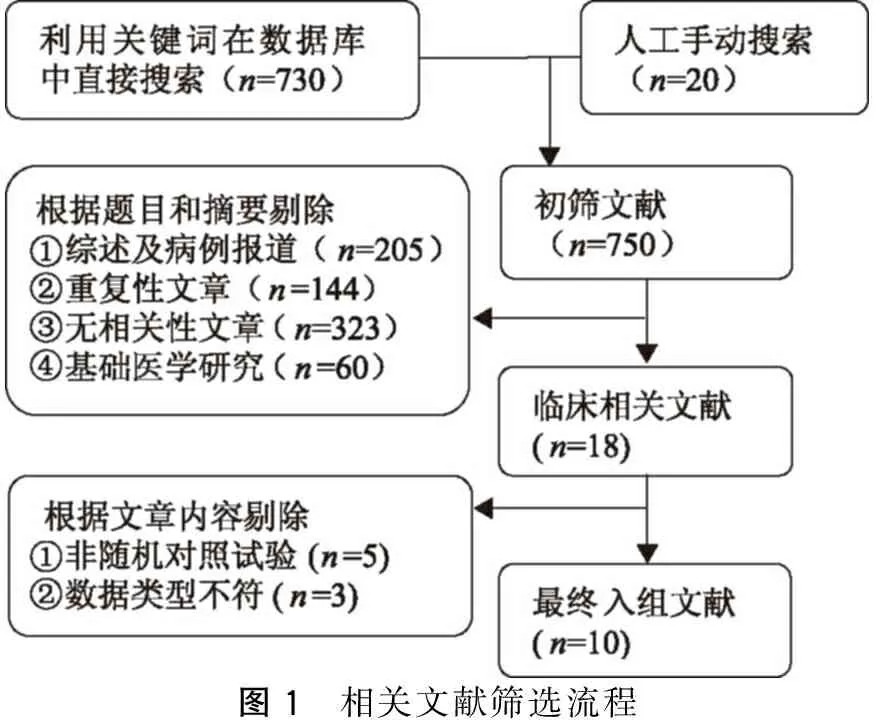
图1 相关文献筛选流程
四、质量评价
依据Newcastle-Ottawa Scale(NOS)文献质量评价量表对纳入文献进行质量评价。条目包括:①病例确定是否恰当(1分);②病例的代表性(1分);③对照的选择(1分);④对照的确定(1分);⑤设计和统计分析时考虑病例和对照的可比性(2分);⑥暴露因素的确定(1分);⑦采用相同的方法确定病例和对照组暴露因素(1分);⑧无应答率(1分)。满分为9分,累积分数越高则纳入的研究质量越高。
五、数据统计分析
采用Stata SE (12.0版)软件进行Meta分析。二分类变量采用比值比(odds ratio,OR),连续变量采用标准化均数差(standardized mean difference,SMD),区间估计均为95%可信区间(confidence interval,CI),显著性水平设定为α=0.05,P<0.05为差异有统计学意义。异质性检验采用Q检验,如果I2<50%或P>0.1,认为研究间异质性较小,选用固定效应模型(fixed effects model,FEM)Mantel-Haenszel法进行数据合并;反之则认为纳入研究间的异质性较大,分析异质性来源,进行亚组分析及敏感性分析判别,如果异质性仍存在则采用随机效应模型(random effects model,REM)M-Hheterogeneity法。
结 果
一、入组文献特征
根据以上标准,共纳入10篇文献,其中英文、中文文献各5篇,合计543例病人,578个病灶,纳入文献基本特征见表1。
二、检出率对比分析结果
按整体、病灶<2 cm、FTs,分3组采集EUS、CT、US、MRI的检出率,比较EUS较CT等其他影像学检查在检出率上的优势。分组比较EUS与CT等的检出率见表2。
1.整体检出率 共10篇文献报告了 EUS与CT在GEP-NETs整体检出率上的比较。异质性检验结果示I2=0.0%,P=0.634,提示统计学异质性小。采用OR为效应指标,以固定效应模型进行Meta分析,结果显示两种检查方式在整体病灶检出率上的差异有统计学意义(OR=4.61,95%CI:2.98,7.13,P=0.000),提示EUS较CT在GEP-NETs的整体检出率上存在优势(图2)。
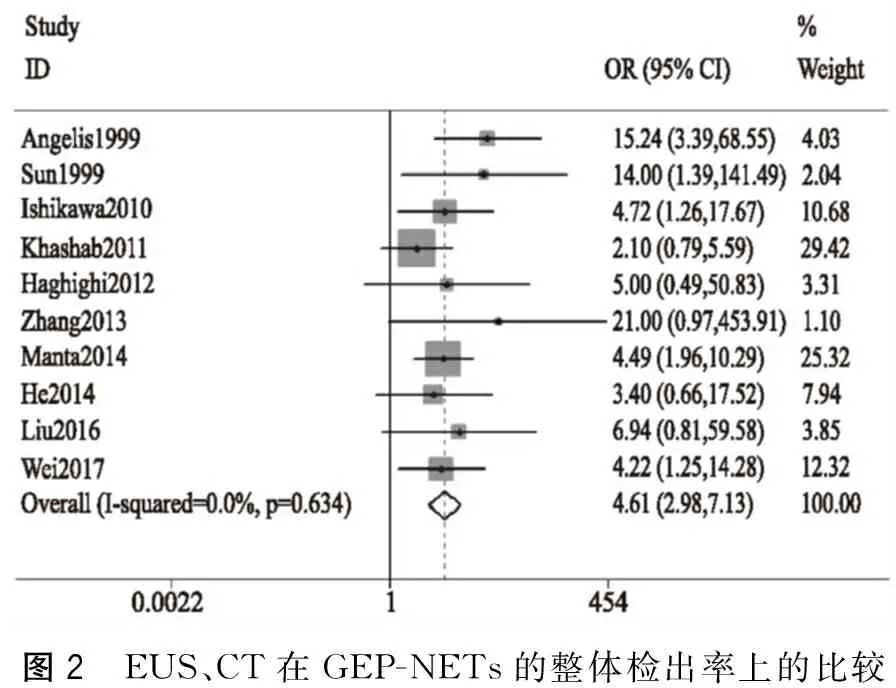
图2 EUS、CT在GEP-NETs的整体检出率上的比较
2.病灶<2 cm 共4篇文献报告了 EUS与CT在病灶<2 cm时的检出率比较。异质性检验结果示I2=27.7%,P=0.246,提示统计学异质性小。采用OR为效应指标,以固定效应模型进行Meta分析,结果显示两种检查方式在整体病灶检出率上的差异有统计学意义(OR=12.66,95%CI:6.06,26.44,P=0.000),提示EUS较CT在GEP-NETs<2 cm时检出率的具有明显优势(图3)。
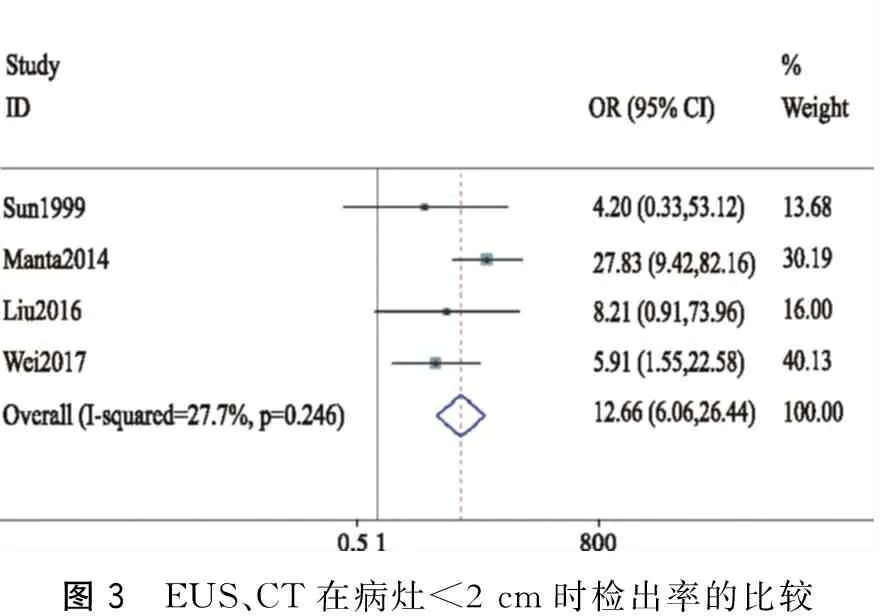
图3 EUS、CT在病灶<2cm时检出率的比较
3.FTs 共有5篇文献报告了EUS、CT在FTs上的检出率比较。异质性检验结果示I2=0.0%,P=0.975,提示统计学异质性小。采用OR为效应指标,以固定效应模型进行Meta分析,结果显示两种检查方式在FTs上检出率的差异有统计学意义(OR=5.74,95%CI:2.97,11.09,P=0.000),提示对FTs行EUS较CT在检出率上具有明显优势(图4)。

图4 EUS、CT在有功能性神经内分泌瘤(FTs)上检出率的比较
三、入组文献的质量评价和偏倚评估
以EUS、CT在GEP-NETs整体检出率上的比较(图5A)、在病灶<2 cm时检出率的比较(图5B)、在FTs上检出率的比较(图5C)分别作散点图,用来评估纳入文献的发表偏倚。结果显示,三者均大致对称分布在纵轴两侧,且基本分布于漏斗图内,提示发表偏倚的风险较小。
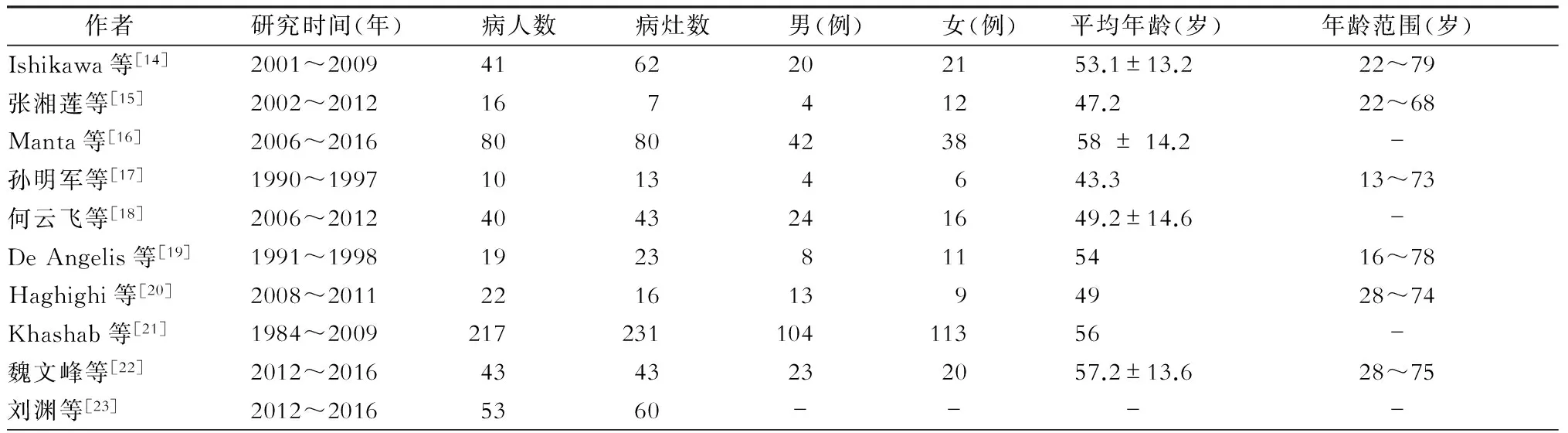
表1 纳入文献基本特征
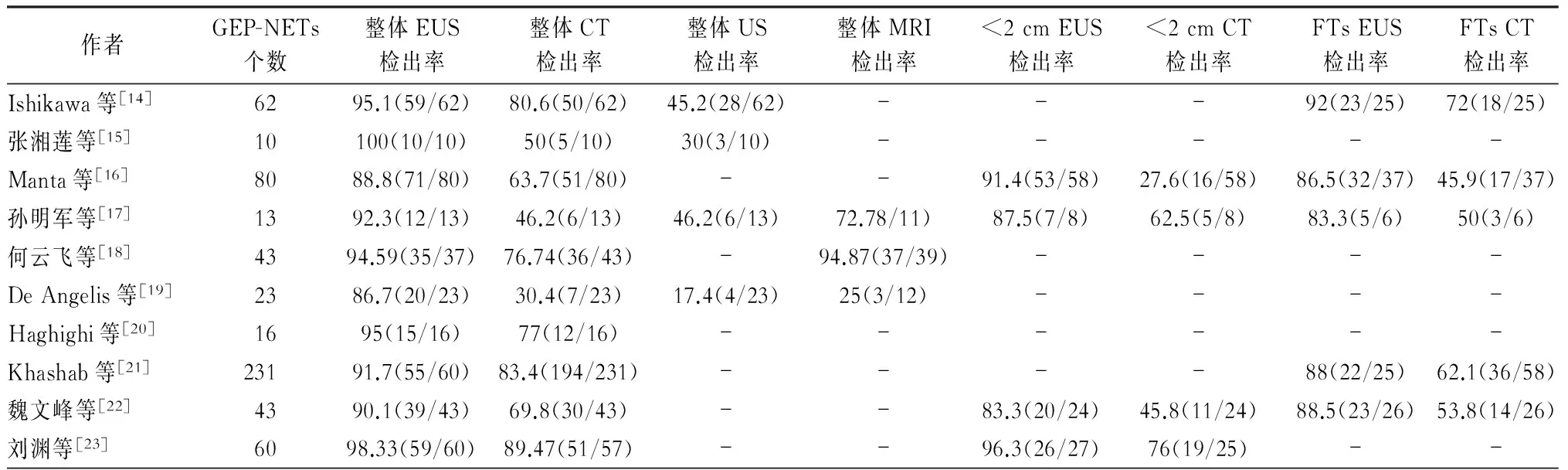
表2 分组比较EUS与CT等的检出率 [%(n/n)]
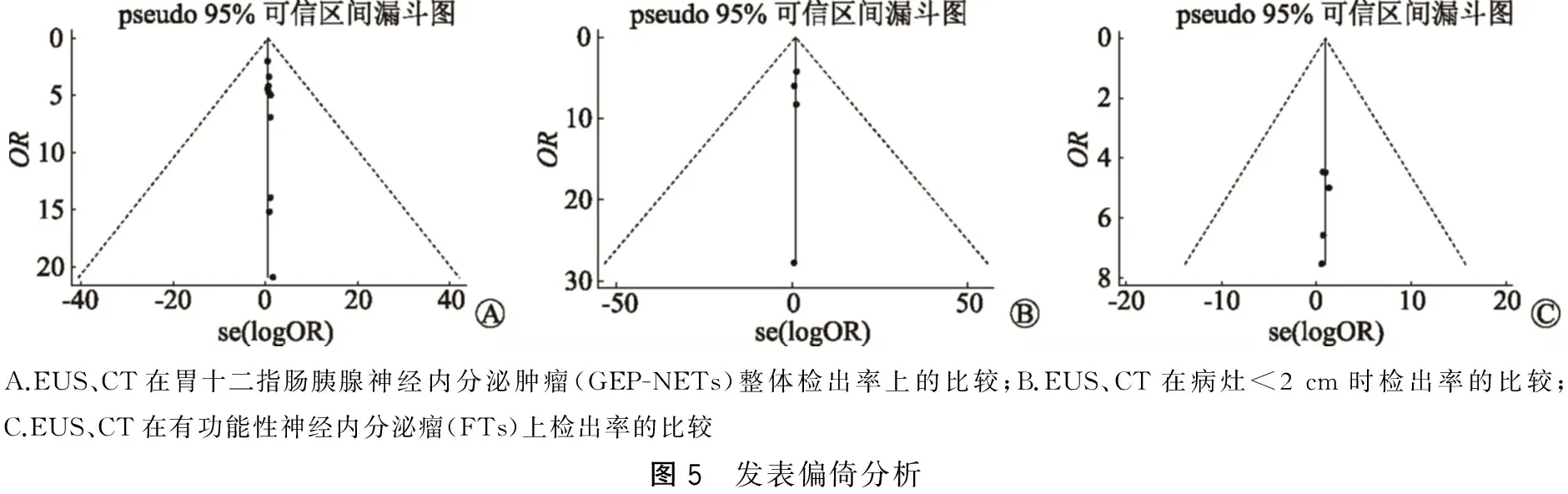
A.EUS、CT在胃十二指肠胰腺神经内分泌肿瘤(GEP-NETs)整体检出率上的比较;B.EUS、CT在病灶<2cm时检出率的比较;C.EUS、CT在有功能性神经内分泌瘤(FTs)上检出率的比较图5 发表偏倚分析
讨 论
EUS是一种20世纪80年代出现的检查技术,结合了内镜和超声的双重功能。由于胃肠道为空腔脏器,胰腺为腹膜后器官,传统的影像学检查受脂肪、肠道内气体、胃肠蠕动以及小病灶与周围组织密度或信号差异低等因素的影响,难以清晰地观察胃十二指肠及胰腺小病灶。对微小GEP-NETs的检出和准确定位一直以来都是对外科、超声科和影像科医生的挑战。EUS在内镜形态学观察的基础上,结合超声从消化道管腔内近距离检查胃十二指肠黏膜下及胰腺的微小病灶,有效避免腹壁及网膜内脂肪和胃肠道内气体的影响,并且在血流探查、细针穿刺、三维成像、弹性成像、增强扫描等技术的帮助下,弥补了内镜难以成像黏膜下病变以及CT、MRI、US等断层成像技术对小病灶(<2 cm)敏感度不够的不足。其对胃肠道管壁解剖层次的清晰显示更使得对肿瘤进行准确分期变得可行。从而使其在胃十二指肠、胰腺实质、胰管、胆管病变的定位应用越来越广。
在诊断及定位上,GEP-NETs有多发的倾向,经CT等检查怀疑此病的病人很可能有合并存在的小病灶被遗漏。 而以胰岛素瘤占绝大多数的FTs较无功能性神经内分泌瘤(NFTs)体积小,靠一般的检查手段难以发现。因此针对影像学检查发现疑似GEP-NETs单个病灶的病人,或由于激素水平升高而怀疑FTs的病人,在CT等常规检查基础上都有加做EUS全面排查胃十二指肠和胰腺的指征,以全面查清所有病灶并提供准确定位。在治疗上,现今虽然对多发、无功能、微小GEP-NETs的治疗方案仍存在争议,但手术仍是公认的治疗以改善预后的最好方法。并且随着微创技术的发展,腹腔镜手术已逐渐成为腹部手术中的主流,腹腔镜虽具有创伤小、恢复快等优点,但难以凭借触摸而只能以视觉图像定位肿瘤的先天不足使得术前精确的定位变得不可或缺。况且对GEP-NETs的切除方式又不一而同,以胰腺神经内分泌瘤中最常见的胰岛素瘤为例,手术方式就分为单纯肿瘤剔除术、胰腺部分切除术、胰体尾切除术、胰头十二指肠切除术。明确肿瘤的大小,位于胰头、胰体还是胰尾,靠近腺体的前被膜还是后被膜,与胰管及肠系膜上血管、脾血管、胰十二指肠血管等胰周重要血管之间的关系,以及是否有隐匿的多发病灶,成为制定手术方案的基础。
本研究通过Meta分析系统地评价了对GEP-NETs行EUS较CT的优势,入选的578个病灶中。EUS的检出率为86.7%~100%,CT的检出率为30.4%~89.5%,EUS较CT存在优势(OR=4.61,95%CI:2.98,7.13,P=0.000);10篇文献中的4篇对<2 cm的肿瘤进行了检出率比较,其中EUS的检出率为83.3%~96.3%,CT的检出率为27.6%~76%,EUS较CT存在明显优势(OR=12.66,95%CI:6.06,26.44,P=0.000)。5篇文献按是否有内分泌功能进行了检出率比较,其中FTs占61%,胰岛素瘤最多(80%),之后依次是类癌(8%)、胃泌素瘤(7%)、胰高血糖素瘤(3%)、血管活性肠肽瘤(1%)、生长抑素瘤(1%);EUS的检出率为83.3%~92%,CT的检出率为50%~72%,EUS较CT存在明显优势(OR=5.74,95%CI:2.97,11.09,P=0.000)。综上,EUS对于GEP-NETs,尤其是<2 cm和FTs的检出和定位较以CT为代表的传统影像学方法更有优势。从而为全面检出病灶,恰当选择治疗方案、精准定位、提高手术的有效性和准确性,最终改善病人的预后具有重要意义。
我院开展EUS诊查技术以来,有病理确诊的GEP-NETs病人26例,其中21例单发,病灶数33枚,全部接受CT检查,发现病灶28枚(85%);12例病人行EUS检查,发现病灶17枚(100%)。有功能肿瘤18枚(胰岛素瘤14枚,胃泌素瘤4枚);其中1枚<1 cm(7%),3枚<1.5 cm(21%),8枚<2 cm(57%);无功能肿瘤15枚,其中2枚<2 cm(13%)。EUS对两者的检出率均为100%,CT的检出率为72%(有功能)和100%(无功能)。CT检查阴性而EUS检查阳性病灶5枚(均小于2 cm)。结果较文献存在一定差异,可能与地区病人就诊时间晚和对EUS检查接受程度不高有关。但EUS对CT的比较优势,特别是当肿瘤有功能或<2 cm时的优势与文献结论相同。今后随着居民就医意识的提高,小病灶所占比例将逐渐提高,并且在腹腔镜手术日益普及的当下,对术前准确定位的要求也更为严格,EUS将越来越明显地体现出其较传统影像学检查的优势。实践过程中,超声内镜在技术上要求同时具备操作内镜和超声检查的能力,技术难度相对较高,其依据超声图像上的病变特征作为诊断依据,除病灶本身性质外,与操作医师的临床经验和操作熟练度密切相关。其中漏诊的重要因素是主观上对多发病灶的可能性缺乏充分认识,满足于只检出一个病灶而未进行全面扫查。
EUS的局限性:因为其需要沿胃、十二指肠壁进行探查,故其对胰腺病灶的检查需要间隔十二指肠壁进行,在准确度上要低于胃十二指肠病灶,而由于扫描距离的增加,胰尾部病灶的检出率也要低于胰头部。另外,由于EUS先端部分较长且硬,当需要深入十二指肠水平部探查胰腺钩突病灶时亦存在一定困难。文献中EUS漏诊的病例多位于胰体尾部的事实也证实了上述观点,但这些病例中CT检查亦为阴性,故对胰尾部肿瘤的诊断上,EUS仍优于CT。然而,当扫描距离更远时,如体积较大肿瘤(肿瘤的一部分远离探头)、远处转移、合并胰外病灶的肿瘤的探查能力要低于CT和MRI。综上,对于某些特殊病例,尚需在EUS的基础上结合其他影像学检查手段相互验证补充。
本文的局限性:NETs的发病率较低,各中心的研究资料较分散,可供分析的大样本临床研究较少,本文搜集的文献时间跨度较长,期间各项影像学技术的发展日新月异,相互之间的比较优势也在不断变化,因此尚需更多的临床研究汇总加以验证。
1 Halfdanarson TR, Rabe KG, Rubin J, et al. Pancreatic neuroendocrine tu-mors (PNETs): incidence, prognosis and recent trend toward improved survival. Ann Oncol, 2008,19:1727-1733.DOI:10.1093/annonc/mdn351.
2 Kimura W, Kuroda A, Morioka Y,et al. Clinical pathology of endocrine tumors of the pancre as analysis of autopsy cases. Dig Dis Sci,1991,36:933-942.
3 Kishi Y, Shimada K, Nara S, et al. Basing treatment strategy for nonfunctional pancreatic neuroendocrine tumors on tumor size. Ann Surg ncol,2014,21:2882-2888.
4 Hill JS, McPhee JT, McDade TP, et al. Pancreatic neuroendocrine tumors:the impact of surgical resection on survival. Cancer,2009,115:741-751.
5 Oberg K, Knigge U, Kwekkeboom D, et al. ESMO Guidelines Working Group.Neuroendocrine gastro-entero-pancreatic tumors: ESMO clinical practice guidelines for diagnosis, treatment and follow-up. Ann Oncol,2012,23(Suppl 7):vii124-130. DOI:10.1093/annonc/mds295.
6 Clark OH, Benson AB 3rd, Berlin JD, et al. NCCN clinical practice guidelines in oncology:neuroendocrine tumors. J Natl Compr Canc, Netw,2009,7:712-747.
7 Kunz PL, Reidy-Lagunes D, Anthony LB, et al. Consensus guidelines for the management and treatment of neuroendocrine tumors. Pancreas,2013,42:557-577. DOI:10.1097/MPA.0b013e31828e34a4.
8 Jensen RT, Cadiot G, Brandi ML, et al. ENETS consensus guidelines for the management of patients with digestive neuroendocrine neoplasms: functional pancreatic endocrine tumor syndromes. Neuroendocrinology,2012,95:98-119. DOI:10.1159/000335591.
9 Falconi M, Bartsch DK, Eriksson B, et al. ENETS consensus guidelines for the management of patients with digestive neuroendocrine neoplasms of the digestive system: well-differentiated pancreatic nonfunctioning tumors. Neuroendocrinology,2012,95:120-134.
10de Herder WW, Niederle B, Scoazec JY, et al. Well-differentiated pancreatic tumor/carcino ma: insulinoma. Neuroendocrinology,2006,84:183-188. DOI:10.1159/000098010.
11Lamberts SW, Reubi JC, Krenning EP. Somatostatin receptor imaging in the diagnosis and treatment of neuroendocrine tumors. J Steroid Biochem Mol Biol,1992,43:185-188.
12Portela-Gomes GM, Stridsberg M, Grimelius L, et al. Expression of the five different soma tostatin receptor subtypes in endocrine cells of the pancreas. Appl Immunohistochem Mol Morp hol,2000,8:126-132.
13Puli SR, Kalva N, Bechtold ML, et al. Diagnostic accuracy of endoscopic ultrasound in pan creatic neuroendocrine tumors: a systematic review and meta analysis.World J Gastroenterol,2013,19:3678-3684. DOI:10.3748/wjg.v19.i23.3678.
14Ishikawa T,Itoh A,Kawashima H,et al.Usefulness of EUS combined with contrast-enhancement in the differential diagnosis of malignant versus benign and preoperative localization of pancreatic endocrine tumors.Gastrointest Endosc,2010,71:951-959.DOI:10.1016/j.gie.2009.12.023.
15张湘莲, 覃山羽, 姜海行,等.超声内镜在诊断消化系统神经内分泌肿瘤中的作用,微创医学,2013,8:127-130. DOI:10.3969/j.issn.1673-6575.2013.02.003.
16Manta R,Nardi E,Pagano N,et al. Pre-operative diagnosis of pancreatic neuroendocrine tumors with endoscopic ultrasonography and computed tomography in a large series.J Gastrointestin Liver Dis,2016, 25: 317-321.DOI:10.15403/jgld.2014.1121.253.ned.
17孙明军, 傅宝玉,姜若兰,等. 超声内镜诊断胰腺内分泌肿瘤的价值.世界华人消化杂志,1999,7:255-257.
18何云飞,罗宴吉,彭振鹏,等. 对比不同影像学方法对胰腺神经内分泌肿瘤的检出率.中国介入影像与治疗学,2014,11:324-327. DOI:10.13929/j.1672-8475.2014.05.017.
19De Angelis C,Carucci P,Repici A, et al. Endosonography in decision making and management of gastrointestinal endocrine tumors.Eur J Ultrasound,1999 ,10:139-150.
20Haghighi S,Molaei M,Foroughi F,et al. Role of endoscopic ultrasound in evaluation of pancreatic neuroendocrine tumors - report of 22 cases from a tertiary center in iran.Asian Pac J Cancer Prev,2012,13:4537-4540.
21Khashab MA,Yong E,Lennon AM. EUS is still superior to multidetector computerized tomography for detection of pancreatic neuroendocrine tumors. Gastrointest Endosc,2011,73:691-696. DOI:10.1016/j.gie.2010.08.030.
22魏文峰,张鹏,陶超超,等. 超声内镜与多层螺旋CT诊断胰腺神经内分泌肿瘤的价值.现代肿瘤医学, 2017,25: 2318-2322. DOI:10.3969/j.issn.1672-4992.2017.14.035.
23刘渊,杨秀疆,孙波,等.内镜超声对胰腺神经内分泌肿瘤的诊断价值研究.中华消化内镜杂志,2016,10:680-683. DOI:10.3760/cma.j.issn.1007-5232.2016.10.007.
Theadvantagesofendoscopicultrasonographyongasteroentero-pancreaticneuroendocrinetumors’preoperativelocalization:aMeta-analysis
LiuYiping,LuoHaifeng,CuiShimeng,WangZhongyu.
DepartmentofHepatobilliarySurgery,theFirstHospitalAffiliatedtoDalianMedicalUniversity,Dalian116011,China
WangZhongyu,Email:fishflowers@hotmail.com
ObjectiveTo assess systematically endoscopic ultrasonography’s (EUS)advantages on preoperative localization of gastroentero-pancreatic neuroendocrine tumors (GEP-NETs).MethodsWe collected the medical literatures published domestically and abroad from Medline, PubMed, Embase, Science Citation Index, CNKI, Wanfang Database, and CQVIP. The eligible literature of studies was screened out according to the inclusion and exclusion criteria, and the reported data were aggregated statistically using StataSE 12.0 software. The inclusion criteria concern the clinical results of patients which have done imageological examinations consisting of EUS at least and confirmed by postoperative biopsy or ultrasound-guided fine needle aspiration (EUS-FNA). Type of literatures included case-control study or retrospective study.ResultsA total of 10 academic literatures were screened out, including 543 patients and 578 lesions. The overall detected rate of EUS was obviously higher than CT (OR=4.61, 95%CI: 2.98, 7.13,P=0.000). The detected rate of EUS on tumors smaller than 2 cm was obviously higher than CT (OR=12.66, 95%CI: 6.06, 26.44,P=0.000). The detected rate of EUS on functional neuroendocrine tumors (FTs) was obviously higher than CT (OR=5.74, 95%CI: 2.97, 11.09,P=0.000).ConclusionsEUS has more advantages than CT and other traditional imageological examinations on GEP-NETs' preoperative localization especially when tumors are smaller than 2 cm or being FTs.
Endoscopic ultrasonography; Computed tomography; Gastroentero-pancreatic neuroendocrine tumors; Meta analysis
116011 辽宁大连,大连医科大学附属第一医院肝胆外科
王忠裕,Email:fishflowers@hotmail.com
R735
A
10.3969/j.issn.1003-5591.2017.05.016
2017-08-16)

