间接能量消耗测定技术在腹部外科重症病人中的应用
陈宏 李非 刘大川 贾建国
·论 著·(临床实践)
间接能量消耗测定技术在腹部外科重症病人中的应用
陈宏 李非 刘大川 贾建国
目的比较外科重症病人间接测热法(indirect calorimetry, IC)与校正Harris-Benedict公式计算的能耗值之间的差异,并且评估接受机械通气的危重症病人能耗水平与疾病严重程度的相关性。方法2015年2月至2016年10月间进入外科重症监护病房、符合本项研究入选标准的成年危重症病人共24例。24例病人在本研究开始时正在接受机械通气治疗。营养治疗期间收集入选病人急性生理与既往健康状况评分(APACHEⅡ评分)和器官功能不全评分(Marshall评分),以评价其疾病严重程度。营养治疗1周内,每日采用IC测定能耗;同时,由依据疾病严重程度而校正的Harris-Benedict公式计算能耗值,以便比较接受机械通气治疗的外科重症病人能耗测定值与计算值的差异。结果营养治疗1周内,24例病人平均能耗计算值为(8 670.88±1 828.53) kJ/d[即(2 072.39±437.03) kcal/d],明显高于平均能耗测定值的(6 683.90±1 981.75) kJ/d [即(1 597.49±473.65) kcal/d],两者间差异具有统计学意义(P<0.001);营养治疗当天、第1、2、4天的能耗计算值明显高于测定值,其差异具有统计学意义(P<0.05)。营养治疗1周内,入选病人的能耗计算值与测定值之间无相关性(r=0.048,P=0.565)。另外,营养治疗1周内的能耗测定值与 APACHEⅡ评分之间也没有相关性(r=-0.032,P=0.602)。结论接受机械通气的外科重症病人的能耗与疾病严重程度无关;基于病情状态和严重程度而校正的Harris-Benedict公式明显高估了病人实际能耗水平;IC是评价危重症病人能耗水平的标准方法。
能量消耗; 间接能量消耗测定仪; 机械通气; 危重症
重症病人营养不足是普遍存在的问题[1]。充分的营养支持可减少病人术后并发症,改善预后,缩短住院时间,降低医疗费用[2]。因此,合理而有效的营养支持是重症监护病房(intensive care unit, ICU)诸多治疗技术和手段中不可或缺的重要组成部分[3],而对病人能量需求或能耗的准确判定又是优化营养支持的前提。低估病人能量需求可能导致营养支持不足,损害组织器官功能,抑制免疫反应和细胞修复,增加术后并发症和延长住院时间[4];高估能量需求又可产生营养过度的损害作用,如机械通气时间延长、高血糖、高渗状态、肝功能异常、氮质血症和免疫功能损伤[5]。临床评估重症病人的能量消耗分为公式计算法与间接测热法(indirect calorimetry, IC),前者不够准确而后者并不普及。近年来在治疗危重疾病理念方面的转变,影响了ICU病人的代谢需求,如广泛应用止痛药、镇静剂、神经肌肉阻断剂、儿茶酚胺类药物、血管活性类药物等,这些因素都对能耗产生作用[6]。还有,近年ICU病人组成结构有了变化,如老年人和营养不良病人的比例有所增加,这是影响能量需求的两个重要因素。上述状况的出现,引发人们对能量消耗预测公式潜在缺陷的忧虑[7]。
对象与方法
一、研究对象
我们运用IC对机械通气治疗的外科重症病人进行静息能量消耗的测定,并且将测定结果与Harris-Benedict(H-B)公式法计算值相比较。本文回顾分析2015年2月至2016年10月间收治外科ICU需营养支持并进行了IC测定且机械通气时间>7 d病人的数据。由经IC操作培训的ICU医师进行静息能耗测定。研究入选标准为同时满足下列条件:①年龄>18岁;②机械通气治疗时间>7 d;③存在营养治疗适应证,并且营养治疗时间>7 d。出现下列情况者不适用于IC测定而不能纳入研究对象,因为这些状况可增加IC测量错误:①血流动力学不稳定而需要血管活性药物或儿茶酚胺类药物维持组织灌注压;②呼吸状态不稳定,需要频繁调整吸入氧浓度或机械通气条件;③体内二氧化碳缓冲储备池变动大,如需要经常输注碳酸氢盐,或者碳酸氢盐通过肾脏、消化道大量丢失;④酮症或代谢性酸中毒。符合入选标准的已入选病人,在以下情况出现时避免应用IC测定能量消耗:①需要维持吸入氧浓度>60%;②术后24 h内;③存在气管插管或呼吸机管路漏气现象;④血液净化过程中;⑤转运或搬动后60 min内;⑥静息60 min仍不能达到稳定状态。
二、营养支持与能耗指标测定
本研究IC测定使用的是由美国MEDICAL GRAPHICS 公司生产的The MedGraphics CCM/D System能量代谢测定系统[IC不是直接测定能耗,是通过测定吸入气与呼出气之间的氧浓度之差(VO2)、呼出气与吸入气间二氧化碳浓度差(VCO2),并且经Weir公式[8]计算后在显示器显示能耗值]。在营养治疗的1周内,每天进行测定。所有入选病人在保持血流动力学相对稳定的情况下,进行早期营养评估;对存在营养治疗适应证的病人给予肠内和(或)肠外营养。若胃肠功能恢复则给予肠内营养(enteral nutrition, EN);因胃肠道功能障碍而不能进行肠内营养者,给予肠外营养治疗(parenteral nutrition, PN)。所有接受EN病人,在营养治疗期间内均未达到完全肠内营养水平,故而采用EN+PN方式进行营养支持。根据IC测定的能耗结果,调整营养治疗配方中的能量供给;蛋白质的提供量为1.6~1.8 g·kg-1·d-1(非蛋白热卡:氮为100∶1~120∶1;糖∶脂为1∶1~2∶1)。
测试前60 min让病人静息无刺激,平静仰卧30 min后接受连续且无干扰的静息能耗测定。控制环境温度23℃~25℃、湿度54%~62%;连接气管导管后适应10 min,收集35 min的呼出和吸入气体测定氧消耗(VO2)与二氧化碳产生(VCO2),根据Weir公式[8]计算出能量消耗值。取30 min内稳定状态时所有读数的平均值(稳态持续时间>15 min),作为此次测量的能耗值。稳定状态的定义是:在任意5 min时间段内,平均每分钟VO2和VCO2的变异系数<5%。
三、H-B公式计算能耗
首先计算基础能耗:男性基础能耗(kcal)=66.47+13.75W+5.00H-6.76A;女性基础能耗(kcal)=655.10+9.56W+l.85H-4.68A[W:理想体重(kg);H:身高(cm);A:年龄]。H-B校正能耗=H-B计算基础能耗×活动系数×应激系数;应激系数:体温在37 ℃以上,每升高1℃增加13%;中等手术为1.2;大手术或严重创伤1.35;全身性感染为1.6。我们认为活动系数为1,因为所有入选病人均为卧床休息。
四、疾病严重程度指标
疾病严重程度采用急性生理与既往健康状况评分Ⅱ(acute physiology and chronic health evaluationⅡ,APACHEⅡ)和多器官功能不全评分(multiple organ dysfunction score,Marshall 评分)进行评估。观察入选病人营养治疗当天至第7 天每日APACHEⅡ评分和Marshall 评分的变化趋势。
五、统计方法
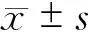
结 果
一、基本资料
共纳入符合上述研究标准的病人24例,其中8例重症急性胰腺炎病人,5例因胰腺坏死感染而接受手术治疗;4例因肠梗阻行手术治疗;5例因胃肠穿孔并腹腔感染而手术治疗;2例因急性胆囊炎、胆囊坏疽接受手术治疗;5例急性梗阻性化脓性胆管炎病人。男性15例,女性9例;年龄27~83岁,平均(65.27±14.36) 岁;身高(169.92±7.34) cm;体重(69.12±15.58) kg。根据H-B公式计算得出基础能耗值为(6 093.03±1 026.42) kJ/d[即(1 456.27±245.32) kcal/d]。入选病人在进入ICU 1周内开始营养支持,其中13 例病人接受PN+EN治疗;11例病人接受PN治疗;所有入选病人在研究期间未发生与营养治疗相关的并发症。
二、疾病严重程度
营养治疗1周内APACHEⅡ、Marshall评分变化见表1。入选病人在营养治疗1周内疾病严重程度明显缓解,APACHEⅡ评分和Marshall评分显著降低,其差异具有统计学意义。

表1 APACHEⅡ和Marshall评分±s)
注:PN0~PN7为营养治疗当天至第7天;P值为营养治疗1周内APACHEⅡ评分和Marshall评分变化趋势的统计值
三、能耗指标
营养治疗1周内,IC能耗测定值(简称测定值)与H-B公式计算值(简称计算值)的变化见表2。营养治疗1周内测定值的变化差异无统计学意义;而计算值呈进行性下降,其差异具有统计学意义。营养治疗1周内,每日测定值均较计算值低,平均每日测定值为(6 683.90±1 981.75) kJ/d [即(1 597.49±473.65) kcal/d],平均每日计算值为(8 670.88±1 828.53) kJ/d [即(2 072.39±437.03) kcal/d],平均每日测定值也明显低于平均每日计算值,其差异具有统计学意义(P<0.001)。

表2 营养治疗1周内能耗值±s,kJ/d)
注:a.营养治疗1周内每日测定值和计算值比较的统计值;b.营养治疗1周内测定值、计算值变化趋势的统计值
四、能耗与其他指标的相关性
营养治疗1周内,能耗测定值与计算值的变化趋势之间无相关性(r=0.048,P=0.565)。随着疾病严重程度的降低,计算值与APACHEⅡ(r=0.618,P<0.001)和Marshall评分(r=0.665,P<0.001)均呈下降趋势,它们之间的变化呈正相关;而测定值与APACHEⅡ评分(r=-0.032,P=0.602)之间无相关性,但与Marshall评分(r=0.361,P=0.001)呈正相关。
五、按理想体重计算的能耗
营养治疗1周内,按理想体重计算的能耗测定值低于按理想体重计算的能耗计算值(表3);平均每日每千克体重测定值为(94.52±22.76) kJ·kg-1·d-1[即(22.59±5.44) kcal·kg-1·d-1],平均每日每千克体重计算值为(124.26±35.64) kJ·kg-1·d-1[即(29.70±8.52) kcal·kg-1·d-1],前者低于后者,其差异具有统计学意义(P<0.001)。

表3 按理想体重计算的能耗比较±s)
注:a.营养治疗1周内每日每千克体重测定值与每日每千克体重计算值比较的统计值;b.营养治疗1周内每日每千克体重测定值、每日每千克体重计算值变化趋势的统计值;根据临床的实际工作以及国内外相关指南,此处的单位仍采用kcal·kg-1·d-1
讨 论
合理的营养治疗可以降低危重症病人病残率和病死率,而营养过度或营养不足导致的并发症对机体是有害的。为满足接受营养治疗病人的能量需求,并且避免营养过度或不足所导致的并发症,准确评估重症病人实际能耗是非常必要的。临床上,能耗的评估分为IC测定法和公式预测法。然而,临床常通过数学公式计算的方法预测接受营养治疗病人的能量需求。由于成本费用、设备利用率、人员培训和耗时等原因,临床很少应用IC测量能耗,而更多地应用H-B公式法预测能耗[9]。另外,临床也有通过理想体重粗略估算能量需求的方法。我们运用IC法测定危重症病人的能量消耗,并将其与公式法和体重法的预测能耗值进行比较。由于危重症病人能量代谢不稳定特点,应当动态监测能量需求的变化,而这正是应用IC测定的优势所在[10]。
H-B公式法的缺陷在于它很少考虑危重症病人的差异性、危重疾病演进过程、伴随疾病状态、并发症发生和治疗等相关的机体代谢变化。有研究显示H-B公式预测的能量消耗超出IC测定的实际能耗5%~15%[11];还有研究显示H-B公式计算值与实际能耗水平间并没有相关性[12];在危重症病人中,其相关性更差[13]。本研究结果也支持这样的结论:IC能耗测定值与H-B公式计算值之间无相关性。根据H-B评估法所制订和实施的营养支持方式,对需要营养支持的病人预后可能会产生不利影响[14]。随着对危重症病人医疗和护理研究的进展、镇静剂应用观念的转变、正性肌力药物的广泛应用,出现了住院病人、特别是ICU病人代谢率降低的趋势[15]。入选本研究的病人都不同程度地受上述因素的影响,因此他们总体上存在比能耗预测值相对低的代谢状态,即IC测定的能耗水平低于校正的H-B公式法计算的能耗值。其原因除H-B公式校正系数存在主观性、片面性外,其他可能的影响因素为:①危重症病人组织细胞氧摄取、利用减少,可能导致能量代谢水平降低;②本研究病人在机械通气治疗期间应用了镇静剂,从而降低了能耗;③呼吸机治疗通过减少呼吸功耗,从而降低能耗。
为了临床应用简便,也有学者建议以体重作为唯一参数预测能量需求,例如按每千克体重设定所需热卡指标。按体重预估能耗法并没有考虑到不同年龄、性别、疾病状态和治疗方法对能耗所产生的不同作用。美国重症医学会(The American College of Critical Care Medicine,ACCM)和美国肠外与肠内营养学会(American Society for Parenteral and Enteral Nutrition, ASPEN)的营养治疗指南[16]中建议危重症病人营养治疗时,能量按20~25 kcal·kg-1·d-1供给;而非危重疾病或严重损伤、也不存在再喂养综合征病人的能量需求按25~30 kcal·kg-1·d-1供给,其中体重为理想体重。ICU病人体重每天都可能发生改变,因为危重症病人存在因组织水肿和细胞内外水平衡的失调,导致体重随病情发展而改变的情况。此时,实际体重的变化并不能反映体内组织细胞群的代谢改变。本研究将能耗IC测定值和H-B公式计算值分别按理想体重计算得到每日每千克体重的测定值和计算值。研究期间,每日每千克体重的测定值均明显低于每日每千克体重的计算值;营养治疗1周内平均每日每千克体重的测定值为(22.59±5.44) kcal·kg-1·d-1,也低于平均每日每千克体重的计算值[(29.70±8.52) kcal·kg-1·d-1]。本研究期间的平均每日每千克体重的测定值与ACCM和ASPEN建议的危重症病人营养治疗的能量供给范围(20~25 kcal·kg-1·d-1)相吻合;而若依据平均每日每千克体重的计算值提供能量,则更可能超出这一范围。基于本项研究结果,若医院没有IC测定系统时,我们不建议临床医生在制定营养配方时使用H-B公式法计算能量需求,而建议采用营养指南推荐的基于体重估算法的能量供给范围,其优势在于简单快捷,且相对准确。在实际临床实践中常常遇到的问题是,我们如何对特定病人设定能量供给值。此时,我们依据主观的病情判断、临床营养经验和所在学科的专业知识估计能量给予值。这种可能带有偏见的评估结果会导致能量给予错误(即高估或低估危重症病人能量需求),而产生营养过度或营养不足。ACCM和ASPEN建议ICU病人能耗评估,应以能反映个体间差异的IC测定为标准的评估方法,指导制订合理、安全而有效的营养治疗配方,减少或避免与营养治疗相关的代谢并发症或器官功能损害[16]。
我们的研究具有一定的局限性:①纳入研究的病人样本量少,结果可靠性受到影响;②本研究仅限于机械通气的普通外科危重症病人,将本研究结果作为其他疾病病人营养治疗目标的依据时应慎重。
1 Singer P, Anbar R, Cohen J, et al. The tight calorie control study (TICACOS): a prospective, randomized, controlled pilot study of nutritional support in critically ill patients. Intensive Care Med, 2011, 37:601-609. DOI: 10.1007/s00134-011-2146-z.
2 Heyland DK, Cahill N, Day AG. Optimal amount of calories for critically ill patients: depends on how you slice the cake! Crit Care Med, 2011, 39:2619-2626.DOI: 10.1097/CCM.0b013e318226641d.
3 Berger MM, Pichard C. Best timing for energy provision during critical illness. Crit Care, 2012, 16:215-221. DOI: 10.1186/cc11229.
4 Faisy C, Lerolle N, Dachraoui F, et al. Impact of energy deficit calculated by a predictive method on outcome in medical patients requiring prolonged acute mechanical ventilation. Br J Nutr, 2009, 101:1079-1087. DOI: 10.1017/S0007114508055669.
5 Alberda C, Gramlich L, Jones NE, et al. The relationship between nutritional intake and clinical outcomes in critically ill patients: results of an international multicenter observation study. Intensive Care Med, 2009, 35:1728-1737. DOI: 10.1007/s00134-009-1567-4.
6 Heyland DK, Dhaliwal R, Jiang X, et al. Identifying critically ill patients who benefit the most from nutrition therapy: the development and initial validation of a novel risk assessment tool. Crit Care, 2011, 15:R268-278. DOI: 10.1186/cc10546.
7 Pinheiro Volp AC, Esteves de Oliveira FC, Duarte Moreira Alves R, et al. Energy expenditure: components and evaluation methods. Nutr Hosp, 2011, 26:430-440. DOI: 10.1590/S0212-16112011000300002.
8 de Weir JB. New methods for calculating metabolic rate with special reference to protein metabolism. J Physiol, 1949, 109:1 9.
9 Lev S, Cohen J, Singer P. Indirect calorimetry measurements in the ventilated critically ill patient: facts and controversies the heat is on. Crit Care Clin, 2010, 26:e1-9.DOI: 10.1016/j.ccc.2010.08.001.
10De Waele E, Spapen H, Honor PM, et al. Introducing a new generation indirect calorimeter for estimating energy requirements in adult intensive care unit patients: feasibility, practical considerations, and comparison with a mathematical equation. J Crit Care, 2013, 28:884.e1-e6. DOI: 10.1016/j.jcrc.2013.02.011.
11da Rocha EE, Alves VG, da Fonseca RB. Indirect calorimetry: methodology, instruments and clinical application. Curr Opin Clin Nutr Metab Care, 2006, 9:247-256. DOI: 10.1097/01.mco.0000222107.15548.f5.
12Wooley JA. Indirect calorimetry: applications in practice. Respir Care Clin N Am, 2006, 12:619-633. DOI: 10.1016/j.rcc.2006.09.005.
13Flancbaum L, Choban PS, Sambucco S, et al. Comparison of indirect calorimetry, the Fick method, and prediction equations in estimating the energy requirements of critically ill patients. Am J Clin Nutr, 1999, 69:461-466.
14Frankenfield DC, Ashcraft CM. Estimating energy needs in nutrition support patients. JPEN J Parenter Enteral Nutr, 2011, 35:563-570. DOI: 10.1177/0148607111415859.
15Singer P. Toward protein-energy goal-oriented therapy? Crit Care, 2009, 13:188-189. DOI: 10.1186/cc8042.
16McClave SA, Taylor BE, Martindale RG, et al. Guidelines for the Provision and Assessment of Nutrition Support Therapy in the Adult Critically Ill Patient: Society of Critical Care Medicine (SCCM) and American Society for Parenteral and Enteral Nutrition (A.S.P.E.N.). JPEN J Parenter Enteral Nutr, 2016, 40:159-211. DOI: 10.1177/0148607115621863
Applicationofindirectcalorimetryforenergyexpendituremeasurementinsurgicalcriticallyillpatients
ChenHong,LiFei,LiuDachuan,JiaJianguo.
DepartmentofGeneralSurgery,XuanwuHospitalofCapitalMedicalUniversity,Beijing100053,China
ChenHong,E-mail:chenhong@medmail.com.cn
ObjectiveTo compare the indirect calorimetry (IC) measured energy expenditure (MEE) with adjusted Harris-Benedict formula calculating energy expenditure (CEE) in the mechanically ventilated surgical critically ill patients and to evaluate the relationship between the energy expenditure (EE) with the severity of illness.MethodsTwenty-four adult patients receiving mechanical ventilation for critical illness in the general surgery intensive care unit between February 2015 and October 2016 were eligible for inclusion of the study. Data during the study period of nutrition support were collected for computation of the severity indices of critical illness, Acute Physiology and Chronic Health Evaluation Ⅱ (APACHE Ⅱ score) and Marshall score. EE was measured for those enrolled critically ill mechanically ventilated patients (n=24) using IC within the first 7 days after nutrition therapy. Predicted EE was obtained at the same time for each patient using the Harris-Benedict equation calculated from the value adjusted with correction factors for illness to determine the discrepancy between MEE and CEE.ResultsIn a group of 24 acutely ill surgical patients, the mean predicted metabolic requirements based on Harris-Benedict equation with the addition of stress factors (8670.88±1828.53) kJ/day [(2072.39±437.03) kcal/day] were greater than the mean metabolic expenditures measured by IC (6683.90±1981.75) kJ/day [(1597.49±473.65) kcal/day],P<0.001. During the first week of nutritional support, the differences between MEE and CEE in these patients were statistically significant on admission and 1, 2, 4 days after nutrition therapy (P<0.05). There was little correlation between MEE and CEE (r=0.048,P=0.565). Moreover, no statistically significant correlation was observed between MEE and APACHEⅡ scores (r=-0.032,P=0.602).ConclusionsIn mechanically ventilated patients, the EE is not correlated with the severity of illness. The Harris-Benedict prediction modified with correction factors for severity of illness systematically overestimates the EE. IC is the criterion method of choice for determining EE for nutrition support in critically ill patients receiving mechanical ventilation.
Energy expenditure; Calorimetry, indirect; Mechanical ventilation; Critical illness
国家卫生计生委重点临床专科建设项目—重症医学科[卫办医政函(2012)649号]
100053 北京,首都医科大学宣武医院普外科
陈宏,Email:chenhong@medmail.com.cn
R459.3
A
10.3969/j.issn.1003-5591.2017.05.014
2017-03-22)

