甲醇+碳酸二甲酯+二乙二醇三元物系等压汽液平衡数据的测定与关联
曹 玲,徐威震,李学琴,程建文
(昌吉学院 化学与应用化学系,新疆 昌吉 831100)
甲醇+碳酸二甲酯+二乙二醇三元物系等压汽液平衡数据的测定与关联
曹 玲,徐威震,李学琴,程建文
(昌吉学院 化学与应用化学系,新疆 昌吉 831100)
在101.3 kPa下,采用改进的Othmer釜测定了甲醇+碳酸二甲酯(DMC)+二乙二醇三元物系的等压汽液平衡数据。实验结果表明,二乙二醇萃取剂的加入,降低了甲醇对DMC的相对挥发度,提高了物系的平衡温度。二乙二醇不适合作为萃取精馏分离甲醇+ DMC物系的萃取剂。用NRTL模型对DMC +甲醇+二乙二醇三元物系溶剂比为0.25,0.5,1时汽液平衡实验数据进行了关联,温度标准偏差最大为0.63 K。
碳酸二甲酯;甲醇;二乙二醇;NRTL模型
碳酸二甲酯(DMC)是一种绿色环保工业原料,可用于替代毒性较大的碳酰氯、氯甲烷、氯甲酸甲酯等有机试剂反应而生成重要的化工产品,在高分子合成、农药生产、医药制备、燃料添加剂及溶剂中有广泛应用[1]。通过酯交换法制备DMC所得产物中常含有未完全反应的甲醇,而在常压下甲醇与DMC易形成共沸物。使用工业上普通精馏的方法难以将共沸物系分离,萃取精馏法是分离共沸物常用的方法,萃取剂的合理使用关系萃取精馏的能耗[2]。目前,可用于分离甲醇+ DMC二元物系的萃取剂包括取代苯类[3-7]、酯类[8-10]、糠醛[11-13]、苯酚[14-15]和离子液体[16-19]。萃取剂的加入,试图削弱待分离组分之间的作用力,从而改变待分离组分之间的相对挥发度。二乙二醇具有沸点高、溶解性好、吸水性强等特点,形成氢键的能力较强,可能适合作为分离甲醇和DMC共沸物的萃取剂。
为检验二乙二醇作为萃取剂分离甲醇+ DMC物系的可行性,本工作在101.3 kPa下,测定了甲醇+ DMC +二乙二醇三元物系的等压汽液平衡数据,并讨论了二乙二醇对甲醇+DMC二元物系相平衡的影响。
1 实验部分
1.1 试剂
甲醇、DMC:分析纯,天津富宇精细化工有限公司;二乙二醇:分析纯,天津光复精细化工有限公司。所有试剂经气相色谱分析无杂质峰。
1.2 测定方法
采用改进的Othmer釜测定汽液平衡数据。具体实验装置见文献[20]。
采用精度为0.000 1 g的电子天平称重法配制甲醇+ DMC二元物系或甲醇+ DMC +二乙二醇三元物系溶液各50 m L,然后把溶液加入平衡釜中,加热至沸腾,平衡室温度恒定不变时认为物系达到平衡,保持平衡状态约30 min,然后采用1 μL微量进样器分别从汽相、液相取样口取样分析。
1.3 分析方法
采用日本岛津公司GC-2010型气相色谱仪分析试样的组成,RTX-1非极性色谱柱,长度30.0 m,内径0.25 mm,膜厚0.25 μm,载气(氮气)流量46.7 m L/m in,气化室温度523 K,FID检测523 K,采用程序升温,柱箱温度见表1。采用面积归一化法定量计算。

表1 程序升温的柱箱温度Table 1 Programmed temperature of oven
2 结果与讨论
2.1 实验装置的可靠性检验
为验证实验装置的可靠性,测定了101.3 kPa下甲醇(1)-DMC(2)二元物系的等压汽液平衡数据,见表2。同时,对二元实验数据进行了面积法的热力学一致性检验[21]。在进行检验时,由式(1)计算组分的活度系数。甲醇和DMC的饱和蒸汽压通过安托因公式计算,所需的安托因系数见文献[22]。式中,γi为组分i的活度系数;yi为组分i的气相摩尔分数;p为系统总压,kPa;为组分i在平衡温度下的饱和蒸气压,kPa。


表2 甲醇(1)+ DMC(2)二元物系等压(101.3 kPa)汽液相平衡数据Table 2 Isobaric vapor-liquid equilibrium data for methanol(1) +dimethyl carbonate(DMC)(2) system at 101.3 kPa
在进行热力学一致性检验时,根据计算的组分的活度系数,做ln(γ1/γ2)- x1图,见图1。A部分的面积(SA)和B部分的面积(SB)为SA= 0.253 1,SB= 0.306 2。按式(2)~(3)计算偏差和压力熵。
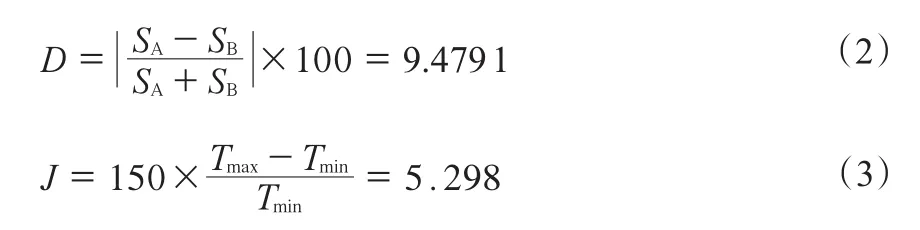
式中,D为偏差;J为压力熵;Tmax(348.8 K)和Tmin(336.9 K)分别为实验中最高和最低平衡温度。

图1 热力学一致性检验Fig.1 Thermodynam ic consistency.
2.2 汽液平衡数据
在101.3 kPa下,测定了二乙二醇在三种不同溶剂比(0.25,0.5,1)下的甲醇+ DMC +二乙二醇三元物系等压汽液平衡数据,见表2。

表2 甲醇(1)+ DMC(2)+二乙二醇(3)三元物系等压(101.3 kPa)汽液相平衡数据Table 2 Vapor-liquid equilibrium data for the methanol(1) + DMC(2) + diethylene glycol(3) system at 101.3 kPa
2.3 数据关联
选用NRTL模型对实验数据进行关联,采用非线性最小二乘法,关联时的目标函数(F)为:
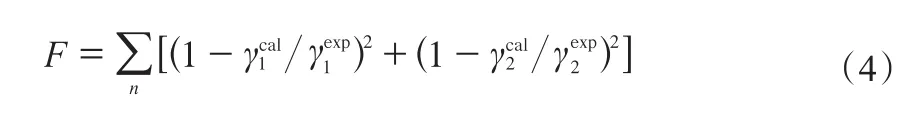
在关联过程中,由二元物系的汽液平衡数据先确定甲醇(1)-DMC(2)二元物系NRTL模型的相互作用参数,然后根据三元物系的汽液平衡数据确定甲醇(1)-二乙二醇(3)、DMC(2)-二乙二醇(3)二元物系NRTL模型的二元相互作用参数,NRTL模型参数及关联偏差结果见表3。由表3可知,温度标准偏差最大为0.63 K。
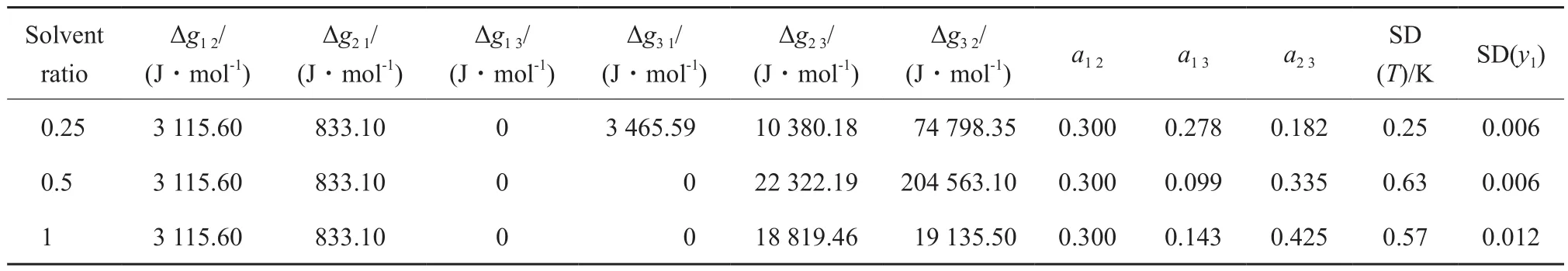
表3 甲醇(1)+ DMC(2)+二乙二醇(3)三元物系NRTL模型的二元相互作用参数及关联偏差Table 3 Binary parameters of the NRTL model Δgij and standard deviations(SD) for the methanol(1) +DMC(2) + diethylene glycol(3) system
2.4 讨论
图2为甲醇+ DMC+二乙二醇三元物系的y1-x′1相图。图3为甲醇+ DMC +二乙二醇三元物系的T - x′1- y相图。图4为二乙二醇对甲醇+ DMC二元物系相对挥发度的影响。由图2~4可知,二乙二醇的加入使汽液平衡线偏离无萃取剂时的汽液平衡曲线,使甲醇+ DMC物系的共沸点向甲醇的低浓度方向移动。随二乙二醇加入量的增多,平衡温度也随之提高。二乙二醇的加入降低了甲醇对DMC的相对挥发度。
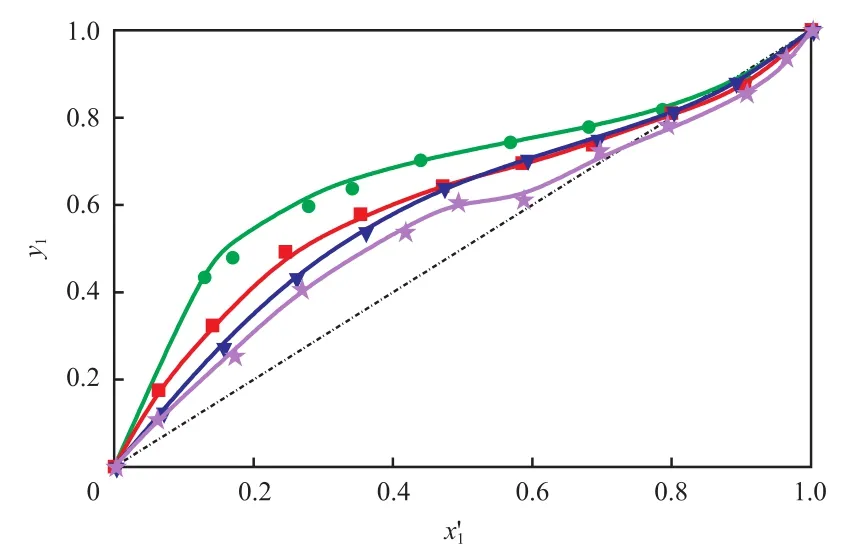
图2 101.3 kPa下甲醇(1)+ DMC(2)+二乙二醇(3)三元物系的 y1-x′1 相图Fig.2 y1-x′1 Diagram for the methanol(1) + DMC(2) + diethylene glycol(3) system at 101.3 kPa.
图5为二乙二醇对甲醇+ DMC活度系数的影响。由图5可知,二乙二醇对甲醇作用力大,使得甲醇的活度系数在甲醇的整个浓度范围减少占主导优势,抑制了甲醇向气相逸出的能力。二乙二醇的加入使得甲醇对DMC的挥发度减少。在溶剂比为1时,不能消除甲醇+ DMC共沸物系的共沸点。随二乙二醇在物系中含量的增加,物系的平衡温度升高,说明在萃取精馏过程中消耗了更多的加热蒸汽。因此,二乙二醇不适合作为萃取精馏分离甲醇+ DMC物系的萃取剂。
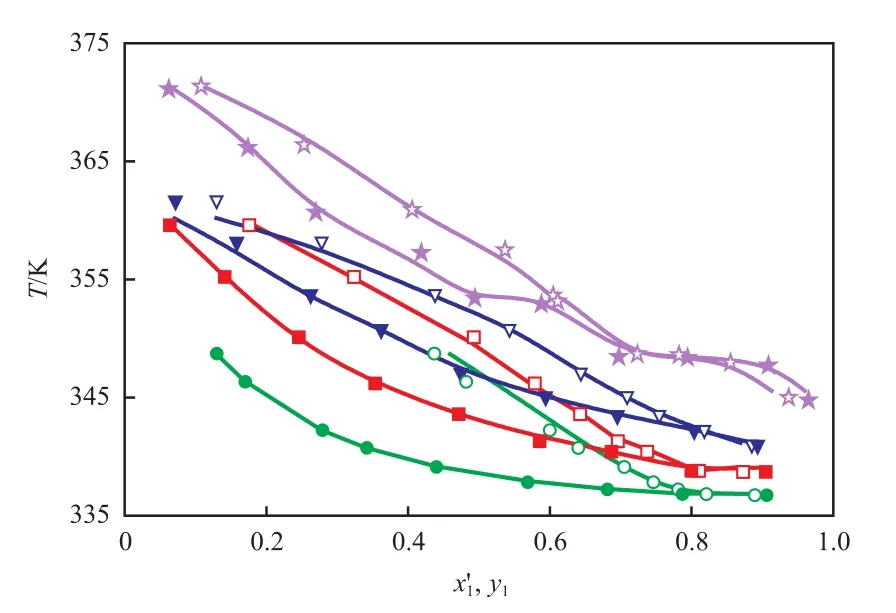
图3 101.3 kPa下甲醇(1)+ DMC(2)+二乙二醇(3)三元物系的 T-x′1 -y 相图Fig.3 T - x′1 - y Diagram for the ternary system of methanol(1) +DMC(2) + diethylene glycol(3) system at 101.3 kPa.
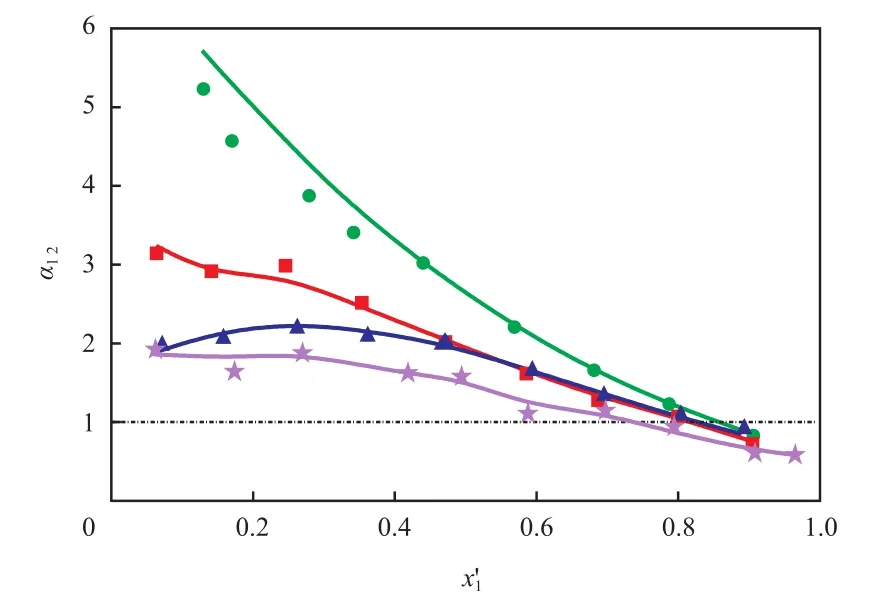
图4 101.3 kPa下二乙二醇(3)对甲醇(1)-DMC(2)相对挥发度的影响Fig.4 The effect of diethylene glycol(3) on relative volatility(α12)of methanol(1) to DMC(2) at 101.3 kPa.

图5 101.3 kPa下二乙二醇(2)对甲醇(1)+ DMC(2)活度系数的影响Fig.5 Effect of diethylene glycol(3) on γi of methanol(1) + DMC(2) at 101.3 kPa.
3 结论
1)在101.3 kPa下,测定了溶剂比为0.25,0.5,1时甲醇+ DMC +二乙二醇三元物系的汽液平衡数据。
2)由实验数据分别回归得到溶剂比为0.25,0.5,1时甲醇+ DMC +二乙二醇物系的NRTL模型二元相互作用参数,温度标准偏差最大为0.63 K。
3)在甲醇+ DMC物系中加入二乙二醇,降低了甲醇对DMC的相对挥发度,提高了物系的平衡温度。二乙二醇不适合作为萃取精馏分离甲醇+DMC物系的萃取剂。
符 号 说 明
aijNRTL模型的非随机性参数
D 偏差
F 目标函数
ΔgijNRTL模型二元交互作用参数,J/mol
J 压力熵
N 实验数据的个数
p 系统总压,kPa
psiat组分i的在平衡温度下的饱和蒸气压,kPa
S 面积,m2
SD 标准偏差
T 平衡温度,K
xi组分i的液相摩尔分数
x′i组分i的液相摩尔分数(不含萃取剂)
yi组分i的气相摩尔分数
αij相对挥发度
γi组分i的活度系数
[1] 应卫勇. 现代煤化工技术丛书——煤基合成化学品[M].北京:化学工业出版社,2010:432-443.
[2] Dai Chengna,Lei Zhigang,Xi Xiaom in,et al. Extractive distillation with a m ixture of organic solvent and ionic liquid as entrainer[J].Ind Eng Chem Res,2014,53(40):15786-15791.
[3] 张立庆,王松岳,钟毓菁,等. 乙苯萃取精馏分离甲醇与碳酸二甲酯二元共沸物[J].石油与天然气化工,2005,34(6):522-524.
[4] 张立庆,钟毓菁,王松岳,等. 甲苯萃取精馏分离甲醇与碳酸二甲酯共沸物[J].天然气化工,2005,30(4):51-54.
[5] 张立庆,李菊清,丁江浩,等. 碳酸二甲酯-甲醇-邻二甲苯三元体系汽液相平衡研究[J].石油与天然气化工,2004,2004(1):4-6.
[6] 翟小伟,杨伯伦,邱鹏,等. 萃取精馏分离甲醇和碳酸二甲酯二元共沸物[J].西安交通大学学报,2008,42(1):91-95.
[7] 贾彦雷. 碳酸二甲酯与甲醇分离的模拟研究[J].青岛科技大学学报:自然科学版,2011,32(1):5-11.
[8] 王海霞,吕效平. 碳酸乙烯酯萃取精馏分离DMC-CH3OH恒沸物模拟[J].天然气化工,2007,32(5):19-22.
[9] 李扬,袁苏霞,吕效平. 间歇萃取精馏分离碳酸二甲酯与甲醇恒沸物[J].化工进展,2008,27(9):1400-1403.
[10] 李群生,朱炜,付永泉,等. 常压下甲醇-碳酸二甲酯汽液平衡测定及其萃取剂选择[J].化学工程,2011,39(8):44-47.
[11] 张立庆,丁江浩,陈建刚. 碳酸二甲酯-甲醇-糠醛三元体系汽液平衡数据的推算与关联[J].计算机与应用化学,2002,19(5):285-286.
[12] 李光兴,熊国玺. 糠醛萃取精馏分离甲醇-碳酸二甲酯二元共沸物研究[J].化学工程,2000,28(4):12-13.
[13] 潘鹤林,田恒水,于水. 萃取精馏分离甲醇—碳酸二甲酯二元恒沸物[J].华东理工大学学报:自然科学版,1998(4):389-392.
[14] 陶荣,杨万典,仲庆. 用ASPEN模拟结果优化甲醇和碳酸二甲酯共沸物萃取精馏[J].化工设计,2015,2015(3):9-11.
[15] Wang Sanjang,Yu Chengching,Huang H P. Plant-wide design and control of DMC synthesis process via reactive distillation and thermally coupled extractive distillation[J].Comput Chem Eng,2010,34(3):361-373.
[16] Li Qunsheng,Zhang Shuang,Ding Bangqin,et al. Isobaric Vapor-liquid equilibrium for methanol+dimethyl carbonate+trifluoromethanesulfonate-based ionic liquids at 101. 3 kPa[J].J Chem Eng Data,2014,59(11):3488-3494.
[17] Cai Fufeng,Wu Xinying,Chen Chang,et al. Isobaric vaporliquid equilibrium for methanol+dimethyl carbonate+phosphoricbased ionic liquids[J].Fluid Phase Equilib,2013,352:47-53.
[18] Chen Xiaochun,Cai Fufeng,Wu Xinying,et al. Isobaric vapor-liquid equilibrium for methanol+dimethyl carbonate+1-butyl-3-methylim idazolium dibutylphosphate[J].J Chem Eng Data,2013,58(5):1186-1192.
[19] Kim H D,Hwang I C,Park S J. Isothermal vapor-liquid equilibrium data at T = 333. 15 K and excess molar volumes and refractive indices at T = 298. 15 K for the dimethyl carbonate+methanol and isopropanol+water with ionic liquids[J].J Chem Eng Data,2010,55(7):2474-2481.
[20] 曹玲,李群生. 乙酸乙酯-乙腈-1-辛基-3-甲基咪唑六氟磷酸盐物系等压汽液相平衡数据的测定与关联[J].石油化工,2016,45(2):194-199.
[21] 朱自强,姚善泾,金彰礼. 流体相平衡原理及其应用[M].杭州:浙江大学出版社,1990:390-397.
[22] Yaws C L. Chem ical properties handbook[M].New York:M c Graw-Hill Professional,1999:A1-A60.
Isobaric vapor-liquid equilibrium for methanol+dimethyl carbonate+diethylene glycol system
Cao Ling,Xu Weizhen,Li Xueqin,Cheng Jianwen
(Department of Chem istry and Applied Chem istry,College of Changji,Changji Xinjiang 831100,China)
Isobaric vapor-liquid equilibrium data of the ternary system methanol+dimethyl carbonate(DMC)+diethylene glycol were measured at 101.3 kPa in a modified Othmer still. With the addition of diethylene glycol,the relative volatility of methanol to DMC deceased and the vapor-liquid equilibrium temperature increased. Diethylene glycol is not suitable as an extracting agent for separation of methanol+DMC using extractive distillation. The NRTL model was used to correlate the experimental data of the system methanol+DMC+diethylene glycol at solvent ratio 0.25,0.5,1. The biggest standard deviation of temperature was 0.63 K.
dimethyl carbonate;methanol;diethylene glycol;NRTL model
1000-8144(2017)09-1168-06
TQ 013.1
A
2017-03-09;[修改稿日期]2017-05-26。
曹玲(1981—),女,新疆维吾尔自治区昌吉市人,博士,副教授,电话 0994-2333824,电邮 1517483346@qq.com。
新疆维吾尔自治区自然科学基金项目(2015211A002)。
10.3969/j.issn.1000-8144.2017.09.012
(编辑 杨天予)

