放射性同位素示踪法研究2-氟-6-三氟甲基吡啶在大鼠体内的吸收、分布和排泄
林立红,余洋,李晓磊,李娜,庞亚男
(沈阳化工研究院有限公司安全评价中心代谢与分析部,辽宁沈阳110021)
放射性同位素示踪法研究2-氟-6-三氟甲基吡啶在大鼠体内的吸收、分布和排泄
林立红,余洋,李晓磊,李娜,庞亚男
(沈阳化工研究院有限公司安全评价中心代谢与分析部,辽宁沈阳110021)
目的 研究2-氟-6-三氟甲基吡啶(JJBD)在大鼠体内的吸收、分布和排泄。方法采用放射性同位素14C标记JJBD,单次ig给予SD大鼠[14C]JJBD 10和100 mg·kg-1(放射性剂量均为3.7 GBq·kg-1),用液体闪烁计数分析仪(LSC)测定大鼠血浆、组织、胆汁、粪便、尿液和笼具清洗液等样品的总放射性,用WinNonlin软件按非房室模型计算毒代动力学参数。结果 SD大鼠单次ig给予JJBD 10和100 mg·kg-1的曲线下面积(AUC(0-t))分别为22 548±1579和(203 395±27 586)h·μg Eq.·L-1;半衰期(t1/2)分别为15.8±1.0和(14.1±0.9)h;达峰时间(Tmax)分别为4.0±3.0和(6.0±5.0)h;峰值浓度(Cmax)分别为1450±355和(7776± 1703)μg·Eq.·L-1。JJBD主要分布于脂肪、肝、肾和胃肠道中,大部分组织在染毒后4 h JJBD达到峰浓度,在肌肉、胸腺、全脑、性腺和脾中未见JJBD分布。染毒后0~168 h,JJBD主要从尿液排出,占染毒量的43.1%;部分从粪便排泄,占染毒量的29.7%;笼具冲洗液占染毒量的9.97%。0~72 h大鼠胆汁的总排泄量占染毒量的28.1%。结论单次ig给予SD大鼠JJBD后,JJBD能够快速吸收入血,缓慢消除,不存在蓄积风险;JJBD在大鼠体内分布较广泛,但在脑中未检出,无法通过血脑屏障;大部分JJBD可经粪尿排泄。
2-氟-6-三氟甲基吡啶;放射性同位素;毒代动力学
DOl:10.3867/j.issn.1000-3002.2017.06.025
2-氟-6-三氟甲基吡啶(2-fluorine-6-trifluoromethylpyridine,JJBD)是一种新型化学物质,广泛用于化学材料、医药和农药合成的中间体原料,具有广阔的发展前景和市场需求。关于该物质在动物体内的毒代动力学特征及毒性安全评价数据,至今未见文献报道。
放射性同位素示踪技术是以放射性核素作为示踪剂对研究对象进行标记并检测的微量分析方法,在药动学及毒动学研究中扮演着不可代替的重要角色。放射性同位素得以广泛应用于活性物质示踪主要依赖于其最重要的2个特点:一是与被示踪的物质有同一性,即放射性核素与其同种元素的非放射性核素在化学和生物学行为上具有高度一致性,不致扰乱和破坏体内外生理过程的平衡状态;二是与被示踪的物质有可区别性,放射性核素的原子核不断衰减,发出能被放射性探测仪所探测的射线,从而实现对标记物的定量及定位[1]。利用放射性同位素不断地放出特征射线的核物理性质,可以用现代放射性检测仪器,如液体闪烁计数仪和在线同位素检测仪等,追踪其在体内的分布、含量变化及其排泄等[2]。人们利用各种现代化分析测试手段开展了大量研究工作。然而,在诸多研究分析方法中,放射性同位素示踪技术以独特的优势成为国际公认的研究药物代谢及处置的最有效的手段之一,其稳定有效的直接测定优势、简单的前处理方法和极低的检测限是其他仪器设备和手段无法代替的[3-11]。
由于JJBD的化学结构为吡啶环的2位和6位分别连接氟和三氟甲基,结构较为简单,导致其在动物体内发生广泛代谢,无法用高效液相色谱(high performance liquid chromatography,HPLC)、气相色谱(gas chromatography,GC)和液相色谱质谱联用(liquid chromatograph mass spectrometer,LC-MS)等分析仪器追踪原型药物在动物体内的动态变化。因此,本研究参考中国环保部有关试验导则[12],将放射性同位素14C标记在受试物质的骨架结构上,研究不同剂量JJBD在大鼠体内的吸收、分布和排泄,揭示其在动物体内的毒代动力学特征,为进一步研究该物质的毒性作用机制和毒性安全评价提供科学依据。
1 材料与方法
1.1 试剂和仪器
JJBD原药(纯度99.0%)由沈阳化工研究院新药所提供;14C标记JJBD([14C]JJBD)(放化纯度>99.5%)委托具有资质单位合成。EDTAK2、KOH、盐酸和醋酸(分析纯),国药集团化学试剂有限公司;异丙醇(分析纯),上海凌峰化学试剂有限公司;闪烁液自行配制;超纯水由Milli-QReference纯水系统制备。
Tri-Carb 2910型液体闪烁计数(liquid scintillation counter,LSC)分析仪,美国Perkin Elmer仪器公司;OX-501型生物氧化燃烧仪,美国Harvey仪器公司;T18型匀质机,德国IKA公司;BP211D型十万分之一电子天平,德国Sartorius公司;3K15型高速离心机,德国Sigma公司;移液器,德国Eppendorf公司。
1.2 动物、分组和处理
雄性SD大鼠,体质量210~280 g,由北京维通利华实验动物技术有限公司提供,许可证号:SCXK(京)2012-0001。动物室温度19~26℃,湿度40%~70%,照明150-300 Lux(明暗各12 h),噪声<60 dB。动物的使用经本中心伦理委员会审批通过。饲料为全价颗粒饲料,饲养于塑料盒内,自由进食饮水。大鼠引入后适应性饲养5 d,适应期结束后每只大鼠饲养于一个代谢笼内,染毒前禁食约18 h,均采用ig方式染毒,染毒容积10 mL·kg-1。实验结束后,大鼠采用CO2法进行安乐死处理。
预实验结果 表明,JJBD 100 mg·kg-1单次ig染毒,SD大鼠出现中毒症状但未出现死亡。因此设定高剂量为100 mg·kg-1,低剂量为高剂量的1/10,即10 mg·kg。依据动物使用3R原则,选择雄性大鼠进行实验[12-14,15]。
雄性SD大鼠33只,随机分组,毒代动力学研究分JJBD 10和100 mg·kg-1组(放射性剂量均为3.7 GBq·kg-1),每组4只;组织分布、粪尿排泄和胆汁排泄研究各1组,分别使用17,4和4只大鼠,单次ig染毒JJBD 100 mg·kg-1(放射性剂量为3.7 GBq·kg-1)。
1.3 JJBD在SD大鼠体内的毒代动力学参数测定
给药后,JJBD 10 mg·kg-1组大鼠进食、饮水、排便和排尿均正常,而JJBD 100 mg·kg-1组大鼠出现进食减少和稀便等轻微中毒症状。JJBD 10和100 mg·kg-1(放射性剂量均为3.7GBq·kg-1)组分别于染毒前和染毒后0.083,0.5,1,2,4,6,8,10,24和72 h眼眶静脉采集血样,每个时间点采约200 μL,用肝素抗凝,11 680×g离心10 min,取上层血浆,-20℃冷冻。血浆样品解冻后经充分涡旋,平行称取2份至7 mL闪烁瓶中,直接加入5 mL闪烁液混合均匀后,使用LSC检测放射性,计算JJBD的质量浓度。质量浓度(ng Eq.·g-1)=总放射性(DPM·g-1)/比活度(DPM·ng-1)。
1.4 JJBD在SD大鼠体内组织分布测定
组织分布使用17只SD大鼠,其中1只作为溶媒对照,其他SD大鼠单次ig染毒JJBD 100 mg·kg-1(放射性剂量为3.7 GBq·kg-1),染毒后0.5,4,24和72 h各取4只SD大鼠解剖。CO2麻醉SD大鼠,于腹主动脉放血后取全脑、心、肺、肝、肾、脾、胃壁、肠壁、肌肉(股骨)、脂肪(腹腔)、胸腺和性腺,-20℃冷冻。
将组织样品匀浆,平行称取2份(每份约0.1 g)至20 mL闪烁瓶内,加入KOH 6 mol·L-1,封口膜密封,70°C水浴加热,待凉至室温后,加入10 mL闪烁液和醋酸混合均匀,旋紧瓶盖振摇混匀,冷冻避光静置,然后使用LSC测定总放射性,计算JJBD的质量浓度。
1.5 JJBD在SD大鼠粪尿中的排泄测定
使用4只SD大鼠,单次ig染毒JJBD 100 mg·kg-1(放射性剂量为3.7GBq·kg-1)后0~8 h,8~24 h(粪便0~24 h),24~48 h,48~72 h,72~96 h,96~120 h,120~144 h和144~168 h收集尿液和粪便,每日冲洗笼具收集冲洗液,-20℃冷冻。将每只大鼠每一时间段粪样解冻,先在粪样中加入适量50%异丙醇水溶液,置于4℃冰箱暂存。匀浆操作前,补加适量50%异丙醇水溶液,称定并记录总质量。用匀浆机进行匀浆化处理。平行称取2份匀浆液至燃烧船中,经氧化燃烧仪充分燃烧,用闪烁液捕获样品燃烧生成的[14C]CO2,然后使用LSC测定总放射性,取平均值进行统计分析。将每一时间段尿液或笼具冲洗液解冻,混合,平行称取2份至7 mL闪烁瓶中,直接加入5 mL闪烁液混合均匀后,使用LSC检测总放射性,计算JJBD的质量浓度。
1.6 JJBD在SD大鼠胆汁中的排泄测定
JJBD胆汁排泄研究使用4只大鼠,大鼠进行胆管插管手术后恢复2~3 d,染毒后置于代谢笼内,于染毒前和染毒后0~4 h,4~8 h,8~24 h,24~48 h和48~72 h收集胆汁样品,-20℃冷冻。将每一时间段胆汁样品解冻,平行称取2份至20 mL闪烁瓶中,直接加入10 mL闪烁液混合均匀后,使用LSC检测总放射性,计算JJBD的质量浓度。
1.7数据计算和统计分析
计算JJBD的质量浓度,采用WinNonlin软件(6.3版,Pharsight)按照非房室模型计算放射性的毒代动力学参数(采用梯形法计算),AUC,Cmax与Tmax均为实测值。数据以x±s表示。
2 结果
2.1 JJBD在SD大鼠体内的血药浓度时间曲线和毒代动力学参数
JJBD血药浓度随时间变化曲线见图1,毒代动力学参数见表1。单次ig给予雄性SD大鼠JJBD 10和100 mg·kg-1后10 min血浆中即可检出放射活性,血药浓度能够在6 h内达峰,半衰期约为15 h,在给药后72 h仍可检测到放射性,但均已降低至Cmax的5%以下。100 mg·kg-1剂量组的AUC0-t约为10 mg·kg-1剂量组的9倍,与剂量比(10∶1)接近,2个剂量组的半衰期t1/2相当。
2.2 JJBD在SD大鼠体内的组织分布
JJBD在不同时间、不同组织中的分布见图2。骨骼肌、性腺、胸腺、脾和全脑等组织未有放射性分布。其余大部分组织在染毒后4 h JJBD质量浓度达到峰值,染毒后0.5 h在脂肪中达到峰值。各组织中的JJBD达峰后,随时间延长逐渐下降。染毒24 h后,脂肪、胃壁、肾、肝和肠道壁的JJBD均降低,在心和肺已检测不到。染毒72 h后,仅肝和肾中可检测到JJBD,约占给药量的0.45%,其余组织均已检测不到。

Fig.1 Concentration-time curves of 2-fluorine-6-trifluoromethylpyridine(JJBD)in rat plasma by liquid scintillation counter(LSC).SD rats were ig administrated with JJBD 10 and 100 mg·kg-1,the blood sample was collected via orbital venous plexus before administration and after 0.083,0.5,1,2,4,6,8,10,24 and 72 h of administration.Total radioactivity was determined by LSC.JJBD concentration(ng Eq.·g-1)= total radioactivity(DPM·g-1)/specific activity(DPM·ng-1).x±s,n=4.

Tab.1 Toxicokinetic parameters of JJBD in rats
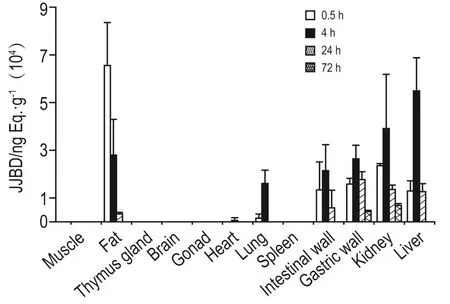
Fig.2 Tissue distribution of JJBD in rats by LSC.Rats were ig administrated with JJBD 100 mg·kg-1,tissues were collected after 0.5,4,24 and 72 h of administration.x±s,n=4.
2.3 JJBD在SD大鼠粪尿中的排泄
JJBD在不同时间段中的累积排泄率见图3。大鼠单次ig染毒后0~168 h内,JJBD的累积排泄率平均值为82.8%,其中尿液的平均总排泄量占染毒量的43.1%,粪便为29.7%,笼具冲洗液为9.97%,尸体中未检测到。表明ig染毒后,JJBD主要经尿液排泄。

Fig.3 Accumulate excretion rate of JJBD in rats by LSC.See Fig.2 for the rat treatment.Urine,feces and cleaning solution were collected at 0-8 h,8-24 h,24-48 h,48-72 h,72-96 h,96-120 h,120-144 h and 144-168 h afer administration.Excretion rate(%)=excretion amount/dosage×100%.x±s,n=4.
2.4 JJBD在SD大鼠胆汁中的排泄
JJBD在不同时间段中的胆汁排泄率见表2。ig染毒后0~72 h放射性的累积排泄率平均值为28.1%,显示JJBD吸收后部分经胆汁排泄,且染毒后48 h累积排泄量占总排泄量的99.7%,表明48 h时大部分受试物质已经经胆汁排泄。
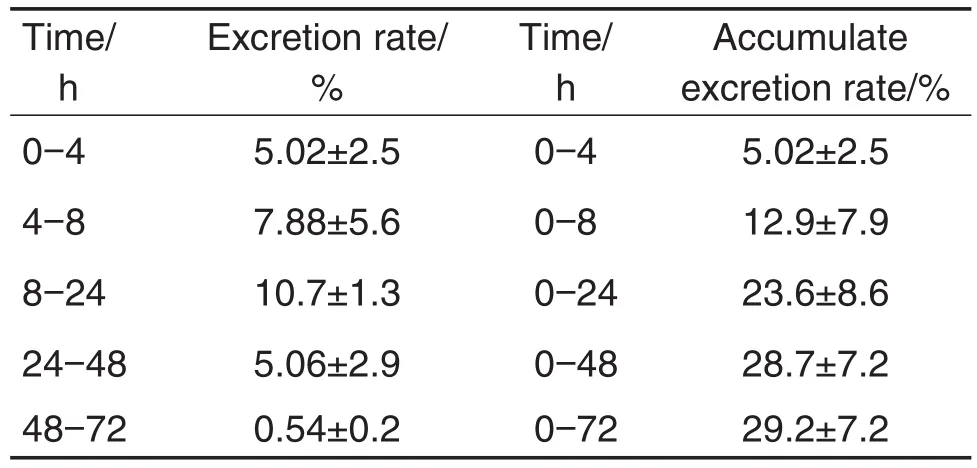
Tab.2 Excretion rate of JJBD in rat bile by LSC
3 讨论
本研究结果 表明,JJBD能够被大鼠快速吸收入血并全身分布,在给药后72 h,大部分的JJBD可以从血液及组织中消除;排泄数据表明,给药后72 h约80%的JJBD可以通过尿液和粪便排出体外,其中,尿液排泄为主要排泄途径。比较胆汁与粪便累积排泄率数据,发现二者的累积排泄率相当,表明JJBD在大鼠胃肠道内吸收较完全,约28%的受试物质可以通过肝肠循环进入粪便排泄。排泄实验表明,仍有部分JJBD通过其他排泄途径排出体外,由于JJBD的分子结构较为简单,推测部分物质在体内转化为CO2排出体外。研究结果 表明,ig给药后JJBD在大鼠体内可快速消除,不存在蓄积风险,该研究为JJBD在人体中的风险评估提供了数据支持。
由于JJBD仅作为合成药物的中间体原料,不用于治疗疾病的药物,本研究参考相关研究选择2个剂量水平[13-15],涵盖了毒理实验剂量水平,满足产品登记资料要求。根据JJBD的用途和理化性质,JJBD潜在的人体暴露途径为经口摄入,因此采用ig给药研究其毒代动力学特征,给药途径与本中心开展的毒理实验相同。
本研究采用放射性同位素示踪法可有效甄别基质和受试物质,避免基质对结果 测定的干扰,大大简化样品的提取和预处理,同时不需要繁琐的分析方法验证,可以节约实验成本并缩短实验周期[16]。与HPLC,GC或LC-MS等分析方法相比,放射性同位素示踪法不需要标准物质就可以对原型及其代谢产物进行全面的定量研究[17],可以更加准确地反映受试物质在动物体内的毒代动力学特征,为受试物质的安全性评估提供数据支持。
[1]Bian YC,Hu HH,Zeng S.Application of radiolabeled drugs in absorption,distribution,metabolism and excretion studies[J].Chin J Pharm Anal(药物分析杂志),2012,32(5):906-911.
[2]Harnud S,Huang LL,Yuan ZH.The use of radiolabeled drugs in drug metabolism and disposition studies[J].Chin J New Drugs(中国新药杂志),2016,25(13):1475-1484.
[3]Jiang GH,Liu ZM.Study on absorption distribution and elimination of nerve growth factor in mice by radioactivity isotope tracing method[J].Mod Instrum(现代仪器),2012,18(1):10-13.
[4]Zhang JR,Luo ZF.Radioisotope technique and its application progress in China[J].Eng Sci(中国工程科学),2008,10(1):61-69.
[5]Long FY,Wang BW,Zhang XH.Applications of isotopic tracer method on animal digestion and metabolism[J].J Agric Sci(农业科学研究),2005,26(3):66-69.
[6]Cao GX,Tan TZ.Biodistribution and metabolism of radio-iodinated IBZM in rats[J].J West China Univ Med Sci(华西医科大学学报),2000,31(2):171-173.
[7]Malhotra BK,Iyer RA,Soucek KM,Behr D,Liao WC,Mitroka JG,et al.Oral bioavailability and disposition of[14C]omapatrilat in healthy subjects[J].J Clin Pharmacol,2001,41(8):833-841.
[8]Nohynek GJ,Skare JA,Meuling WJ,Wehmeyer KR,de Bie AT,Vaes WH,et al.Human systemic exposure to[14C]-paraphenylenediamine-containing oxidative hair dyes:absorption,kinetics,metabolism,excretion and safety assessment[J].Food Chem Toxicol,2015,81:71-80.
[9]Wu C,Huang L,Tang S,Li Z,Ye Q.Enantioselective absorption and transformation of a novel chiral neonicotinoid[14C]-cycloxaprid in rats[J].Environ Pollut,2016,213:770-775.
[10]Lee SH,Kim N,Ford G,Wood S,Mair S,Walker H.Absorption,metabolism and excretion of[14C]-gemigliptin,a novel dipeptidyl peptidase 4 inhibitor,in humans[J].Drug Metab Pharmacok,2017,32(1):S78.
[11]Gaultier J,Farenhorst A,Cathcart J,Goddard T. Degradation of[carboxyl-14C]2,4-D and[ring-U-14C]2,4-D in 114 agricultural soils as affected by soil organic carbon content[J].Soil Biol Biochem,2008,40(1):217-227.
[12]Chemical Registration Center of Ministry of Environmental Protection.The Guidelines for the Testing of Chemicals-Health Effects(化学品测试方法-健康效应卷)[M].Beijing:China Environmental Press,2013:121-139.
[13]Bai B,Li XF,Yang K,Song YJ,Sun Y,Ding GH. Pharmacokinetics and toxicokinetics of arsenic after oral administration of realgar in rats[J].China Pharm(中国药师),2010,13(5):626-629.
[14]Song YJ,Ding GH,Liu Y,Sun JW,Liu DY. Determination of cypermethrin and its toxico-kinetics in rats[J].Ind Health Occup Dis(工业卫生与职业病),2010,36(1):7-10.
[15]Liu Y,Song YJ,Chen LP,Tao Y,Ding GH.Toxicokinetics of phenytoin after intravenous injection administration to rats[J].China Pharm(中国药师),2009,12(11):1513-1516.
[16]Prakash C,Johnson KA,Schroeder CM,Potchoiba MJ.Metabolism,distribution,and excretion of a next generation selective estrogen receptor modulator,lasofoxifene,in rats and monkeys[J].Drug Metab Dispos,2008,36(9):1753-1769.
[17]Wait JC,Vaccharajani N,Mitroka J,Jemal M,Khan S,Bonacorsi SJ,et al.Metabolism of[14C]gemopatrilat after oral administration to rats,dogs,and humans[J].Drug Metab Dispos,2006,34(6):961-970.
Absorption,distribution and excretion of 2-fluorine-6-trifl-uoromethylpyridine in rats by radioactivity isotope tracing method
LIN Li-hong,YU Yang,LI Xiao-lei,LI Na,PANG Ya-nan
(Metabolism and Analysis Department,Safety Evaluation Center of Shenyang Research Institute of Chemical Industry,Shenyang 110021,China)
OBJECTlVETo study the absorption,distribution and excretion of 2-fluorine-6-trifluoromethylpyridine(JJBD)in rats.METHODS[14C]Radioactivity isotope tracing method was used.Male SD rats were ig given a single dose of JJBD 10 and 100 mg·kg-1(radioactivity:3.7 GBq·kg-1).Concentrations of rat plasma,tissue,feces,urine and bile were determined with a liquid scintillation counting (LSC)analyzer.Toxicokinetics(TK)parameters were fitted using WinNonlin.RESULTSTK parameters of JJBD 10 and 100 mg·kg-1in male SD rats were as follows:area under the curve(AUC(0-t))was 22 548±1579 and(203 395±27 586)h·μg Eq.·L-1,half time(t1/2)was 15.8±1.0 and(14.1±0.9)h,peak time(Tmax)was 4.0±3.0 and(6.0±5.0)h,peak concentration(Cmax)was 1450±355 and(7776±1703)μg Eq.·L-1. JJBD was mainly distributed in fat,livers,kidneys,stomachs and intestinal walls.The concentration of JJBD in most of the tissues reached peak values after 4 h.However,JJBD couldn′t be detected in the muscle, thymus gland,brain,gonad or spleen.Excretion rate of JJBD was 43.1%in urine,29.7%in feces and 9.97%in cleaning solution within 0-168 h.JJBD could be excreted through bile at a rate of 28.1%within 0-72 h.CONCLUSlONJJBD can be absorbed immediately and excreted slowly in SD rat.There is no accumulation risk.The distribution of JJBD in vivo is very extensive,but cannot go through the blood-brain barrier.JJBD is mostly excreted through feces and urine.
2-fluorine-6-trifluoromethylpyridine;radioactive isotope;toxicokinetics
The project supported by National Science and Technology Major Project of China(2013ZX09302304)
LIN Li-hong,E-mail:linlihong@sinochem.com,Tel:(024)62353405
R969.1
A
1000-3002-(2017)06-0670-05
2017-02-04接受日期:2017-05-18)
(本文编辑:贺云霞)
国家科技重大专项(2013ZX09302304)
林立红,女,理学博士,高级工程师,主要从事医药、农药及化学品的毒代动力学研究。
林立红,E-mail:linlihong@sinochem.com,Tel:(024)62353405

