超高效液相色谱法测定五子衍宗丸中五味子甲素的含量
孙 琳,梁 锐,严维花,张 娜,柴 智
(山西中医学院中药学院,晋中 030619;*通讯作者,E-mail:chaizhi008@126.com)
超高效液相色谱法测定五子衍宗丸中五味子甲素的含量
孙 琳,梁 锐,严维花,张 娜,柴 智*
(山西中医学院中药学院,晋中 030619;*通讯作者,E-mail:chaizhi008@126.com)
目的 建立五子衍宗丸中五味子甲素含量测定的超高效液相色谱法(UPLC),并比较不同溶剂对五味子甲素的提取效果。 方法 色谱柱:Waters ACQUITY UPLC BEH C18(2.1 mm×100 mm,1.7 μm);流动相ACN ∶0.2%HAc=49 ∶51;流速0.4 ml/min,柱温30 ℃,进样体积1 μl,检测波长250 nm。 结果 五味子甲素在0.001 3-0.05 μg范围内具有良好的线性关系(r=0.999 9);平均回收率为101.73%,RSD 为2.29%;70 ℃蒸馏水、常温蒸馏水、70%乙醇、无水乙醇和DMSO 5种溶剂提取五味子甲素得率分别为,0.013%,0.012%,0.008%,0%和0%。 结论 UPLC简便、准确、重现性好,可用于五子衍宗丸中五味子甲素的含量测定。
五味子甲素; 五子衍宗丸; 超高效液相色谱法
五子衍宗丸是由枸杞子、菟丝子、覆盆子、五味子和车前子经炮制加工制成的水蜜丸,是中医临床常用的补肾益精类经典方药[1]。现代医学研究结果显示,五子衍宗丸不仅对男性生殖系统疾病有较好的疗效,且对阿尔茨海默病[2]和Leber遗传性视神经病变[3]也有一定的治疗作用,同时还具有增强免疫力[4]、抗衰老[5]和降血糖血脂[6,7]等作用。五子衍宗丸中的化学成分以金丝桃苷、五味子甲素、五味子醇甲、山柰素等为主[8],2010版《中国药典》一部收载的五子衍宗丸质量标准中仅有枸杞子和五味子甲素的TLC鉴别方法,未见含量测定方法。目前文献报道的五子衍宗丸含量测定多以HPLC为主,本文以五味子甲素为指标成分,建立了五子衍宗丸中五味子甲素的UPLC测定方法,为五子衍宗丸的质量控制提供了评价方法。
1 材料
1.1 实验仪器
Waters UPLC;千分之一电子分析天平(上海精科天美科学仪器有限公司);TD6M离心机(湖南湘式科学仪器有限公司);HH-2水浴锅(金坛市杰瑞尔电器有限公司);KQ3200E型超声波清洗器(昆山市超声仪器有限公司)。
1.2 试剂与药材
五味子甲素标准品(中国食品药品检定研究院);五子衍宗丸(规格:10 g/100粒,北京同仁堂股份有限公司同仁堂制药厂);无水乙醇(天津市科密欧化学试剂有限公司);DMSO(Sigma);乙腈(Merke);冰乙酸(天津市光复科技发展有限公司)。
2 方法与结果
2.1 色谱条件
色谱柱:Waters ACQUITY UPLC BEH C18(2.1 mm×100 mm,1.7 μm);流动相为ACN ∶0.2%HAc=49 ∶51;流速0.4 ml/min,柱温30 ℃,进样体积1 μl,检测波长250 nm。
2.2 对照品溶液的制备
精密称取五味子甲素对照品0.50 mg,置于10 ml容量瓶中,加入乙腈溶解并稀释至刻度,摇匀,得50 μg/ml的五味子甲素对照品溶液,作为母液备用。将母液分别稀释至25,12.5,5,2.5,1.25 μg/ml。经0.22 μm微孔滤膜过滤后,作为对照品溶液备用。
2.3 供试品溶液的制备
称取五子衍宗丸粉末约0.4 g放入15 ml EP管中,加入10 ml提取溶剂,称重,超声提取20 min,取出,冷却至室温,补足减失的重量。将补重后的EP管置离心机以6 000 r/min离心20 min,取上清液,经0.22 μm微孔滤膜过滤后,作为供试品溶液备用。
2.4 线性关系考察
精密吸取对照品溶液,按“2.1”项下色谱条件进行测定,记录色谱图。以样品浓度(μg/ml)为横坐标(X),峰面积为纵坐标(Y),制备标准曲线。计算五味子甲素的回归方程为Y五味子甲素=0.000 2X+0.008 7(r=0.999 9),线性范围0.001 3-0.05 μg。
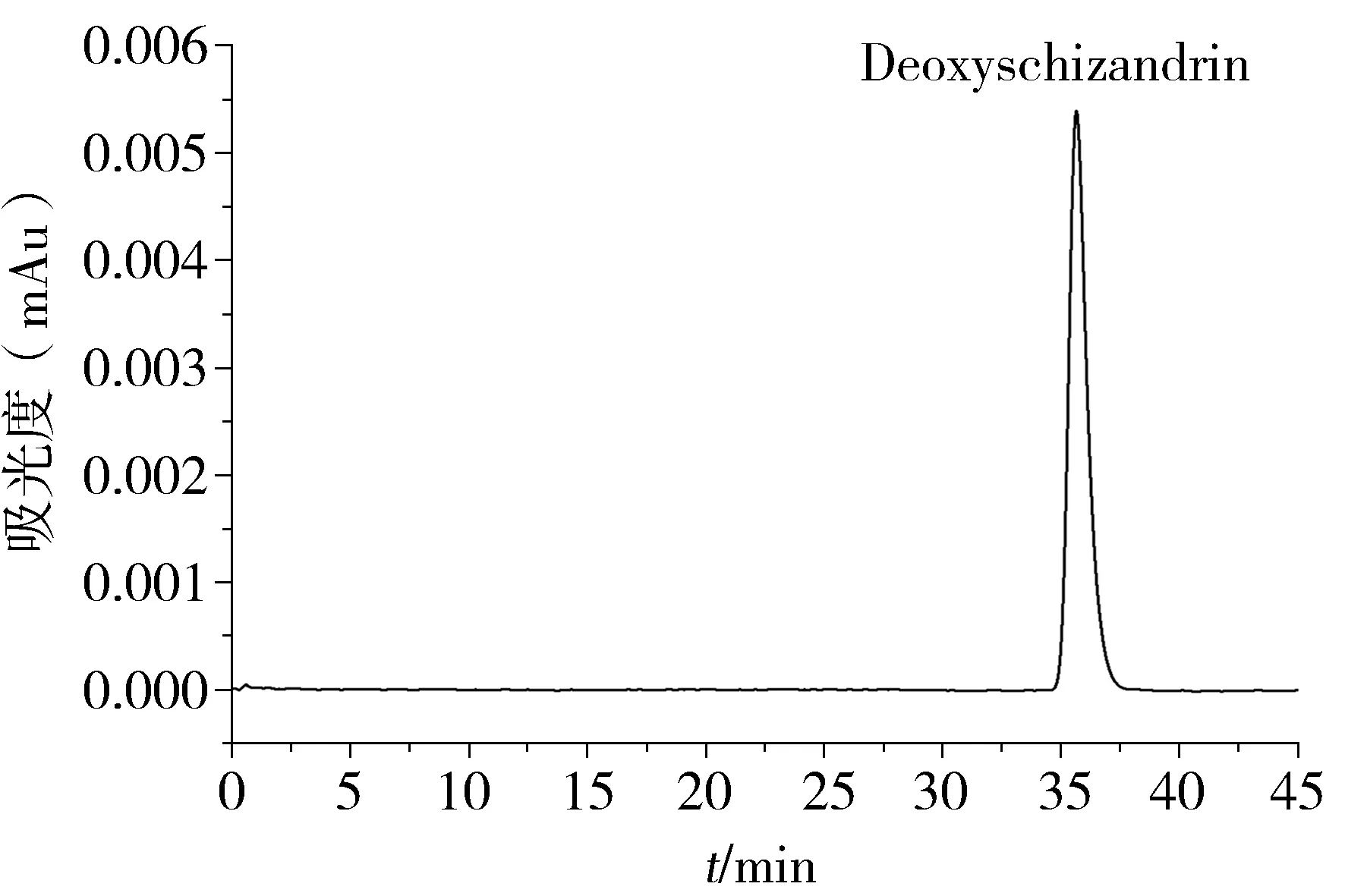
图1 五味子甲素标准品UPLC图谱Figure 1 Chromatograms of deoxyschizandrin
2.5 精密度试验
精密吸取高、中、低3个浓度的对照品溶液,连续进样测定6次,以色谱峰的峰面积计算得五味子甲素的RSD均小于1%(见表1),表明仪器精密度良好。
表1 五味子甲素精密度试验结果
Table 1 Results of precision test
2.6 稳定性试验
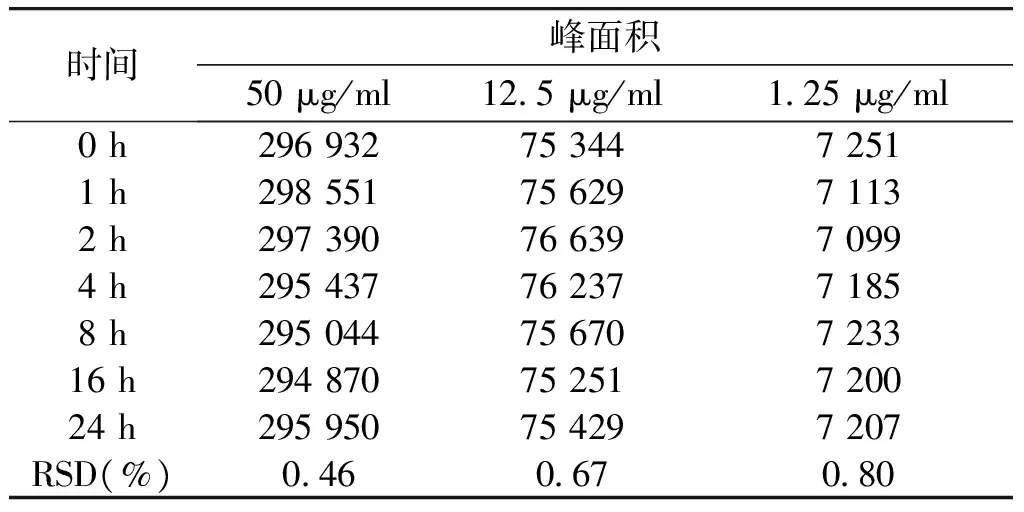
精密吸取同一对照品溶液,分别于0,1,2,4,8,16,24 h 进行测定,记录峰面积,计算表明供试品在24 h内稳定(见表2)。
表2 五味子甲素稳定性试验结果
Table 2 Results of stability test
时间峰面积50μg/ml125μg/ml125μg/ml0h2969327534472511h2985517562971132h2973907663970994h2954377623771858h29504475670723316h29487075251720024h295950754297207RSD(%)046067080
2.7 重复性试验
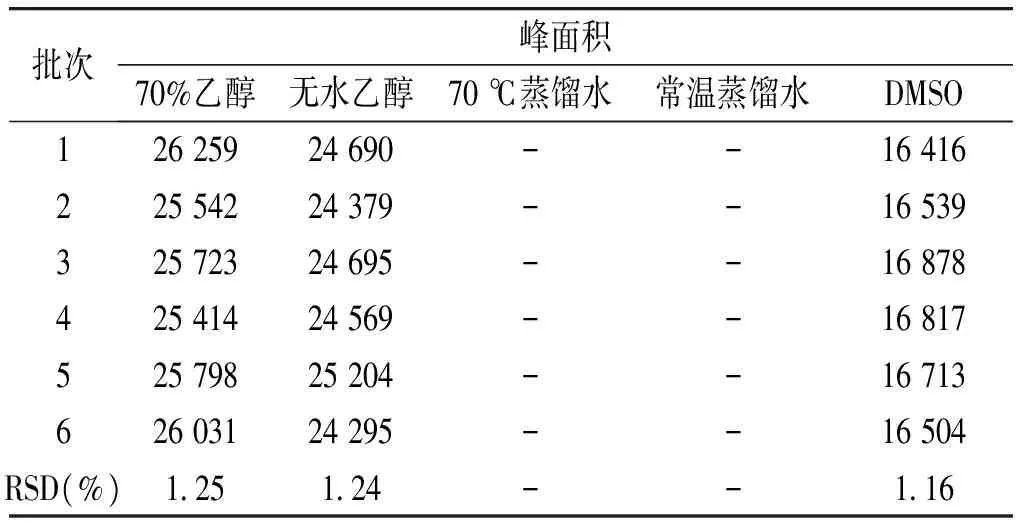
取五子衍宗丸粉末6份,每份约0.4 g,精密称定,以70%乙醇为溶剂,按“2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件进行测定,得五味子甲素RSD均小于2%(见表3),表明方法重复性良好。
表3 五味子甲素重复性试验结果
Table 3 Results of repeatability test
批次峰面积70%乙醇无水乙醇70℃蒸馏水常温蒸馏水DMSO12625924690--1641622554224379--1653932572324695--1687842541424569--1681752579825204--1671362603124295--16504RSD(%)125124--116
2.8 回收率试验
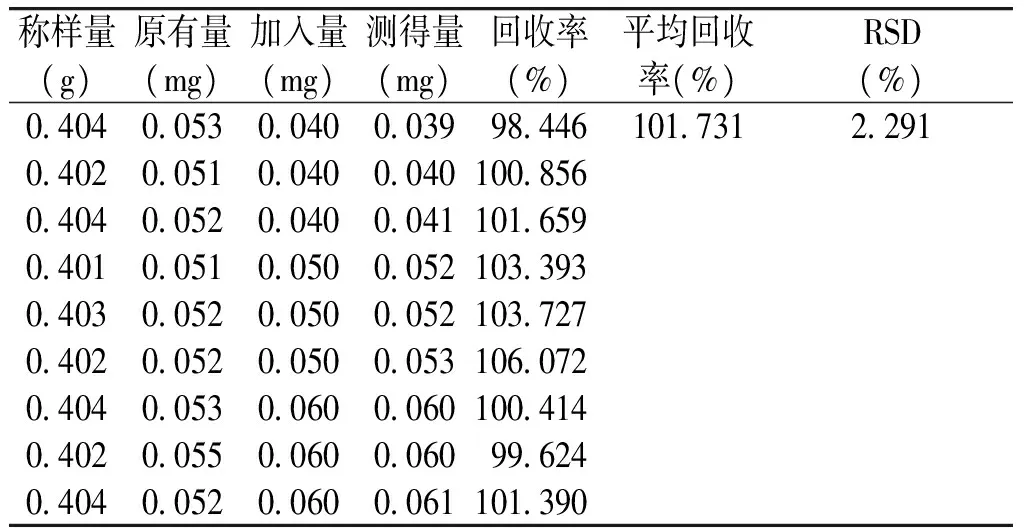
取五子衍宗丸粉末9份,每份约0.4 g,精密称定,置具塞锥形瓶中,精密加入五味子甲素对照品溶液适量(3种水平,各3份),按“2.3”项下方法操作、测定,计算得五味子甲素的平均回收率为101.731 %(见图4)。
表4 五味子甲加样回收率试验结果
Table 4 Results of sample recovery test
称样量(g)原有量(mg)加入量(mg)测得量(mg)回收率(%)平均回收率(%)RSD(%)04040053004000399844610173122910402005100400040100856040400520040004110165904010051005000521033930403005200500052103727040200520050005310607204040053006000601004140402005500600060996240404005200600061101390
2.9 样品测定
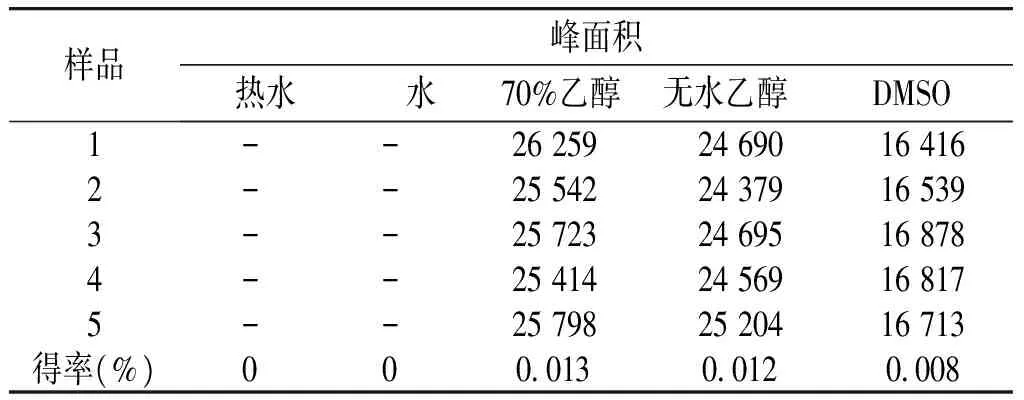
平行称取五子衍宗丸粉末5份,每份约0.4 g,精密称定,分别加入70%乙醇、无水乙醇、DMSO、热蒸馏水(约70 ℃)、蒸馏水(室温)各10 ml,按“2.3”项下方法制备供试品溶液,按“2.1”项下色谱条件进行测定,结果显示,70%乙醇对五子衍宗丸中五味子甲素的提取效率最高(见图2,表5)。
表5 不同溶剂提取五味子甲素得率
Table 5 Extraction of deoxyschizandrin by different solvents
样品峰面积热水水70%乙醇无水乙醇DMSO1--2625924690164162--2554224379165393--2572324695168784--2541424569168175--257982520416713得率(%)00001300120008
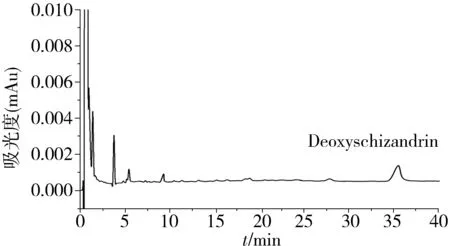
图2 样品溶液UPLC图谱Figure 2 Chromatograms of sample
3 讨论
3.1 检测波长的确定
取五味子甲素对照品溶液,在200-400 nm处扫描,结果表明,五味子甲素在250 nm处有最大吸收峰,在此波长下测得的色谱峰峰形对称且无干扰峰,所以本实验选定250 nm为五味子甲素的检测波长。
3.2 流动相的选择
本实验比较了乙腈-水、乙腈-0.1%冰醋酸、乙腈-0.2%冰醋酸和乙腈-1%冰醋酸4种流动相的洗脱效果,结果选择乙腈-0.2%冰醋酸进行洗脱,干扰峰较少且五味子甲素分离度良好。此外,随着流动相中乙腈比例的增加,各物质的保留时间明显缩短,但分离效果变差。以乙腈 ∶0.2%冰醋酸=41 ∶59进行洗脱,五味子甲素保留时间适中,分离度良好。
3.3 提取溶剂的选择
本实验考察了70%乙醇、无水乙醇、DMSO、热蒸馏水(约70 ℃)和蒸馏水(室温,约25 ℃)5种提取溶剂,UPLC含量测定结果显示,热蒸馏水和室温蒸馏水提取液中检测不到五味子甲素,可能是由于五味子甲素的极性较小,不溶于水,因此水提液中五味子甲素含量较低,未能被仪器检测到;5种提取溶剂中,以70%乙醇对五味子甲素的提取效率最高。
3.4 结果分析
本研究建立了五子衍宗丸中五味子甲素的UPLC含量测定方法,并比较了不同溶剂对五味子甲素的提取效果。实验结果表明,本方法线性关系及重现性良好,为五味子甲素提供了快速、准确、简便的测定方法,可用于五子衍宗丸的质量控制;采用70%乙醇超声提取五子衍宗丸所得五味子甲素的得率最高,以此提取液回收乙醇蒸干后所得浸膏能够被细胞培养基完全溶解,为五子衍宗丸细胞干预液的制备提供了实验基础。
[1] 国家药典委员会.中华人民共和国药典:一部[M].北京:中国医药科技出版社,2010:532.
[2] 李娌,蔡浩然,李琳,等.加味五子衍宗方总黄酮对大鼠海马锥体细胞VGCC通道的影响[J].中国中药杂志,2009,34(15):1975-1978.
[3] 李成武,庄曾渊,张守康,等.五子衍宗汤治疗Leber遗传性视神经病变的临床研究[J].中国中西医结合杂志,2009,29(12): 1078-1080.
[4] 许凯霞,王永辉,杨向竹,等.补肾方剂对子代小鼠非特异性免疫功能的影响[J].中国实验方剂学杂志,2010,18(9):161-164.
[5] 王学美,富宏,刘庚信.五子衍宗丸及其拆方对老年大鼠心脑线粒体DNA缺失、线粒体呼吸链酶复合体及ATP合成的影响[J].中国中西医结合杂志,2001,21(6):437-440.
[6] 李育浩,吴清和,赵文昌,等.五子衍宗丸药理研究对正常小鼠血糖和四氧嘧啶糖尿病小鼠的影响[J].中药药理与临床,1994,8(5):52-54.
[7] 陈淑英,李育浩,吴清和,等.五子衍宗丸对链脲佐菌素所致糖尿病大鼠的影响[J].新中医,1992 (11):52-54.
[8] 刘伟,周建良,陈碧莲,等.HPLC同时测定五子衍宗丸中5种活性成分的含量[J].中国实验方剂学杂志,2014,20(3):74-78.
Determination of deoxyschizandrin in the Wuzi Yanzong pill by ultra performance liquid chromatography
SUN Lin,LIANG Rui,YAN Weihua,ZHANG Na,CHAI Zhi*
(CollegeofTraditionalChineseMedicine,ShanxiUniversityofTraditionalChineseMedicine,Jinzhong030619,China;*Correspondingauthor,E-mail:chaizhi008@126.com)
ObjectiveTo establish the method for determining the content of deoxyschizandrin in Wuzi Yanzong pills by ultra performance liquid chromatography(UPLC) and compare the efficacy of extraction of deoxyschizandrin with different solvents.MethodsThe analysis was carried out on Waters ACQUITY UPLC BEH C18(2.1 mm×100 mm,1.7 μm) with ethanol-0.2% glacial acetic acid (49∶51) as mobile phase,flow rate of 0.4 ml/min and wave length of 250 nm at 30 ℃.The 70% ethanol,100% ethanol,DMSO,70 ℃ distilled water and distilled water at room temperature were used as the solvents to extract the deoxyschizandrin.ResultsThe deoxyschizandrin showed a good linear relationship between concentration and peak area in the range of 0.001 3-0.05 μg (r=0.999 9).The recovery was 101.73% with RSD of 2.29%.The extraction rates of 70% ethanol,100% ethanol,DMSO,70 ℃ distilled water and distilled water at room temperature were 0.013%,0.012%,0.008%,0%and 0%.ConclusionThe method has good reproducibility and sensitivity to determine the content of deoxyschizandrin in Wuzi Yanzong pills.The 70% ethanol is the best extraction solvent.
deoxyschizandrin; Wuzi Yanzong pills; ultra performance liquid chromatography
国家自然科学基金资助项目(81303262,81102552);山西省中医药管理局科研基金资助项目(2016ZYYC28);山西中医学院博士科研启动基金资助项目;山西省国际科技合作项目(2014081049-4);山西中医学院方药药效及其作用机制研究重点科技创新团队(20150401)
孙琳,女,1984-01生,博士,讲师,E-mail:sunlin115@aliyun.com
2017-03-16
R927.2
A
1007-6611(2017)06-0543-04
10.13753/j.issn.1007-6611.2017.06.007

