毛细管电泳法快速定量检测连多硫酸盐
李国防,凌翠霞,刘瑛,张富强
(1.商丘师范学院 化学化工学院 河南 商丘 476000;2.山西师范大学 化学与材料科学学院,山西 临汾 041004)
毛细管电泳法快速定量检测连多硫酸盐
李国防1,凌翠霞1,刘瑛1,张富强2
(1.商丘师范学院 化学化工学院 河南 商丘 476000;2.山西师范大学 化学与材料科学学院,山西 临汾 041004)
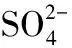
连多硫酸盐;毛细管电泳;快速检测
因连多硫酸及其盐在化学工程、环境监测和某些微生物的新陈代谢中具有重要作用,对连多硫酸盐的研究又呈现复苏趋势[1].由于高纯度连多硫酸盐的合成和快速定量检测是推进相关领域研究的基础,在我们已经找到了简便合成高纯度连多硫酸盐新工艺的前提下[2,3],探讨快速定量检测连多硫酸盐的合适方法是促进连多硫酸盐相关研究的重要工作之一.
化学滴定法是测定连多硫酸盐最原始的方法,但滴定法存在操作步骤多和由于误差传递测定结果准确度不高的弊端,而且该分析方法也不适合于痕量分析[1].相比而言,某些色谱技术如离子色谱[4-6]、高效液相色谱[7-10]和毛细管电泳[11-14]可以快速测定低含量的连多硫酸盐混合物.三类色谱分析法中,高效液相色谱需使用含乙腈的强极性流动相,因此,操作时需做好毒性防护.离子色谱测定的离子种类有一定局限性.毛细管电泳法使用无机盐缓冲溶液做电泳运行液,操作安全而且分析速度快.但用于定量分析时,必须严格控制操作条件才能获得好的重现性[11-14].而且,我们发现,利用毛细管电泳法测定连多硫酸盐的文献工艺存在基线不稳和峰型不好的缺陷[12].因此,有必要对现行毛细管电泳法测定连多硫酸盐的检测条件进行改进.鉴于自制连多硫酸钾的工艺,连多硫酸盐含微量的氯离子和硫酸根杂质[2,3],因此,实验也探索了CE法简便测定氯离子和硫酸根的条件.
1 实验部分
1.1 仪器与试剂
毛细管电泳仪Beckman Coulter P/ACE MDQ(美国贝克曼库尔特商贸有限公司),光电二极管阵列检测器(Photo Diode Array Detector,PDA),检测波长195 nm、214 nm和254 nm,32 Karat数据处理工作站.聚酰亚胺涂层熔融硅毛细管(河北永年锐沣光导纤维厂)长57.5 cm(有效长度为50 cm),内外径分别为75 μm i.d.和375 μm o.d..实验所用试剂除二氯化硫和二氯化二硫由淄博大荣精细化工有限公司提供,五水硫代硫酸钠、亚硫酸氢钠、三氯化铁、磷酸氢二钾、磷酸二氢钾、硝酸钾、氢氧化钾、氯化钠、硫酸钾、磷酸、四氯化碳、盐酸、硫酸、甲醇和乙醇均为市售分析纯,用前未经进一步处理.溶液配制均采用Millpore MilliQ超纯水系统所制超纯水(≥ 18.2 MΩ·cm).
1.2 实验用料连多硫酸钾的合成
实验所用连三、连四、连五和连六硫酸钾按先前报道的工艺制备[2,3].
1.3 氯离子、硫酸根和连多硫酸根的毛细管电泳法测定

2 结果与讨论
2.1 CE法测定连多硫酸盐的缓冲溶液

图1 K2S3O6、K2S4O6 和K2S5O6在不同缓冲体系下的电泳谱图Fig.1 Electropherograms of K2S3O6, K2S4O6 and K2S5O6 under different buffer
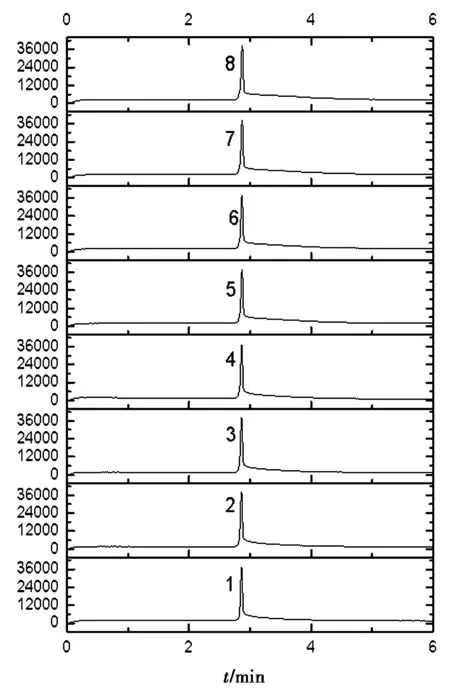
图2 0.6 mM K2S6O6的电泳谱图Fig.2 Electropherograms of 0.6 mM K2S6O6
为了确立最佳的分析条件,我们对连多硫酸盐分析的CE色谱条件进行了较为系统的研究.为了便于比较选择条件的优劣,每次测定试样前,毛细管柱均先活化处理.由于磷酸盐与石英管壁的平衡需要很长的时间,会出现分离的时间进程,因此,冲洗干净的毛细管先用磷酸盐缓冲溶液冲洗60 min并浸泡过夜后再用.通过实验我们发现,单独使用10 mM KH2PO4的电解液,谱图基线较5 mM KH2PO4-5 mM (NH4)2SO4电解液的体系平稳,但峰面积与药剂浓度的关联性差.使用10 mM K2HPO4-10 mM KH2PO4缓冲溶液,基线平稳,而且峰面积与药剂浓度在适宜的范围内呈线形关系,但以上两种电泳条件下的样品出峰时间均逐渐后延.样品出峰时间逐渐后延的原因与缓冲溶液的pH值有关,由于毛细管表面硅羟基的PKa约为2.2[11-14],当缓冲溶液的pH值大于此值时,毛细管壁与磷酸盐作用强而且形成平衡的时间长,易造成出峰时间不稳.因此,为了稳定出峰时间,必需消除毛细管管壁硅羟基的影响.由于连多硫酸盐在酸性介质下的化学性质稳定[15,16],而且连多硫酸盐是强电解质,在水中存在的离子形式可以在较宽的pH值范围内保持不变,所以,我们重点探索了使用pH值为2.12的KH2PO4-H3PO4缓冲溶液测定连多硫酸盐的CE条件.
图2是0.6 mM K2S6O6在使用10 mM KH2PO4-10 mM H3PO4电泳液的CE谱图.图1和图2说明,使用10 mM KH2PO4-10 mM H3PO4电泳液,谱图基线平稳,出峰时间稳定.在分离电压-30 kV时,电流约55 μA,所有连多硫酸根2~3 min出峰;分离电压-20 kV时,电流约37 μA, 3~4 min出峰.如果降低电解质溶液一半的浓度,在分离电压-30 kV时,电流约55 μA,2~3 min出峰;分离电压-20 kV,电流约23.5 μA,3~4 min出峰.研究发现KH2PO4-H3PO4缓冲体系下的所有谱图的基线均平稳,而且出峰时间稳定.使用低浓度的KH2PO4-H3PO4缓冲体系,虽然检测灵敏度高,但峰型变差,影响定量分析.考虑到快速定量分析连多硫酸盐的实验目的,使用10 mMKH2PO4-10 mMH3PO4缓冲溶液做电泳液是合适的.
2.2 CE法测定连多硫酸根、氯离子和硫酸根的线性范围和检出限
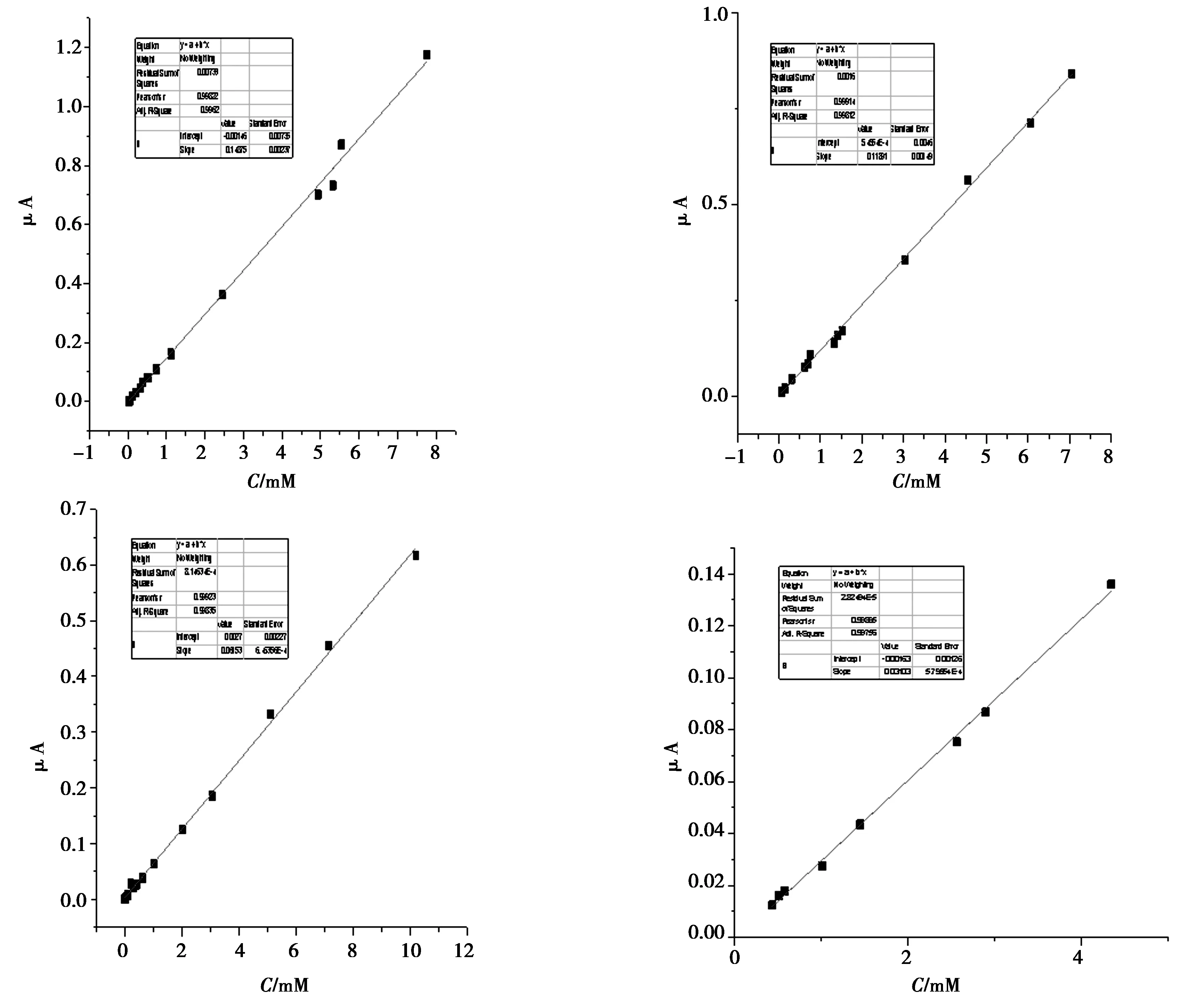
图3 K2S6O6(左上)、K2S5O6(右上)、K2S4O6(左下)和K2S3O6(右下)的浓度标准曲线Fig.3 Standard concentration-absorbency curve of potassium polythionates.K2S6O6(upper left figure), K2S5O6(upper right figure),K2S4O6(lower left figure)and K2S3O6 (lower right figure)
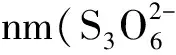
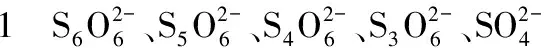
表和 Cl-的浓度线形范围和检出限
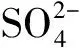
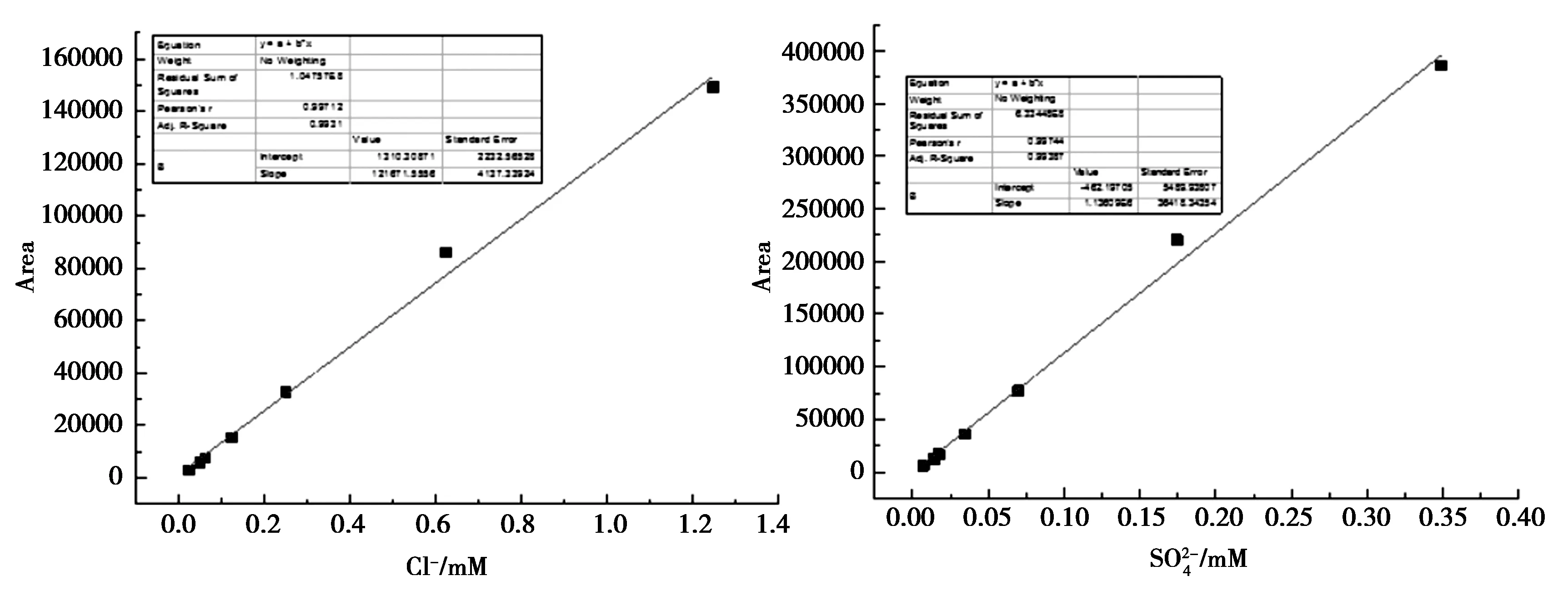
图4 氯离子(左)和硫酸根(右)的浓度标准曲线Fig.4 Standard concentration-absorbency curve of chloride ion (light figure) and sulfate radical (right figure), respectively
3 结 论

[1]李国防, 张富强.连多硫酸盐的合成、检测与应用[J].商丘师范学院学报, 2016, 32(3):33-39.
[2]Li G, Zhao Y, Li P, Zhang F, et al.Antibacterial activities of polythionates enhanced by carbonates[J].Med.Chem.Commun., 2015(6):1643-1648.
[3]Li G, Xia Y, Zhao Y, Li P,et al.Solid-Liquid Reaction Synthesis of High-Purity Potassium Hexathionate and Its Antibacterial Properties[J].Aust.J.Chem., 2016, 69:267-272.
[4]Miura Y, Saitoh A, Koh T.Determination of sulfur oxyanions by ion chromatography on a silica ODS column with tetrapropylammonium salt as an ionpairing reagent[J].J.Chromatog.A, 1997, 770:157-164.
[5]O’Reilly J W, Shaw M J, Dicinoski G W, Grosse A C,et al.Separation of polythionates and the gold thiosulfate complex in gold thiosulfate leach solutions by ion-interaction chromatography[J].Analyst, 2002, 127:906-911.
[6]Miura Y, Kawaoi A.Determination of thiosulfate, thiocyanat and polythionates in a mixture by ion-pair chromatography with ultraviolet absorbance detection[J].J.Chromatog.A, 2000, 884:81-87.
[7]Zou H, Jia Z, Zhang Y, Lu P.Separation of aqueous polythionates by reversed-phase ion-pair liquid chromatography with suppressor-conductivity detection[J].Anal.Chim.Acta, 1993, 284:59-65.
[9]Wolkoff A W, Larose R H.Separation and Detection of Low Concentrations of Polythionates by High Speed Anion Exchange Liquid Chromatography[J].Anal.Chem., 1975, 47:1003-1008.
[10]Takano B, McKibben M A, Barnes H L.Liquid Chromatographic Separation and Polarographic Determination of Aqueous Polythionates and Thiosulfate[J].Anal.Chem., 1984, 56:1594-1600.
[11]óReilly J W, Dicinoski G W, Miura Y, Haddad P R.Separation of thiosulfate and the polythionates in gold thiosulfate leach solutions by capillary electrophoresis[J].Electrophoresis, 2003, 24:2228-2234.
[12]Padarauskas A, Paliulionyte V, Ragauskas R, Dikcius A.Capillary electrophoretic determination of thiosulfate and its oxidation products[J].J.Chromatog.A, 2000, 879:235-243.
[13]OReilly J W, Dicinoski G W, Shaw M J, Haddad P R.Chromatographic and electrophoretic separation of inorganic sulfur and sulfur-oxygen species[J].Anal.Chim.Acta., 2001, 432:165-192.
[14]Timerbaev A R.Inorganic biological analysis by capillary electrophoresis[J].Analyst, 2001, 126:964-981.
[15]Pan C, Liu Y, Horvaöth A K, Wang Z, et al.Kinetics and Mechanism of the Alkaline Decomposition of Hexathionate Ion[J].J.Phys.Chem.A, 2013, 117:2924-2931.
[16]Pan C, Wang W, Horváth A K, Xie J,et al.Kinetics and Mechanism of Alkaline Decomposition of the Pentathionate Ion by the Simultaneous Tracking of Different Sulfur Species by High-Performance Liquid Chromatography[J].Inorg.Chem., 2011, 50:9670-9677.
[责任编辑:徐明忠]
Rapid quantitative determination of polythionates by capillary electrophoresis
LI Guofang1, LING Cuixia1, LIU Ying1, ZHANG Fuqiang2
(1.School of Chemical & Engineering, Shangqiu Normal University, Shangqiu 476000,China; 2.School of Chemistry and Material Science,Shanxi Normal University, Linfen 041004,China)
polythionates; capillary electrophoresis; rapid detection
2016-10-21
国家自然科学基金资助项目(21271125)
李国防(1970—),男,河南睢县人,商丘师范学院副教授,博士,主要从事抗菌材料制备与应用的研究.
O657.8
A
1672-3600(2017)06-0032-05

