魔芋葡甘露聚糖与木薯淀粉复配溶胶及协效性研究
,, , ,
(广西大学轻工与食品工程学院,广西南宁 530004)
魔芋葡甘露聚糖与木薯淀粉复配溶胶及协效性研究
李坚斌,刘培华,陈雨,李敏,邓秋燕
(广西大学轻工与食品工程学院,广西南宁 530004)
以魔芋葡甘露聚糖(konjac glucomannan,KGM)和木薯淀粉(cassava starch,CS)为原料进行复配研究,探讨魔芋葡甘露聚糖/木薯淀粉复配溶胶的复配协同增效性,研究多糖总浓度、复配比例、温度和pH对复配溶胶粘度和透光率的影响。结果表明:KGM与CS复配,可产生协同增效性,复配溶胶的粘度大于两者之和;KGM/CS复配溶胶的最佳条件:多糖的总浓度3.0%,KGM/CS比值为3∶7,溶胀温度80 ℃,pH7,最优条件下的KGM/CS复配溶胶的粘度为41.391×103cP,透光率为7.339%。
魔芋葡甘露聚糖,木薯淀粉,复配溶胶,协同增效
魔芋葡甘露聚糖(konjac glucomannan,KGM)来源于魔芋属魔芋胶的根部和块茎,是一种天然高分子可溶性的非离子型多糖[1]。葡甘露聚糖的线性骨架是由β-D甘露糖单元和β-D葡萄糖单元以1∶1.5或1∶1.6通过β-1,4糖苷键连接而成,少量分支(约8%)通过β-1,6葡糖基连接[2-3]。魔芋葡甘露聚糖是目前所发现的自然界中粘度最高的多糖之一,其水溶胶的粘度很大,具有优良的成膜性,可溶性,增稠性,良好的生物相容性等优点,且资源丰富,来源广泛,可生物降解,适用于多种方法的改性[4-5]。这些优势使KGM可以广泛应用于各种食品和保健食品。其不仅可以作为食品添加剂,如乳化剂、增稠剂、肉粘合剂应用于食品工业中[3];KGM还具有许多生理功效,如抑制肥胖,调节血糖和胆固醇含量,预防结肠癌等[6-9];此外,由于KGM还可与其他物质复合改性得到可生物降解,对环境友好的膜材料、控制释放材料、固定化载体等生物材料[10-12]。然而,天然KGM固有一些缺陷,如魔芋葡甘露聚糖不能快速溶胀和水合,溶解速度慢,溶胶稳定性差等,限制了其应用[5]。将魔芋葡甘露聚糖与其他多糖复配改性,能改善其溶胶粘度和透光率等性能,生产新型的,低成本的,集合多种胶体优良性能的产品,达到良好的协同效应,拓宽葡甘聚糖的应用范围[13-14]。木薯淀粉(ccassava starch,CS)是一种具有独特性质的天然淀粉,渗透力强,成膜性好,能直接用于食品和工业上[15]。本文研究了魔芋葡甘露聚糖/木薯淀粉复配溶胶形成的最佳条件及复配溶胶的协同增效性,能够在提高粘度的同时保持透光率,希望为魔芋材料的进一步研发和应用提供理论依据。
1 材料与方法
1.1材料与仪器
魔芋葡甘露聚糖(KGM)3APF-040v0 由北海多环保健品有限公司;木薯淀粉(CS) 明阳淀粉厂。
DV-Ⅱ+Pro粘度计 美国Brookfield公司;HJ-3数显恒温磁力搅拌器 江苏天由有限公司;868酸度计 美国Orion公司;D40-2F电动搅拌机 杭州仪表电机厂;SP-721紫外分光光度计 上海光谱仪器有限公司;AL204电子天平 梅特勒-托利多仪器(上海)有限公司。
1.2实验方法
1.2.1 KGM/CS复配溶胶的制备 按比例分别称取一定量的KGM和CS分散于蒸馏水中,室温下搅拌均匀后,在一定温度下搅拌30 min后冷却至室温。
1.2.2 粘度的测定 采用粘度计进行溶胶粘度测定,溶胶置于Brookfield测量杯中,将探头浸入溶胶至刻度线,30 s后读取粘度值。
1.2.2.1 KGM粘度的测定 将KGM配制成浓度为0.2%、0.4%、0.6%、0.8%、1.0%、1.2%、1.4%的溶液,70 ℃水浴搅拌30 min,后冷却至室温测定其粘度。
1.2.2.2 CS粘度的测定 将CS配制成浓度为3%、3.5%、4%、4.5%、5%、5.5%、6%、7%的悬浊液,70 ℃加热糊化15 min,冷却至室温测定其粘度。
1.2.2.3 KGM/CS复配溶胶粘度的测定 取0.2%、0.3%、0.4%、0.5%的KGM分别与2.5%、3.0%、3.5%、4%、4.5%的CS复配,室温下测其复配溶胶的粘度。
1.2.3 透光率的测定 采用紫外分光光度计,以去离子水为参比,于556 nm波长处测量溶胶的吸光度A,其透光率T为:
透光率T(%)=102-A
式(1)
1.2.4 KGM/CS配比对复配溶胶粘度和透光率的影响 多糖的总浓度控制在3.0%,pH7.0,按比例:KGM∶CS为0∶10、1∶9、2∶8、3∶7、4∶6分别称取一定量的KGM和CS分散于蒸馏水中,室温下搅拌均匀后,在70 ℃的水浴中加热搅拌30 min,然后冷却至室温,测定溶胶粘度和透光率。
1.2.5 多糖浓度对复配溶胶粘度和透光率的影响 多糖总浓度为2.0%、2.2%、2.4%、2.6%、2.8%、3.0%、3.2%,pH7.0,按KGM∶CS为3∶7称取一定量的KGM和CS,室温下搅拌均匀后,在70 ℃的水浴中加热搅拌30 min,然后冷却至室温,测定溶胶粘度和透光率。
1.2.6 不同溶胀温度对复配溶胶的粘度和透光率的影响 多糖总浓度控制为3.0%,pH7.0,按KGM∶CS为3∶7称取一定量的KGM和CS,室温下搅拌均匀后,将烧杯分别置于温度为40、50、60、70、80、90、100 ℃的水浴中加热搅拌30 min,然后冷却至室温,测定溶胶粘度和透光率。
1.2.7 pH对复配溶胶粘度和透光率的影响 多糖总浓度控制为3.0%,pH分别设定为3、4、5、6、7、8、9,按KGM∶CS为3∶7称取一定量的KGM和CS,室温下搅拌均匀后,将烧杯分别置于温度为80 ℃的水浴中加热搅拌30 min,然后冷却至室温,测定溶胶粘度和透光率。
1.2.8 数据处理 对实验数据采用Origin 8.6 软件进行处理。
2 结果与分析
2.1复配溶胶的协同增效性
2.1.1 KGM与粘度的关系 KGM是一种水溶性高分子多糖,基本上不带电荷,含有丰富的羟基,易溶于水,吸水膨胀,粘度很高[1]。结果如图1所示。从图1中可看出,随着KGM浓度的增加,溶胶粘度也随之增加。KGM浓度低时,粘度增加缓慢;随着浓度增加,粘度迅速增加,呈现假塑性流体特征[16]。多糖的流变学行为取决于它们的结构、分子量、浓度等[17]。KGM的这种变化可能是因为KGM溶胶浓度较小时,分子间的距离较大,分子间不能直接形成氢键,分子间相互作用弱,溶胶粘度小。KGM溶胶浓度增大,分子间的距离减小,受分子热运动的影响,分子间交联,形成氢键,粘度值增加[18]。
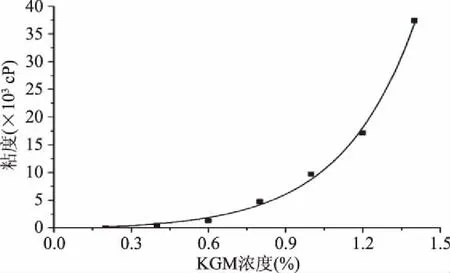
图1 KGM浓度对溶胶粘度的影响Fig.1 Effect of concentration of KGM sol on the viscosity
2.1.2 CS与粘度的关系 从图2中可以看出,随着CS浓度的增加,CS溶胶的粘度也增加,CS溶胶的粘度与浓度呈线性正相关。(y=2.6315x-8.1965,R2=0.9850)。

图2 CS浓度对溶胶粘度的影响Fig.2 Effect of concentration of CS sol on the viscosity
2.1.3 KGM/CS复配溶胶粘度变化规律 由图3~图6可知,KGM/CS复配溶胶的粘度都大于KGM与CS的粘度之和,产生增稠效应和协同效应。主要是KGM与CS分子之间形成氢键,增加溶胶分子间内摩擦力,使得溶胶的粘性增加,粘度增大。从图中还可以看出,KGM添加量为0.2%、0.3%、0.4%时,KGM/CS溶胶粘度随CS浓度的增加而增加;当KGM浓度增加到0.5%,而CS浓度小于3.0%时,KGM/CS溶胶粘度上升较慢,CS浓度大于3.0%时,复配溶胶的粘度急剧上升,与KGM溶胶粘度-浓度的变化规律相同。KGM含量少时,KGM在溶胶中呈无规线团分子,与螺旋状的CS分子缠绕较少,分子间结合力弱,当KGM浓度增加到一定值,KGM分子构象由无规线团分子过渡为球形分子结构,包裹住CS小分子,KGM与CS之间形成氢键,流动阻力增加[19],因此,粘度随CS溶胶浓度增加近乎呈指数递增。

图3 0.2% KGM溶胶与不同浓度CS溶胶复配Fig.3 The viscosity of various concentration of CS sol mix with 0.2% KGM sol

图4 0.3% KGM溶胶与不同浓度CS溶胶复配Fig.4 The viscosity of various concentration of CS sol mix with 0.3% KGM sol

图5 0.4% KGM溶胶与不同浓度CS溶胶复配Fig.5 The viscosity of various concentration of CS sol mix with 0.4% KGM sol

图6 0.5% KGM溶胶与不同浓度CS溶胶复配 Fig.6 The viscosity of various concentration of CS sol mix with 0.5% KGM sol
2.2复配溶胶粘度的影响因素
2.2.1 KGM/CS比例对复配溶胶粘度和透光率的影响 由图7可知,KGM/CS的配比不同,复配溶胶的粘度和透光率也有所变化。复配溶胶的粘度随着KGM含量的增加而逐渐增大,透光率则随着KGM含量的增加而逐渐降低。这可能是因为同等浓度下,CS的粘度远远小于KGM的粘度,所以复配溶胶的粘度随着KGM的浓度增加而增加。实验发现继续增加KGM的比例,复配溶胶的粘度呈指数倍数增加,粘度已超出粘度计的测量量程。透光率是考察溶胶性能的一项重要指标,透光率越高,高分子在分散介质水中分散越均匀。透光率随着KGM的含量增加而降低,可能是因为KGM分子比CS分子大,吸光度大,随着KGM含量的增加,复配溶胶中的CS含量的减少,吸光度增加,透光率减少。当KGM∶CS为3∶7时,达到较高粘度同时透光率不至于太低,减少了透光度降低带来的不利影响,选择合适的KGM/CS比值为3∶7。

图7 不同KGM/CS比对复配溶胶粘度和透光率的影响Fig.7 Effects of the concentration ratio about KGM and CS on viscosity and transmittancy of blending sol
2.2.2 多糖总浓度对复配溶胶粘度和透光率的影响 粘度是高分子化合物溶胶流变学性质的一项重要指标,表观粘度可以直观的表现溶胶中的水分子与高分子化合物的相互作用,对于高分子复配物而言,可以同时反映复配物分子间的相互作用。由图8可知,不同多糖浓度对复配溶胶的粘度和透光率都有影响。粘度随着多糖浓度的增加而增加,相反,透光率随着多糖浓度的增加而降低。多糖浓度的增加,单位体积中的分子数量也随之增加,分子间相互作用力也增加,粘度也随之升高;单位体积中的分子数量的增加也降低了光线的透过率,吸光度增大,透光率降低。多糖浓度为3.0%时,与2.8%相比,透光率虽然从3.899%降低到3.628%,但粘度却从28.844×103cP升高到了40.693×103cP。因此多糖浓度选择3.0%较为合适。

图8 不同多糖浓度对复配溶胶粘度和透光率的影响Fig.8 Effects of the concentration about polysaccharide on viscosity and transmittancy of blending sol
2.2.3 不同溶胀温度对复配溶胶的粘度和透光率的影响 由图9可知,随着溶胀温度的增加,复配溶胶的粘度呈现出先增加后减少的变化规律,在80 ℃时粘度最高,达到了41.848×103cP。可能是在该溶胀温度下,KGM分子与CS分子间氢键作用增强,分子结合更紧密。当温度继续升高时,分子运动加剧,KGM分子与CS分子间作用力减弱,两者形成的氢键不牢固,数量下降,不能形成稳定的复配体系,导致了复配溶胶粘度的下降[19]。随着溶胀温度的增加,复配溶胶的透光率也逐渐增大。小于60 ℃时,还没有达到CS的糊化温度,体系的透光率较低,随着溶胀温度的增加,CS糊化速率增加,糊化更完全。因此,选择80 ℃的溶胀温度较为合适。

图9 不同溶胀温度对复配溶胶粘度和透光率的影响Fig.9 Effects of the swelling temperature on viscosity and transmittancy of blending sol
2.2.4 pH对复配溶胶粘度和透光率的影响 由图10可知,体系pH对复配溶胶的粘度和透光率影响较大。pH为4时,溶胶粘度最低,在强碱环境下能使复配溶胶的粘度明显增加,pH5~8时则保持相对稳定。透光率在强酸强碱环境中都呈下降趋势,pH4~7时呈现明显的上升趋势,pH为7时,溶胶的透光率最大,pH大于7时,又呈现下降趋势。粘度和透光率随pH不稳定的变化可能是由KGM复杂的分子结构所决定的,KGM分子中含有醇羟基,他在不同pH情况下解离程度不同,导致pH对复配体系的粘度和透光率影响产生波动,这一影响有待进一步研究。因此,选择pH为7较为合适,粘度为41.391×103cP,透光率为7.339%。

图10 不同pH对复配溶胶粘度和透光率的影响Fig.10 Effects of pH on viscosity and transmittancy of blending sol
3 结论
KGM的浓度与粘度呈指数关系,CS的浓度与粘度呈线性关系,KGM的浓度增加到0.5%时,复配溶胶的粘度与浓度关系呈指数关系。KGM与CS复配,可产生协同增效性,复配溶胶的粘度大于两者之和。KGM/CS复配溶胶的最佳条件是:多糖的总浓度3.0%,KGM/CS比值为3∶7,溶胀温度80 ℃,pH7。KGM/CS复配溶胶的粘度随KGM比例、总糖浓度的增加而增加,随溶胀温度的增加先增加后减少。KGM/CS复配溶胶的粘度与pH的关系比较复杂,pH为4时粘度最小,pH大于4时,随pH的增加而增加。KGM/CS复配溶胶的透光率随KGM、总糖浓度增加而减小,随溶胀温度增加而增加,随着pH增加呈现先下降后上升再下降的趋势。在最优条件下制备KGM/CS复配溶胶,测定其粘度为41.391×103cP,透光率为7.339%。KGM/CS复配溶胶具有一定的协同增效性。
[1]Chua M,Chan K,Hocking T J,et al. Methodologies for the extraction and analysis of konjac glucomannan from corms ofAmorphophalluskonjacK. Koch[J]. Carbohydrate Polymers,2012,87(3):2202-2210.
[2]Abbaszadeh A,Macnaughta W,Swom G,et al. New insights into xanthan synergistic interactions with konjac glucomannan-A novel interaction mechanism proposal[J]. Carbohydrate Polymers,2016,144:168-177.
[3]Marcano J,Hemando I,Fiszman S.Invitromeasurements of intragastric rheological properties and their relationships with the potential satiating capacity of cheese pies with konjac glucomannan[J]. Food Hydrocolloids,2015,51:16-22.
[4]徐焱春,丁保淼,李顺,等. 魔芋葡甘露聚糖一羧甲基淀粉复配溶胶协效性研究[J]. 长江大学学报:自然科学版-石油/农学(中旬),2013,10(2):64-67.
[5]任文静,张爱清. 基于魔芋葡甘露聚糖阳离子聚合物的合成及表征[J]. 广州化工,2015,43(21):96-98.
[6]Yanai H,Adachi H,Katsuyama H,et al. Anti-atherosclerotic effects of konjac[J]. Functional Foods in Health and Disease,2015,5(4):136-144.
[7]Tester R F,Al-ghazzewi F H. Mannans and health,with a special focus on glucomannans[J]. Food Research,International,2013,50:384-391.
[8]Guardamagna O,Abello F,Cagliero P,et al. Could dyslipidemic children benefit from glucomannan intake?[J]. Nutrition,2013,29(7):1060-1065.
[9]金灵红,朱伟云. 魔芋葡甘露聚糖功能及其应用研究进展[J]. 畜牧与兽医,2014,2-030.
[10]Wei X,Pang J,Zhang C,et al. Structure and properties of moisture-resistant konjac glucomannan films coated with shellac/stearic acid coating[J]. Carbohydrate Polymers,2015,118:119-125.
[11]Wang J,Liu C,Shuai Y,et al. Controlled release of anticancer drug using graphene oxide as a drug-binding effector in konjac glucomannan/sodium alginate hydrogels[J]. Colloids and Surfaces B-Biointerfaces,2014,113:223-229.
[12]Liang H,Ye T,Zhou B,et al. Fabrication of gastric floating controlled release tablet based on konjac glucomannan[J]. Food Research International,2015,72:47-53.
[13]Zhao X,Li J,Jin W,et al. Preparation and characterization of a novel pH-response dietary fiber-Chitosan-coated konjac glucomannan[J]. Carbohydrate Polymers,2015,117:1-10.
[14]Harding S E,Smish I H,Lawson C J,et al. Studies on macromolecular interactions in ternary mixtures of konjac glucomannan,xanthan gum and sodium alginate[J]. Carbohydrate Polymers,2011,83(2):329-338.
[15]刘亚伟,王瑞娟,曹立松,等. 氧化羟丙基木薯淀粉的流变特性[J]. 食品科学,2015,36(17):59-64.
[16]Wang C,Xu M,Lv W,et al. Study on rheological behavior of konjac glucomannan[J]. Physics Procedia,2012,33:25-30.
[17]Paqueté,Hussain R,Bazinet L,et al. Effect of processing treatments and storage conditions on stability of fruit juice based beverages enriched with dietary fibers alone and in mixture with xanthan gum[J]. LWT-Food Science and Technology,2014,55(1):131-138.
[18]Xiao C,Lu Y,Zhang L.Preparation and physical properties of konjac glucomannan polyacrylamide blend films[J]. Journal of Applied Polymer Science,2001(b),1(4):882-888.
[19]许时婴,钱和. 魔芋葡甘露聚糖的化学结构与流变性质[J]. 无锡轻工业学院学报,1991(1):1-12.
[20]Russ N,Zielbauer B I,Ghebremedhin M,et al. Pre-gelatinized tapioca starch and its mixtures with xanthan gum and ι-carrageenan[J]. Food Hydrocolloids,2016,56:180-188.
Synergisticcharacteristicsandmixedsolofkonjacglucomannanandcassavastarch
LIJian-bin,LIUPei-hua,CHENYu,LIMin,DENGQiu-yan
(School of Light Industry and Food Engineering,Guangxi University,Nanning 530004,China)
The mixed sol of konjac glucomannan(KGM)and cassava starch(CS)were prepared.The consistency of mixed sol of konjac mannan/tapioca starch and combined synergies were studied. The effects of the concentration of polysaccharides,mixed proportion,temperature and pH on the viscosity of mixed sol were investigated. The experimental results indicated that consistency of mixed sol of konjac mannan/cassava starch was similar to KGM,but better than cassava starch sol. KGM could form synergistic gels with CS. The viscosity of mixed sol was greater than sum of KGM and CS.The optimal conditions were polysaccharide of total concentration 3.0%,the mixed proportion 3∶7(KGM∶CS),swell temperature 80 ℃,pH7.The viscosity of mixed sol in optimal conditions was 41.391×103cP,transmittance was 7.339%.
konjac glucomannan;cassava starch(CS);mixed sol;synergistic interaction
2016-12-14
李坚斌(1970-),女,博士,教授,研究方向:糖类物质生物利用及其污染控制,E-mail:437362893@qq.com。
国家自然科学基金项目(20864001,31160326);广西科学研究与技术开发项目(桂科能10100025);2016广西区特色本科专业建设项目。
TS201.7
:A
:1002-0306(2017)12-0039-05
10.13386/j.issn1002-0306.2017.12.008

