血液透析联合血液灌流治疗尿毒症周围神经病变的临床观察
王 蕾
河南平煤神马医疗集团总医院 平顶山 467000
血液透析联合血液灌流治疗尿毒症周围神经病变的临床观察
王 蕾
河南平煤神马医疗集团总医院 平顶山 467000
目的 观察血液透析联合血液灌流治疗尿毒症周围神经病变的临床疗效。方法 选取尿毒症周围神经病变患者94例,按随机表分为实验组和对照组,对照组应用血液透析治疗,实验组应用血液透析联合血液灌流治疗,对2组疗效进行比较。结果 治疗前,2组PTH(甲状旁腺激素)水平及感觉神经(正中神经、腓总神经及胫神经)传导速度均无显著差异(P>0.05);治疗后,实验组PTH水平显著低于对照组,且感觉神经传导速度快于对照组,实验组治疗总有效率(93.6%)高于对照组(76.6%)差异有统计学意义(P<0.05)。结论 尿毒症周围神经病变患者应用血液透析联合血液灌流治疗,能够显著降低PTH水平,加快感觉神经传导速度,提高治疗效果。
血液透析;血液灌流;尿毒症;周围神经病变
尿毒症是慢性肾衰的终末期,不是一种独立的疾病,而是各种肾脏疾病在晚期所共有的临床综合征,在临床上主要以代谢性酸中毒及水电解质平衡紊乱为常见,另外还有其他系统如心血管系统、血液系统、神经肌肉系统及胃肠道等临床症状,其中早期神经症状有失眠、不能集中注意力、记忆力减退等,还可常见一些周围神经病变,如肢体远端为主的对称及混合性多发性神经炎,感觉运动神经障碍等,症状以下肢较为严重,一旦尿毒症患者发生周围神经病变,则可能会给患者带来严重的影响[1]。目前采用血液透析法治疗尿毒症周围神经病变,虽然这种治疗方法能够控制病情的发展,但仅能够改善少数的症状,多数患者疗效不佳。现将血液透析联合血液灌注方法应用于尿毒症周围神经病变的患者中,取得较好疗效,现报告如下。
1 资料与方法
1.1 一般资料 选取2013-09-2016-09我院收治的尿毒症周围神经病变患者94例,按随机表分为实验组和对照组各47例,实验组男31例,女16例,年龄43~78(54.3±2.1)岁;病程3~12(6.7±0.9)a;透析时间2~6(4.1±0.7)a;原发病:慢性肾小球肾炎17例,高血压肾病14例,慢性肾间质肾炎11例,梗阻性肾病5例。对照组男29例,女18例,年龄45~76(53.9±1.8)岁;病程4~12(7.4±1.1)a;透析时间3~7(4.8±1.1)a;原发病:慢性肾小球肾炎18例,高血压肾病13例,慢性肾间质肾炎9例,梗阻性肾病7例。2组一般资料比较差异均无统计学意义(P>0.05),具有可比性。
1.2 纳入和排除标准 纳入标准:(1)病史、临床症状、辅助检查均符合尿毒症的诊断标准;(2)有周围神经病变症状;(3)同意加入实验,并签署知情同意书[2]。排除标准:(1)其他原因(维生素缺乏、药物因素、糖尿病等)所致的周围神经病变症状者;(2)拒绝加入实验者。
1.3 方法 (1)对照组应用血液透析治疗,采用费森尤斯公司的血液透析机,在治疗中,保持血流量约为300 mL/min,透析液流量约为500 mL/min,治疗4 h,每周3次。(2)实验组应用血液透析联合血液灌注治疗,血液灌注方法:采用珠海健帆公司的HA130型血液灌流器,首先应用5%的葡萄糖溶液500 mL冲洗灌流器,其次都采用0.9%的氯化钠注射液500 mL加入20 mg肝素对灌流器及管路冲洗,连接好透析器及灌流器,在进行治疗的过程中,维持血流量约为250 mL/min,透析液流量约为500 mL/min,并在治疗的过程中,给予静脉推注肝素,依据患者的病情特点调整肝素剂量,如患者出血,则可给予低分子肝素,剂量依据出血情况进行选取;治疗2 h,如灌流器的吸附情况达到饱和状态,治疗方法同对照组,治疗2 h,每周3次。
1.4 观察指标 观察2组治疗效果,并对治疗前后的感觉神经(以正中神经、腓总神经及胫神经为例)传导速度及血浆PTH(甲状旁腺激素)水平进行比较。治疗效果:(1)显效:患者肢体疼痛、四肢无力、感觉异常等症状明显缓解或基本消失;(2)有效:患者的肢体疼痛、四肢无力、感觉异常等症状有所减轻;(3)无效:患者肢体疼痛、四肢无力、感觉异常等症状无变化,甚至加重[3]。治疗总有效率=显效率+有效率。
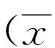
2 结果
2.1 2组疗效比较 实验组治疗总有效率高于对照组,差异有统计学意义(P<0.05)。见表1。
2.2 2组治疗前后血浆PTH水平比较 治疗前,2组PTH水平无显著差异(P>0.05),治疗后实验组PTH水平显著低于对照组(P<0.01)。见表2。
2.3 2组治疗前后感觉神经传导速度比较 治疗前,2组正中神经、腓总神经及胫神经的传导速度无显著差异(P>0.05);治疗后,实验组正中神经、腓总神经及胫神经的传导速度均快于对照组(P<0.01)。见表3。
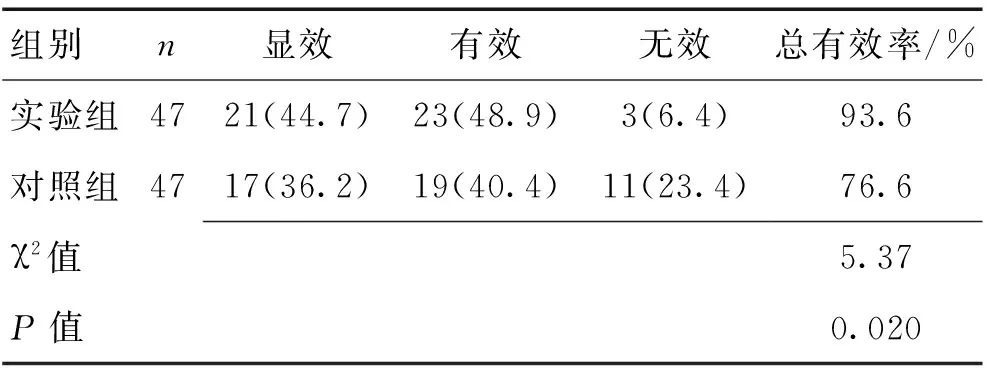
表1 2组疗效比较 [n(%)]
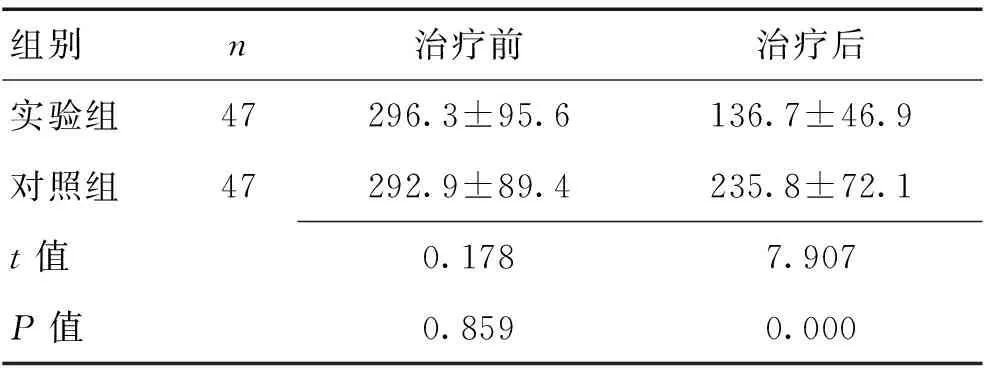
表2 2组治疗前后血浆PTH水平比较 (ng/L)
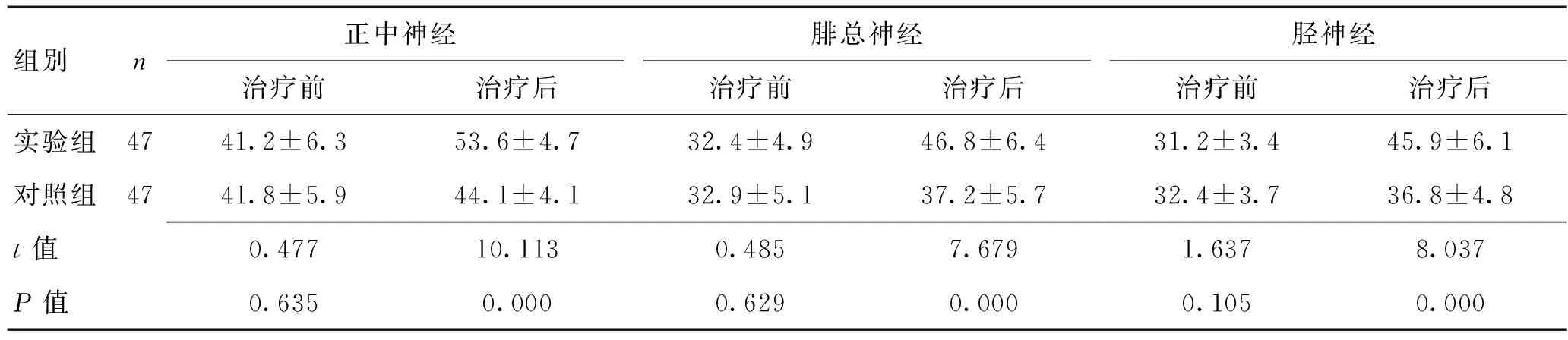
表3 2组治疗前后感觉神经传导速度比较 (m/s)
3 讨论
尿毒症是一组由各种原因引起的慢性肾功能不全患者体内集聚了多种代谢产物,其中部分代谢产物作为毒素引起机体发生病变的临床综合征[4]。尿毒症周围神经病变是尿毒症患者常见的并发症,临床以远端、对称运动及感觉神经等多种神经病变为特点,主要临床表现有四肢无力、萎缩、远端肢体灼烧感,严重者可丧失运动功能发生瘫痪[5]。部分患者无明显临床症状,但肌电图检查发现感觉、运动神经传导速度减慢,其中以感觉神经传导速度减慢最为明显[6]。
目前临床上主要是采用血液透析的方法治疗,它能够有效的清除血液中的小、中分子类毒素物质,在一定程度上控制病情的发展,缓解患者的周围神经病变,但对血液中、大分子毒素物质难以清除,导致治疗效果差强人意[7]。血液灌流应用的是人工合成的树脂技术,在临床应用的过程中以多空、高表面积、能够迅速吸附等特点,故而能够有效的吸附并清除尿毒症患者血液中的大分子毒性物[8]。
尿毒症患者出现周围神经病变的发病机制,目前尚未清楚,但可能与下列因素有关:(1)毒性物质在体内积聚,损伤周围神经,出现周围神经病变;(2)甲状旁腺激素在体内浓度过高时,可引起肾性骨病等情况[9]。甲状旁腺激素(PTH)是甲状旁腺主细胞分泌的碱性单链多肽类激素,是由多个氨基酸组成的多肽,它主要功能是调节钙、磷代谢,能够升高血钙水平、血磷水平下降,当体内的血钙降低时,PTH会释放到血液中,导致血液中PTH升高。甲状旁腺激素(PTH)过多,是引起尿毒症异常的毒素之一,且终末期的甲状旁腺激素升高是导致肾性骨病、周围神经病变等并发症的重要原因[10]。本次实验中,治疗前PTH水平升高,经治疗后2组PTH水平均有所下降,但实验组下降的更为明显(P<0.01),表明血液透析联合血液灌流能够降低PTH水平,调节钙磷代谢。
结果显示,治疗前,2组PTH(甲状旁腺激素)水平及感觉神经(正中神经、腓总神经及胫神经)传导速度无明显差异,且一般情况也无明显差异;治疗后,实验组PTH水平显著低于对照组,表明血液灌注能够有效的清除尿毒症患者体内的大分子有毒物质,与血液透析相结合,能够更好的清除尿毒症患者体内的有毒物质,从而显著缓解症状,提高治疗效果。当有毒物质有效清除后,尿毒症患者体内的毒性物质积聚减少,对周围神经的损伤降低,改善周围神经病变导致的临床症状,提高治疗效果。实验结果显示,实验组感觉神经传导速度快于对照组,表明血液灌注能够有效的改善尿毒症患者神经传导减慢的情况,这可能是由于尿毒症患者体内的有毒物质积聚,对周围神经造成损伤,在一定程度上影响了外周神经的传导速度,由于在正常情况下,感觉神经的传导要快于运动神经,因此在两者都受到影响的情况下,感觉神经的传导影响更为明显。总之,实验结果可知,尿毒症合并周围神经病变患者,应用血液透析联合血液灌注,能够有效的清除患者血液中的毒性物质,减少毒性物质对周围神经的影响,从而改善患者的临床症状,提高治疗效果。
综上所述,尿毒症周围神经病变患者应用血液透析联合血液灌流治疗,能够显著降低PTH水平,加快感觉神经传导速度,提高治疗效果。
[1] 滕舰,袁东,柳晓明.高压氧对维持性血液透析尿毒症患者周围神经病变的作用[J].中华航海医学与高气压医学杂志,2011,18(2):121-122.
[2] 沈学飞,韩晓云,殷爱民,等.神经妥乐平联合血液透析滤过治疗尿毒症周围神经病变疗效观察[J].中国全科医学,2012,15(17):1 984-1 985.
[3] 高民,汤日宁,马坤岭,等.血液净化方式对尿毒症周围神经病变的疗效[J].江苏医药,2012,38(23):2 806-2 809.
[4] 于秀峙,陆石,张金元,等.尿毒症性周围神经病的特点与生活质量评价[J].中国中西医结合肾病杂志,2012,13(10):873-875.
[5] 于秀峙,陆石,张金元.尿毒症性周围神经病诊治进展[J].中国中西医结合肾病杂志,2011,12(11):1 027-1 029.
[6] 曹炎生,詹悦.卡马西平治疗尿毒症性周围神经病变的临床疗效观察[J].湖北师范学院学报(自然科学版),2012,32(3):30-32.
[7] 徐炳侠,张云霞,陈学勋,等.血液透析滤过、血液透析联合血液灌流对尿毒症周围神经病变患者感觉定量检测的影响[J].中国当代医药,2016,23(27):65-68.
[8] 王小红.左卡尼汀联合血液透析治疗尿毒症性周围神经病变的临床疗效分析[J].黑龙江医药科学,2015, 38(5):117-118.
[9] 赵璐杰,李超林,邱君,等.左卡尼汀联合血液透析治疗尿毒症性周围神经病变的临床疗效观察[J].中国血液净化,2013,12(7):371-374.
[10] 张洪浩,林春环,王洪杰.甲钴胺胶囊联合血液灌流治疗尿毒症周围神经病变临床疗效观察[J].中国医师进修杂志,2013,36(1):49-50.
(收稿2016-11-23)
R745
B
1673-5110(2017)10-0080-03

