MIS-TLIF下单纯椎间植骨融合与椎间Cage融合治疗腰椎间盘突出症疗效对比研究*
杨佳宁,陈 宾,宋有鑫,甄瑞鑫,李玉波,赵成亮,赵丽丽,孔庆柱,李 戈
(承德医学院附属医院脊柱外二科,河北承德 067000)
论著·临床研究
MIS-TLIF下单纯椎间植骨融合与椎间Cage融合治疗腰椎间盘突出症疗效对比研究*
杨佳宁,陈 宾△,宋有鑫,甄瑞鑫,李玉波,赵成亮,赵丽丽,孔庆柱,李 戈
(承德医学院附属医院脊柱外二科,河北承德 067000)
目的 对微创经椎间孔腰椎椎体间融合(MIS-TLIF)下单纯椎间植骨融合与椎间Cage融合治疗单节段腰椎间盘突出症疗效的对比分析,以判断2种融合方法的术后疗效及对比临床价值。方法 采用MIS-TLIF手术治疗的单节段腰椎间盘突出症患者共61例,根据融合方法的不同分为单纯椎间植骨融合组(A组)和椎间Cage融合组(B组)。比较两组患者的手术时间,术中出血量,术后引流量,临床疗效采用腰、腿疼痛视觉模拟评分(VAS)、Oswestry 功能障碍指数(ODI)评分、日本骨科协会(JOA)评分和Macnab标准,行腰椎动力位X线片和CT三维重建检查评价椎间融合情况。结果 两组患者性别、年龄、病程、病变节段等一般资料比较,差异均无统计学意义(P>0.05),具有可比性。两组患者术中出血量,术后引流量差异无统计学意义(P>0.05)。术后两组的VAS评分、ODI评分、JOA评分和Macnab标准,末次随访椎间融合率,差异无统计学意义(P>0.05)。两组患者的手术时间,手术后椎间隙高度变化,差异有统计学意义(P<0.05)。结论 MIS-TLIF下单纯植骨融合治疗腰椎间盘突出症可获得与Cage融合相当的临床疗效和植骨融合率,并且治疗费用低,无排斥反应,可供临床选择。
微创经椎间孔椎体间融合;单纯椎间植骨融合;Cage融合;腰椎间盘突出症
通道下由于微创经椎间孔椎体融合术(minimally invasive TLIF,MIS-TLIF)自Foley等[1]提出后,逐渐在临床开展应用,多数患者术后疗效满意[2-3]。经过不断完善发展,MIS-TLIF已成为脊柱外科最常见的微创术式之一。但目前针对MIS-TLIF下不同椎体融合技术对治疗腰椎间盘突出症疗效的对比方面报道较少。本研究回顾性地分析比较了本院2012年1月至2014年12月分别以椎体间单纯植骨融合和Cage融合治疗的腰椎间盘突出症患者的术后疗效,现报道如下。
1 资料与方法
1.1 一般资料 入选标准:(1)诊断为腰椎间盘突出症,经保守治疗3个月无效;(2)经CT/MRI检查证实均为单节段腰椎间盘突出,并且均有腰椎间盘突出症临床表现,腰椎动力位X线片均合并腰椎不稳;(3)患者及家属同意参加入组并参与本次研究。排除标准:(1)合并腰椎肿瘤、感染等疾病;(2)合并严重内科系统疾病不能耐受手术者;(4)患者本人不同意参与本次研究者。本研究共纳入患者61例,其中男27例,女34例,平均年龄50.6岁。两组患者性别(χ2=0.026,P=0.873)、体质量(t=0.138,P=0.891)、病程(t=1.070,P=0.289)、发病节段(确切概率法P=0.739)比较,差异均无统计学意义,具备可比性,见表1。
1.2 方法 A组:患者采用硬膜外麻醉或全身麻醉,取俯卧位,腹部垫空,C型臂X射线机腰椎侧位确定手术侧上下椎弓根体表投影点,沿两中心点连线,旁开1~2 cm即为手术切口,切口长度约4 cm,经多裂肌外侧与最长肌肌间隙入路,钝性剥

表1 患者一般情况比较
离后再置入扩张管道微创系统。暴露上、下关节突关节,人字脊定位法植入椎弓根螺钉固定。直视下用咬骨钳去除病变节段下关节突和上关节突内侧缘,连同神经根管内侧壁,必要时需要去除部分下位椎体椎板上缘,彻底达到椎管及神经根管的减压,完成症状侧神经根松解。如患者为双侧症状,可实现单侧入路经椎板穹窿减压,实现对侧神经根松解。对于双节段患者,采用有限延长切口通过调整通道方向即可完成相邻双节段减压,本次研究未纳入双节段减压病例。术中可采用双极电凝及明胶海绵止血处理周围血管。摘除椎间盘,将取下的自体骨块咬成绿豆大小植入椎间隙。术后常规放置负压引流管。B组:患侧减压及固定同A组,将取下的自体骨打压植入椎间融合器(Cage),随后将Cage植入椎间隙进行椎间融合。
1.3 术后处理 术后3 d常规使用抗菌药物预防伤口感染,并应用脱水剂和激素减轻神经根水肿;术后24~48 h拔除引流管,术后第1天开始腰背肌及直腿抬高功能训练;鼓励患者早期腰围支具保护下床活动;术后3个月内避免过度弯腰及负重等活动。随访期内两组均未发现固定失败;均未发现植骨块或Cage移位、脱出;无伤口感染。
1.4 疗效评价 所有患者均获得有效随访。分别于术前1天、术后3个月、术后6个月和术后1年行疼痛视觉模拟评分(VAS)、Oswestry 功能障碍指数评分(ODI)和术后1年Mac nab[4]标准评价临床疗效。根据日本骨科协会(JOA)评分29分法评定术后效果[5]。同时比较分析两组手术时间,术中出血量,术后引流量及相关并发症。术后随访时常规查腰椎正侧位片,腰椎动力位片,部分患者选择行腰椎间盘CT平扫或腰椎磁共振检查。判断椎间植骨融合及椎间隙高度丢失情况。影像学评价参照X射线或CT平扫Suk法[6],以终板界面的桥接骨小梁长入和(或)穿越椎间融合器作为融合标准[7]。椎间融合的标准[8]:(1)腰椎X线侧位片见椎间隙上下椎体间有连续骨小梁形成或融合器周围有连续骨桥出现;(2)椎间融合器无移位滑脱,无植骨沉降,内固定无松动滑脱,植骨周围无透亮影出现;(3)动力位椎间角度变化小于10°,前后移位小于4 mm。融合率=融合数/总例数×100%。椎间隙高度为椎体前缘与后缘高度的平均值。椎间隙高度丢失率=(术后椎间隙恢复有效高度-某时间点椎间隙高度/术后椎间隙恢复有效高度)×100%。
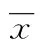
2 结 果
2.1 手术时间、术中出血量、术后引流量比较 A组的手术时间与B组比较,差异有统计学意义(P<0.01),可见选择植入Cage的患者可延长手术时间;A组与B组术中出血量、术后引流量比较,差异无统计学意义(P>0.05)。见表2。

表2 两组手术时间、术中出血量、术后引流量比较±s)
2.2 临床结果比较 JOA评分,重复测量方差分析 Mauchly 的球形度检验P=0.000,不同时间点比较F=1 521.947,P=0.000;同一组不同时间点比较采用Bonferroni法,A组、B组术后6个月与术后1年差异无统计学意义(P>0.05),其他时间点间均有差别;A、B两组比较F=0.160,P=0.691,两组间差异无统计学意义。VAS评分,重复测量方差分析 Mauchly 的球形度检验P=0.000 ,不同时间点比较F=1925.279,P=0.000;同一组不同时间点比较采用Bonferroni法,A组、B组各时间点间差异均有统计学意义(P<0.05);A、B两组比较F=0.916,P=0.342,两组间差异无统计学意义。ODI评分,重复测量方差分析 Mauchly 的球形度检验P=0.000,不同时间点比较F=4 425.938,P=0.000;同一组不同时间点比较采用Bonferroni法,A组、B组各时间点间差异均有统计学意义(P<0.05);A、B两组比较F=0.058,P=0.810,两组间差异无统计学意义。Macnab标准评价,术后1年同级别组间比较,秩和检验z=-0.138,P=0.890,差异无统计学意义,见表4。
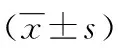
表3 术前及术后的JOA、VAS、ODI评分情况
a:P<0.01,与同组术前1 d比较;b:P<0.01,与同组术后3个月比较;c:P<0.05,与同组术后6个月比较。

表4 Macnab标准手术疗效比较
-:此项无数据。
2.3 影像结果比较 两组患者术后椎间隙高度均有不同程度的丢失。椎间隙高度比较重复测量方差分析 Mauchly 的球形度检验(P=0.089),不同时间点比较,差异有统计学意义(F=30.947,P=0.000),同一组不同时间点比较采用LSD法,A组术前与术后1个月、术后3个月与术后6个月、术后3个月与术后1年、术后6个月和术后1年差异无统计学意义(P>0.05),其余时间点差异有统计学意义(P<0.05);B组术前与术后1个月、术后3个月与术后6个月、术后6个月与术后1年差异无统计学意义(P>0.05),其余时间点差异有统计学意义(P<0.05);A、B两组组间比较(F=116.397,P=0.810),同一时间点两组间比较采用多变量方差分析,术前A、B两组差异无统计学意义(P>0.05),其余时间点两组差异有统计学意义(P<0.05)。术后1年丢失率差异有统计学意义(t=17.891,P=0.000),说明单纯植骨可以影响椎间隙高度的丢失,见表5。两组患者术后融合率比较,术后6个月融合率差异有统计学意义(t=4.469,P=0.000);术后1年融合率差异无统计学意义(t=0.127,P=0.899),见表6。

表5 两组术后不同随访时间椎间隙高度±s,mm)

表6 两组患者术后融合率比较(%)
3 讨 论
腰椎间盘突出症是骨科的常见病、多发病。部分患者常合并腰椎不稳,保守治疗通常很难达到理想效果,需通过手术充分地减压。但是由于需要将椎间盘、椎板、黄韧带和部分关节突切除,使脊柱的稳定性进一步破坏,因此重建脊柱的稳定性得到了越来越多的专家学者的重视。脊柱融合固定手术是治疗腰椎退行性变的金标准[9-10]。近年来随着微创技术的迅猛发展,由于MIS-TLIF具有创伤小,出血少,术后下地活动时间早且尽可能地保护椎旁肌肉,减少患者术后腰背部疼痛的发生率[11]等技术优势而逐渐得到专家学者的广泛认可和应用。而保持腰椎稳定性最关键的就是椎体间植骨融合情况。根据Dennis的三柱理论,椎体间植骨融合最符合脊柱的生理要求,稳定性最好。根据Wolf定律,椎体间植骨起到了椎体间支撑的作用,椎体间植骨床面积大,融合质量与融合率高,因而融合强度也大,在一定程度上可以防止椎间隙塌陷和进一步退变[12-13]。满意的椎间融合能够有效减少继发性椎管狭窄而引起的神经根及硬膜囊受压所引起的相关症状。它还可以有效防止脊柱畸形,缓解腰背部及腿部疼痛,利于神经根减压和恢复脊柱正常矢状面上的曲线。
本研究,将目前临床上应用最为常见的两种椎体间植骨融合方式,单纯椎间植骨融合和Cage融合进行对比,分别从围术期参数和术后疗效等方面进行观察分析。从两组患者手术时间差异有统计学意义(P<0.05),可见单纯植骨减少了术中反复使用融合器试模,进行Cage型号的选择等操作,从而缩短了手术时间。此外与Cage融合相比单纯椎间植骨融合具有操作简单,学习曲线短,更利于初学者的掌握[14]。两组患者1年内的随访节点期,JOA评分,VAS评分,ODI评分,Macnab标准评价,均获得随访记录,经统计学分析,两组患者的两种融合方法均可获得满意的临床疗效,并且组间比较差异无统计学意义(P>0.05)。
从两组患者的术后1年随访融合率比较来看,本研究发现远期融合率的差异无统计学意义(P>0.05)。但笔者认为自体骨打压植骨可提供充足的骨量,植骨面积大,排斥反应轻且自体骨不存在Cage与椎间隙不匹配的问题。Cage融合器是一种界面固定装置,对压力载荷有较强的承受力,而对牵张力的控制则是靠融合器上下锯齿界面[15-16]。因此有报道称Cage融合器由于弹性过高,易致应力集中在对抗屈伸运动的牵张力作用时上下锯齿摩擦骨性终板,造成椎体切割及上下终板的磨损,从而导致骨性终板破坏,在术后由椎间融合器和钉棒系统共同承担手术节段的负荷[17],增加了钉棒系统承担负荷,从而造成融合器下沉。特别是部分老年患者合并骨质疏松,植骨融合慢,骨性融合率降低,最终导致腰背部疼痛可能性更大[18]。而且Cage内植骨量较少,植骨面积较小,有可能致椎间融合器移位沉降的风险。有报道称融合器界面间存在微动,导致局部纤维组织形成过多,妨碍骨长入[16],通过组织病理学研究表明因应力遮挡作用,融合器的中央为纤维瘢痕组织,无骨痂穿过,故融合器的骨融合仅发生在上、下骨性界面处,而单纯的椎间自体植骨可以促进植骨块与上下终板间融合时有更多血管长入,增加融合质量。Cage融合虽然是自体骨植入但骨量相对较少。Togawa等[19]研究显示Cage内植骨成活的同时也可能存在骨坏死。Cage融合器作为一种异物将永久性的置入体内,不能被自体所吸收。
手术后1年随访两组患者椎间隙高度丢失率比较,差异有统计学意义(P<0.05),说明单纯植骨融合较Cage融合比较,高度丢失率更大些。虽然单纯椎间植骨融合常由于植骨块溶解、塌陷吸收从而导致支撑力不足致使椎体间高度丢失率略高于Cage融合[20]。而通过随访两组患者中单纯植骨组的椎间隙高度丢失主要发生在术后早期,12个月以后的丢失率较低,融合器组的椎间隙高度在6~12个月变化不大。有报道,部分Cage融合患者术后12~24个月仍可出现一定的丢失率,但未给ODI、VAS评分带来本质影响[21]。然而有文献报道,可能由于椎间植入Cage时用力敲打震荡而导致融合器组存留了更多的下肢痛和麻木的临床表现[22]。另外,在大号Cage试模或Cage植入过程中还可能对神经根过分牵拉或对神经根或硬膜囊瞬间的暴力挤压造成损伤,而导致一些术后并发症的发生。
综上所述,MIS-TLIF下单纯椎间植骨融合和Cage融合对于治疗单节段腰椎间盘突出症均具有明确的临床疗效,椎间隙高度得到明显恢复,椎间植骨融合效果确切。笔者认为Cage融合较适用于椎间隙狭窄较严重,骨质疏松不严重的患者;而单纯植骨融合更适合于经济条件较差,或是腰椎负荷较小的患者,或是骨质疏松较严重植入Cage容易造成Cage下沉或滑移的患者。因此,术前应对患者的病情做出详细的评估,结合患者的实际情况,合理选择个体化手术方案。
[1]Foley KT,Holly LT,Schwender JD.Minimally invasive lumbar fusion[J].Spine(Phila Pa 1976),2003,28(15 Suppl):S26-35.
[2]Orpen NM,Corner JA,Shetty RR,et al.Micro-decompression for lumbar spinal stenosis:the early outcome using a modified surgical technique[J].J Bone Joint Surg Br,2010,92(4):550-554.
[3]Macnab I.Negative disc exploration[J].An analysis of the causes of nerve-root involvement in sixty-eight patients[J].J Bone Joint Surg Am,1971,53(5):891-903.
[4]左进步,余磊,黄凯,等.靶向定位THESSYS椎间孔镜技术治疗腰椎间盘突出症[J].中国疼痛医学杂志,2015,21(11):869-872.
[5]Fujiwara A,Kobayashi N,Saiki K,et al.Association of the Japanese orthopaedic association score with the oswestry disability index,Roland-Morris disability questionnaire,and short-form 36[J].Spine(Phila Pa 1976),2003,28(14):1601-1607.
[6]Suk SI,Lee CK,Kim WJ,et al.Adding posterior lumbar interbody fusion to pedicle screw fixation and posterolateral fusion after decompression in spondylolytic spondylolisthesis[J].Spine(Phila Pa 1976),1997,22(2):210-220.
[7]Shah RR,Mohammed S,Saifuddin A,et al.Comparison of plain radiographs with CT scan to evaluate interbody fusion following the use of Titanium interbody cages and transpedicular instrumentation[J].Eur Spine J,2003,12(4):378-385.
[8]Coe JD,Vaccaro AR.Instrumented transforaminal lumbar interbody fusion with bioresorbable polymer implants and iliac crest autograft[J].Spine(Phila Pa 1976),2005,30(17 Suppl):S76-83.
[9]Cakir B,Richter M,Huch K,et al.Dynamic stabilization of the lumbar spine[J].Orthopedics,2006,29(8):716-722.
[10]Buchowski JM,Kuhns CA,Bridwell KH,et al.Surgical management of posttraumatic thoracolumbar kyphosis[J].Spine J,2008,8(4):666-677.
[11]Madhok R,Kanter AS.Extreme-lateral,minimally invasive,transpsoas approach for the treatment of far-lateral lumbar disc herniation[J].J Neurosurg Spine,2010,12(4):347-350.
[12]Madan S,Boeree NR.Outcome of posterior lumbar interbody fusion versus posterolateral fusion for spondylolytic spondylolisthesis[J].Spine(Phila Pa 1976),2002,27(14):1536-1542.
[13]Wang JC,Mummaneni PV,Haid RW.Current treatment strategies for the painful lumbar motion segment:posterolateral fusion versus interbody fusion[J].Spine (Phila Pa 1976),2005,30(16 Suppl):S33-43.
[14]Lee JC,Jang HD,Shin BJ.Learning curve and clinical outcomes of minimally invasive transforaminal lumbar interbody fusion:our experience in 86 consecutive cases[J].Spine (Phila Pa 1976),2012,37(18):1548-1557.
[15]吴文坚,梁裕,张兴凯,等.微创腰椎经椎间孔椎体间融合术的并发症分析:131例病例回顾和文献复习[J].中国骨与关节外科,2012,5(2):103-108.
[16]Chrastil J,Patel AA.Complications associated with posterior and transforaminal lumbar interbody fusion[J].J Am Acad Orthop Surg,2012,20(5):283-291.
[17]Fischgrund JS.The argument for instrumented decompressive posterolateral fusion for patients with degenerative spondylolisthesis and spinal stenosis[J].Spine (Phila Pa 1976),2004,29(2):173-174.
[18]陈云生,陈荣春,郭朝阳,等.微创经椎间孔腰椎椎间融合术治疗老年腰椎退变性疾病[J].中国脊柱脊髓杂志,2013,23(12):1079-1085.
[19]Togawa D,Bauer TW,Brantigan JW,et al.Bone graft incorporation in radiographically successful human intervertebral body fusion cages[J].Spine (Phila Pa 1976),2001,26(24):2744-2750.
[20]Mcafee PC.Interbody fusion cages in reconstructive operations on the spine[J].J Bone Joint Surg Am,1999,81(6):859-880.
[21]Kasliwal MK,Deutsch H.Clinical and radiographic outcomes using local bone shavings as autograft in minimally invasive transforaminal lumbar interbody fusion[J].World Neurosurg,2012,78(12):185-190.
[22]Nandyala SV,Fineberg SJ,Pelton M,et al.Minimally invasive transforaminal lumbar interbody fusion:one surgeon′s learning curve[J].Spine J,2014,14(8):1460-1465.
The effect of pure interbody fusion and interbody cage fusion under MIS-TLIF treating lumbar disc herniation
YangJianing,ChenBin△,SongYouxin,ZhenRuixin,LiYubo,ZhaoChengliang,ZhaoLili,KongQingzhu,LiGe
(SecondDepartmentofSurgery,AffiliatedHospitalofChengdeMedicalCollege,Chengde,Hebei067000,China)
Objective To research the effect of pure interbody fusion and interbody cage fusion under minimally invasive transforaminal lumbar interbody fusion treat to single segment of lumbar disc herniation,analysis clinical value the two methods.Methods A total of 61 cases single segment lumbar disc herniation were treated with MIS-TLIF surgery,were divided into pure interbody fusion group (group A) and interbody fusion Cage group (group B) according to different fusion methods.Operative time,blood loss and postoperative drainage were recorded in two groups,the clinical efficacy were tested by using of visual analogue score(VAS),Japanese Orthopedic Association scores (JOA),Oswestry disability index (ODI) score and Macnab standard,the interbody fusion ability were evaluated by power lumbar X-ray film and CT 3D reconstruction.Results The gender,age,disease duration and disease segments in two gracps were not found statistically significant difference (P>0.05).Also,two groups of patients,blood loss,postoperative drainage has no significant difference (P>0.05).After the operation,the VAS score,ODI score,JOA score and Macnab criteria,the last follow-up of intervertebral fusion rate in in tuo groups were not found statistically significant difference (P>0.05).While the operative time,postoperative disc height changes were found significant difference between two groups(P<0.05).Conclusion MIS-TLIF simple fusion for lumbar disc herniation will be available with equal clinical efficacy fusion rate compared with cage fusion.
minimally invasive TLIF;pure interbody fusion;cage fusion;lumbar disc herniation
10.3969/j.issn.1671-8348.2017.08.013
承德市科学技术研究与发展计划(20142045)。 作者简介:杨佳宁(1982-),主治医师,硕士,主要从事脊柱微创外科研究。△
,E-mail:drchenbing@VIP.sina.com。
R687.3
A
1671-8348(2017)08-1048-04
2016-10-19
2016-11-17)

