经皮经肝穿刺同期胆道镜取石治疗复发性肝胆管结石
林树文 方颖华丁新民 袁智明 万里鹏 吉成岗
经皮经肝穿刺同期胆道镜取石治疗复发性肝胆管结石
林树文 方颖华#丁新民 袁智明 万里鹏 吉成岗
目的总结应用经皮经肝穿刺同期胆道镜治疗复发性肝胆管结石的治疗经验。方法回顾性分析我院2014年10月~2016年6月22例复发性肝胆管结石患者,在同一次麻醉下,B超引导下经皮经肝胆道穿刺成功后,同期行胆道镜碎石取石的手术疗效。结果21例患者穿刺后。取石成功,仅1例穿刺失败后中转开腹;1次取尽结石成功17例(81.0%),2次取尽结石者3例,3次取尽结石者1例,无严重并发症及死亡。随访至今无发现结石复发。结论对于复发性肝胆管结石患者,严格把握适应证,经皮经肝穿刺胆道镜同期治疗是可行、有效和安全的。
经皮经肝胆道造瘘;胆道镜取石;肝胆管结石;复发性
肝内外胆管结石是常见的胆道疾病,传统的手术治疗虽然几经改进,但由于炎症、狭窄、结石的恶性循环导致术后结石复发率可高达70%[1]。患者往往需要经历多次开腹手术,创伤大,难以接受。经皮经肝胆道镜(percutaneous transhepatic cholangioscopy,PTCS)取石,是一种治疗肝内外胆管结石的微创技术,发展至今已有30余年历史,对于复发性肝胆管结石更能体现其优越性。传统方法操作复杂,费时,并发症多,发展受到很大限制。虽然经历多次改良,但基本上仍需分期完成。为了更好的体现此技术的微创性,我们进一步改进,对于复发性肝胆管结石进行同期治疗,收到了很好的疗效。现报告如下。
1 资料与方法
1.1 一般资料
2014年10月至2016年6月期间,我科收治22例复发性肝胆管结石患者。患者男7例、女15例,年龄44~82岁,平均58岁;所有患者均有肝胆管结石手术史,其中1次手术史11例,2次手术史9例,3次手术史2例;单纯右肝内胆管结石患者1例,左肝内胆管合并胆总管结石6例,右肝内胆管结石合并胆总管结石8例,左、右肝内胆管结石合并胆总管结石7例。所有患者入院前3小时至1个月发病,均表现为剑突下或右上腹疼痛。合并胆道感染者14例,其中发热者9例,血白细胞升高者9例,最高为30.4×109/L;合并黄疸者15例,最高血总胆红素为344 μmol/L。所有患者术前均经彩色超声、CT或MRCP检查确诊为肝胆管结石患者,无发现肝萎缩或胆道肿瘤。
1.2 器械
Wolf硬式胆道镜,Olympus CYF⁃VA2型纤维胆道镜,TCS⁃B(胆道镜下)液电冲击波碎石仪,带穿刺引导探头的彩超机,光源与摄像系统,可调压脉冲式腔内灌注泵,斑马导丝,8⁃18 F系列筋膜扩张器,14 F、16 F、18 F peel⁃away鞘管,取石钳,Cook网篮,胆道球囊扩张器,多型号造瘘引流管。
1.3 手术方法
根据术前B超、CT或MRCP检查而确定穿刺点,做好术前评估及备用方案,一般位于剑突下右缘腹壁穿刺左侧肝管,位于右侧腋中线第10~11肋间穿刺右肝内胆管。气管插管全麻下或神经安定+局麻下,在彩超引导下按常规进行穿刺操作。穿刺过程中若顺利无出血,且患者无异常时继续沿导丝再逐级扩张经皮肝窦道,直至14~18F,后将相应的鞘管套在扩张器上并送入肝内胆管,后拔出扩张器,留下鞘管,鞘管的另一端留在体外,以建立一条外界与肝内扩张胆管直通的窦道。如多次反复穿刺目标胆管失败,灵活中转开腹传统手术。成功建立通道后,硬质胆道镜通道接可调压脉冲式腔内灌注泵,由导丝引入经鞘管直达目标胆管寻找结石。较小结石直接用水流“冲吸”技巧将碎石经鞘管冲出,也可用网篮套取、钳夹取出碎石。对于较大结石,用液电碎石仪击碎后,再利用上述方法取出结石。部分胆管因角度较大不能进入者改用纤维胆道镜取石。取石完成后,留置相应大小的造瘘引流管,按常规缝合并妥善固定,完成同期穿刺及碎石取石。所有操作在鞘内、胆道内进行,器械不与窦道壁直接接触。操作过程中,若患者出血较多、不能耐受或病情不允许,可随时中止操作,如窦道壁出血,可鞘管内置入扩张器,压迫止血后再行操作;如胆管壁出血,可置入造瘘管压迫,或者注入去甲肾上腺素稀释液冲洗,止血后再行操作;部分患者暂时压迫不能止血,需终止手术,置入造瘘管,经皮肝胆道引流3~7 d,再行二期手术。
术后处理:术后常规补液和使用抗生素。术后3~7 d,行胆道造影或CT检查证实无残石,拔除造瘘管;如有残余结石,可隔2~7 d再多次取石。
2 结果
21例患者穿刺取石成功,手术时间50~310 min,平均147 min;1次取尽结石者81.0%(17/21),2次取尽结石者14.3%(3/21),3次取尽结石者4.7%(1/21)。所有患者结石较大,均使用液电碎石仪,击碎后较大结石用取石网篮或取石钳取出,碎石则水流直接冲出。无胆瘘、胆管损伤及胰腺炎等其他并发症的发生,主要的不良反应为穿刺部位疼痛不适。住院12~32 d,平均住院时间20 d。
本组1例因反复穿刺失败后即中转开腹传统手术。本例穿刺失败患者既往曾行胆囊切除+肝左外叶切除+胆总管切开取石术,此次术前CT提示肝右后叶胆管及胆总管多发结石,左内叶胆管稍扩张,未见结石。拟穿刺目标胆管为左内叶胆管,术中B超引导下反复穿刺目标胆管,均未能成功置入导丝,遂中转开腹行胆总管切开取石。
2次取尽结石患者中2例因术中出血不止,被迫终止手术,术后经止血后再次取尽结石;另1例术中胆道镜检查未见明显残余结石,术后CT提示左肝内胆管残余结石,胆总管下段斑片样结石,经第2次手术完全取尽结石。
3次取尽者为左右肝内胆管合并胆总管结石,采用神经安定+局麻,第1次取石时间225 min,患者出现右上腹疼痛,难以耐受进一步手术,遂终止;第2次取石后胆道造影提示右肝内残余结石,行第3次取尽结石。
21例中有3例出现术中出血:1例为窦道壁出血,置入扩张器压迫止血后继续手术;2例为胆管壁出血,术中压迫不能止血,放置造瘘管后终止手术,1例术后出血约200 mL,经引流管灌注稀释去甲肾上腺生理盐水等非手术方式治愈,1周后再次完全取尽结石;另1例因合并肝硬化、凝血功能差,行经引流管灌注稀释去甲肾上腺生理盐水等非手术方式后仍出血不止,出血量约1500 mL,予输注同型浓缩红细胞,急诊行介入栓塞止血。止血后经2周护肝、纠正凝血功能后,再次完全取尽结石。
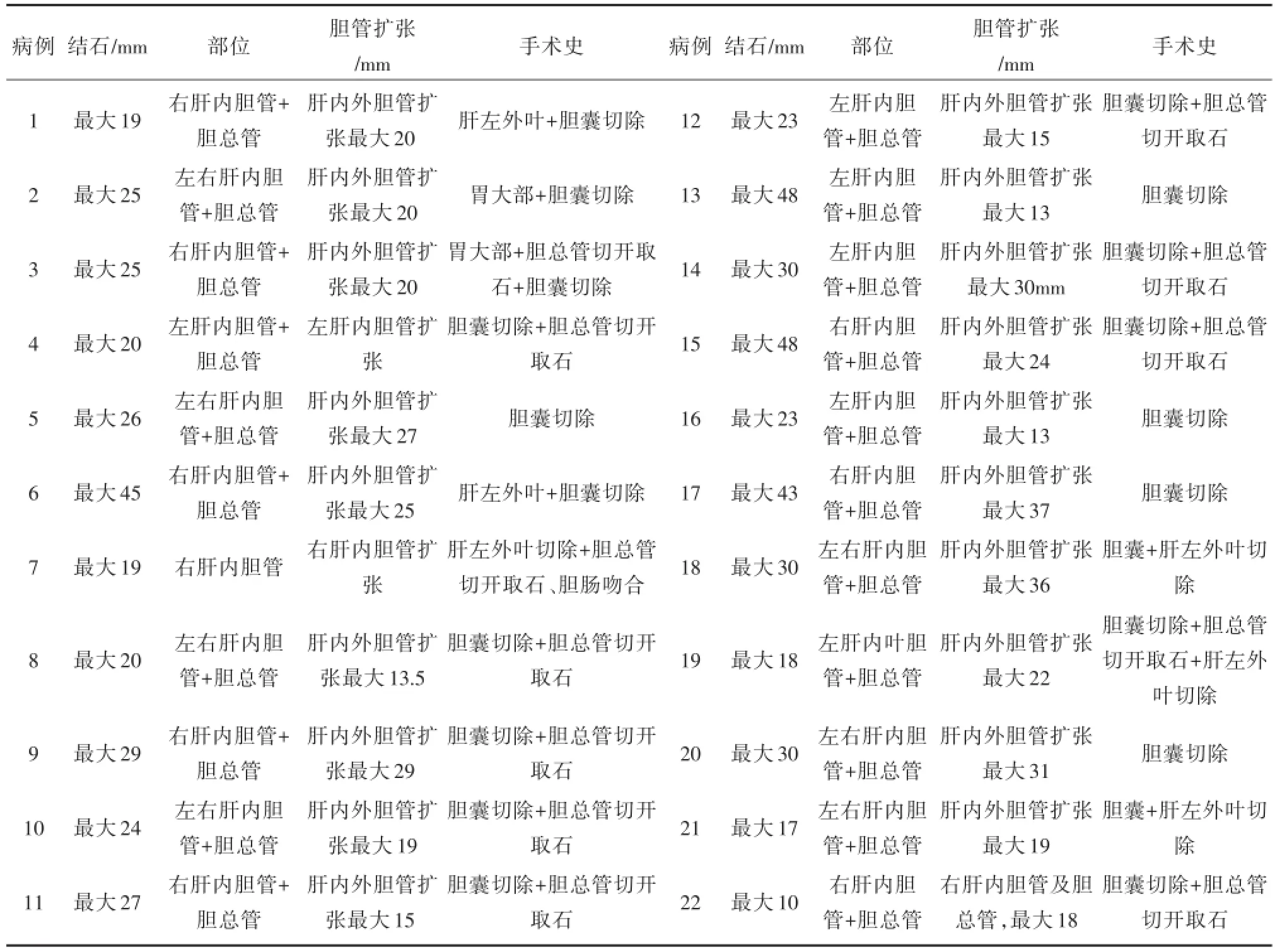
表1 22例肝内胆管结石的临床资料
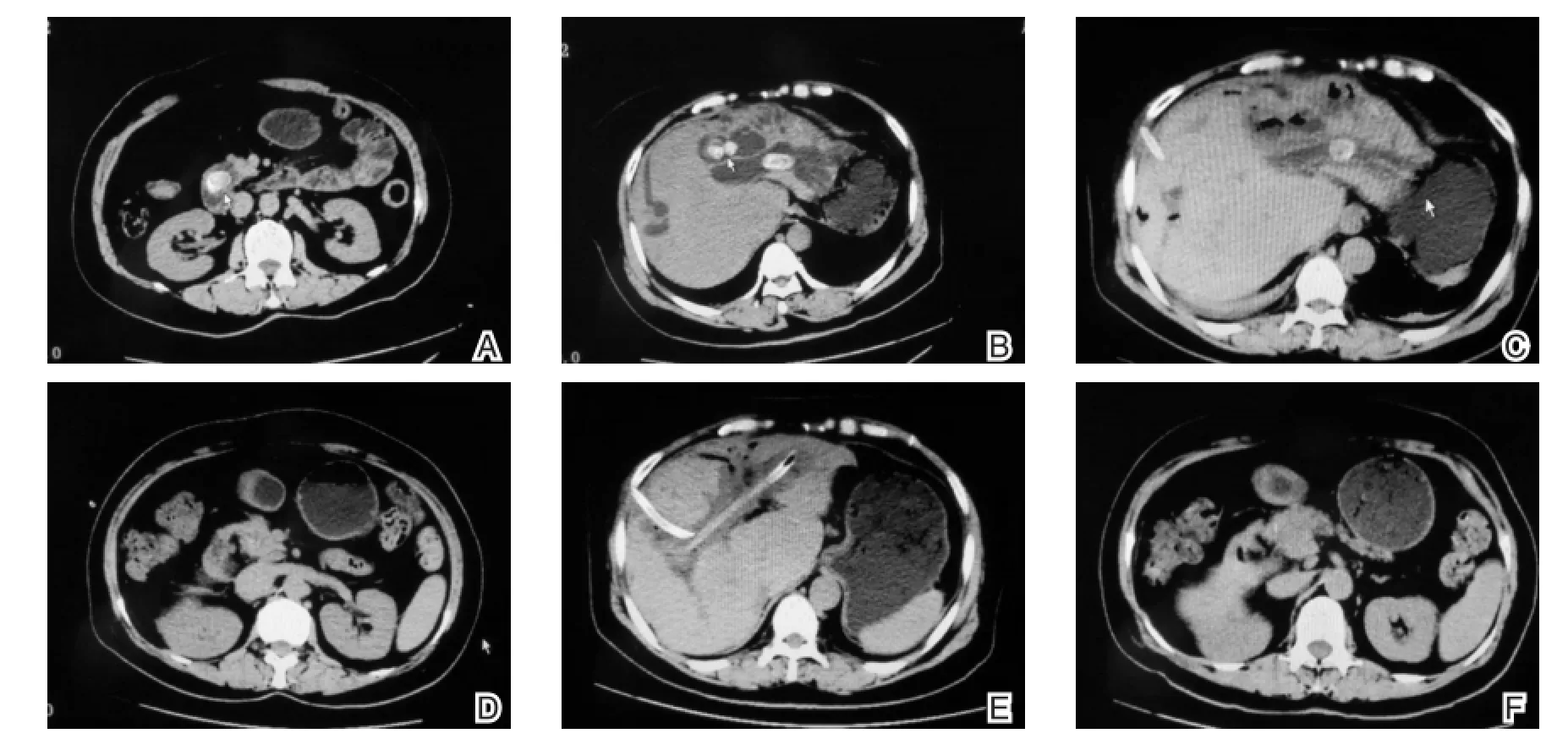
图1 女性,61岁,右上腹痛伴恶心、呕吐1天,既往行胆囊切除+胆总管切开取石术,经2次PTCSL后,取尽结石,症状完全缓解;A、B术前:胆总管及左肝内胆管多发结石;C、D第1次PTCS后:左肝内胆管残余结石,胆总管下段残余斑片样结石;E、F第2次PTCS后:左肝内胆管结石及胆总管结石已取尽,造瘘管在位
出院后采用门诊复诊、电话形式随访,第一年每半年随访一次,第二年开始每年随访一次,或者当患者出现腹痛、发热等相关症状时返院随访。随访内容包括血常规,肝功能,B超、CT或MRCP等。随访时间8~28个月,平均17.4月。其中5例出现一次复发性胆管炎来诊,主要表现为右上腹疼痛、血白细胞偏高,无伴发热,经抗感染等保守治疗后缓解。所有病例均未发现肝功能异常,结石复发、胆管癌或胆汁性肝硬化。
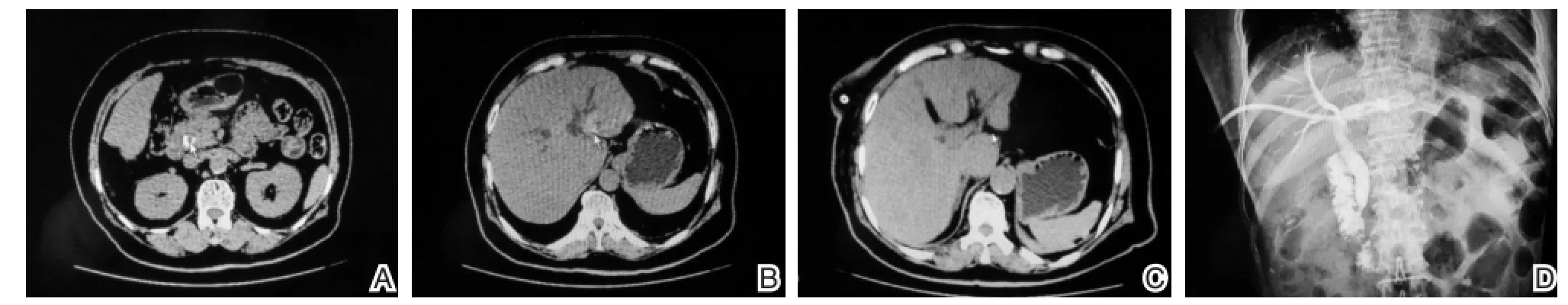
图2 女性,72岁,上腹部胀痛12小时,既往胆囊切除术,CT提示:左肝内胆管、胆总管多发结石。经1次PTCSL后,取尽结石,症状完全缓解;A、B术前:胆总管及左肝内胆管结石;C、D术后:左肝内胆管及胆总管结石已取出
3 讨论
对于复发肝胆管结石,传统手术方法包括胆管切开取石、肝切除、胆肠吻合等,部分患者需经历多次手术,创伤大,往往难以接受,很多患者拒绝接受再次手术。近年来,PTCS和肝切除成为肝胆管结石主要的治疗方法。实践表明,伴与不伴胆管狭窄的肝胆管结石均可采用PTCS治疗,且根据文献[2,3]报道,PTCS治疗胆总管结石的清除率可达100%,肝内胆管结石的清除率在76.8%~98.5%。
经皮经肝胆道镜(percutaneous transhepatic cholangioscopy,PTCS)于1972年由日本学者率先于临床应用,我国于1985年引进该技术[4],但至今尚未得到广泛应用,主要原因是原技术耗时长、住院时间长、多次手术操作、病人较痛苦并可能发生胆瘘、大出血、感染等并发症[2,5]。虽然有人根据经验和患者的情况,在使用方法进行已一些改良,但基本仍需分期才能完成,住院时间仍较长,微创性不突出[6,7]。为此,我们在前人的基础上,并且借鉴他人的经验,进一步改进,采用了同期经皮肝穿刺胆道镜碎石取石,取得了很好的疗效,突显微创性。我们的改进的方法主要是应用一步造瘘法同期取石,而非分期取石,术中应用鞘管隔绝窦道,可避免窦道毁损及出血;应用硬式胆道镜,可到达末梢胆管,尽量取尽肝内胆管结石,如遇胆道成角过大,仍可应用软式胆道镜进入。并且术中结合液电碎石仪,取出大结石及嵌顿结石。目前大部分学者提倡分期造瘘取石,主要基于动物实验[8]证明PTBD术后5~7 d(1周)经皮肝瘘道壁形成,壁内血管栓塞,纤维组织增生,瘘道周围肝面与胸腹壁有粘连,此时经皮肝扩张后造瘘碎石取石比较安全。但是根据我们的观察,严格把握适应症,同期行造瘘取石也是安全有效的。考虑主要因为本组患者均有上腹部手术史,腹腔形成黏连,空间局限,不易造成腹腔广泛出血及胆瘘;同时置入鞘管与窦道壁隔绝,即时形成人工窦道,避免穿刺窦道壁毁损出血。
本组所有患者胆道穿刺及取石均在一次麻醉下完成,穿刺点一般选择剑突下穿刺左肝内胆管矢状部,右侧肋间穿刺右前叶胆管,术中根据结石分布情况可作适当调整,穿刺方向需与目标胆管成锐角并朝肝门。其中有一例患者穿刺失败后即行开腹手术处理,这样能减少患者经济负担,缩短住院时间。扩张窦道时我们遵循逐步扩张,直至瘘道扩张至14-18F后行胆道镜操作。在扩张的瘘道内置支撑鞘管,全部操作在鞘管和扩张之胆管内进行,操作时器械不与瘘道壁接触,不伤及瘘道壁;手术过程由于有鞘管的保护,碎石取石时胆道内注水压力稍高也不易溢入腹腔;鞘管还将胆道相对“拉直”,使碎石取石可以像泌尿外科的PCN一样用硬镜操作,甚至可用液电碎石仪碎石,降低消耗成本。碎石的同时用水冲洗,使其经又直又光滑的管道流出,提高了取石速度,但应注意控制注水压力及注水量,以免发生腹胀、胆道逆行感染及水中毒等,有研究者[9]建议注水量控制在6000 mL。如术中发现腹部鼓胀明显,需留置胃管减压引流。在固定或推进鞘管时,动作要求轻柔,防止鞘管前端损伤窦道壁或胆管,引起大出血或胆漏。如遇窦道壁出血,需暂时终止手术,扩张器套入鞘管压迫,一般能达到止血效果;如较大血管出血不止,可选择介入栓塞,甚至开腹止血。胆道出血一般能自止,有时需用去甲肾素冲洗,或者放入扩张器或引流管压迫,对于出血不止者需通过介入或手术处理。本研究中有一例患者存在肝硬化合并凝血功能障碍,在手术过程中出现胆道壁渗血不止,及时终止手术放入造瘘管压迫后仍持续出血,去甲肾素冲洗后效果不佳,最后行介入栓塞止血,再行二期取石。因此,对于凝血机制异常有明显出血倾向者,采取PTCS治疗应慎重。根据我们的经验及Yoon[10]的一项研究显示,严重心肺功能异常、肝功能严重异常有大量腹水、肝内胆管不扩张、凝血机制异常有明显出血倾向是PTCS治疗的主要禁忌证,该类患者不宜采取PTCS治疗。
本研究表明在严格把握适应证的基础上,择期采用经皮经肝穿刺胆道镜同期治疗复发性肝胆管结石是安全可行的,最大限度减少患者反复开腹带来的痛苦,有效降低手术相关并发症,真正体现微创治疗的优越性。但因病例数较少,没有做到随机、双盲、对照研究,希望能有大宗随机、双盲、对照临床研究进一步证实其安全有效性。同时,本研究为复发性肝胆管结石患者,均有胆道手术史,而对于无胆道手术史的初发肝胆管结石患者,该技术是否仍安全可行,这是我们以后可以研究的方向。
[1]Kim JH,Lee SK,Kim MH,et al.Percutaneous transhepatic cholangioscopic treatment of patients with benign bilio⁃enteric anastomotic strictures[J].Gastrointest Endosc,2003,58(5):733-738.
[2]Ahmed S,Schlachter TR,Hong K.Percutaneous transhepatic cholangioscopy[J].Tech Vasc Interv Radiol,2015,18(4):201-209.
[3]时鑫,刘衍民,文辉清,等.经皮肝胆道造瘘硬质胆道镜治疗肝内胆管结石[J].中华腔镜外科杂志(电子版)[J]. 2010,3(5):393-395.
[4]张宝善,山川达郎,三芳端.经皮经肝胆道镜的临床应用[J].中华外科杂志,1985,23(5):353-355.
[5]Oh HC,Lee SK,Lee TY,et al.Analysis of percutaneous tran⁃shepatic cholangioscopy⁃related complications and the risk fac⁃tors for those complications[J].Endoscopy,2007,9(8):731-736
[6]刘衍民,曾可伟,王纯忠,等.改良的经皮经肝胆道镜术治疗肝内胆管结石_附15例报告[J].外科理论与实践,2004,9(6):485-486.
[7]温子龙,薛平,卢海武,郑强.改良经皮肝胆道镜治疗复杂肝内外胆管结石[J].岭南现代临床外科,2011,11(3):161-164.
[8]陆光生,刘衍民.经皮肝穿刺胆道引流管周瘘道形成的实验研究[J].中国内镜杂志,2004,11:51-53+57.
[9]王平,方兆山,孙北望,等.内置保护性鞘管和硬质胆道镜辅助治疗肝胆管结石临床研究[J].河北医学,2014,20(11):1761-1764.
[10]Yoon JH.Biliary papillomatosis:correlation of radiologic find⁃ings with percutaneous transhepatic cholangioscopy[J].J Gas⁃trointestin Liver Dis,2013,22(4):427-433.
Synchronous treatment of percutaneous transhepatic and choledochoscopy for recurrent hepatoli⁃ thiasis
LIN Shuwen Lin,FANG Yinghua,DING Xinming,YUAN Zhiming,WAN Lipeng,JI Cheng⁃gang.Department of Hepatobiliary Surgery,the Fifth People's Hospital of Dongguan City,Dongguan,Guangdong 523900,China
ObjectiveTo Summarize our experience on percutaneous transhepatic one⁃stage li⁃thotomy with choledochoscope in treatment of recurrent hepatolithiasis.MethodsA retrospective analy⁃sis of clinical data in 22 cases with recurrent hepatolithiasis in our hospital from October 2014 to June 2016 was performed.The patients were treated by direct puncture of hepatic duct under B⁃ultrasound guidance to establish a percutaneous tract,and then lithotomy with choledochoscope for extraction of the bile duct stones was performed contemporaneously.ResultsTwenty⁃one patients were successful to be extracted stone,only one patient was converted to laparotomy.Of 21 cases,17 were healed in one⁃time stone removal,three underwent two⁃time operation,one received three⁃time operation.The main compli⁃cation was hemobilia and was treated conservatively,and no serious complications and death.No recur⁃rence was found in all patients followed up until now.ConclusionIn properly selected patients of recur⁃rent hepatolithiasis,synchronous treatment of percutaneous transhepatic and choledochoscopy is feasi⁃ble,effective and safe.
percutaneous transhepatic;choledochoscopy;hepatolithiasis;recurrent
R657.3
A
10.3969/j.issn.1009⁃976X.2017.02.014
2017-02-16)
523900广东东莞东莞市第五人民医院肝胆外科
林树文,E-mail:42982832@qq.com
#并列第一作者

