一种卟啉-螺吡喃化合物的合成及其离子响应行为研究
高康莉,邓兆静,李郭成,韩国志
(南京工业大学 理学院,江苏 南京 210009)
一种卟啉-螺吡喃化合物的合成及其离子响应行为研究
高康莉,邓兆静,李郭成,韩国志*
(南京工业大学 理学院,江苏 南京 210009)
合成了一种卟啉-螺吡喃化合物,并对其结构进行详细表征。在此基础上,通过紫外光谱研究了其光致异构与离子响应特征,并提出了一种解释卟啉环与螺吡喃之间耦合行为的新机制。研究结果表明,金属离子会诱导合成的卟啉-螺吡喃分子产生新的构象,从而影响螺吡喃的光致异构。此外,随着离子半径以及亲电能力的不同,卟啉-螺吡喃衍生物的光学特性也产生明显差异。这种卟啉-螺吡喃化合物为构建新型离子探针提供了一种思路。
螺吡喃;卟啉;光致异构;离子响应
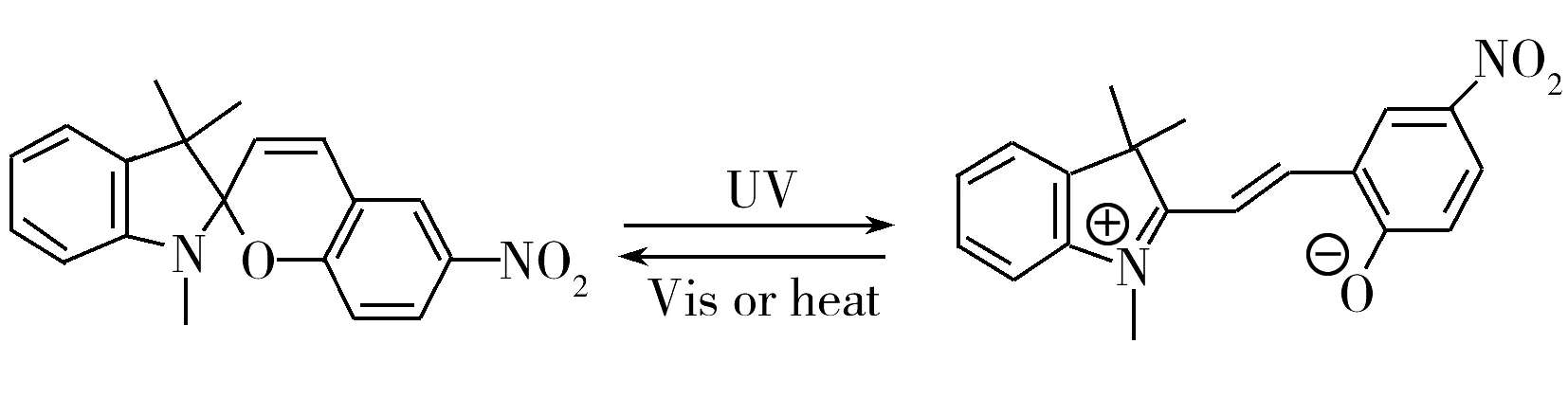
图 1 螺吡喃闭环体和开环体的光致异构过程Fig.1 Photochemical transformations of the spiropyran merocyanine system
光致异构是指化合物在一定波长的光照下,发生特定化学异构反应,而在另一波长的光照或热的作用下,又能恢复到原来分子结构的一种可逆变化[1-4]。在此过程中,由于结构与共轭程度的改变,导致其光学特性发生明显的变化。因此光致异构在信息存储、光学器件和分子识别等领域具有广泛的应用前景[5-8]。其中,螺吡喃及其衍生物是一类被广泛研究的光致变色物质[9-11]。在紫外光照射下,螺吡喃结构中的螺环C—O键断裂开环,导致整个分子体系的π电子共轭程度增加,形成有色开环体。在加热或可见光照射下有色开环体又重新逆向生成无色闭环体[12]。反应过程如图1所示。
目前,与其他功能基团进行复合拓展螺吡喃衍生物的应用领域是其重要的研究方向[13]。在此类研究中,基于螺吡喃分子异构的离子探针的设计与合成是一个新兴的研究领域,受到极大关注。通过金属离子诱导螺吡喃结构发生开环,从而对其光致异构行为产生影响[14-15]。但关于螺吡喃复合体系的离子响应行为鲜有报道。本文将具有离子配位能力的卟啉环引入螺吡喃分子结构,合成了一种双官能团化合物,并研究了两种官能团的耦合行为。结果表明,卟啉结构的引入对螺吡喃分子的光学行为产生了重要影响。尤其是加入金属离子后,螺吡喃的光致异构受到明显抑制,与现有的螺吡喃分子离子响应特征的报道截然相反。在此基础上,进一步提出了新的响应机制,为构建新型离子传感提供了新思路。卟啉螺吡喃(化合物5)分子的合成路线如图2所示。
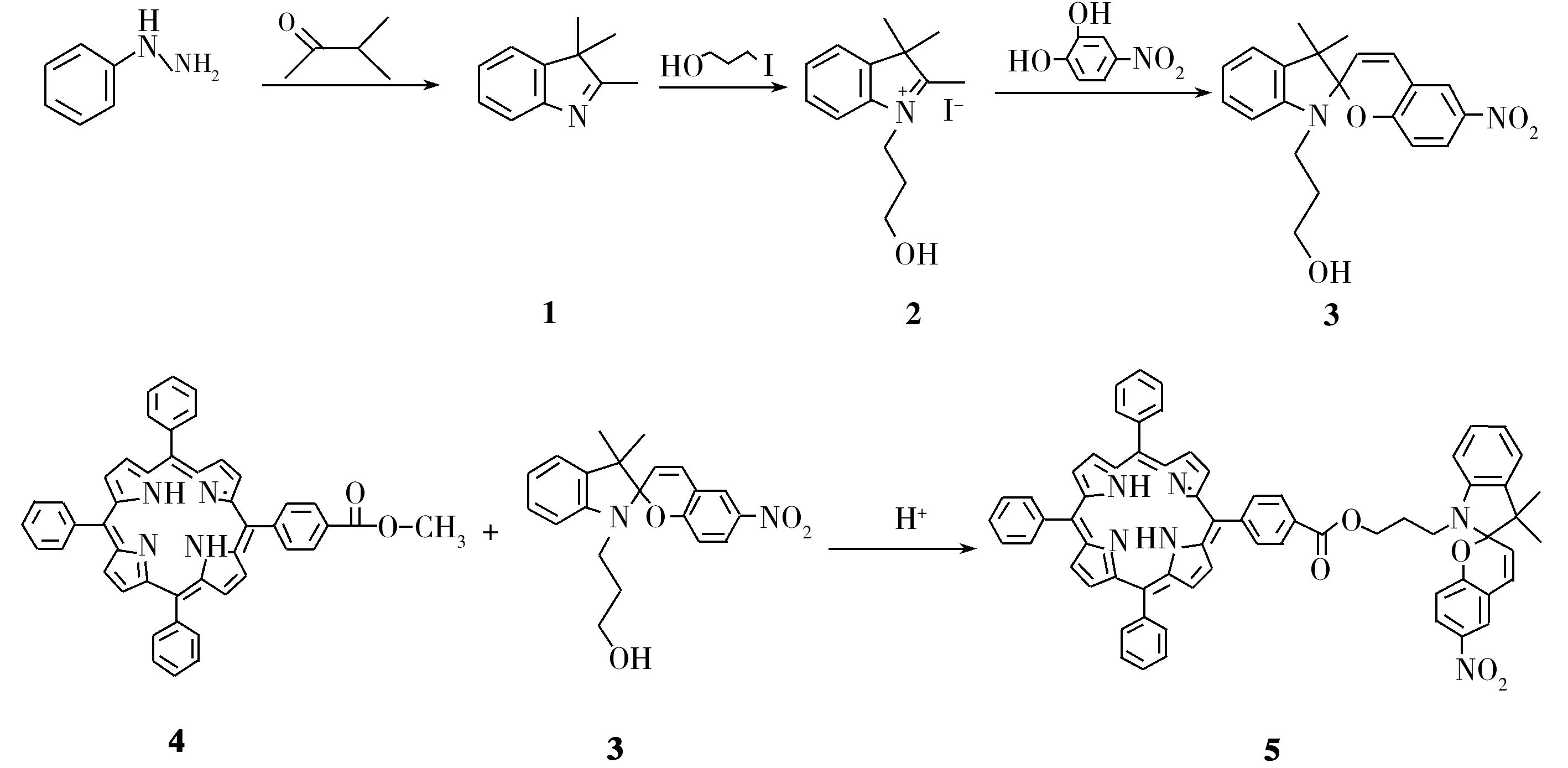
图 2 目标化合物5的合成路线Fig.2 Synthetic routes of compound 5
1 实验部分
1.1 试剂与仪器
苯肼、5-硝基水杨醛(上海阿拉丁试剂公司);苯甲醛、对甲酰基苯甲酸甲酯、吡咯(国药集团化学试剂有限公司);甲基异丙基酮(上海德默医药科技有限公司);3-碘丙醇(南京精瑞久安生物技术有限公司),以上试剂均为分析纯。
Bruker Avance 300 型核磁共振仪(以四甲基硅为内标,德国 Bruker公司);Shimadzu 3150 -PC 型紫外分光光度计(UV-Vis,日本岛津公司);WRS-2A型熔点仪(上海精密仪器有限公司)。
1.2 实验方法
1.2.1 2,3,3-三甲基吲哚(1)的合成 在250 mL三颈瓶中,加入苯肼(5.4 g,50 mmol)、甲基异丙基酮(4.4 g,51 mmol)和120 mL醋酸-乙醇-水(4∶1∶1)的混合溶剂,加热回流3 h,TLC 监测反应终点。之后冷却至室温,用饱和氢氧化钠水溶液调至pH 8.0。乙酸乙酯(2×40 mL)萃取,合并有机相,减压蒸馏收集116~118 ℃的馏分,得淡黄色油状液体(6.3 g,收率80%)。1H NMR(500 MHz,CDCl3),δ:7.15-7.52(m,4H,ArH),1.27(s,6H,CH3),2.25(s,3H,CH3)。
1.2.2 1-(3-羟丙基)-2,3,3-三甲基-3H-吲哚碘化物(2)的合成[16]在N2保护下将化合物1(1.6 g,10 mmol)、3-碘-1-丙醇(1.86 g,10 mmol)溶解于4 mL甲苯中,110 ℃下回流反应2 h。冷却至室温,旋干溶剂得油状物。未经进一步纯化,直接用于下一步反应。
1.2.3 1-(3-羟丙基)-3,3-二甲基-6-硝基苯并螺吡喃(3)的合成[16]将油状物2溶于30 mL异丙醇中,再加入5-硝基水杨醛(1.67 g,10 mmol)、三乙胺(1 g,10 mmol),在N2保护下回流反应4 h。TLC 监测反应终点。冷至室温后,旋干溶剂。剩余物用CH2Cl2提取,除去CH2Cl2后,用乙醇重结晶得紫红色固体(1.1 g,收率61.1%)。1H NMR(500 MHz,DMSO),δ:8.05(d,J=7.9 Hz,1H,ArH),8.00(d,J=7.7 Hz,1H,ArH),7.13-7.20(m,2H,ArH),6.86(d,J=8.9 Hz,1H,ArH),6.77-6.83(m,2H,ArH),6.64(d,J=7.8 Hz,1H,CH),5.97(d,J=10.5 Hz,1H,CH),4.33(t,J=6.0 Hz,2H,CH2),3.29-3.43(m,2H,CH2),1.64-1.75(m,2H,CH2),1.15(s,6H,CH3)。
1.2.4 单脂基卟啉(4)的合成[17]将对甲酰基苯甲酸甲酯(0.16 g,0.001 mol)、苯甲醛(0.3 g,0.003 mol)溶解于150 mL丙酸中,加热至沸腾后,以2 s/滴的速度将吡咯(0.26 g,0.004 mol)加入上述反应液中,回流反应3 h,TLC监测至反应终点[17]。冷却至室温后,旋干,采用二氯甲烷-石油醚(1∶1)柱层析分离得到目标产物(0.33 g,收率49.2%)。1H NMR(500 MHz,CDCl3),δ:8.79(s,8 H,pyrrole),8.42 (s,2H,ArH),8.30-8.23(t,3H,J=6.4 Hz,ArH),8.10(s,6H,ArH),7.75-7.77(d,8H,J=6.4 Hz,ArH),3.95(s,2H,NH),0.86(s,3H,CH3)。
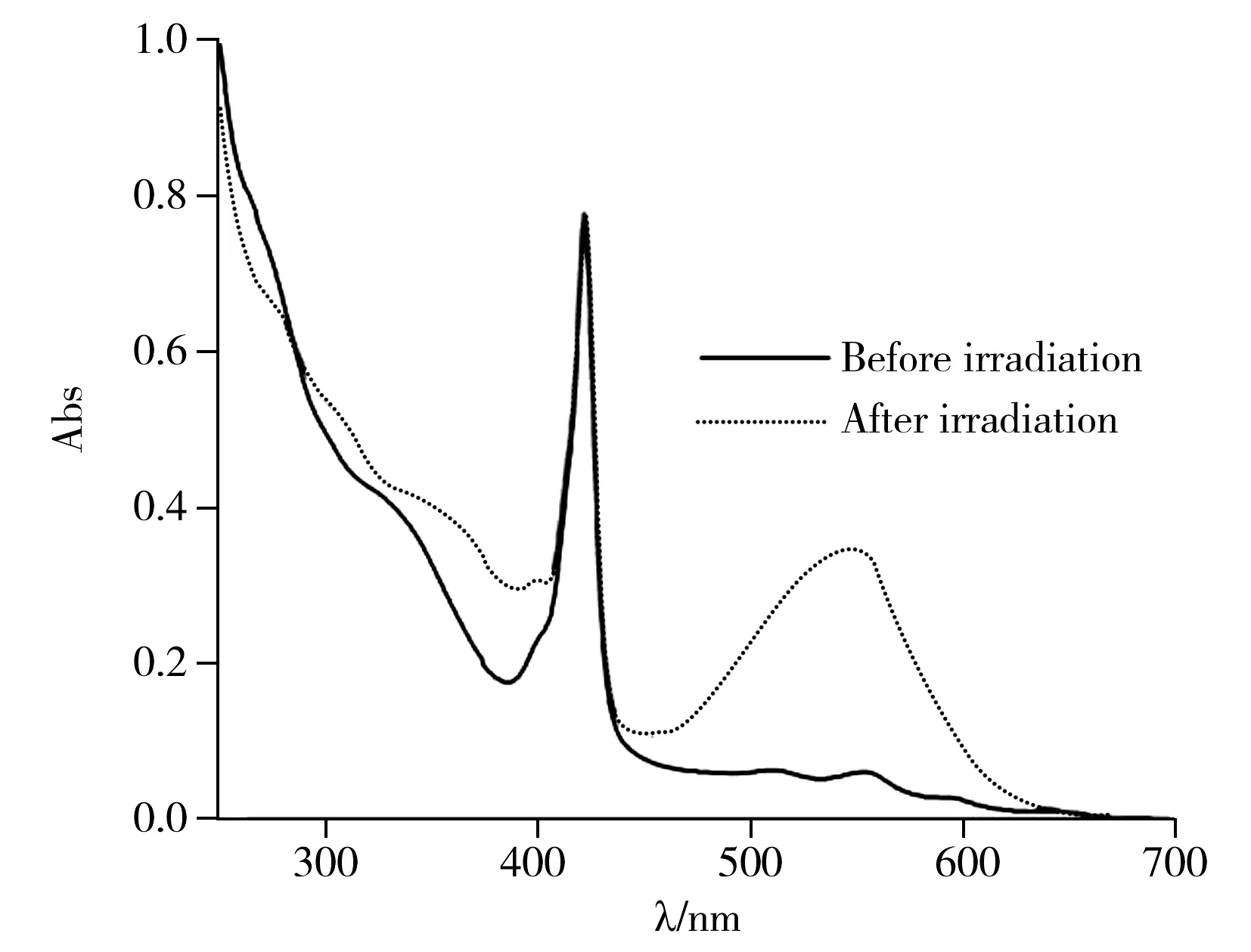
图3 化合物5的乙醇溶液紫外光照射前后的紫外-可见光谱Fig.3 UV-Vis spectra of compound 5 in ethanol solution before and after UV irradiation(254 nm,20 ℃)
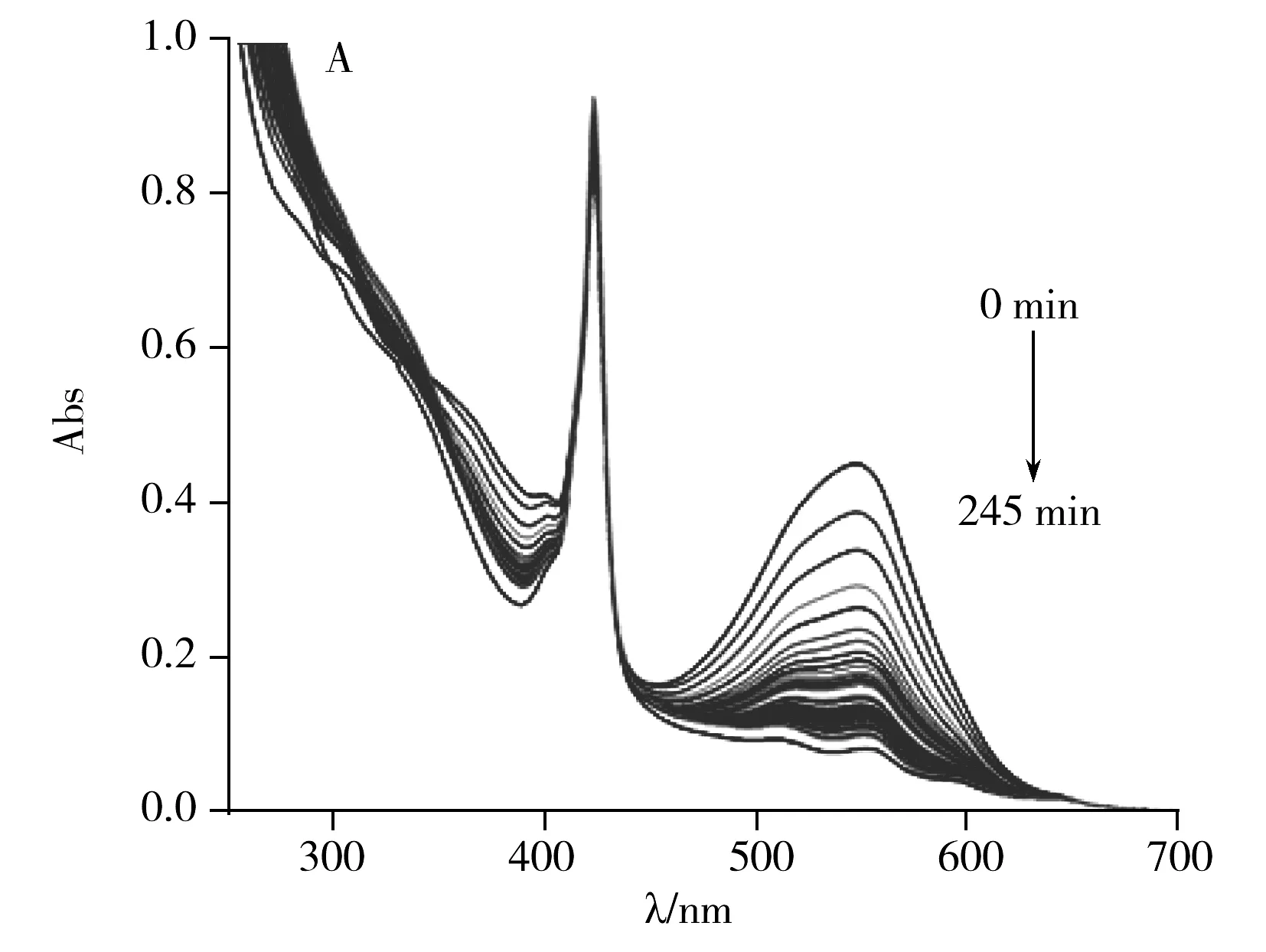

图4 化合物5(A)及化合物3的褪色曲线(B)Fig.4 Decay curve of compound 5(A) and compound 3(B) in ethanol solution
1.2.5 卟啉-螺吡喃衍生物(5)的合成[18-19]将化合物3(0.044 g,0.12 mmol)、单酯基卟啉4(0.06 g,0.09 mmol)溶解于100 mL甲苯中,再加入催化量的醋酸,回流反应12 h,TLC 监测反应终点。冷却至室温后,旋干,采用乙酸乙酯-石油醚(1∶3)柱层析分离,得目标产物(0.06 g,收率66.7%)。1H NMR(500 MHz,CDCl3),δ:8.89(s,8H,pyrrole),8.42(d,J=8.2 Hz ,3H,ArH),8.22(d,J=6.4 Hz ,2H,ArH),8.00(d,J=5.2 Hz ,8H,ArH),7. 74(d,J=7.2 Hz ,8 H,ArH),7.60(d,J=9.5 Hz ,3H,ArH),6.98(d,J=7.8 Hz ,1H,ArH),6.88-6.91(t,J=10.2 Hz ,3H,ArH),6.58(d,J=7.3 Hz ,1H,CH),5.83(d,J=5.4 Hz,1H,CH),4.11(s,2H,NH),2.32-2.37(m,2H,CH2),2.17(s,3H,CH3),1.26(s,3H,CH3),0.88(m,2H,CH2)。1.2.6 离子响应行为的光谱分析 为了避免卟啉环对光照前后溶液颜色变化的影响,配制浓度为0.25×10-4mol/L的化合物3乙醇溶液和化合物5乙醇溶液。在此浓度下,溶液颜色呈无色。再分别配制相同浓度的CuSO4乙醇溶液、Pb(NO3)2乙醇溶液、SnCl2乙醇溶液和FeSO4乙醇溶液。首先用254 nm的紫外光照射化合物3和化合物5,分别测量其光照前后的紫外-可见光谱,再将光照后样品置于黑暗中,每隔2 min分别测其对应的紫外可见光谱,绘制褪色曲线。最后,分别取2 mL金属离子乙醇溶液和2 mL化合物3与化合物5乙醇溶液于石英比色皿充分混合,再分别测量其经紫外光照射 (波长为254 nm) 前后的紫外-可见光谱。
2 结果与讨论
2.1 卟啉螺吡喃(5)的光致异构特性
图3为化合物5光照前后的紫外光谱。光照前,化合物5在420 nm以及500~600 nm之间的特征吸收分别对应卟啉的S带和Q带。在270 nm 处有螺吡喃的特征吸收峰。随着紫外光的照射,在556 nm处出现一增强的吸收峰,对应螺吡喃的共轭开环体,同时溶液颜色由无色变为红色。
研究发现,卟啉螺吡喃分子中卟啉环对螺吡喃的光学活性具有重要影响。图4是两种螺吡喃分子(化合物3与化合物5)在乙醇溶液中的褪色曲线。从图4可以看出,卟啉螺吡喃(化合物5)与 羟基螺吡喃(化合物3)开环体的特征吸收峰分别在556 nm和543 nm处,说明N上取代基会影响螺吡喃共轭开环体的电子跃迁。此外,实验结果表明,卟啉螺吡喃的开环体较为稳定,在黑暗中完全褪色需245 min。而羟基螺吡喃的开环体稳定性比卟啉螺吡喃的稳定性差,在180 min内可以恢复到无色闭环状态。本文分析认为,卟啉螺吡喃分子中卟啉环的电子密度较大,与开环体中的氧负离子存在较强的电性排斥力,使该开环体结构变得稳定,褪色速度更慢。
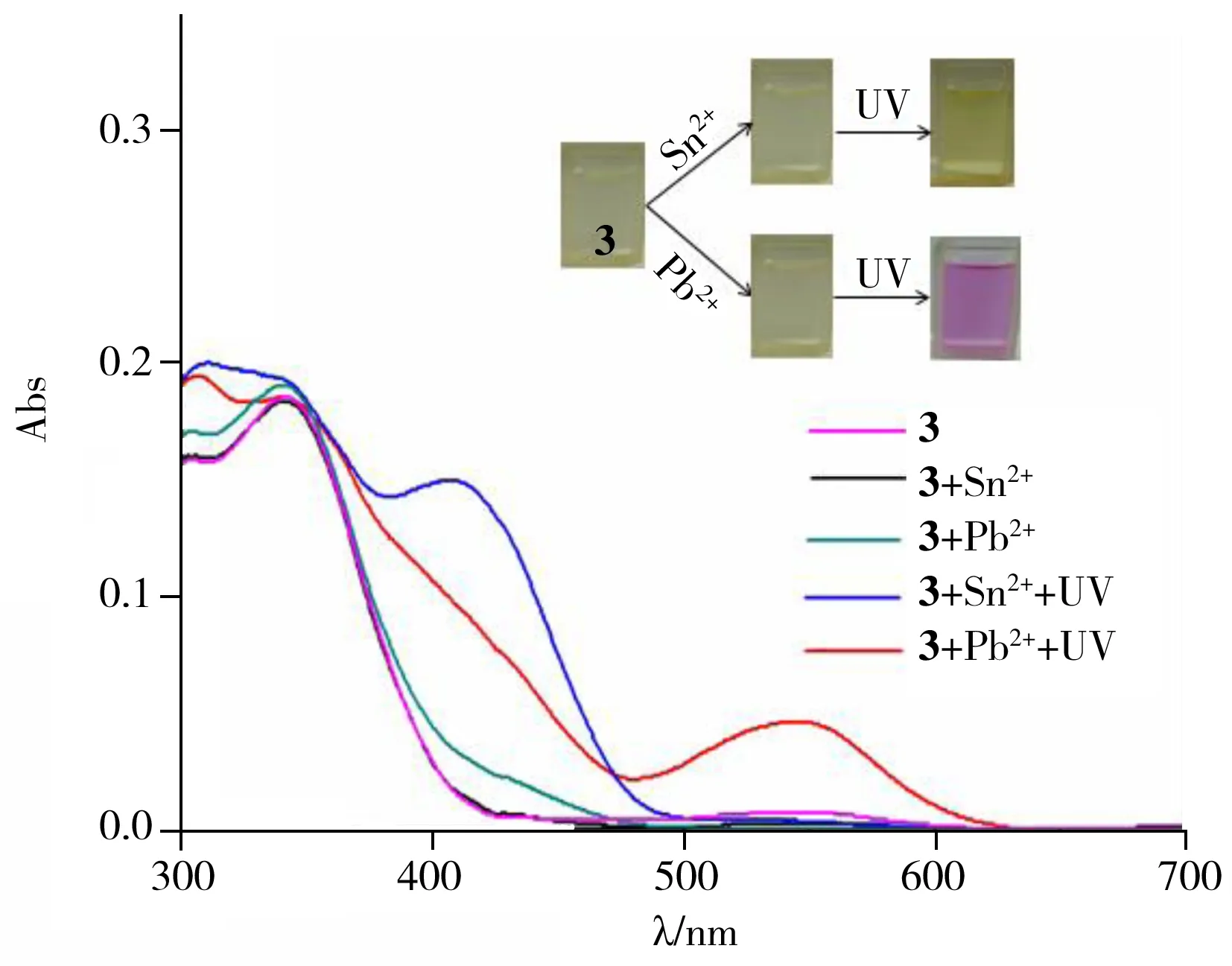
图5 化合物3与不同金属离子等量混合后在紫外光照射前后的光谱变化Fig.5 UV-Vis spectra of compound 3 in the presence of metal ions before and after UV irradiation
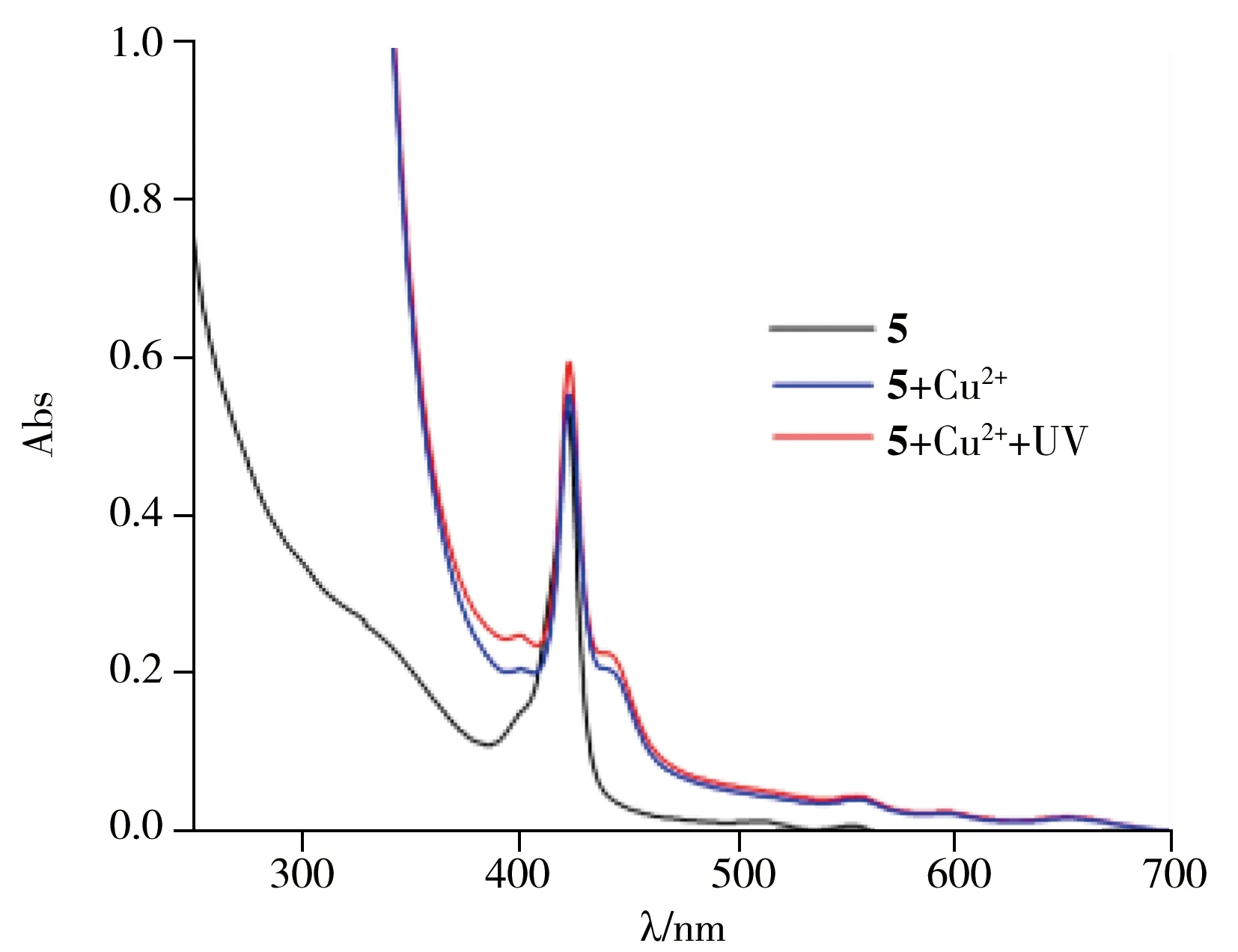
图6 化合物5与铜离子等量混合后在紫外光照射前后的光谱变化Fig.6 UV-Vis spectra of compound 5 in the presence of metal ions before and after UV irradiation
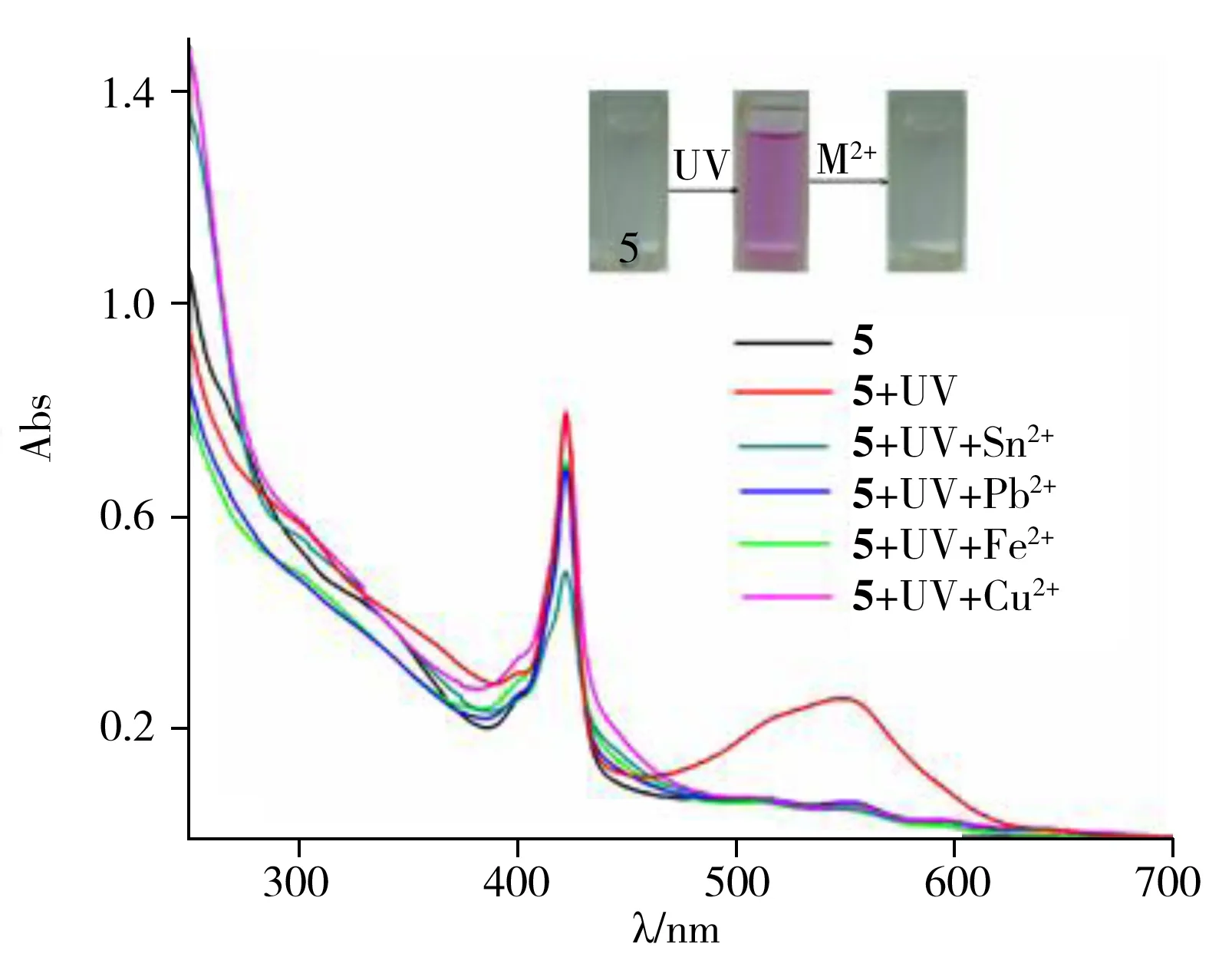
图7 不同金属离子对化合物5开环体的影响Fig.7 Influence of metal ions on the merocyanine of compound 5
2.2 卟啉螺吡喃(5)的离子响应行为
螺吡喃分子开环之后,氧负离子可与部分金属离子络合,从而导致其光学特性发生变化,图5为化合物3与两种离子响应的紫外光谱。由图5可见,化合物3与Sn2+混合再进行光照之后,颜色从无色转变为淡黄色,对应的开环体的特征吸收峰从556 nm蓝移至420 nm,这主要是因为Sn2+与开环体络合使其以Sn2+-MC的形式存在[20],从而开环体在556 nm处的特征吸收峰消失,该络合物在420 nm处的特征吸收峰出现,表明化合物3的开环体实现了对Sn2+的识别 。而与Pb2+混合,再经光照后,颜色从无色转变为红色,对应开环体的特征峰依然在556 nm左右,说明化合物3的开环体对Pb2+无识别作用,原因可能是铅离子的亲电性较弱。进一步的实验表明,化合物3的开环体对Hg2+和Cu2+也具有响应识别作用,与理论分析相一致。
但当在N上取代基中引入卟啉环后,化合物5的离子响应行为发生了重大变化。图6是化合物5与铜离子的响应紫外光谱,从图中可以看出,化合物5与Cu2+混合后,再经光照,其紫外光谱的特征吸收基本无变化,光致异构特性消失。
当卟啉螺吡喃光致开环后,金属离子同样能够将其猝灭。图7是对应的紫外光谱,由图可见,有色开环体与4种金属离子混合后颜色均消失,对应长波处的吸收峰也随之降低,褪色程度为Cu2+> Sn2+>Pb2+>Fe2+,这可能与金属离子的半径以及离子亲电性有关。
根据以上实验结果,本文研究认为,卟啉螺吡喃与金属离子形成了一种类似“夹心”的结构,如图8所示。当卟啉螺吡喃与金属离子混合之后,金属离子处于卟啉环和螺吡喃中的吡喃环之间,金属离子与两个环上的电子静电络合,环上电子的离域能力增强,电子密度平均化程度升高,形成了一种稳定的空间构象,从而抑制了化合物5的光致异构。
进一步通过紫外光谱对提出的机理进行了验证。图9是卟啉螺吡喃与Sn2+和Na+混合后在长波长处的紫外-可见光谱。当金属离子与卟啉环上的N原子形成配位键会导致卟啉环分子结构的对称性提高,能级简并,表现为Q带吸收峰的个数减少。而图9中Q带吸收峰个数并未减少,但在655 nm处的吸收峰明显增强,归属于卟啉环电子S0-S1的跃迁,表明金属离子未与卟啉环形成典型配位键但存在相互作用。作为对比,本文用亲电性较弱的Na+与化合物5混合,光谱几乎无变化(图9插图),表明Na+未与卟啉环上的电子静电络合,从侧面验证了该机理。
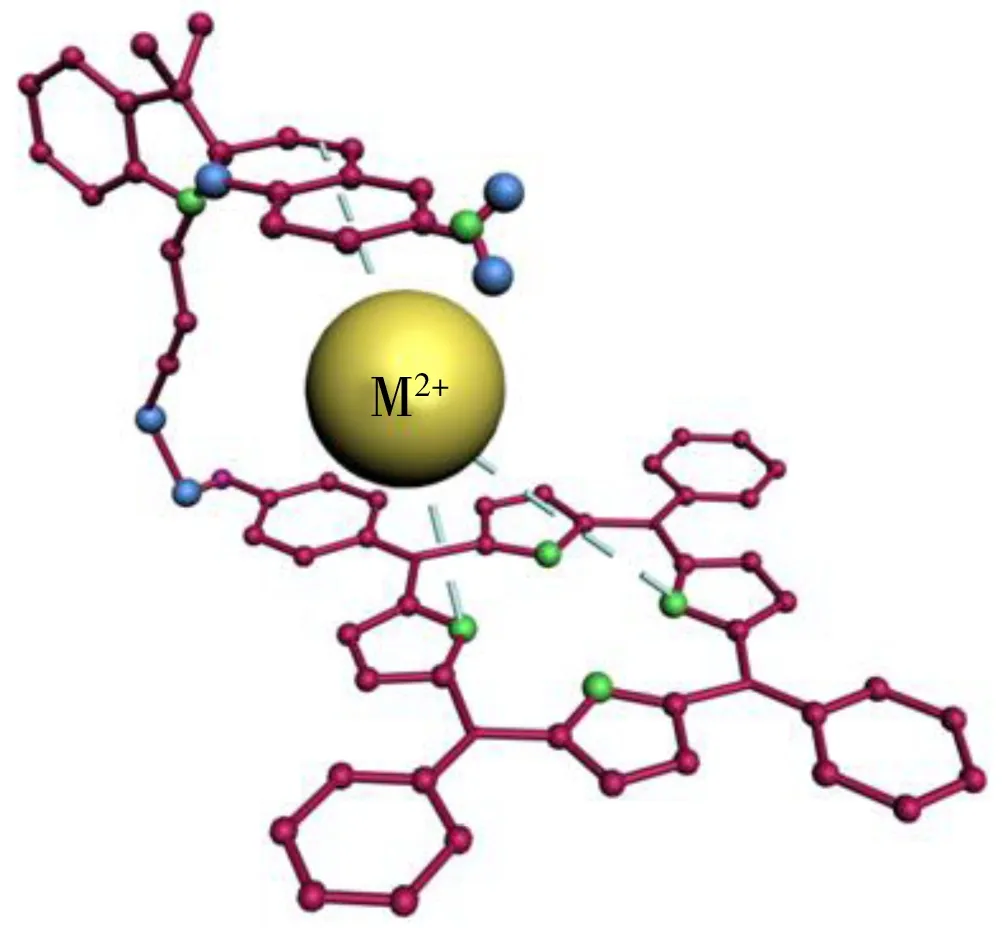
图8 化合物5与金属离子作用的机理图Fig.8 Schematic map of metal ion response behavior of compound 5
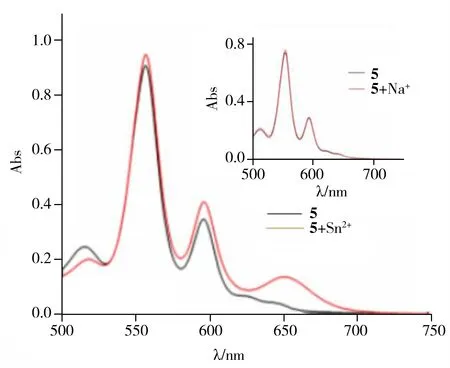
图9 化合物5与Sn2+等量混合后的紫外-可见光谱Fig.9 UV-Vis spectra of compound 5 in the presence of Sn2+insert:UV-Vis spectra of compound 5 in the presence of Na+
3 结 论
本文设计合成了一种卟啉-螺吡喃衍生物,通过紫外光谱研究了其光致异构与离子响应特征,并提出了一种新的机制,解释了卟啉环与螺吡喃之间的耦合行为。研究结果表明,金属离子会诱导合成的卟啉-螺吡喃分子产生新的构象,从而影响螺吡喃的光致异构,并且随着离子半径以及亲电能力的不同,卟啉-螺吡喃衍生物的光学特性也产生明显差异。
[1] Chen J,Zeng F,Wu S Z,Chen Q M,Tong Z.Chem.Eur.J.,2008,14:4851-4860.
[2] Zhang P,Meng J B,Li X L,Matsuura T,Wang Y M.J.Heterocycl.Chem.,2002,39:179-184.
[3] Fries K H,Sheppard G R,Bilbrey J A,Locklin J.Polym.Chem.,2014,5:2094-2102.
[4] Zhang M,Gao C,Tian H Y,Yue P,Wang M C,Wang M,Zhao X W.J.Instrum.Anal.(张敏,高潮,田宏远,岳璞,王民昌,王明,赵效文.分析测试学报),2007,26:335-336.
[5] Cao J J,Wu S F,Zhai B Q,Wang Q C,Li J,Ma X.DyesandPigments,2014,103:89-94.
[6] Cui H Q,Liu H,Chen S,Wang R M.DyesandPigments,2015,115:50-57.
[7] Tao J,Li Y H,Zhao P,Li J S,Duan Y,Zhao W J,Yang R H.Biosens.Bioelectron., 2014,62:151-157.
[8] Lü Q,Yan B Z.J.Instrum.Anal.(吕强,严宝珍.分析测试学报),2001,20(4):33-35.
[9] Bretler S,Margel S.Polymer,2015,61:68-74.
[10] Zhang H,Wang C X,Jiang T,Guo H M,Wang G,Cai X H,Yang L,Zhang Y,Yu H C,Wang H,Jiang K.Anal.Chem.,2015,87:5216-5222.
[11] Osborne E A,Jarrett B R,Tu C Q,Louie A Y.J.Am.Chem.Soc.,2010,132:5934-5935.
[12] Hirakura T,Nmura Y,Aoyama Y,Akiyoshi K.Biomacromolecules,2001,5:1804-1809.
[13] Takumi K,Sakamoto H,Uda R M,Sakurai Y,Kume H,Kimura K.Physicochem.Eng.Aspects,2001,301:100-105.
[14] KIm I,Jeong D C,Lee M,Khaleel Z H,Satheeshkumar C,Song C.TetrahedronLett.,2015,56:6080-6084.
[15] Zhao C,Ge Y H,Han P.Chem.Ind.Times(赵春,葛裕华,韩沛.化工时刊),2010,24(5):4-8.
[16] Darwish T A,Evans R A,James M,Malic N,Triani G,Hanley T L.J.Am.Chem.Soc.,2010,132:10748-10755.
[17] Sun L,Chen H S,Zhang Z L,Yang Q,Tong H B,Xu A H,Wang C D.J.Inorg.Biochem.,2012,108:47-52.
[18] Bahr J L,Kodis G,Garza L D L,Lin S,Moore A L,Moore T A,Guat D.J.Am.Chem.Soc.,2011,123:7124-7133.
[19] Hur D Y,Park T J,Shin E J.Spectrom.Chim.ActaA,2014,117:541-547.
[20] Ren J Q,Tian H.Sensors,2007,7(12):3166-3178.
Synthesis of a Prophyrin-Spiropyrane Compound and Its Ionic Response Behavior
GAO Kang-li,DENG Zhao-jing,LI Guo-cheng,HAN Guo-zhi*
(College of Science,Nanjing Tech University,Nanjing 210009,China)
A kind of porphyrin-spiropyrane derivative was synthesized and detailedly characterized.On this basis,the photoisomerization and ionic response behaviors of the compound were studied by UV-Vis spectrometry,and a new mechanism to explain the coupling behavior between porphyrin ring and spiropyrane was proposed.The experiental results showed that metal ions could induce porphyrin-spiropyran molecule to generate a new conformation which will affect the photoisomerization properties of spiropyrane.In addition,with the changes of ionic radius and electrophilic ability,the optical properties of the porphyrin-spiropyrane derivative presented significant differences.This study provides an idea for constructing a new ionic probe.
spiropyrane;porphyrin;photoisomerization;ionic response
2016-04-14;
2016-05-18
江苏省博士后基金(1002006C)
10.3969/j.issn.1004-4957.2016.10.018
O657.3;O741.6
A
1004-4957(2016)10-1323-05
*通讯作者:韩国志,副教授,研究方向:功能分子材料的合成与应用,Tel:025-8347581,E-mail:han@njtech.edu.cn

